Согласно современным клиническим рекомендациям Международной ассоциации по сексуальной медицине (ISSM), выделяют первичную и вторичную формы преждевременного семяизвержения (ПС). При этом к первому варианту описанного сексуального расстройства относят эякуляцию, возникающую приблизительно менее чем через 1 мин после начала коитуса или до интроекции и характеризующуюся возникновением с начала половой жизни, отсутствием контроля над эякуляторным процессом и негативным психологическим фоном у обоих партнеров. Вторичная форма ПС отличается приобретенным характером и временем интравагинальной задержки семяизвержения (ВИЗС) менее 3 мин [1].
Общепризнанно, что ПС относится к распространенным сексуальным нарушениям, так как, по разным данным, оно встречается у 20–40% мужской популяции. Вместе с тем, согласно клиническим рекомендациям Европейской ассоциации урологов, с учетом имевших в недавнем прошлом несоответствий между существующими дефинициями и диагностическим критериям описанного полового расстройства, нельзя исключить его гипердиагностику [2].
Одной из основных причин первичного ПС считают дисрегуляцию церебрального 5-гидрокситриптамина (5-ГТ) или серотонина, описанную авторами нейробиологической теории возникновения ускоренной эякуляции. Имеются доказательства генетической обусловленности недостатка данного нейромедиатора у обсуждаемой категории пациентов в синаптических щелях серотонинэргических нейронов головного мозга [3]. Описанная особенность связана с генотипом гена транспортера серотонина. Имеются доказательства того, что к ПС наиболее предрасположены мужчины с S-аллельсодержащими вариантами строения данного белка [4].
Состоятельность нейробиологической теории еще до ее официального возникновения доказал в 1973 г. H. Eaton, впервые успешно применивший при ускоренной эякуляции трициклический антидепрессант кломипрамин, обладающий мощной способностью блокировать обратный нейрональный захват 5-ГТ. Впоследствии в начале 1990-х гг. были синтезированы антидепрессанты группы селективных ингибиторов обратного захвата серотонина (СИОЗС), которые прицельно воздействовали на серотонинэргические нейроны. Руководствуясь имевшимися в то время данными о роли церебрального серотонина в регуляции эякуляторной функции, в зарубежных странах их стали активно применять не по показаниям при первичноим ПС [5]. Примечательно, что принадлежность СИОЗС к психотропным лекарствам группы антидепрессантов в ряде стран не позволяет назначать их по поводу ПС, так как это не оговорено в зарегистрированных инструкциях. В Российской Федерации возможность использования любого препарата определяется врачом в рамках, ограниченных официальными показаниями, заявленными производителем. В США и в ряде государств Западной Европы назначение лекарств не по зарегистрированным основаниям допустимая практика, при этом ответственность за жизнь и здоровье пациента целиком ложится на доктора, что предусмотрено в юридических полномочиях врачебной лицензии [6, 7].
В отношении СИОЗС следует учитывать, что на сегодняшний день подтверждена повышенная вероятность суицидальных тенденций при их отмене. Это дополнительно обосновывает нежелательность их назначения пациентам без депрессии, которая должна быть диагностирована психиатром [8].

С учетом указанных обстоятельств специально для лечения преждевременного семяизвержения был разработан СИОЗС дапоксетин. В отличие от остальных препаратов данной группы, имеющих галогенированные молекулы, в его молекулярной структуре содержится нафтильный фрагмент [9]. Именно он обусловливает быструю абсорбцию препарата в желудочно-кишечном тракте и короткий период полувыведения, что обеспечивает значительно меньшее число побочных эффектов по сравнению с другими СИОЗС. Максимальная концентрация в плазме крови достигается через 1,5 ч после приема [10]. Быстрое снижение плазменного содержания препарата не позволяет обнаруживать более 4% данного препарата спустя 24 ч.
После продолжительных ежедневных приемов обсуждаемого СИОЗС доказано отсутствие его значимого накопления [11].
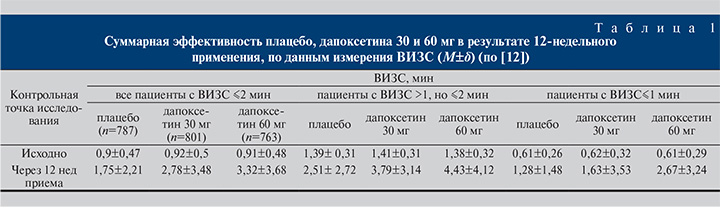
Впервые эффективность дапоксетина в рамках рандомизированного двойного слепого плацебо-контролируемого исследования изучили J. Pryor и соавт. в 2006 г. [12]. Участие в нем принял 2351 пациент, который был разделен на 3 группы по 787, 801 и 763 человека, получавших в течение 12 нед соответственно плацебо, дапоксетин 30 и 60 мг. Препарат назначался по требованию за 1–3 ч до предполагаемой сексуальной активности. К концу исследования обе дозы дапоксетина были достоверно более эффективны по сравнению с плацебо (p<0,0001), при этом 60 мг значимо превышали по эффекту 30 мг лекарства (p=0,0007). К 12-й неделе 109 (14%), 232 (29%) и 261 (34%) пациент 1-й, 2-й и 3-й групп соответственно имели показатель ВИЗС, превысивший 3 мин. Прием первой дозы дапоксетина по эффективности достоверно превосходил плацебо. В группах, получавших плацебо, дапоксетин 30 и 60 мг, ВИЗС от базового уровня увеличилось на 1,38; 2,05 и 2,41 мин соответственно (табл. 1).
 При оценке профиля безопасности лечения обсуждаемым СИОЗС (в дозировке 30 и 60 мг) были соответственно отмечены тошнота (8,7 и 20,1%), диарея (3,9 и 6,8%), головная боль (5,9 и 6,8%) а также головокружение (3,0 и 6,2%) [12].
При оценке профиля безопасности лечения обсуждаемым СИОЗС (в дозировке 30 и 60 мг) были соответственно отмечены тошнота (8,7 и 20,1%), диарея (3,9 и 6,8%), головная боль (5,9 и 6,8%) а также головокружение (3,0 и 6,2%) [12].
В 2009 г. J. Kaufman и соавт. [13] провели двойное слепое плацебо-контролируемое исследование эффективности дапоксетина при ПС, в котором завершили участие 652 пациента. Основная оценка эффективности лечения проведена по анкете Профиля преждевременного семяизвержения (ППС; табл. 2). В результате лечения пациенты, получавшие дапоскетин, отметили статистически значимое снижение обеспокоенности по поводу состояния эякуляторной функции, уменьшение выраженности межличностных конфликтов в паре, а также улучшение контроля над семяизвержением и удовлетворение от полового акта.
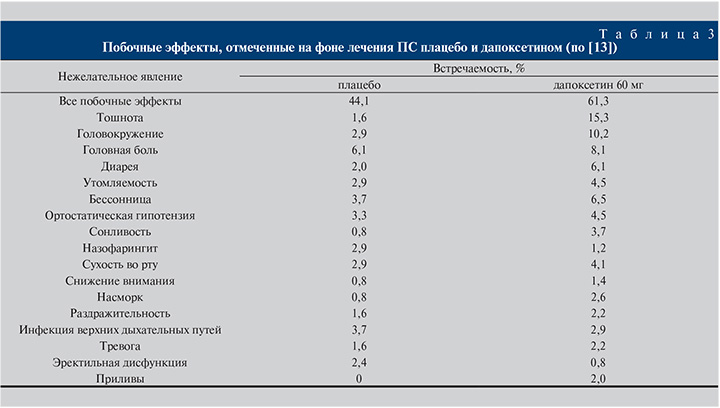
Дополнительно всем пациентам, участвовавшим в данном исследовании, проведено анкетирование по шкале общего впечатления об изменении эякуляторной функции в результате лечения. Наивысшую степень удовлетворения от проведенной терапии отметили 41,3 и 20,8% больных, получавших дапоксетин и плацебо соответственно (p<0,001). Кроме того, оценен клинический профиль безопасности указанного СИОЗС (табл. 3). Было отмечено, что частые побочные эффекты, имевшие место более чем в 5% наблюдений, среди которых тошнота, головокружение, головная боль, диарея и бессонница, чаще возникали при приеме 60 мг дапоксетина. Отказ от продолжения лечения по причине нежелательных явлений был констатирован у 10 и 2% пациентов, принимавших указанное лекарство и плацебо соответственно. При этом наиболее часто причиной отмены дапоксетина служили тошнота и бессонница [13].
J. Buvat и соавт. [14] провели 24-недельное плацебо-контролируемое исследование эффективности дапоксетина при ПС, которое завершили 618 пациентов. Среднее ВИЗС возросло при применении плацебо, а также дапоксетина 30 и 60 мг с 0,9 до 1,9; 3,2 и 3,5 мин соответственно. Таким образом, применение данного СИОЗС в обеих дозах позволило статистически значимо увеличить продолжительность полового акта (p<0,001). Наиболее частыми нежелательными явлениями при приеме дапоксетина были тошнота, головокружение, диарея и головная боль. Отказ от лечения по причине тяжелых побочных эффектов в группах, получавших плацебо, а также обсуждаемый СИОЗС в дозировках 30 и 60 мг отмечены в 1,3, 3,9 и 8,2% наблюдений соответственно [14].
В 2010 г. С. McMahon и соавт. [15] провели двойное слепое рандомизированное плацебо-контролируемое исследование эффективности дапоксетина при ПС в Азиатско-Тихоокеанском регионе. Участие в нем завершили 858 пациентов. Среднее ВИЗС при применении плацебо, а также дапоксетина 30 и 60 мг увеличилось с 1,1 мин до 2,4; 3,9 и 4,2 мин соответственно. Удовлетворенность произошедшими в результате лечения дапоксетином изменениями эякуляторной функции была статистически значимо выше (p<0,005) по сравнению с группой пациентов, принимавших плацебо [15].
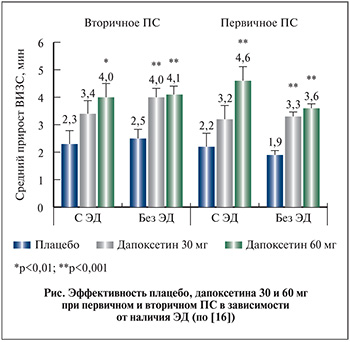
H. Porst и соавт. [16] провели обобщенный анализ 3 рандомизированных плацебо-контролируемых исследований эффективности обсуждаемого СИОЗС, включивший 2228 наблюдений. При этом авторы акцентировали усилия на сравнении существующих дозировок дапоксетина и плацебо при первичном и вторичном ПС в зависимости от наличия эректильной дисфункции (ЭД; см. рисунок). Авторами показано статистически значимое увеличение ВИЗС по сравнению с плацебо при применении указанного лекарства в дозировке 30 мг пациентами с обеими формами эякуляторного нарушения только в отсутствие нарушений эрекции. Вместе с тем еще более значимое возрастание продолжительности коитуса было отмечено у больных ПС при приеме 60 мг дапоксетина вне зависимости от формы ускоренной эякуляции и наличия ЭД [16].
В 2011 г. С. McMahon и соавт. [17] представили результаты анализа крупнейших рандомизированных плацебо-контролируемых исследований III фазы, проведенных в 25 странах и включивших 6081 пациента. Через 12 и 24 нед приема 30 мг дапоксетина было отмечено достоверное возрастание ВИЗС с 0,9 до 3,1 и 2,0 мин соответственно. При лечении препаратом в дозировке 60 мг продолжительность полового акта в указанные контрольные сроки возросла с 0,8 до 3,6 и 2,3 мин соответственно. Применение обеих дозировок дапоксетина позволило достигать положительной динамики по показателю ВИЗС, особенно через 12 нед от начала терапии (p<0,0001) [17].
В работе [18] проведена оценка эффективности 12-недельного комбинированного назначения дапоксетина пациентам с ПС и сопутствующей ЭД, получавших ингибиторы фосфодиэстеразы 5-го типа (ИФДЭ-5). Исследование завершили 429 пациентов. Авторы отметили, что продолжительность полового акта одинаково статистически значимо возросла при комбинированной терапии с СИОЗС по сравнению с группой пациентов, получавших плацебо+ИФДЭ-5 (5,2 против 3,4 мин; p<0,01). Общая удовлетворенность лечением при анкетировании также достоверно различалась в основной и контрольной группах (56,6 против 35,4%; p<0,001).
Авторы не отметили каких-либо лекарственных взаимодействий при совместном назначении с коротко- (силденафил) и длительнодействующим (тадалафил) ИФДЭ-5.
Частота побочных явлений при применении плацебо и дапоксетина в составе комбинированной терапии с эректогенными препаратами первой линии составила 20,9 и 29,6% соответственно. Отказ от лечения по причине нежелательных эффектов был отмечен в 1,6% наблюдений в основной и контрольной группах. Наиболее частыми побочными явлениями, ассоциированными с СИОЗС, были тошнота (9,2%), головная боль (4,4%), диарея (3,6%), головокружение (2,4%) и постуральная гипотензия (2,4%) [18].
Единственный на данный момент мета-анализ 5 рандомизированных плацебо-контролируемых клинических исследований эффективности дапоксетина был проведен F. Yue и соавт. в 2015 г. [19]. Установлено, что данный препарат значимо эффективней плацебо по показателю ВИЗС – в 1,47 раза (95% доверительный интервал [ДИ] – 1,22–1,71; p<0,00001). По данным анкетирований, оценивавших диагностические критерии ПС, дапоксетин лучше плацебо в 3,19 раза (95% ДИ – 2,47–4,11; p<0,00001). Преимущества указанного СИОЗС по сравнению с плацебо отмечены в отношении удовлетворения от полового акта (в 1,89 раза; 95% ДИ – 1,68–2,12; p<0,00001) и снижения обеспокоенности сексуальной пары в 0,72 раза (95% ДИ – 0,57–0,9; p<0,00001). Авторы пришли к выводу, что дапоксетин является достаточно эффективным и хорошо переносимым препаратом для лечения первичного и вторичного ПС. Вместе с тем было указано, что отдаленные результаты терапии и переносимости требуют дополнительной оценки [19].
В настоящий момент дапоксетин одобрен к применению в клинической практике для лечения ПС в 50 странах. Он рекомендован пациентам с ПС в возрасте от 18 до 64 лет. Применять его следует в начальной дозировке 30 мг за 1–3 ч до полового акта при максимальной регулярности применения 1 раз в сутки. В случае необходимости дозировка дапоксетина может быть увеличена до 60 мг.
Препарат противопоказан при выраженной сердечной недостаточности, нарушениях проводимости, наличии искусственного водителя ритма, тяжелой ишемической болезни сердца и заболеваниях его клапанов, а также тяжелой почечной недостаточности. Кроме того, дапоксетин не следует назначать при среднетяжелых и тяжелых формах печеночной недостаточности и пациентам, которым проводится параллельное лечение лекарствами, ингибирующими активность цитохромов-P450 и любыми психотропными препаратами. Следует также избегать его совместного применения с алкоголем [20].
В сентябре 2016 г. в России был зарегистрирован официальный генерик дапоксетина – Примаксетин®, выпускаемый в традиционных дозировках 30 и 60 мг. Осенью 2017 г., он поступил в продажу в отечественные аптечные сети, что позволяет применять его в клинической практике российским врачам-урологам [21, 22]. Препарат отпускается по рецепту врача. Оригинальный препарат дапоксетина Прилиджи® так и не успел выйти на российский рынок до окончания действия патентной защиты, при этом регистрация его состоялась в 2013 г. и действует по настоящее время.
Таким образом, в настоящий момент доказана хорошая эффективность и достаточная безопасность дапоксетина при терапии всех форм ПС. Появление его на российском рынке открывает новые перспективы в консервативном лечении многочисленных пациентов с ускоренной эякуляцией в нашей стране.



