Обоснование
Среди различных вариантов панкреатогенного сахарного диабета ([СД], диабета, обусловленного патологией поджелудочной железы) наибольшие сложности контроля гликемии возникают у пациентов после тотальной дуоденопанкреатэктомии (ТДПЭ) прежде всего в связи с наличием абсолютной недостаточности инсулина [1]. Он характеризуется гипергликемией, частыми эпизодами гипогликемии во время инсулинотерапии, редко развивается кетоацидоз [2]. В дополнение к регулированию уровня глюкозы в крови инсулин является основным анаболическим гормоном, который увеличивает синтез белка и усиливает инфильтрацию макрофагов в ранах, тем самым способствуя восстановлению тканей после операции [3].
Показания к ТДПЭ: злокачественные новообразования головки поджелудочной железы (ПЖ), невозможность проведения неопухолевых резекций R0 по краю ПЖ, невозможность выполнения панкреатического анастомоза или высокий риск развития послеоперационного панкреатического свища после резекции ПЖ (из-за местных интраоперационных условий, таких как атрофическая жировая ПЖ, или из-за тяжелого общего состояния), рецидивирующий рак ПЖ в культе ПЖ, удаление оставшейся ПЖ после операции Уиппла (панкреатическое кровотечение), мультифокальные внутрипротоковые папиллярные муциновые новообразования во всех отделах ПЖ, мультифокальные нейроэндокринные опухоли ПЖ с множественными эндокринными неоплазиями в анамнезе, наследственный рак ПЖ или семейный анамнез (это показание спорно), а также неразрешимые боли, вызванные хроническим панкреатитом или многократными приступами рецидивирующего острого панкреатита [4].
За последние 15 лет ТДПЭ стала проводиться значительно чаще благодаря усовершенствованию хирургической техники, оптимизированным анестезиологическим и реанимационным алгоритмам ведения таких пациентов в постоперационном периоде. Расширение диагностических и терапевтических возможностей за последние десятилетия значимо улучшило прогноз при злокачественных новообразованиях ПЖ, в т.ч. у пациентов после ТДПЭ, продолжительность и качество жизни которых в значительной степени зависят от контроля гликемии [5].
Сложность контроля гликемии у пациентов после ТДПЭ как в отделении реанимации и интенсивной терапии (ОРИТ), так и в стационаре хирургического отделения связана со значимыми колебаниями потребности в инсулине, что обусловлено диареей, мальабсорбцией, возможными инфекционными осложнениями, частой сменой объема парентерального питания, плохо прогнозируемым временем начала полноценного самостоятельного энтерального питания и нюансами формирования пищевых привычек [1, 6].
В настоящее время нет общепринятых протоколов инсулинотерапии и контроля гликемии у пациентов после ТДПЭ в постоперационном периоде, в связи с чем нами разработан собственный протокол. В нашей клинике в большинстве случаев до момента полного прекращения парентерального питания пациентам вводится инсулин короткого действия внутривенно с использованием перфузора. По данным ряда исследований, титрование дозы инсулина, вводимого внутривенно под ежечасным контролем гликемии, позволяет минимизировать риски гипогликемии, максимально увеличивать время в целевом диапазоне гликемии у пациентов на парентеральном питании [7]. При переводе пациента на энтеральное питание внутривенная инсулинотерапия заменялась на подкожное введение инсулина, параллельно осуществлялось обучение по структурированной программе «Школа сахарного диабета для пациентов после удаления поджелудочной железы», состоявшей из 12 разделов, включившей как общие принципы о СД, так и обучение методам инъекции инсулина, контроля гликемии, расчета хлебных единиц и подбора доз инсулина. Обучение проводилось ежедневно после перевода пациента в отделение стационара по 15–60 минут.
Системы непрерывного мониторирования гликемии (НМГ) в последние годы стали рутинно использоваться в амбулаторной практике как за рубежом, так и в России. В то же время остается открытым вопрос, какие из систем мониторинга гликемии могут рассматриваться как безопасные для использования в стационаре. Использование систем НМГ приводит к улучшению гликемического контроля и времени в целевом диапазоне по сравнению с глюкометром. Системы НМГ помогают снижать число гипогликемических событий, в т.ч. ночных, а также гипергликемических событий по сравнению с контролем глюкометром. Кроме того, при использовании НМГ тяжелые гипогликемии развивались реже, чем при контроле глюкометром. Эти результаты свидетельствуют о том, что использование систем НМГ безопасно при корректировке скорости подачи инсулина внутривенно у госпитализированных пациентов с СД [8].
В нашей клинике проведен пилотный проект по оценке безопасности использования системы НМГ Guardian Connect в стационаре и в ОРИТ. Нами выбрана данная система, прежде всего, в связи с тем, что она позволяет анализировать показатели глюкозы на экране любого компьютера (например, на рабочем месте врача, посту среднего медицинского персонала), мобильного телефона в реальном времени.
Цель исследования: оценить безопасность использования системы НМГ Guardian Connect в раннем послеоперационном периоде у пациентов после ТДПЭ на этапе внутривенной и подкожной инсулинотерапии.
Методы
Проведено одноцентровое когортное ретроспективное исследование с 06.2020 по 08.2023. Медиана срока госпитализации составила 22 дня [10; 122]. Медиана периода на внутривенной инсулинотерапии – 10 дней [2; 70]. Медиана периода на подкожной инсулинотерапии – 8 дней [2; 52]. Метод формирования групп и метод распределения пациентов: сплошная выборка (рис. 1). В исследование были включены 28 пациентов с панкреатогенным СД в исходе ТДПЭ.
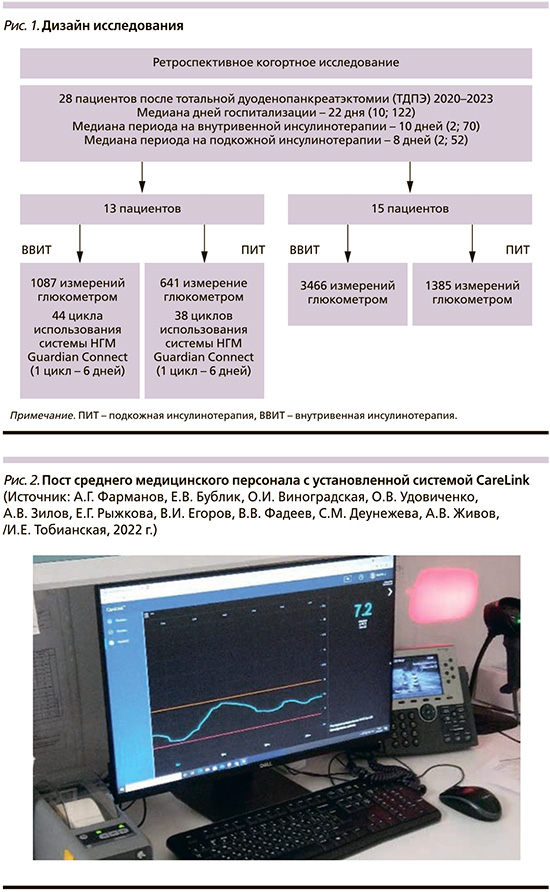
Была проведена ретроспективная оценка показателей уровня глюкозы, зарегистрированных в электронной медицинской карте пациентов после ТДПЭ в раннем послеоперационном периоде. В зависимости от метода контроля гликемии все пациенты были распределены в две группы. В группе 1 контроль показателей гликемии с использованием системы НМГ проводили 13 пациентам (параллельно с традиционным методом контроля гликемии с использованием глюкометра). В группе 2 контроль показателей гликемии провели 15 пациентам с помощью глюкометров One Touch Verio Pro+ (Lifescan, США) или Accu-Chek Performa (Roche, Швейцария).
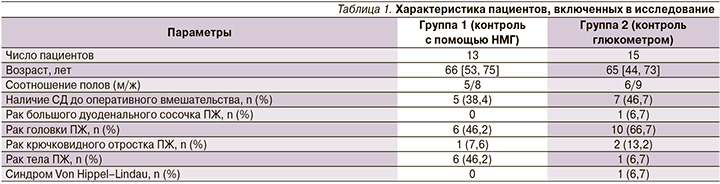
В группе 1 каждое измерение, полученное посредством глюкометра и средств НМГ, перенесли в электронную медицинскую карту пациента. Сенсор глюкозы Enlite (Medtronic International Trading Sarl.) устанавливали подкожно в область плеча или живота. После установки сенсор в течение 5 минут подключали к системе Carelink с помощью смартфона с необходимым программным обеспечением. После нескольких часов периода инициализации средний медицинский персонал проводил измерение гликемии с помощью глюкометра и вводил показания в систему НМГ для первой калибровки. После первоначальной калибровки устройство калибровали каждые 8 часов в течение всего периода работы сенсора. Смартфон располагался у постели пациента и получал от сенсора данные каждые 5 минут. Все полученные данные синхронизировались с компьютером на посту среднего медицинского персонала через систему Carelink (Medtronic International Trading Sarl.) (рис. 2). Средний медицинский персонал регистрировал в электронной медицинской карте значения глюкозы по НМГ параллельно с измерением глюкометром для калибровки у койки пациента каждый раз, когда измерение глюкометром было завершено. Сенсор использовался в течение 6 дней, после чего производилась его замена на новый сенсор.
В группе 2 пациентам проводили контроль показателей гликемии с помощью глюкометров One Touch Verio Pro+ (Lifescan, США) или Accu-Chek Performa (Roche, Швейцария). Частота контроля гликемии колебалась от 16 до 24 измерений в сутки.
В среднем частота контроля составляла 18 раз в сутки, т.к. по Алгоритмам специализированной медицинской помощи больным сахарным диабетом (11-й выпуск, 2023) при стабилизации показателей гликемии возможен контроль глюкозы крови 1 раз в 2 часа [9].
Внутривенная инсулинотерапия проводилась по алгоритму коррекции скорости инфузии инсулина, согласно клиническим рекомендациям, отраженным в Алгоритмах специализированной медицинской помощи больным сахарным диабетом (11-й выпуск, 2023) [9], однако время приостановления введения инсулина было персонифицированным.
Оценка безопасности использования методов контроля уровня глюкозы проводилась по следующим критериям:
- число гипогликемических событий;
- число тяжелых гипогликемий (потребовавших вмешательства медицинского персонала);
- число измерений в целевом диапазоне (5,7–10 ммоль/л);
- число измерений в диапазоне 4,3–11,6 ммоль/л.
Исследование было одобрено Локально-этическим комитетом Сеченовского университета от 20.01.2022, протокол № 01-22. Все необходимые документы рассмотрены и одобрены.
Сбор данных, их последующая коррекция, систематизация исходной информации и визуализация полученных результатов осуществляли в электронных таблицах Microsoft Office Excel (2016). Статистическую обработку результатов проводили средствами языка Питон (Python 3.8). Для расчетов были использованы встроенные функции из модулей Statsmodels.api и Scipy.
Количественные показатели оценивали на предмет соответствия нормальному распределению, для этого использовался критерий Шапиро–Уилка. В качестве центра распределения была посчитана медиана (Me), а в качестве показателей вариации – квартили [Q1; Q3]. Для сравнения двух несвязанных выборок использовали U-критерий Манна–Уитни.
Результаты качественных признаков выражены в абсолютных числах с указанием долей (%). Сравнение номинальных данных в группах проводили при помощи χ2-критерия Пирсона. В тех случаях, когда число ожидаемых наблюдений в любой из ячеек четырехпольной таблицы было менее 10, для оценки уровня значимости различий использовали точный критерий Фишера.
В качестве количественной меры эффекта при сравнении относительных показателей нами использовался показатель отношения шансов (ОШ). С целью проецирования полученных значений ОШ на генеральную совокупность нами рассчитывались границы 95% доверительного интервала (ДИ). Исходя из полученных данных, значимость взаимосвязи исхода и фактора считалась доказанной в случае нахождения ДИ за пределами границы отсутствия эффекта, принимаемой за 1.
В качестве количественной меры эффекта при сравнении относительных показателей использовали показатель относительного риска (ОР).
С целью проецирования полученных значений ОР на генеральную совокупность рассчитывали границы 95% ДИ. Исходя из полученных данных, значимость взаимосвязи исхода и фактора считалась доказанной в случае нахождения ДИ за пределами границы отсутствия эффекта, принимаемой за 1.
Статистически значимыми считались различия при p≤0,05.
Результаты
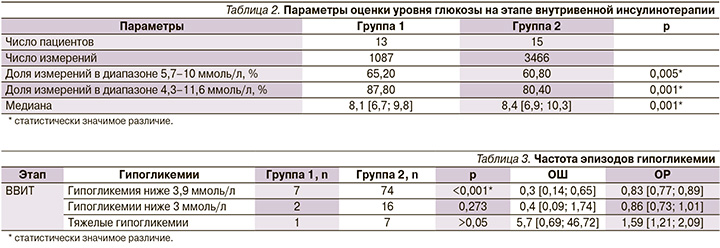
Была проведена ретроспективная оценка показателей глюкозы, зарегистрированных в электронной медицинской карте 28 пациентов после ТДПЭ в раннем послеоперационном периоде, находившихся в клинике с 2020 по 2023 г. (табл. 1).
Оценка уровня глюкозы на этапе внутривенной инсулинотерапии
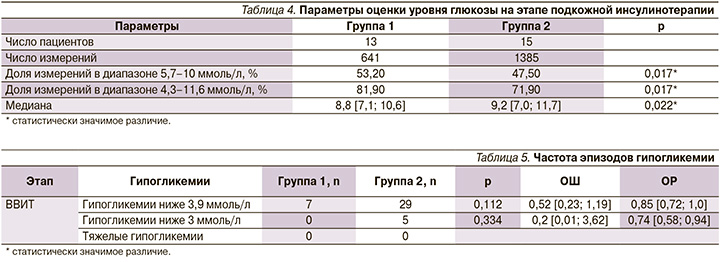
В группе 1 проанализировано 44 цикла (1 цикл – 6 дней, 44 – 270 дней) НМГ и введенные для калибровки 1087 измерений глюкометром: медиана гликемии – 8,1 [6,7; 9,8] ммоль/л. В группе 2 проанализировано 3466 измерений глюкометром: медиана гликемии – 8,4 [6,9; 10,3] ммоль/л. Медианы гликемии в группах 1 и 2 статистически значимо различались на этапе внутривенной инсулинотерапии (р<0,001).
Показатели уровня глюкозы в группе 1(использовалась система НМГ) статистически значимо чаще были в целевом диапазоне 5,6–10,0 ммоль/л (65,2 против 60,8%; р=0,005) и диапазоне от 4,3 до 11,6 ммоль/л (87,8 против 80,4%; р=0,001) по сравнению с группой 2 (контроль гликемии проводился только глюкометром) (табл. 2).
Данные параметры имели статистически значимые различия между обсуждаемыми группами, однако, на наш взгляд, полученные различия (на 4,7 и 7,4% соответственно) не имеют большого клинического значения.
Оценка частоты эпизодов гипогликемии
При оценке числа эпизодов гипогликемии ниже 3,9 ммоль/л выявлено, что риск развития данного нежелательного явления был статистически значимо ниже в группе 1 (использовалась система НМГ), чем в группе 2 (контроль уровня глюкозы проводился только глюкометром): 7 против 74 (р<0,001) ОШ=0,3 [0,14; 0,65], ОР=0,83 [0,77; 0,89]) (табл. 2).
Результаты анализа эпизодов тяжелых гипогликемий (потребовавших вмешательства медицинского персонала) показал более низкую частоту данных жизнеугрожающих состояний в группе 1, однако различия были статически незначимыми: 1 против 7 (р>0,05), ОШ=5,711 [0,698; 46,722], ОР=1,59 [1,21; 2,09]) (табл. 3).
Оценка параметров уровня глюкозы на этапе подкожной инсулинотерапии
В группе 1 проанализированы 38 циклов (1 цикл – 6 дней, 38 циклов – 228 дней) НМГ и вводимые для калибровки 641 измерение глюкометром: медиана показателей глюкозы – 8,8 [7,1; 10,6] ммоль/л, в группе 2 проанализировано 1385 измерений глюкометра: медиана показателей глюкозы – 9,2 [7,0; 11,7] ммоль/л. Медианы показателей глюкозы в группах 1 и 2 статистически значимо различались на этапе подкожной инсулинотерапии (р=0,022).
Показатели уровня глюкозы в группе 1 (использовалась система НМГ) статистически значимо чаще были в целевом диапазоне 5,6–10,0 ммоль/л (53,2 против 47,5%; р=0,017) и диапазоне от 4,3 до 11,6 ммоль/л (81,9 против 71,9%; р=0,017) по сравнению с группой 2 (контроль гликемии проводился только глюкометром) (табл. 4).
Оценка частоты эпизодов гипогликемии
При оценке числа эпизодов гипогликемии ниже 3,9 ммоль/л не было выявлено статистически значимых различий между группами: 7 против 29 (р=0,112) ОШ=0,52 [0,23; 1,19], ОР=0,85 [0,72; 1,0]) (табл. 5).
Эпизодов тяжелых гипогликемий (потребовавших вмешательства медицинского персонала) в обеих группах выявлено не было.
Обсуждение
Представленные результаты исследования в условиях реальной клинической практики пациентов после ТДПЭ показывают, что использование системы НМГ в раннем послеоперационном периоде на этапе внутривенной и подкожной инсулинотерапии может повышать безопасность проводимой инсулинотерапии.
Анализ данных также показал, что данная система НМГ может вносить клинически значимый вклад в снижение частоты эпизодов гипогликемии на этапе внутривенной инсулинотерапии в данной группе пациентов.
К настоящему времени исследований, изучающих возможность использования систем НМГ в отношении пациентов после ТДПЭ в послеоперационном периоде, не проводилось. В аналогичных работах, в которых исследовали безопасность использования систем НМГ в стационаре, не оценивали влияния способа введения инсулина на выбор метода контроля гликемии [8, 10].
Ранее проводили исследования, в которых оценивали возможность использования систем НМГ в стационаре и ОРИТ, где показано, что системы НМГ обладают достаточной точностью и могут быть эффективными в снижении частоты эпизодов гипогликемии у госпитализированных пациентов, улучшают время в целевом диапазоне гликемии, а также помогают снижать нагрузку на медсестер, дополнительно снижая стоимость стационарного ухода как для больницы, так и для пациента [10, 11].
Ограничения исследования
1. Одноцентровый и ретроспективный характер исследования.
2. Отсутствие рандомизации пациентов по выбору метода контроля гликемии.
3. Выбор пациентов, которым контроль проводился с помощью систем НМГ, определялся исходя из наличия в клинике на момент госпитализации пациента сенсоров Enlite.
4. Отсутствие полноценной оценки показателя «время в целевом диапазоне» в группе 2 в связи с тем, что измерения проводились не ежечасно.
5. Использование двух видов глюкометров могло вводить к систематической ошибке.
Заключение
Использование системы НМГ Guardian Connect является безопасным методом контроля уровня глюкозы в раннем послеоперационном периоде у пациентов после ТДПЭ.
Вклад авторов. Авторы подтверждают, что каждый представленный в рукописи графический объект и таблицы являются авторскими и не заимствованы из других источников. Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Выражение признательности. Хотим выразить благодарность всему среднему медицинскому персоналу Ильинской больницы в лице старшей медицинской сестры Васянкиной Ядвиги Сергеевны и старшего медицинского брата Глотова Сергея Валерьевича за осуществление скоординированной клинической работы в ходе проводимого исследования; специалисту по медицинской статистике Щепкиной Елене Викторовне за помощь c систематизацией исходной информации и визуализацию полученных результатов; генеральному директору Ильинской больницы Гапееву Артему Борисовичу за всестороннюю поддержку всех научных проектов Ильинской больницы.



