Главной предотвратимой причиной преждевременной смерти в экономически развитых странах мира является артериальная гипертензия (АГ). Улучшение прогноза, в частности снижение смертности, является конечной целью антигипертензивной терапии. Поэтому в действующих Рекомендациях РМОАГ/ВНОК [1] и новых Рекомендациях ESH/ESC [2] по лечению АГ предпочтение отдается пяти классам антигипертензивных препаратов, которые вместе со снижением артериального давления (АД) способны уменьшать риск развития сердечно-сосудистых осложнений (ССО). Это ингибиторы ангиотензинпревращающего фермента (АПФ), блокаторы рецепторов ангиотензина II — АТII (БРА), антагонисты кальция, диуретики и β-адреноблокаторы.
Гиперактивация ренин-ангиотензин-альдостероновой системы (РААС) является одним из главных механизмов развития АГ и, соответственно, — мишенью антигипертензивной терапии. С целью ингибирования РААС у больных АГ более 30 лет применяют ингибиторы АПФ, с середины 90-х годов XX века — БРА II, в течение нескольких лет — прямой ингибитор ренина [3]. Антагонист альдостерона может дополнительно назначаться при рефрактерной/резистентной АГ [1, 2]. Ряд исследований отдельных ингибиторов РААС у больных АГ не обладали достаточной статистической мощностью для определения их влияния на смертность. Недавние мета-анализы рандомизированных контролируемых исследований эффективности ингибиторов АПФ и БРА II выявили существенные различия по влиянию такой антигипертензивной терапии на общую и сердечно-сосудистую смертность (ССС) пациентов.
В наиболее крупном из них объединены результаты 158 998 наблюдений из 20 исследований с оценкой сердечно-сосудистой заболеваемости и смертности [4]. В каждом включенном проекте минимум у 2/3 пациентов имелся диагноз АГ; они были рандомизированы для лечения ингибиторами РААС (n=71 401) или иной терапии (n=87 597; контроль). Прием ингибиторов РААС сопровождался снижением общей смертности на 5% (относительный риск — ОР 0,95 при 95% доверительном интервале — ДИ от 0,91 до 1,00; р=0,032) и уменьшением ССС на 7% (ОР 0,93 при 95% ДИ от 0,88 до 0,99; р=0,018). Наблюдаемый эффект лечения полностью обеспечивался ингибиторами АПФ, которые снижали смертность от всех причин на 10% (ОР 0,90 при 95% ДИ от 0,84 до 0,97; р=0,004), тогда как прием БРА II не влиял на смертность (ОР 0,99 при 95% ДИ от 0,94 до 1,04; р=0,683). Различие в действии ингибиторов АПФ и БРА II на общую смертность оказалось статистически значимым (р=0,036 для гетерогенности). Подобным образом терапия ингибиторами РААС в целом также значительно снижала ССС на 7% (ОР 0,93 при 95% ДИ от 0,88 до 0,99; р=0,018). При этом БРА II не влияли на ССС (ОР 0,96 при 95% ДИ от 0,90 до 1,01; р=0,14), а применение ингибиторов АПФ сопровождалось отчетливой тенденцией к снижению этого показателя на 12% (ОР 0,88 при 95% ДИ от 0,77 до 1,00; р=0,051).
Ранее о различии между ингибиторами АПФ и БРА II во влиянии на смертность сообщили М. Strauss и А. Hall [5]. В мета-анализе 11 рандомизированных контролируемых исследований у 55 050 пациентов, перенесших инфаркт миокарда (ИМ), БРА II по сравнению с активной терапией или плацебо повышали риск развития ИМ на 8% (ОР 1,08 при 95% ДИ от 1,01 до 1,16; р=0,03) и не влияли на общую смертность (ОР 1,01 при 95% ДИ от 0,96 до 1,06; р=0,80). В то же время у 150 943 подобных пациентов в 42 исследованиях ингибиторы АПФ снижали смертность от всех причин на 9% (ОР 0,91 при 95% ДИ от 0,86 до 0,95), ССС — на 12% (ОР 0,88 при 95% ДИ от 0,82 до 0,95) и риск развития ИМ — на 14% (ОР 0,86 при 95% ДИ от 0,82 до 0,90) при сравнении с плацебо или активным лечением, включая БРА II (все р<0,001).
В дальнейшем S. Bangalore и соавт. [6] в систематическом обзоре 37 исследований БРА II, включавшем 147 020 пациентов с АГ, сердечной недостаточностью (СН), инсультом, ИМ, ишемической болезнью сердца или впервые выявленным сахарным диабетом (СД), снова отмечали отсутствие снижения общей смертности (ОР 1,00 при 95% ДИ от 0,97 до 1,02; р=0,75) и ССС (ОР 0,99 при 95% ДИ от 0,94 до 1,04; р=0,73) по сравнению с контрольной группой.
Наконец, мета-анализ G. Savarese и соавт. [7] объединил результаты 26 рандомизированных исследований, сравнивавших ингибиторы АПФ или БРА II с плацебо у 108 212 пациентов с высоким риском развития осложнений, но без СН. И в этот раз только ингибиторы АПФ снижали общую смертность на 9% (ОР 0,91 при 95% ДИ от 0,85 до 0,98; р=0,008).
Общепринято, что ингибиторы АПФ и БРА II объединяют несколько клинических эффектов: снижение АД и риска развития инсульта, уменьшение симптомов хронической СН [8]. В последние годы отмечается сближение показаний к применению препаратов этих двух классов при лечении сердечно-сосудистых заболеваний (ССЗ). При этом имеется немного рандомизированных сравнительных исследований по данной проблеме у больных с повышенным АД. Более того, необходимо признать, что ингибиторы АПФ и БРА II сходны лишь на первый взгляд.
В 2 рандомизированных контролируемых проектах проспективно сопоставляли ингибиторы АПФ и БРА II: рамиприл и телмисартан — в крупнейшем проекте ONTARGET (у пациентов с высоким риском развития ССО) [9], эналаприл и телмисартан — в небольшом исследовании DETAIL (у больных с диабетической нефропатией) [10]. Основные результаты сравнивавшейся (реально комбинированной) терапии не различались, хотя средний уровень систолического АД в группах приема телмисартана оказался на 4,0 и 1,0 мм рт.ст. ниже, чем при лечении рамиприлом или эналаприлом соответственно. Следует отметить, что в обоих случаях длительно действующий БРА II противопоставлялся коротко действующим ингибиторам АПФ, назначавшимся один раз в день утром.
Не только в ONTARGET и DETAIL, но и в других исследованиях значительное снижение АД с помощью БРА II не приводило к уменьшению риска развития ССО и смертности. Так, различие систолического АД 4,0 мм рт.ст. в TRANSCEND [11] и 3,8 мм рт.ст. в PRoFESS [12] не позволяло телмисартану улучшить прогноз у пациентов с АГ по сравнению с плацебо. В нескольких мета-анализах также показано, что снижение АД с помощью БРА II, независимо от препарата сравнения, не уменьшало риск развития ИМ [13—15]. Напротив, по данным мета-анализа 26 рандомизированных контролируемых исследований с участием 146 838 пациентов с АГ [16], при исключении влияния снижения АД ингибиторы АПФ уменьшали риск развития ишемической болезни сердца на 9%, а БРА II повышали его на 8%, и различие между двумя классами препаратов оказалось достоверным (р=0,002).
Эти данные обусловливают необходимость анализа различий по эффектам ингибиторов АПФ и БРА II, не зависящих от снижения АД, таких как уменьшение окислительного стресса и дисфункции эндотелия, улучшение метаболизма глюкозы, влияние на атеросклеротическую бляшку [17]. Кроме того, необходимо понимание особенностей действия ингибиторов АПФ и БРА II на РААС, что в итоге позволит объяснить различия их влияния на смертность.
Ингибиторы АПФ подавляют превращение ангиотензина I в АТII — мощный вазоконстриктор, оказывающий в высокой концентрации многочисленные негативные эффекты [18] (увеличение окислительного стресса и снижение биодоступности оксида азота с активацией апоптоза эндотелия, ремоделирование сосудов, повышение артериальной жесткости, ускорение развития атеросклероза). АТII является ключевым медиатором поражения органов-мишеней при АГ. В сердце он вызывает гипертрофию миокарда, сужение коронарных артерий и удлинение интервала QT на электрокардиограмме, в головном мозге — повышение активности симпатической части вегетативной нервной системы, воспаление и ухудшение мозгового кровообращения, в почках — увеличение продукции ренина, нефропатию, альбуминурию и фиброз. АТII также повышает секрецию альдостерона, что увеличивает реабсорбцию натрия, задержку воды, повышает объем циркулирующей крови и АД. Поражение органовмишеней может привести к развитию ИМ, инсульта, СН и почечной недостаточности.
Угнетение образования АТII с помощью ингибиторов АПФ способствует улучшению функции эндотелия, снижению уровней маркеров воспаления и тромбообразования, замедлению атерогенеза [18].
Хотя ингибиторы АПФ уменьшают образование АТII, с течением времени его концентрация и уровень альдостерона повышаются вследствие образования через иные механизмы (химазный путь и др.) [19]. Важной особенностью действия ингибиторов АПФ является торможение распада и повышение уровня брадикинина (механизм возникновения сухого кашля у некоторых больных), который угнетает РААС, способствует освобождению оксида азота и дилатации артерий, снижает АД и оказывает кардиопротективный эффект, предотвращает апоптоз [17].
 БРА II также ослабляют отрицательные сердечно-сосудистые эффекты АТII, но это происходит вследствие селективной блокады АТ1-рецепторов [20]. В результате уменьшаются вазоконстрикция, симпатическая стимуляция, окислительный стресс, высвобождение воспалительных факторов и альдостерона. Преимуществом БРА II является не ослабевающее со временем предупреждение действия АТII на АТ1-рецепторы. Между тем селективность блокады АТ1-рецепторов может иметь негативные последствия, поскольку приводит к компенсаторному увеличению образования АТII, но не препятствует его действию на другие рецепторы (AT2, AT3 и AT4), что приводит к разнонаправленным клиническим эффектам. Активация АТ2-рецепторов способна приводить к дестабилизации атеросклеротической бляшки, индуцированной матриксной металлопротеиназой-1, и разрыву покрышки бляшки с образованием тромба [5]. Стимуляция АТ2-рецепторов также способствует гипертрофии, усилению воспаления и апоптоза, повышению концентрации альдостерона [21], но также вазодилатации и уменьшению пролиферации. Эффект стимуляции АТ3рецепторов во многом неясен. Известно, что активация АТ4-рецепторов ведет к тромбозу [20]. Совокупность этих процессов с трудно прогнозируемым итогом помогает объяснить различия в действии ингибиторов АПФ и БРА II на общую смертность и ССС.
БРА II также ослабляют отрицательные сердечно-сосудистые эффекты АТII, но это происходит вследствие селективной блокады АТ1-рецепторов [20]. В результате уменьшаются вазоконстрикция, симпатическая стимуляция, окислительный стресс, высвобождение воспалительных факторов и альдостерона. Преимуществом БРА II является не ослабевающее со временем предупреждение действия АТII на АТ1-рецепторы. Между тем селективность блокады АТ1-рецепторов может иметь негативные последствия, поскольку приводит к компенсаторному увеличению образования АТII, но не препятствует его действию на другие рецепторы (AT2, AT3 и AT4), что приводит к разнонаправленным клиническим эффектам. Активация АТ2-рецепторов способна приводить к дестабилизации атеросклеротической бляшки, индуцированной матриксной металлопротеиназой-1, и разрыву покрышки бляшки с образованием тромба [5]. Стимуляция АТ2-рецепторов также способствует гипертрофии, усилению воспаления и апоптоза, повышению концентрации альдостерона [21], но также вазодилатации и уменьшению пролиферации. Эффект стимуляции АТ3рецепторов во многом неясен. Известно, что активация АТ4-рецепторов ведет к тромбозу [20]. Совокупность этих процессов с трудно прогнозируемым итогом помогает объяснить различия в действии ингибиторов АПФ и БРА II на общую смертность и ССС.
Усилия ряда фармацевтических компаний, активная промоционная деятельность нацелены на преимущественное назначение врачами БРА II вместо ингибиторов АПФ. Однако крупные клинические исследования, предназначенные для демонстрации протективных эффектов БРА II, в основном по сравнению с плацебо в дополнение к обычному лечению, не смогли показать дополнительную защиту сердечно-сосудистой системы и выявили более тяжелое поражение почек.
Исследование LIFE — единственный крупный проект, который установил превосходство БРА II над другой антигипертензивной терапией в профилактике ССО у пациентов с АГ или высоким риском развития ССО [22]. Тем не менее его выводы малоубедительны, поскольку атенолол является недостаточно эффективным препаратом сравнения [23], и пациенты в группе лозартана чаще получали диуретики [24]. Ретроспективно полученные данные о снижении риска возникновения фибрилляции предсердий в группе лечения лозартаном [25] не удалось подтвердить в четырех специально организованных проспективных исследованиях БРА II GISSI-AF [26], ACTIVE I [27], ANTIPAF [28] и J-RHYTHM II [29].
Данные одного из мета-анализов [6] о том, что БРА II не увеличивают риск развития ИМ по сравнению с плацебо (ОР 0,93 при 95% ДИ от 0,81 до 1,07), предлагается рассматривать в качестве преимущества класса препаратов, претендующего на роль предотвращающего ССО.
В современных клинических исследованиях, оценивающих сердечно-сосудистые исходы, неэтично сравнивать антигипертензивные препараты с плацебо, так как вся или бо'льшая часть их эффективности является производным от снижения АД [2]. С использованием БРА II такие исследования продолжали проводить, но они не приносили желаемых результатов.
В проекте SCOPE у 4964 пожилых пациентов суммарная частота случаев сердечно-сосудистой смерти, нефатального инсульта и нефатального ИМ составляла 26,7 на 1000 человеко-лет у получавших кандесартан и 30,0 на 1000 человеко-лет у принимавших плацебо (р=0,19) [30].
В исследование TRANSCEND включили 5926 пациентов с ССЗ или СД с поражением органов-мишеней, которые не переносили ингибиторы АПФ. Сердечнососудистая смерть, ИМ, инсульт или госпитализация по поводу СН регистрировались в 15,7% случаев при лечении телмисартаном по сравнению с 17% в группе плацебо (р=0,22) [12].
Телмисартан сравнивался с плацебо в исследовании вторичной профилактики инсульта PROFESS, в котором участвовали 20 332 пациентов. Повторный инсульт развивался в 8,7% случаев в группе телмисартана и в 9,2% — на плацебо (р=0,23) [11].
В исследовании NAVIGATOR изучали эффективность валсартана для предотвращения различных сердечнососудистых исходов и СД у 9306 пациентов с нарушенной толерантностью к глюкозе и ССЗ или факторами риска. Частота основных сердечно-сосудистых исходов оказалась одинаковой у пациентов, получавших валсартан или плацебо, — по 8,1% (р=0,85) [31].
В исследовании ACTIVE I суммарная частота развития инсульта, ИМ или смерти от сосудистых причин также была одинаковой (по 5,4%; р=0,85) у 9016 пациентов с фибрилляцией предсердий, получавших ирбесартан или плацебо [27].
Медицинская общественность обычно с оптимизмом встречает новые лекарственные препараты, тем более относящиеся к наиболее широко распространенным классам. Олмесартан — одно из таких новшеств. В рандомизированном двойном слепом исследовании ROADMAP участвовали 4447 пациентов с СД 2-го типа, в дополнение к стандартной терапии получавшие олмесартан в дозе 40 мг 1 раз в день или плацебо в течение в среднем 3,2 года [32]. В группе лечения БРА II офисное АД поддерживалось на 3,1/1,9 мм рт.ст. ниже, а время до первого появления микроальбуминурии («первичная конечная точка») увеличивалось на 23% (ОР 0,77 при 95% ДИ от 0,63 до 0,94; р=0,01). Неожиданно большее число фатальных сердечно-сосудистых исходов зарегистрировано в группе олмесартана (15 против 3 на плацебо; р=0,01), что вызвало естественную озабоченность, но не исключало случайность. В этой связи представляли интерес результаты исследования ORIENT, в котором 577 больных СД 2-го типа с явной протеинурией после рандомизации дополнительно получали олмесартан (10—40 мг/сут) или плацебо в среднем 3,2 года. Несмотря на значительное снижение АД и уменьшение протеинурии, ССС также была выше в группе олмесартана (10 случаев против 3 в группе плацебо; р=0,09) [33]. Этот пример наглядно демонстрирует возможность несоответствия между позитивным результатом лечения в отношении важной суррогатной «конечной точки» и негативным влиянием на смертность.
Вызывает беспокойство и сообщение о редком, но тяжелом побочном эффекте олмесартана — энтеропатии типа спру, обусловленной, по данным гистологического исследования, воспалением и атрофией ворсинок кишечника. Стойкая диарея сопровождалась снижением массы тела в среднем на 18 (от 2,5 до 57) кг, в 2/3 случаев обусловливала необходимость госпитализации и проходила только после отмены олмесартана [34]. По требованию Управления по контролю за качеством пищевых продуктов и лекарственных препаратов США этот неблагоприятный эффект внесен в инструкцию к препарату.
В течение нескольких лет ярким примером эффективности БРА II служили результаты двух японских исследований валсартана. В Jikei Heart Study 3081 пациенту, получавшему обычное лечение АГ, ишемической болезни сердца, СН или сочетания этих заболеваний, назначали валсартан (40—160 мг/сут) или другую терапию без БРА II. При равном АД в группах в течение в среднем 3,1 года наблюдалось значительное суммарное снижение сердечно-сосудистой заболеваемости и смертности в группе валсартана (ОР 0,61 при 95% ДИ от 0,47 до 0,79; р=0,0002) [35]. В Kyoto Heart Study 3031 пациента с неконтролируемой АГ рандомизировали для дополнительного приема валсартана или другого лечения (не БРА II). В среднем 3,3 года АД строго поддерживалось на одном уровне в двух группах, но валсартан выраженно снижал общую частоту фатальных и нефатальных ССО (ОР 0,55 при 95% ДИ от 0,42 до 0,72; р=0,00001) [36]. Предполагали, что эти необычные результаты связаны с особой чувствительностью японцев к БРА II. Затем появились обоснованные сомнения в их реальности [37]. Наконец, редакция European Heart Journal сообщила об исключении публикации 2009 г., не рекомендовала делать ссылки на эту статью [38] по причине преднамеренного искажения представленных в ней данных.
Заслуживают доверия результаты исследования VALUE, в котором не выявлено различий по суммарной частоте развития ССО у 15 245 пациентов с АГ, получавших валсартан или амлодипин (р=0,49). Частота развития смертельного и несмертельного ИМ (заранее определенная «вторичная конечная точка») оказалась выше у пациентов, получавших валсартан (р=0,02) [39].
Определенные надежды связывались с блокатором РААС, обладающим принципиально новым механизмом действия, — прямым ингибитором ренина алискиреном. В двойном слепом исследовании ALTITUDE 8561 пациент c СД 2-го типа после рандомизации получал алискирен (300 мг/сут) или плацебо в качестве дополнения к терапии ингибиторами АПФ или БРА II. Проект был остановлен досрочно при среднем периоде наблюдения 33 мес, когда исходы, включенные в «первичную конечную точку» (суммарная частота развития ССО и почечных осложнений), произошли у 18,3 и 17,1% больных в группе алискирена и плацебо соответственно (ОР 1,08 при 95% ДИ от 0,98 до 1,20; р=0,12). Прием алискирена чаще сопровождался выраженной гиперкалиемией и гипотензией, был признан потенциально вредным для такого контингента пациентов [40].
Не противоречит этим результатам сообщение J. Mihai и соавт. [41], которые отмечали уcкорение прогрессирования атеросклероза аорты по данным трехмерной магнитно-резонансной томографии при приеме алискирена в течение 36 нед по сравнению с плацебо.
Еще одно разочарование принесло сообщение об итогах исследования ASTRONAUT, в котором добавление алискирена к стандартной терапии систолической СН не снижало суммарную частоту смертельных исходов и госпитализаций, одновременно повышая риск развития гиперкалиемии, гипотензии и почечной недостаточности по сравнению с плацебо [42].
 Оценка вклада отдельных представителей класса ингибиторов АПФ в снижение общей смертности и ССС больных АГ показала существенное влияние периндоприла на результаты мета-анализа [4]. В исследованиях с использованием периндоприла наблюдалось наибольшее снижение смертности от всех причин (–13%; ОР 0,87 при 95% ДИ от 0,81 до 0,93; р<0,001). В 3 крупных проектах по оценке периндоприла (ASCOT-BPLA, ADVANCE и HYVET), включавших 34 242 пациентов с АГ, достигалось снижение ССС на 22% (ОР 0,78 при 95% ДИ от 0,70 до 0,87; р<0,001) [43—45], тогда как в 4 исследованиях других ингибиторов АПФ у 42 373 пациентов этого не отмечалось (ОР 1,02 при 95% ДИ от 0,92 до 1,11; р=0,75) [46—49].
Оценка вклада отдельных представителей класса ингибиторов АПФ в снижение общей смертности и ССС больных АГ показала существенное влияние периндоприла на результаты мета-анализа [4]. В исследованиях с использованием периндоприла наблюдалось наибольшее снижение смертности от всех причин (–13%; ОР 0,87 при 95% ДИ от 0,81 до 0,93; р<0,001). В 3 крупных проектах по оценке периндоприла (ASCOT-BPLA, ADVANCE и HYVET), включавших 34 242 пациентов с АГ, достигалось снижение ССС на 22% (ОР 0,78 при 95% ДИ от 0,70 до 0,87; р<0,001) [43—45], тогда как в 4 исследованиях других ингибиторов АПФ у 42 373 пациентов этого не отмечалось (ОР 1,02 при 95% ДИ от 0,92 до 1,11; р=0,75) [46—49].
Периндоприл отличается большой продолжительностью антигипертензивного действия (через 24 ч после приема сохраняется 75—100% пикового эффекта), выраженным снижением центрального давления в аорте, вариабельности АД и его ночного уровня. Этому ингибитору АПФ присуща высокая липофильность, обеспечивающая проникновение в ткани, с длительным ингибированием локальных РААС. Периндоприл восстанавливает сниженный уровень брадикинина, что приводит к улучшению функции и уменьшению апоптоза эндотелия, неоваскуляризации, снижению артериальной жесткости и регрессии атеросклероза [50].
В новых Рекомендациях ESH/ESC по лечению АГ [2] подтверждается известное положение о том, что монотерапия обеспечивает достижение целевого АД у меньшего числа пациентов с АГ, а большинство из них нуждаются в комбинации минимум 2 антигипертензивных средств. Рациональное сочетание препаратов не только более эффективно снижает АД, но и вызывает меньше побочных эффектов. В отсутствие достижения целевого уровня АД на фоне применения двойной комбинации лекарственных средств их дозы могут быть увеличены [2].
Проведено лишь одно крупное рандомизированное исследование, с самого начала которого назначались двойные комбинации антигипертензивных препаратов, и одна из них превзошла другую во влиянии на прогноз, несмотря на сходное снижение АД. В проекте ACCOMPLISH у 11 506 больных АГ терапия беназеприлом и амлодипином по сравнению с лечением беназеприлом и гидрохлоротиазидом сопровождалась снижением риска развития суммы осложнений (сердечно-сосудистая смерть, нефатальный ИМ, нефатальный инсульт, госпитализация по поводу стенокардии, реанимация при остановке сердца и коронарная реваскуляризация) на 20% (ОР 0,80 при 95% ДИ от 0,72 до 0,90; р<0,001) [51]. По мнению экспертов, этот неожиданный результат требует повторения, поскольку терапия, основанная на антагонисте кальция, никогда ранее не превосходила терапию, основанную на диуретике [2].
Не следует назначать терапию двумя различными блокаторами РААС. Сочетание ингибитора АПФ с БРА II [9] и алискирена с ингибитором АПФ или БРА II [40] сопровождается значительным повышением частоты развития хронической почечной недостаточности. Эти данные также не соответствовали ожиданиям, поскольку ингибиторы АПФ и БРА II признаются нефропротекторами. В то же время в исследовании ROADMAP [32] у пациентов, получавших олмесартан, несмотря на уменьшение частоты развития микроальбуминурии, отмечалось ускоренное снижение скорости клубочковой фильтрации. В проекте ACTIVE I [27] частота нарушений функции почек, ведущих к отмене препарата, наблюдалась почти в 2 раза чаще у больных, получавших ирбесартан (0,95%), по сравнению с плацебо (0,53%). В исследовании TRANSCEND [52] снижение скорости клубочковой фильтрации в группе телмисартана оказалось более выраженным, чем в группе плацебо (р<0,001).
В 2 хорошо известных исследованиях антигипертензивная терапия периндоприлом и индапамидом снижала общую смертность больных АГ: в исследовании ADVANCE у больных СД 2-го типа на 14% (p=0,03) [44] и в исследовании HYVET у пациентов старше 80 лет на 21% (р=0,02) [45]. Недавно была изучена фиксированная полнодозовая комбинация периндоприла аргинина 10 мг и индапамида 2,5 мг — нолипрел А би-форте.
В программе FALCO FORTE участвовали 2327 пациентов, получавших неэффективное лечение АГ (69%), плохо переносивших терапию (4%) или с впервые диагностированной АГ (27%). У отдельных больных потребовалось применение наибольших доз периндоприла/ индапамида (нолипрел А би-форте). Через 3 мес целевое АД достигалось в 87% случаев. Лечение хорошо переносилось и не вызывало существенных изменений лабораторных показателей, качество жизни значительно улучшалось [53].
В открытом наблюдательном проекте PICASSO фиксированная комбинация периндоприл 10 мг/индапамид 2,5 мг назначалась 9257 пациентам с АГ, неэффективно леченной в повседневной медицинской практике. В течение 3 мес среднее АД снижалось со 159/93 до 132/80 мм рт.ст. (р<0,001), частота сердечных сокращений — с 79 до 73 уд/мин (р<0,001). Целевое АД регистрировалось у 72,7% больных. Наблюдались позитивные изменения ряда метаболических показателей [54].
Крупное исследование нолипрела А би-форте ФОРТИССИМО проведено в России у 2120 больных с плохо контролируемой АГ. Через 3 мес АД в среднем снижалось со 171/99 до 130/80 мм рт.ст. (до 149/89 мм рт.ст. уже через 2 нед лечения) и достигало целевого уровня у 84% пациентов. Отмечалось повышение приверженности больных к лечению. Фиксированная комбинация периндоприла и индапамида хорошо переносилась и оказалась эффективной в контроле АД независимо от проводимой ранее терапии [55].
Нами выполнено небольшое открытое проспективное исследование нолипрела А би-форте у 46 пациентов с АГ, не контролируемой при лечении фиксированными комбинациями ингибитора АПФ или БРА II с гидрохлоротиазидом, и гипертрофией левого желудочка. Некоторые клинические и демографические показатели больных приведены в табл. 1.
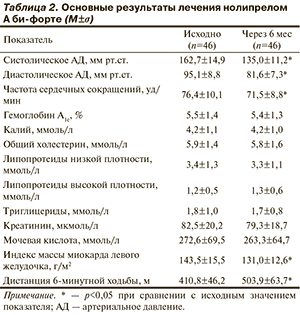
После отмены антигипертензивной терапии назначалось лечение нолипрелом А би-форте, контролировавшееся в течение 6 мес. Исходно и в конце наблюдения регистрировались офисное АД и частота сердечных сокращений, проводились биохимическое исследование крови, ультразвуковое исследование сердца, тест с 6-минутной ходьбой. Основные результаты исследования представлены в табл. 2.
Целевое систолическое АД (ниже 140 мм рт.ст.) достигалось у 40 (87%) больных с ранее неконтролируемой АГ. Изменения параметров гемодинамики соответствовали результатам ранее проведенных исследований [53—55]. Мы констатировали метаболическую нейтральность нолипрела А би-форте, но полагаем, что существенное улучшение показателей углеводного и липидного обмена препарат может вызывать при его назначении вместо терапии с негативным влиянием на метаболизм (β-адреноблокаторы, хлорталидон, высокие дозы гидрохлоротиазида). Необходимо отметить значительный регресс гипертрофии левого желудочка и улучшение функционального статуса пациентов, достигавшиеся через 6 мес лечения нолипрелом А би-форте.
Результаты крупных клинических исследований БРА II и алискирена показали, что они не снижают риск развития ССО и смертность при широком спектре клинических состояний, способны оказывать негативное влияние на функцию почек. Эти результаты не согласуются с действующими рекомендациями, поэтому роль БРА II в профилактике ССО и почечных осложнений нуждается в переоценке. Различия во влиянии на смертность больных с АГ свидетельствуют о том, что ингибиторам АПФ, в частности периндоприлу, следует отдавать предпочтение, а назначение БРА II должно быть ограничено пациентам с непереносимостью ингибиторов АПФ. Фиксированная комбинация периндоприл 10 мг/индапамид 2,5 мг обеспечивает достижение целевого АД у больных с неконтролируемой АГ, обладает хорошей переносимостью, метаболической нейтральностью, высокими органопротективными свойствами и доказанной способностью улучшать прогноз пациентов.



