Миома матки является не только медицинской, но и социальной проблемой на современном этапе развития медицины и общества. Данные визуализирующих методик свидетельствуют о распространении данной патологии среди 80% женщин, в том числе женщин детородного возраста – до 35% [1, 2]. В настоящее время предпочтение отдается органосохраняющим оперативным вмешательствам, ведущие позиции среди которых занимает лапароскопическая консервативная миомэктомия [3, 4]. Сокращение объема хирургической агрессии уменьшает количество периоперационных осложнений, но не исключает их полностью [3–6].
Трудноразрешимой задачей периоперационного периода является коррекция анемического синдрома на фоне рецидивирующих менометроррагий, а риск клинически значимой интраоперационной кровопотери делает эту проблему еще более актуальной и требует комплексного подхода для ее решения, включая использование гемостатической терапии, в частности ингибиторов фибринолиза [7–10]. Одновременно необходимо обязательное решение вопроса профилактики венозно-тромбоэмболических осложнений (ВТЭО), частота которых при гинекологических вмешательствах колеблется от 0,98 до 5,3% [11–14], а при использовании активного диагностического поиска с использованием ультразвукового скрининга и/или теста с поглощением фибриногена возрастает до 5,1–12% [12]. Кроме того, длительность операции при множественной миоме матки, как правило, превышает 45 минут [15], что, согласно стратификации риска по шкале J. Caprini, значительно увеличивает риск развития ВТЭО. У части пациенток ВТЭО не проявляются клинически в ближайшем послеоперационном периоде, но могут манифестировать после выписки из стационара [12, 14]. Истинная частота ВТЭО после органосохраняющих лапароскопических операций на матке остается неуточненной. Не до конца ясны и механизмы развития этих осложнений. Достаточно информативным является исследование гемостаза с помощью тромбоэластографии, в том числе при операциях гинекологического профиля [16]. Количество исследований изменений показателей гемостаза при малоинвазивных гинекологических вмешательствах ограничено.
Таким образом, вопросы динамического контроля системы гемостаза как для уменьшения объема интраоперационной кровопотери, так и для профилактики ВТЭО у пациенток с миомой матки являются актуальными и требуют оптимизации лечебно-диагностических и профилактических мероприятий.
Цель исследования: оценить динамику изменений в системе гемостаза и определить наличие или отсутствие наклонности к тромбообразованию при профилактическом применении транексамовой кислоты во время консервативной лапароскопической миомэктомии.
Материалы и методы
В исследование были включены 33 пациентки гинекологического отделения НИИКЭЛ – филиал ИЦиГ СО РАН с симптомной множественной миомой матки и железодефицитной анемией с подтвержденным на амбулаторном этапе дефицитом железа, и плановым хирургическим лечением в объеме лапароскопической консервативной миомэктомии. Критерии включения: показатели гемоглобина от 90 до 105 г/л, отсутствие личного и семейного анамнеза ВТЭО; оценка риска ВТЭО по шкале J. Caprini не более 2 баллов (низкий риск); степень анестезиологического риска не более II по шкале Аmerican Society of Anesthesiologists (АSA).
Всем пациенткам проведены динамический контроль общего анализа крови (ОАК) и комплексный динамический анализ изменений свертывающей системы с оценкой изменений показателей как тромбоэластограммы (ТЭГ), так и базовых показателей коагулограммы: активированного частичного тромбопластинового времени (АЧТВ), протромбинового индекса (ПТИ), содержания фибриногена, D-димера и растворимых фибрин-мономерных комплексов (РФМК).
Исследование коагулограммы проводилось на автоматическом коагулометре ACL Elit Pro с использованием реактивов фирмы HemosIL. Клотинговыми методами определяли АЧТВ, ПТИ, турбидиметрическим методом – фибриноген, иммунологическим методом – D-димер. С использованием реактивов фирмы «Технология-стандарт» проводили определение РФМК орто-фенантролиновым тестом. Исследование ТЭГ проводилось с венозной кровью, стабилизированной цитратом натрия с применением каолиновых кювет на аппарате TEG 5000 (HАEМONETICS), контролировались показатели: R, К, угол α°, показатель 30-минутного лизиса (LY30), максимальная амплитуда (МА).
Сканирование и допплерография вен нижних конечностей проводились в день поступления в клинику с использованием аппарата Voluson-Е8 Expert ВТ-12. Контрольное исследование с целью выявления субклинических форм тромбоза проводилось на 6-е сутки послеоперационного периода.
Контроль параметров ОАК, гемостаза и ТЭГ производился: 1 – в день госпитализации; 2 – после достижения хирургического гемостаза во время операции; 3 – через сутки после миомэктомии; 4 – через 6 суток после миомэктомии.
Поскольку все пациентки, включенные в данное исследование, имели низкую степень риска развития ВТЭО, медикаментозная профилактика не применялась. В периоперационном периоде использовались эластическая компрессия вен нижних конечностей в сочетании с ранней активацией.
За двое суток до операции пациенткам производилась внутривенная инфузия карбоксимальтозата железа с индивидуальным расчетом дозы в миллиграммах элементарного железа. Общий дефицит железа вычислялся с использованием формулы Ганзони: общий дефицит железа (мг) = масса тела (кг) × (целевое содержание гемоглобина – фактическое содержание гемоглобина) × 0,24 + депонированное железо (мг). За целевое значение гемоглобина принимается 150 г/л, показатель депонированного железа составляет 500 мг для пациентов массой более 35 кг.
Всем пациенткам была выполнена лапароскопическая миомэктомия по стандартной методике в условиях общей анестезии. С целью уменьшения интраоперационной кровопотери всем пациенткам в операционной после премедикации проводилась инфузия транексамовой кислоты в дозе 20 мг/кг.
Исследование одобрено локальным этическим комитетом НИИКЭЛ – филиал ИЦиГ СО РАН.
Статистический анализ
Для статистической оценки использовался программный пакет Statistica 10.0. Оценка нормальности распределения проводилась с применением критерия Шапиро–Уилка, при соблюдении данного критерия рассчитывали среднюю арифметическую величину (М) и стандартное отклонение (SD). При несоблюдении критериев нормального распределения вычисляли медиану (Мe), первый (Q1) и третий (Q3) квартили. Для оценки статистической значимости различий показателей, полученных в разные моменты времени, применялся критерий Фридмана. В случае соответствия нормальному закону распределения при сопоставлении с исходными показателями использовался парный критерий Стьюдента. Для выборок, не соответствующих нормальному распределению, применялся критерий Вилкоксона. При сравнении двух показателей статистически значимым считалось различие при р<0,05.
Результаты
Возраст всех пациенток в исследовании был менее 40 лет, в среднем 35,16 (3,81) года. По данным ультразвукового исследования, количество миоматозных узлов было множественным: минимально – 2, максимально – 8, расположение – интерстициальное либо интерстициально-субсерозное. Средний диаметр узлов составлял 47,51 (17,68) мм, максимальный диаметр доминирующего узла – 120,3 мм. Объем матки в дооперационном периоде в среднем составил 324 (29,68) мл.
У всех пациенток регистрировалась анемия легкой степени со средними показателями гемоглобина при поступлении 101,9 (5,6) г/л, после введения карбоксимальтозата железа в день операции – 115,7 (6,7) г/л, на 2-е сутки после оперативного лечения – 105,3 (5,1) г/л.
Сопутствующая соматическая патология, имеющаяся у пациенток, была в стадии компенсации или ремиссии. Риск ВТЭО при оценке по шкале J. Caprini составлял не более 2 баллов.
Оперативное вмешательство в объеме лапароскопической консервативной миомэктомии проводилось в плановом порядке в условиях общей анестезии по эндотрахеальному способу с использованием севофлурана, фентанила и рокурония. Средняя длительность оперативного вмешательства составила 1,43 (0,26) ч. С учетом массы пациенток 69,47 (5,36) кг, расчетный объем циркулирующей крови (ОЦК) составил 4,86 (0,38) л. Средний объем интраоперационной кровопотери – 0,383 (0,047) мл, что составляет 7,9 (0,97)% ОЦК. Всем пациенткам во время операции устанавливался дренаж, который удаляли в 1-е сутки послеоперационного периода. Средний объем дренажных потерь составил 30 (6,3) мл. Послеоперационные осложнения отсутствовали.
В предоперационном периоде базовые показатели коагулограммы АЧТВ и ПТИ были в пределах референсных значений. Показатели РФМК и D-димера в пределах нормативных значений свидетельствовали об отсутствии тромбинемии и фибринолиза. По данным ТЭГ наблюдалась нормокоагуляция.
Изменения показателей коагуляционного гемостаза в послеоперационном периоде характеризовались уменьшением АЧТВ на 15% и увеличением ПТИ на 22% от дооперационного уровня. Через 24 ч после операции зафиксированы минимальная длительность АЧТВ – 22,56 (21,55; 24,87) и максимальное увеличение ПТИ – 118,30 (104,77; 126,34)%. В ходе исследования выявлено динамическое увеличение концентраций фибриногена, РФМК, D-димера. Увеличение концентраций данных показателей зарегистрировано интраоперационно на фоне введения и пика действия транексамовой кислоты с дальнейшим нарастанием и достижением максимальных значений на 6-е сутки послеоперационного периода: фибриноген – 6,41 (5,02; 6,88) г/л, РФМК – 10,65 (7,83; 13,47) мг/100 мл, D-димер – 545 (498,54; 601,24) нг/мл. Изменения показателей коагулограммы представлены в таблице 1.
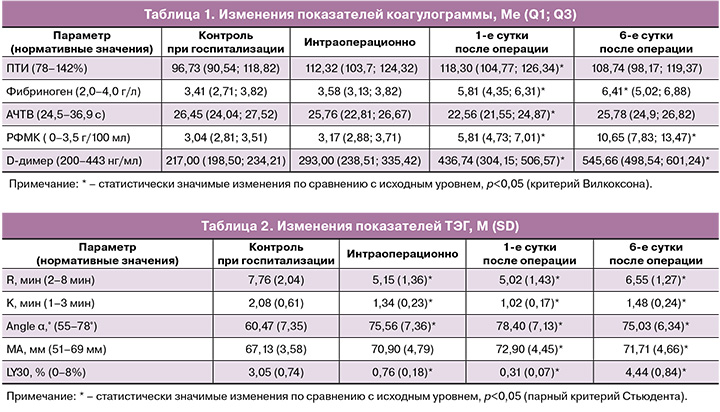
Совокупная оценка показателей ТЭГ свидетельствует об интраоперационном увеличении скорости образования тромбопластина, тромбина и фибриногена – уменьшение показателей R и К до 5,02 (1,43) и 1,02 (0,17) соответственно; увеличении скорости формирования сгустка в целом и его прочности – увеличение угла α до 78,4 (7,13), повышение величины MA до 72,9 (4,45) мм, что в целом говорит о периоперационном увеличении вязкости крови. Статистически значимые изменения данных показателей от исходных величин сохранялись на 6-е сутки после миомэктомии.
Наблюдаемое уменьшение показателя LY30 во время операции до 0,76 (0,18)% и на 1-е сутки после операции до 0,31 (0,07)%, при исходных значениях 3,05 (0,74)% (р<0,05), свидетельствует о блокировании фибринолиза и формировании полноценного сгустка на фоне специфического направленного действия транексамовой кислоты. Данные изменения показателей ТЭГ представлены в таблице 2.
В ходе исследования во время пребывания в стационаре клинических проявлений тромбозов вен нижних конечностей ни у одной пациентки не выявлено. По данным ультразвукового скрининга вен нижних конечностей тромбозов не зафиксировано.
Обсуждение
Наличие анемического синдрома, частота которого при миоме матки достигает 60–80% [8, 9], в сочетании с риском значимой интраоперационной кровопотери, усугубляющей выраженность анемии, детерминирует необходимость комплексного подхода: использование современных антианемических средств, щадящей хирургической техники с периоперационным введением антифибринолитических препаратов.
Исходя из концепции комплексного подхода, в своем исследовании мы использовали, во-первых, для коррекции предоперационной анемии карбоксимальтозат железа, высокая эффективность которого доказана у пациенток с рецидивирующими метроменоррагиями [9, 17]. Преимуществом данного препарата является относительная безопасность при внутривенном применении с возможностью быстрого восполнения дефицита железа и быстрым повышением показателей гемоглобина и эритроцитов [9].
Во-вторых, с целью уменьшения интраоперационной кровопотери мы использовали ингибитор фибринолиза – транексамовую кислоту. Относительно эффективности применения блокаторов фибринолиза при лапароскопической миомэктомии мнения исследователей разнятся [18–23]. Учитывая морфологические изменения миометрия, обусловленные множественным ростом узлов, изменения периузловых и внутриузловых сосудов с нарушением их архитектоники и моторики, приводящие к повышенной кровоточивости, в том числе интраоперационной, назначение транексамовой кислоты, блокирующей фибринолиз и способствующей формированию полноценного сгустка, считаем патогенетически оправданным и целесообразным. Выбор относительно высокой дозировки 20 мг/кг обусловлен тем, что удаление миоматозных узлов и хирургический гемостаз при лапароскопических миомэктомиях технически являются более сложной и длительной процедурой, чем при лапаротомических операциях. Ранее нами доказано, что применение транексамовой кислоты позволяет сократить интраоперационную кровопотерю и избежать значимого усугубления анемического синдрома [22].
С другой стороны, закономерным спутником применения средств, влияющих на звенья гемостаза, является увеличение риска развития ВТЭО. Известно, что эффективная антифибринолитическая концентрация транексамовой кислоты в тканях сохраняется в течение 17 ч, в плазме –до 7–8 ч. В ходе исследования нами установлено, что в период действия транексамовой кислоты данные совокупной оценки показателей коагулограммы и ТЭГ свидетельствуют о тенденции к гиперкоагуляции (уменьшение АЧТВ, увеличение ПТИ), увеличении скорости образования и прочности сгустка (уменьшение R, K, увеличение угла α, МА, уменьшение L30), однако остаются в пределах референсных значений. При этом концентрации основных маркеров тромбинемии и фибринолиза РФМК и D-димера статистически значимо не изменяются. Полученные данные свидетельствуют о том, что гиперкоагуляционные сдвиги на фоне действия транексамовой кислоты не выходят за рамки компенсаторно-приспособительных реакций.
Сохраняющаяся тенденция к гиперкоагуляции на 6-е сутки послеоперационного периода: увеличение концентраций маркеров активации свертывающей системы (фибриногена, D-димера, РФМК), превышающих референсные значения, увеличение вязкости по данным ТЭГ – по всей видимости, связана с объемом оперативного вмешательства при множественной миоме матки на фоне исходного анемического синдрома, сопровождающегося увеличением незрелых ригидных форм эритроцитов, дисфункцией эндотелия, нарушением реологических свойств и активации агрегации тромбоцитов. Полученные в ходе исследования данные свидетельствуют о сохраняющемся риске ВТЭО у пациенток с анемическим синдромом с исходно низкой оценкой по шкале J. Caprini, в том числе риске развития скрытых тромбозов в отдаленном послеоперационном периоде.
Выводы
1. Динамический контроль коагуляционных тестов и показателей ТЭГ свидетельствует о том, что применение транексамовой кислоты для ограничения интраоперационной кровопотери не создает дополнительные риски тромбоэмболических осложнений при лапароскопической миомэктомии.
2. Сохраняющаяся на 6-е сутки после лапароскопической консервативной миомэктомии тенденция к гиперкоагуляции у пациенток с множественной миомой матки и сопутствующей железодефицитной анемией детерминирует необходимость комплексного контроля свертывающей системы, а также необходимость системы эффективных мер предупреждения ВТЭО, включая использование низкомолекулярных гепаринов в сочетании с мерами немедикаментозной профилактики.



