Ишемическая болезнь сердца (ИБС) — важная медико‑социальная проблема, относящаяся к приоритетам национальных систем здравоохранения большинства стран мира. Распространенность хронической сердечной недостаточности (ХСН) в развитых странах мира составляет не менее 1—2% и непрерывно возрастает. По данным последних эпидемиологических исследований, в Российской Федерации (РФ) у 8,1 млн человек имеются четкие признаки ХСН [1]. Распространенность тяжелой ХСН III—IV функционального класса (ФК) в Европейской части России составляет 3,4 млн случаев.
Годичная смертность больных с клинически выраженной ХСН достигает 26—29%, т.е. за один год в РФ умирают от 880 до 986 тыс. больных с ХСН [2].
Результаты крупных эпидемиологических исследований позволили установить, что частота сердечных
сокращений (ЧСС) является независимым фактором риска, увеличивающим частоту общей смертности, внезапной смертности и смертности от сердечно‑сосудистых заболеваний (ССЗ) [3]. Только β-адреноблокаторы, блокируя нейрогормональные системы, прежде всего симпатико‑адреналовую систему, способны урежать ЧСС и улучшать прогноз у пациентов с ССЗ [4].
Применение β-адреноблокаторов ограничивается за счет таких побочных эффектов, как артериальная гипотония, депрессия, эректильная дисфункция, атриовентрикулярная блокада, липидные нарушения, неселективное влияние на бронхи, периферические сосуды. Это определило интерес фундаментальной науки к поиску новых препаратов специфического действия, способных избирательно снижать ЧСС. Таким препаратом является ивабрадин (кораксан), действующий только на снижение частоты сердечных сокращений. Он является ингибитором ионных токов If избирательного
и специфического действия, уменьшающим скорость медленной спонтанной диастолической деполяризации [5]. Снижая ЧСС, ивабрадин снижает потребность миокарда в кислороде и повышает доставку кислорода к миокарду, что определяет показания к его использованию при стенокардии напряжения. Селективность действия на ЧСС в отсутствие отрицательного инотропного эффекта позволяет сохранить сократимость миокарда, что особенно актуально в отношении пациентов
с систолической дисфункцией [6]. Антиангинальная и противоишемическая эффективность ивабрадина была доказана в крупных рандомизированных исследованиях с применением двойного слепого метода по сравнению с плацебо, β-адреноблокатором — атенололом и антагонистом кальция — амлодипином [7,8].
Роль ивабрадина у пациентов со стабильной стенокардией и ХСН в настоящее время изучается.
Цель исследования: изучить динамику структурно‑функциональных показателей ССС у больных стабильной стенокардией с ХСН ишемической природы на фоне комплексной терапии, включающей ивабрадин.
Материал и методы
В исследование включены 78 пациентов со стабильной стенокардией и симптомами ХСН, развившимися после перенесенного инфаркта миокарда. Критерии включения: информированное согласие пациента на участие в исследовании, анамнез стабильной стенокардии III— IV функционального класса в течение 3 мес до момента включения в исследование, наличие симптомов ХСН, развившихся после перенесенного инфаркта миокарда, число сердечных сокращений больше 70 ударов в минуту на фоне максимально переносимой дозы рекомендуемых β-адреноблокаторов. Критерии исключения:
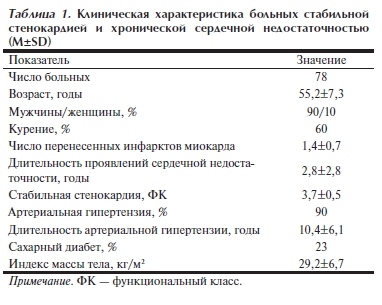
гиперчувствительность к ивабрадину или к какому‑либо из входящих в его состав дополнительных компонентов, нестабильная стенокардия, повторный инфаркт миокарда в течение 3 мес перед исследованием, тяжелая почечная или печеночная недостаточность, синдром слабости синусового узла, синоатриальные блокады, атриовентрикулярные блокады II—III степени, фибрилляция и трепетание предсердий, наличие пейсмекера. Обследовали 70 мужчин (90%) и 8 женщин (10%) в возрасте от 46 до 67 лет, средний возраст составил 55,2±7,3 года. Почти 60% больных курили. У обследованных пациентов среднее число инфарктов составило 1,4±0,7, длительность проявлений сердечной недостаточности — около 3 лет (2,8±2,8 года), имелся высокий ФК стабильной стенокардии – 3,7±0,5. Артериальная гипертензия встречалась у 90% пациентов, ее длительность составила 10,4±6,1 года. У 18 (22,5%) больных имелся сахарный диабет 2-го типа. Индекс массы тела достигал 29,2±6,7 кг/м² (табл. 1).
Все больные, вошедшие в исследование, получали стандартную терапию в соответствии с Национальными рекомендациями по лечению стабильной стенокардии и ХСН. Если на фоне терапии β-адреноблокаторами в максимально переносимой дозе ЧСС сохранялась более 70 уд/мин, то больного включали в исследование. Все пациенты, вошедшие в исследование, были рандомизированы в 2 группы. Больным 1-й группы (n=40) к стандартной терапии добавляли ивабрадин (кораксан, Лаборатории Сервье, Франция), пациенты 2‑й группы (n=38) получали общепринятое лечение стабильной стенокардии и ХСН. Ивабрадин назначали в начальной дозе 5 мг, по 1 таблетке 2 раза в сутки с последующей титрацией дозы. Один раз в месяц посредством телефонного контакта осуществляли контроль приема препаратов, титрации дозы, эффективности и переносимости терапии. Длительность лечения составила 6 мес. Средняя доза ивабрадина в ходе титрации составила
5,25±2,5 мг/сут. В течение 6 мес наблюдения в каждой группе обследуемых 90% больных получали ингибиторы ангиотензинпревращающего фермента (АПФ), 90% пациентов — β‑адреноблокаторы, 90% — антиагреганты, 80% — нитраты, 75% — статины, 65% антагонисты альдостерона, 25% — мочегонные препараты.
Обследование проводили до начала терапии и через 6 мес лечения.
Тест с 6-минутной ходьбой проводили по стандартной мето дике [10]. Эхокардиографию (ЭхоКГ) выполняли на комплексе Acuson 128 XP/10. Использовали М‑модальный режим, двухмерный (В) режим, режимы импульсной и непрерывноволновой допплерографии в стандартных эхокардиографических позициях. Оценка вариабельности ритма сердца (ВРС) осуществлялась с использованием временны`х и спектральных показателей. Использованы короткие 5-минутные отрезки записи на аппарате фирмы «Волготех» [11]. Активность фактора Виллебранда определяли по его способности вызывать агглютинацию тромбоцитов в присутствии антибиотика ристомицина [12]. Для проведения данных исследований использовали наборы реагентов НПО «Ренам». Вазорегулирующую функцию эндотелия исследовали в пробах с реактивной гиперемией и нитроглицерином [13, 14]. Анализ пульсовой волны выполняли с использованием оригинальной программы «Tensiomed» на артериографе «TensioClinic» [15]. Для оценки качества жизни (КЖ) больных применяли Сиэтлский опросник для больных со стабильной стенокардией и Миннесотский опросник для пациентов с ХСН.
В динамике исследуемые параметры изучали у всех 78 больных.
Анализ данных осуществляли с помощью пакета прикладных программ STATISTICA 7.0. Использовали следующие методики статистического анализа: проверку нормальности распределения количественных признаков, описательную статистику, t-критерий Стьюдента для зависимых групп и независимых групп, критерий Вилкоксона для парных сравнений. Выборочные параметры, приводимые в таблицах, представлены в виде M (SD) или med (Lq; Uq), где M — среднее, SD — стандартное отклонение, med — медиана, Lq; Uq — межквартильный размах. Критическое значение уровня значимости принимали равным 5%.
Результаты
Известно, что у больных, перенесших инфаркт миокарда, β‑адреноблокаторы эффективно урежают ЧСС. Вместе с тем существует категория пациентов, у которых не удается добиться снижения ЧСС на адекватных дозах β‑адреноблокаторов. Это может быть обусловлено симптоматической гипотонией или генетически обусловленным изменением чувствительности β‑адренорецепторов к β‑адреноблокаторам.
До лечения ЧСС у обследуемых больных составляла 74,6±3,1 уд/мин. Через 6 мес терапии у пациентов,
получающих в составе комплексной терапии ивабрадин, ЧСС составила 63,9±3,2 уд/мин, что достоверно меньше исходной (р<0,01). При этом ЧСС снизилась на 15%. На фоне урежения ЧСС отмечено уменьшение числа приступов стенокардии с 10,5±8,5 до 5,8±4,2 в неделю и потребности в нитроглицерине с 10,4±8,6 до 5,6±4,3 таблетки в неделю (р<0,05). Таким образом, на фоне комплексной терапии, включающей ивабрадин, число приступов стенокардии и потребность в нитроглицерине уменьшились практически на 50%.
На фоне стандартной терапии через 6 мес также произошло достоверное урежение ЧСС до 69,3±3,1 уд/мин по сравнению с исходной (р<0,05), но при этом ЧСС уменьшилась только на 7%, т.е. ее урежение на фоне стандартной терапии было существенно меньше, чем у больных на фоне терапии, включающей ивабрадин (р<0,05). На фоне стандартной терапии отмечено уменьшение числа приступов стенокардии с 10,3±7,5 до 7,8±4,1 в неделю и потребности в нитроглицерине с 10,4±8,5 до 7,6±4,2 таблетки в неделю (р>0,05), однако клиническое улучшение по данным показателям было
менее выраженным и составило только 30%.
За период наблюдения отмечены стабилизация клинического состояния пациентов и уменьшение ФК ХСН. Так, в 1‑й группе число больных с III и IV ФК ХСН уменьшилось на 25%, т.е. у каждого четвертого больного с III и IV ФК ХСН повысилась переносимость физической нагрузки. Во 2-й группе число больных с III и IV ФК ХСН уменьшилось только на 10%, т.е. на фоне 6‑месячной комплексной терапии, включающей ивабрадин, у большего числа пациентов возросла толерант‑
ность к физической нагрузке (табл. 2).
Таблица 2. Изменения ФК ХСН и параметров ЭхоКГ у больных стабильной стенокардией и ХСН на фоне 6 месячной терапии (M±SD).
У пациентов, получающих стандартную терапию, выявлено улучшение КЖ — по Сиэтлскому опроснику
на 15%, по Миннесотскому — на 8%. У больных, получающих в составе комплексной терапии ивабрадин, отмечено улучшение КЖ по данным Сиэтлского опросника на 28%, по показателям Миннесотского — на 14,7%. Следовательно, у пациентов, получающих в составе комплексной терапии ивабрадин, КЖ на фоне 6‑месячной терапии улучшилось в большей степени.
Анализируя показатели ЭхоКГ у пациентов, получающих в составе комплексной терапии ивабрадин,
мы выявили увеличение ударного объема (УО) левого желудочка (ЛЖ) с 79,2±18,1 до 83,9±18,9 мл, конечного диастолического объема (КДО) ЛЖ с 199,1±56,6 до 219,4±54,0 мл (р<0,05). Фракция выброса (ФВ) ЛЖ при этом не изменилась и составила 38%. У больных, получающих стандартную терапию, не отмечено достоверных изменений параметров ЭхоКГ.
На фоне 6-месячной комплексной терапии, включающей ивабрадин, изменения временных показатели ВРС были умеренными и заключались в повышении общей мощности спектра (табл. 3). Это находило отражение в статистически значимом увеличении среднего значения всех интервалов RR c 871 (779; 920) до 957 (821; 1028) мс, среднего значения стандартных отклонений за 5-минутный период (SDNN‑in) с 714 (639; 754) до 785 (666; 843) мс. В группе больных, получающих стандартную терапию, достоверных изменений не выявлено.
Таблица 3. Изменения вариабельности ритма сердца у больных стабильной стенокардией и ХСН на фоне 6 месячной терапии, med (Lq; Uq).
Таблица 4. Изменения активности фактора Виллебранда и вазорегулирующей функции эндотелия у больных со стабильной стенокардией и ХСН на фоне 6 месячной терапии, med (Lq; Uq).
Таблица 5. Изменения показателей жесткости артерий у больных стабильной стенокардией и ХСН на фоне 6 месячной терапии, med (Lq; Uq).
У больных стабильной стенокардией с ХСН выявлено снижение низкочастотного компонента (LF) спектра, отражающего преимущественно симпатические влияния, высокочастотного компонента (HF) спектра, свидетельствующего о парасимпатическом воздействии на ритм сердца, а также отношение низкочастотных волн к высокочастотным (LF/HF), представляющее уровень вагосимпатического баланса (см. рисунок). На фоне 6‑месячной терапии отмечена лишь тенденция к снижению симпатических влияний на ритм сердца.
Рисунок. Спектральный анализ ВРС у больных со стабильной стенокардией и ХСН на фоне 6 месячной комплексной терапии.
Как видно из табл. 4, активность фактора Виллебранда у больных стабильной стенокардией
с ХСН до лечения составила 178%. Через 6 мес терапии у пациентов обеих групп медиана активности фактора Виллебранда составила 160%, что свидетельствует лишь о некотором снижении его активности.
У больных стабильной стенокардией с ХСН на фоне терапии не выявлено существенной динамики сосудодвигательной функции эндотелия (табл. 4). У больных стабильной стенокардией с ХСН повышена жесткость магистральных артерий (табл. 5). Скорость пульсовой волны в аорте составляла 10,4 м/с, индекс аугментации аорты — 29,9%, индекс аугментации плечевой артерии — 6,1%. На фоне 6-месячной терапии указанные параметры не претерпели существенных изменений у больных обеих групп.
Обсуждение
Антиангинальная и антиишемическая эффективность ивабрадина доказана в крупных международных и российских исследованиях [8, 9, 16]. Ивабрадин опосредует свое действие через урежение ЧСС. Снижение ЧСС вызывает уменьшение потребности миокарда в кислороде, а удлинение диастолы приводит к улучшению коронарной перфузии. Кроме того, описана роль повышения ЧСС в прогрессировании коронарного атеросклероза [17]. В исследованиях, охвативших более 2700 пациентов с ХСН, показатель ЧСС более 100 уд/мин расценивался как прогностический фактор декомпенсации деятельности сердца в ближайшие сроки с увеличением риска до 61% [18]. В нашем исследовании у пациентов с исходной ЧСС более 70 уд/мин на фоне терапии β-адреноблокаторами
отмечено снижение ЧСС на 10 уд/мин. Антиишемическое действие комплексной терапии, включающей ивабрадин, могло способствовать повышению толерантности пациентов к физическим нагрузкам: так, у 25% пациентов 6‑месячная терапия привела к снижению ФК ХСН, что согласуется с данными литературы [20].
Согласно нейрогуморальной теории развития ХСН гиперактивность адренергической системы и постоянно увеличивающийся уровень плазменных катехоламинов играют отрицательную роль в прогрессировании сердечной недостаточности. Одним из методов оценки нейрогуморальных влияний на ССС является определение ВРС.
На фоне 6‑месячной комплексной терапии, включающей β‑адреноблокаторы, ингибиторы АПФ и ивабрадин, отмечено умеренное изменение параметров ВРС. Установлена тенденция к увеличению стандартного отклонения всех анализируемых интервалов RR (SDNN), квадратного корня суммы разностей последовательных интервалов RR (rMSSD), общей мощности спектра и спектра ультранизких частот (см. рисунок). Увеличение этих параметров свидетельствует об уменьшении симпатического влияния на сердце. Необходимо также отметить, что увеличение SDNN составило 15 мс в условиях базовой терапии ингибиторами АПФ и β‑адреноблокаторами. Для пациентов с ХСН это достаточно значимый результат, так как, согласно данным исследования CHF-STAT, увеличение указанного параметра на 10 мс снижает риск смерти у таких больных на 20% [21].
С современных позиций эндотелий рассматривается как орган, выполняющий ряд гомеостатических функций, к которым относятся поддержание сосудистого тонуса и структуры сосудистой стенки, участие в процессах воспаления, гемостаза, сохранение реологических свойств крови [22]. У больных с ССЗ закономерно развивается ХСН, и объективными методами подтверждается наличие дисфункции эндотелия, под которой понимают дисбаланс между продукцией вазодилатирующих, антитромбогенных, противовоспалительных, антипролиферативных факторов, с одной стороны, и вазоконстриктивных, протромбогенных, провоспалительных, пропролиферативных факторов, с другой [23].
Одним из маркеров активации/повреждения эндотелия служит активность фактора Виллебранда. На фоне 6‑месячной стандартной терапии и комплексной терапии с включением ивабрадина у пациентов отмечено лишь незначительное (на уровне тенденции) снижение активности фактора Виллебранда. В то же время в литературе имеются данные, свидетельствующие об улучшении функции эндотелия сосудистой стенки по мере уменьшения ФК ХСН [24].
Сосудодвигательная функция эндотелия была изучена в пробах с реактивной гиперемией и нитроглицерином [25]. В течение 6 мес наблюдения мы не обнаружили достоверных изменений эндотелийзависимой и эндотелийнезависимой вазодилатации, что обусловлено, видимо, небольшой продолжительностью наблюдения.
С конца 90‑х годов XX века определение жесткости артериальной стенки и центрального давления
предложены в качестве тестов для оценки риска развития ССЗ [26, 27]. Считается, что параметры жесткости артерии могут меняться на фоне различной терапии. В нашем исследовании на фоне 6-месячной терапии, включающей ивабрадин, скорость пульсовой волны, индексы аугментации аорты и плечевой артерии не изменились.
В целом благоприятное влияние комплексной терапии, включающей ивабрадин, на клиническое состояние больных, состояние их ССС способствовало улучшению КЖ пациентов, что совпадает с данными литературы [28].
В нашем исследовании отмечена хорошая переносимость ивабрадина. У 2 (5%) больных наблюдалась фотопсия, которая описывается как преходящее усиление яркости в ограниченных участках зрительного поля. Ивабрадин может взаимодействовать с h‑каналами сетчатки, которые по структуре сходны с f-каналами синусного узла сердца. Это приводит к временному нарушению световосприятия вследствие снижения реакции сетчатки на яркие световые стимулы. Триггерные факторы (резкая смена освещения), частичное ингибирование h‑каналов обусловливают возможность развития фотопсии [29—31]. Однако в нашем исследовании проявления фотопсии были умеренными и не послужили поводом к отмене ивабрадина.
Заключение
Использование ивабрадина (кораксана) в комплексной 6‑месячной терапии у больных стабильной стенокардией с хронической сердечной недостаточностью при исходной частоте сердечных сокращений более 70 уд/мин на фоне терапии β-адреноблокаторами способствует дополнительному урежению пульса, уменьшению числа приступов стенокардии напряжения и потребности в короткодействующих нитратах, повышению толерантности к физической нагрузке, улучшению качества жизни пациентов. Ивабрадин хорошо переносится, побочные эффекты встречаются в единичных случаях и не требуют прекращения приема препарата.



