Нарушения углеводного обмена (НУО) не только способствуют развитию всех форм ишемической болезни сердца (ИБС), но и существенно влияют на их прогноз [1]. По результатам многих исследований, госпитальная и постгоспитальная смертность при инфаркте миокарда (ИМ) значительно выше при наличии сахарного диабета (СД) [2, 3], применение же реваскуляризирующих процедур в остром периоде ИМ оптимизирует прогноз у пациентов данной категории [4, 5]. Тем не менее выбор метода реваскуляризации у больных ИБС с СД во многом определяется индивидуальными особенностями поражения коронарного русла [6].
 Анализ отечественных и зарубежных последних публикаций, посвященных проблемам ведения больных ИМ в сочетании с НУО, выявил ограниченное количество работ, в которых оценивается роль нарушения толерантности к глюкозе (НТГ) в этом процессе [7]. Кроме того, использование чрескожного коронарного вмешательства (ЧКВ) как метода экстренной реваскуляризации у больных ИМ с НТГ также нуждается в дальнейшем изучении ввиду отсутствия общепринятых позиций относительно ее эффективности у пациентов этой категории.
Анализ отечественных и зарубежных последних публикаций, посвященных проблемам ведения больных ИМ в сочетании с НУО, выявил ограниченное количество работ, в которых оценивается роль нарушения толерантности к глюкозе (НТГ) в этом процессе [7]. Кроме того, использование чрескожного коронарного вмешательства (ЧКВ) как метода экстренной реваскуляризации у больных ИМ с НТГ также нуждается в дальнейшем изучении ввиду отсутствия общепринятых позиций относительно ее эффективности у пациентов этой категории.
Цель исследования: оценить роль ЧКВ в госпитальном и годовом прогнозе у пациентов после перенесенного ИМ с подъемом сегмента ST (ИМпST) в сочетании с СД 2-го типа и НТГ.
Материал и методы
Протокол исследования соответствовал стандартам Этического комитета ФГБУ НИИ комплексных проблем сердечно-сосудистых заболеваний СО РАМН, разработанным в соответствии с Хельсинкской декларацией Всемирной ассоциации «Этические принципы проведения научных медицинских исследований с участием человека» с поправками 2000 г. и «Правилами клинической практики в Российской Федерации», утвержденными Приказом Минздрава РФ № 266 от 19.06.2003 г. Перед проведением исследования все пациенты подписывали информированное согласие на участие в нем.
Критерии включения: наличие ИМпST в пределах 24 ч до поступления в клинику без возрастных ограничений. Критерии исключения: ИМ, осложнивший ЧКВ или коронарное шунтирование, терминальная стадия почечной недостаточности, известная онкологическая патология, хронические заболевания внутренних органов в стадии обострения, а также наличие других заболеваний, влияющих на продолжительность жизни.
В регистровое исследование включен 601 пациент с ИМпST, поступивший в стационар в пределах 24 ч от начала клинических проявлений в течение одного календарного года. Клинико-анамнестическая характеристика пациентов представлена в табл. 1.
При поступлении в стационар у всех пациентов определяли уровень глюкозы в крови. На 8—14-е сутки больным без установленных НУО и уровнем глюкозы в крови натощак или после приема пищи менее 11,1 ммоль/л проводили пероральный тест на толерантность к глюкозе (ПТТГ).
СД 2-го типа, впервые выявленный, диагностировали в течение госпитального периода лечения с учетом данных повторного определения уровня глюкозы в крови, а также по результатам ПТТГ, анамнестически СД учитывали по данным медицинской документации пациентов. НТГ диагностировали в течение госпитального периода по результатам ПТТГ [8].
В течение госпитального периода лечение больных проводили с учетом рекомендаций Всероссийского научного общества кардиологов (2007) по диагностике и лечению больных острым ИМпST. Всем пациентам в кратчайшие сроки определяли метод реперфузии миокарда: баллонная ангиопластика (БАП), стентирование симптомзависимого поражения коронарной артерии (КА), проведение интракоронарной тромболитической терапии (ТЛТ). При наличии противопоказаний к экстренной коронарографии (КГ) проведена системная ТЛТ. При наличии противопоказаний к ТЛТ или ЧКВ ограничивались консервативной тактикой. Основным противопоказанием к ТЛТ служило позднее время поступления пациента, для ЧКВ — диффузное поражение КА без возможности определения инфарктзависимой артерии.
Суммарное поражение коронарного русла оценивали по шкале SYNTAX (в баллах), учитывающей локализацию поражения и ряд морфологических показателей стенозов (наличие окклюзии сосуда, бифуркационное поражение, устьевой стеноз, продленное поражение, кальциноз, интракоронарный тромбоз и др.) [9] с использованием on-line калькулятора (www. rnoik.ru).
В настоящем исследовании КГ проведена 436 (72,55%) больным ИМпST. С учетом данных КГ, первичному ЧКВ по поводу индексного ИМ подверглись 373 (62,06%) больных (см. табл. 1), для 228 (37,94%) пациентов выбрана неинвазивная тактика лечения. Из 373 пациентов с успешно выполненным ЧКВ имплантацию стента провели 301 (80,70%), 14 (3,75%) проведен интракоронарный тромболизис, 75 (20,10%) — БАП. Коронарная реваскуляризация выполнялась по экстренным показаниям в ближайшее время после госпитализации пациентов, среднее время от поступления в стационар до проведения вмешательства составило 78 мин и существенно не различалось в группах больных ИМпST с НУО и без такового.
 В госпитальном периоде зарегистрировано 59 (9,81%) летальных исходов — все от осложнений ИМ (разрыв сердца, кардиогенный шок, отек легких). У 15 (25,42%) умерших выявлен СД, у 2 (3,38%) — НТГ.
В госпитальном периоде зарегистрировано 59 (9,81%) летальных исходов — все от осложнений ИМ (разрыв сердца, кардиогенный шок, отек легких). У 15 (25,42%) умерших выявлен СД, у 2 (3,38%) — НТГ.
В период стационарного лечения все пациенты получали комбинированную коронароактивную и антитромботическую терапию (антикоагулянты, дезагреганты, β-адреноблокаторы, ингибиторы ангиотензинпревращающего фермента, статины, антагонисты кальция) с учетом индивидуальных противопоказаний. Всем больным с диагностированными НУО даны рекомендации по коррекции образа жизни, включая рациональную физическую активность с учетом сроков ИМ, диету, нормализацию массы тела при необходимости. По показаниям рекомендован прием сахароснижающих препаратов (бигуанидов), при необходимости осуществлен подбор доз инсулина. В среднем длительность госпитального периода лечения составила 14 сут, значимых различий по продолжительности пребывания в стационаре у больных ИМпST с НУО и без такового не выявлено.
Годовой прогноз оценен у 470 (78,20%) пациентов, со 132 (21,96%) не удалось установить контакт. Всего выявлено 155 (32,98%) конечных точек — 59 (12,55%) смертельных исходов, 86 (18,30%) повторных ИМ, 52 (11,06%) случая нестабильной стенокардии, 18 (3,83%) — острое нарушение мозгового кровообращения (ОНМК), 20 (4,26%) госпитализаций по поводу декомпенсации хронической сердечной недостаточности (СН), 40 (8,51%) — ЧКВ по экстренным показаниям.
Статистическую обработку результатов исследования осуществляли с помощью пакета SPSS 21.0 (США). Для определения нормальности распределения количественных данных использовали критерий Шапиро—Уилка. Большинство данных имело статистически значимые отклонения от нормального распределения, поэтому при описании результатов использовали медианы (Ме) и интерквартильный размах (25-й и 75-й процентили). Для проверки гипотез о различиях выборок применяли непараметрический критерий U Манна—Уитни. Анализ различий качественных переменных несвязанных выборок проводили с помощью критерия χ2 с поправкой Йетса на непрерывность. Оценку частоты признаков в группах проводили с помощью расчета отношения шансов. Различия считали статистически значимыми при p<0,05.
Результаты
По признаку наличия НУО пациенты с ИМпST были разделены на 3 группы: без НУО (n=429; 71,38%), с НТГ (n=32; 5,33%), с СД (n=140; 23,29%), из них у 16 (11,42%) — впервые выявленный СД.
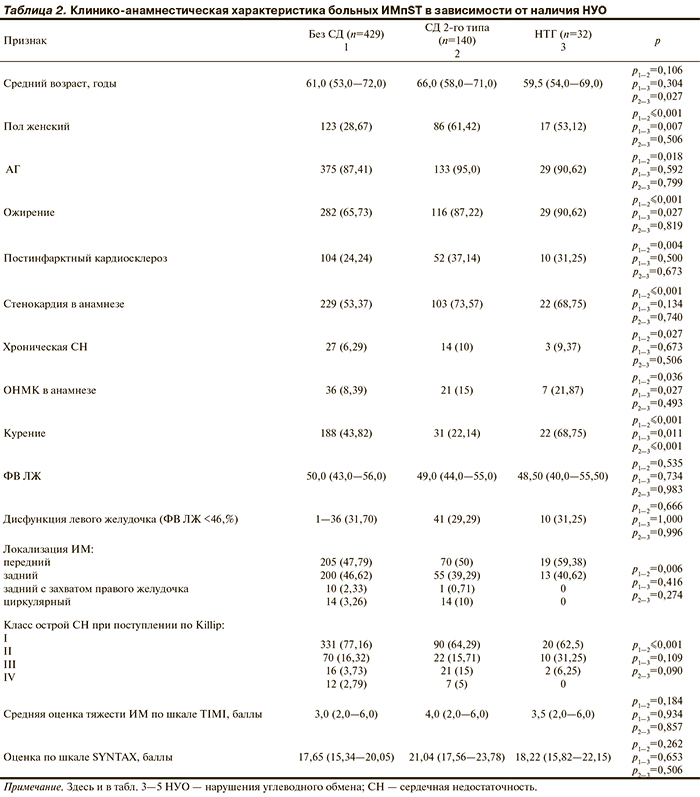
Анализ клинико-анамнестических характеристик больных ИМпST в зависимости от наличия НУО показал, что самой «тяжелой» группой оказались пациенты с СД, самой «легкой» — без НУО, пациенты с НТГ имели «промежуточное» положение (табл. 2). У пациентов с СД 2-го типа в сравнении с группами больных без НУО чаще наблюдались артериальная гипертензия (АГ), постинфарктный кардиосклероз, стенокардия и застойная СН в анамнезе, пациенты имели более высокий средний балл по шкале TIMI, чаще регистрировалась острая СН III и IV классов по Killip, наблюдалась высокая частота ретромбозов в период стационарного лечения. В группе НТГ по сравнению с группами больных с СД и без НУО чаще выявлялись пациенты с ожирением, застойной СН и ОНМК в анамнезе. Кроме того, отмечено преобладание женщин как в группе больных ИМпST с СД, так и среди пациентов с НТГ по сравнению с группой без НУО.
Больные ИМ в сочетании с СД характеризовались более высокой степенью суммарного поражения КА (по шкале SYNTAX) в сравнении с группами больных без НУО, которые имели одинаково тяжелое суммарное поражение коронарного русла, однако эти различия не достигали статистической значимости (см. табл. 2).
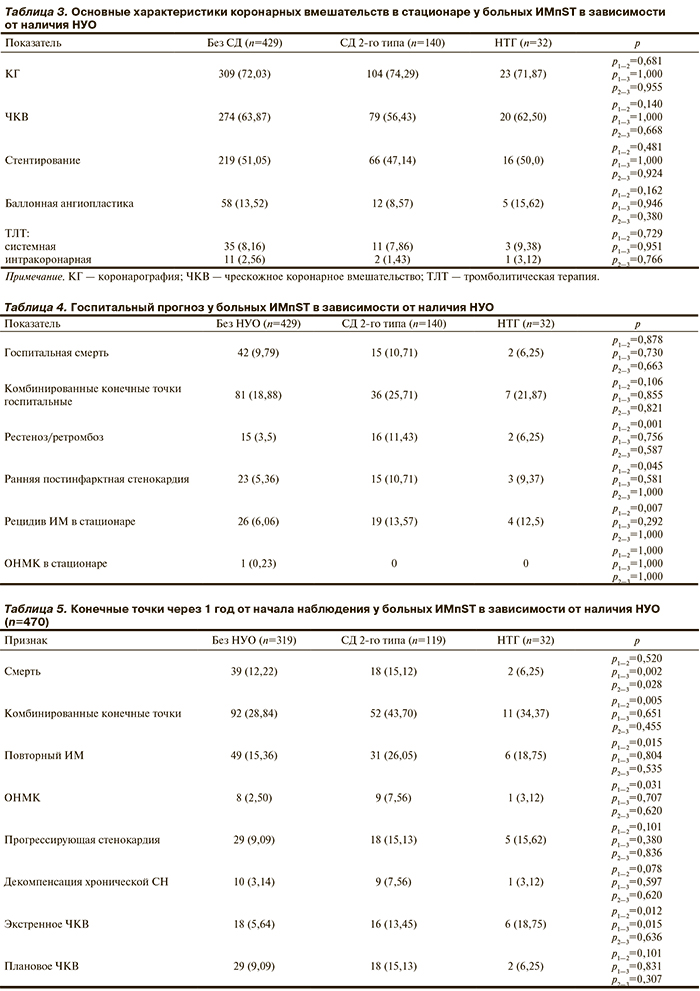
Статистически значимых различий во всех группах в отношении проведения КГ и ЧКВ не получено (табл. 3). Однако при анализе выполненного эндоваскулярного вмешательства по поводу индексного ИМ следует отметить, что в группе СД частота проведения стентирования, БАП и интракоронарной ТЛТ оказалась меньше, чем в других группах.
В период стационарного лечения у больных ИМпST с СД при сравнении с больными без НУО наблюдалась бóльшая частота развития ранней постинфарктной стенокардии (ПС), ретромбоза и рецидива ИМ (табл. 4). У пациентов с НТГ также была более высокой частота развития ранней ПС и рецидива ИМ при сравнении с пациентами без НУО.
При анализе исходов через 1 год после перенесенного ИМ выявлено, что пациенты с СД имели в 1,5 раза больше (р=0,005) конечных точек по сравнению с пациентами без НУО и в 1,3 раза больше по сравнению с больными с НТГ (табл. 5). Несмотря на то что больные ИМ с НТГ по количеству конечных точек не отличались от больных без НУО, выявлено, что в данной группе был наибольший процент госпитализаций по поводу прогрессирующей стенокардии, и им чаще проводили экстренную реваскуляризацию в течение года. Таким образом, наличие не только СД, но и НТГ у пациентов с ИМ определяет более тяжелый прогноз.
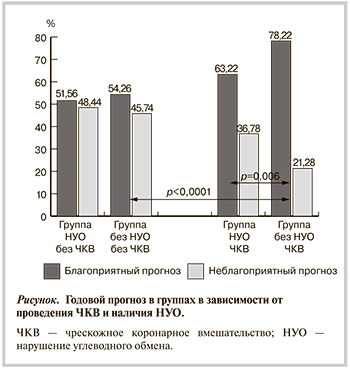
Анализируя влияние ЧКВ, выполненного в остром периоде ИМ, на исходы в течение последующего года, мы выявили, что эндоваскулярная реваскуляризация значимо улучшает годовой прогноз у больных ИМпST с НУО и без такового (см. рисунок). Причем положительный эффект восстановления коронарного кровотока особенно ожидаем у больных ИМ в сочетании с СД или НТГ.
У пациентов с НУО нами выявлено значимое уменьшение числа неблагоприятных исходов в течение года. В этом отношении группа пациентов с НТГ сохраняет общие закономерности течения отдаленного постинфарктного периода, характерные для пациентов с СД.
Таким образом, результаты настоящего исследования демонстрируют, что наличие как СД, так и НТГ у пациентов с ИМ в равной мере определяет не только более тяжелое течение индексного ИМ, но и неблагоприятный годовой прогноз. Вместе с тем применение ЧКВ у больных ИМпST в сочетании с СД или НТГ имеет большую прогностическую «выгоду» по снижению частоты развития неблагоприятных исходов в течение 1 года наблюдения.
Обсуждение
Прежде всего следует отметить, как показано во многих исследованиях, что пациенты с СД получают тот же, если не больший эффект от лечения ИМ по сравнению с лицами без НУО. Этот факт во многом может быть обусловлен тем, что абсолютный риск развития сердечно-сосудистых осложнений (ССО) у больных ИМ в сочетании с СД больше, соответственно, и абсолютная польза от терапии увеличивается [10]. Тем не менее, несмотря на наличие показаний к применению инвазивной тактики ведения у пациентов с СД и ИМпST, даже в крупных исследованиях использование инвазивного подхода у пациентов с СД недостаточное. В российской популяции больные СД, несмотря на более высокий риск развития осложнений ИМ, не получают адекватной инвазивной терапии [11]. Результаты настоящего исследования подтверждают данные регистра РЕКОРД о явной тенденции в российских инвазивных клиниках к выполнению эндоваскулярных процедур у больных с меньшим риском смерти [12]. Вероятнее всего, нежелание проводить «агрессивное» лечение у пациентов с ИМпST в сочетании с НУО можно объяснить тем, что при уменьшении базового риска развития ССО у пациента увеличивается вероятность получения им более полноценного лечения. Этот феномен назван авторами одной из работ [13] «парадокс лечения-риска» (treatment-risk paradox).
Однако факт негативного влияния СД на исходы у больных ИМ при выполнении ЧКВ продемонстрирован в ряде наших работ [5]. Действительно, несмотря на обнадеживающие результаты, наличие СД до сих пор является фактором риска развития ранних и поздних осложнений после первичного ЧКВ [14]. Доказано, что у пациентов с СД высок риск рестеноза и повторных реваскуляризаций [15]. Больные СД отличаются более высокими темпами прогрессирования атеросклероза не только в реваскуляризированных, но и в нереваскуляризированных областях [16].
Следует подчеркнуть, что ранее нами получены данные, подтверждающие негативное влияние НТГ, сопоставимое с СД, на прогноз у больных ИМ [17]. Так, показано, что больные ИМпST с консервативной тактикой ведения, особенно с наличием СД, — более «тяжелая» группа пациентов, с бóльшей долей пожилых лиц, характерными особенностями этих больных являются наличие сочетанной патологии, более высокий класс острой СН при поступлении [5]. Но и при уравнивании пациентов по клинико-анамнестическим характеристикам проведение коронарной реваскуляризации сохраняет свое положительное влияние на исходы у больных ИМ, особенно в сочетании с СД. Доказано, что наличие СД у пациентов с консервативной тактикой ведения острого периода заболевания по сравнению с инвазивной предопределяет бóльшую частоту развития всех событий в течение года после ИМ. Вместе с тем проведение ЧКВ у пациентов с СД достоверно снижает частоту развития всех неблагоприятных исходов в 2 раза, а у пациентов без СД — в 1,5 раза по сравнению с группой пациентов с консервативной тактикой ведения.
Обсуждая механизмы менее благоприятного прогноза заболевания у пациентов с НУО, необходимо учитывать, что для пациентов с СД в условиях хронической гипергликемии и дислипидемии характерны проявления активности внутрисосудистого воспаления, которые наряду с повышенной активностью тромбоцитов, также свойственной СД, являются условием для более высоких темпов прогрессирования атеросклероза [18].
В ранее опубликованных нами работах продемонстрировано, что высокий провоспалительный потенциал, оцененный повышением уровня лабораторных биомаркеров (С-реактивный белок, интерлейкин-12, sCD40L), установлен у больных ИМ не только с СД, но и с НТГ. Данный факт позволяет расценивать воспаление в качестве ведущего механизма реализации неблагоприятных сосудистых исходов у пациентов как с клинически выраженными, так и субклиническими проявлениями НУО [19].
Полученные в настоящем исследовании результаты позволяют утверждать, что НТГ имеет столь же важное влияние на прогноз, как и СД. Таким образом, влияние НТГ на отдаленный прогноз у больных ИМ сопоставимо с влиянием на него СД, а НТГ служит маркером различного по продолжительности воздействия таких факторов риска развития ССО, как АГ, ожирение, дислипидемия, гипергликемия, инсулинорезистентность, и, кроме того, является предиктором развития СД [20]. Кроме того, НТГ оказывает многофакторное влияние, связанное с воспалительным ответом, окислительным стрессом и снижением прокоагулянтной защиты. Коррекция выявленных нарушений оказывает существенное влияние на прогноз у больных после ИМ [21, 22].
К сожалению, в реальной клинической практике диагностика НУО у больных острым ИМ происходит с использованием ПТТГ после окончания стационарного этапа лечения, ввиду предполагаемой низкой диагностической информативности этого теста в остром периоде заболевания, а выявление НУО по уровню гликемии натощак существенно уступает по значимости пероральному тесту [17]. Однако диагностическая ценность этого теста, проведенного в течение госпитального периода у больных ИМ, продемонстрирована во многих исследованиях, в том числе организованных по принципу регистра [23]. Приведенные факты служат основанием для повышения эффективности своевременной диагностики НУО, в том числе НТГ, в период стационарного этапа лечения больных ИМ, тщательного соблюдения рекомендаций по рациональной антитромботической, коронароактивной и липиднормализующей терапии, контролю уровней артериального давления и глюкозы в крови. Кроме того, следует подчеркнуть необходимость индивидуального подхода к определению инвазивной тактики лечения больных ИМ в сочетании с НУО, включая НТГ.
В рамках настоящего исследования не проведен анализ различных подходов к коррекции липидов, гликемии у пациентов с НУО, а также других факторов риска развития ССО; не оценено число случаев развития СД в группе НТГ в течение года после перенесенного ИМ. Данные ограничения будут предметом для дальнейших исследований.
Выводы
Негативное влияние нарушения толерантности к глюкозе на прогноз больных инфарктом миокарда с подъемом сегмента ST сопоставимо с таковым при сахарном диабете.
Применение чрескожного коронарного вмешательства у больных инфарктом миокарда с подъемом сегмента ST в сочетании с сахарным диабетом или нарушением толерантности к глюкозе имеет бóльшую прогностическую «выгоду» по снижению частоты развития неблагоприятных исходов в течение одного года наблюдения по сравнению с пациентами без нарушения углеводного обмена.



