Аллапинин — антиаритмический препарат (ААП), относящийся к классу IС по классификации Vaughan—Williams, высоко эффективен при лечении больных с желудочковой экстрасистолией (ЖЭ) [1]. Однако современные рекомендации существенно ограничивают его применение при этой форме аритмии, допуская лишь использование при лечении клинически проявляющихся доброкачественных желудочковых аритмий (ЖА). Обоснованием тому служит отрицательный опыт использования ААП класса IС при лечении ЖА у больных с органическими заболеваниями сердца (ОЗС) и при сердечной недостаточности [2, 3]. При этом специальных исследований препаратов класса IС у больных с ЖЭ в отсутствие ОЗС не проводили, а указанные рекомендации основаны на анализе эффективности и безопасности ААП в смешанной группе больных с доброкачественными и потенциально опасными ЖА [2]. Клиническое изучение аллапинина также проводили в смешанной группе больных, в связи с чем целью настоящей работы является ретроспективная оценка его эффективности и безопасности в изолированной группе больных с доброкачественными ЖА.
Материал и методы
В Институте кардиологии им. А.Л. Мясникова с 1982 г. проводили исследования в рамках двух фаз клинических испытаний препарата аллапинин, которые продолжались до 1991 г. В базе данных этих исследований содержатся результаты обследования 194 больных с частой ЖЭ, у которых аллапинин применяли для краткосрочного и длительного лечения (данные 128 больных составили материалы прежних публикаций [4—7]). Из их числа для настоящей работы отобраны 73 пациента, у которых ЖА отнесена к разряду доброкачественной.
 Во всех случаях ЖА проявлялась клиническими симптомами в виде ощущения неритмичных сердцебиений, часто коротких эпизодов учащенного сердцебиения, что сопровождалось разнообразными психоэмоциональными реакциями. Длительность выявленной и документированной на электрокардиограмме (ЭКГ) ЖА составляла не менее 1 года, хотя точный срок существования аритмии оценке не подлежал. Ни у кого из пациентов не было указаний на внезапную смерть у родственников, анамнестических указаний на синкопальные состояния. В анализ не включали пациентов с выявленной в результате контрольных холтеровских мониторных наблюдений устойчивой желудочковой тахикардией (ЖТ) (более 30 с), полиморфной ЖТ или мономорфной ЖТ, приобретающей хотя бы на короткий период времени непрерывно-рецидивирующий характер.
Во всех случаях ЖА проявлялась клиническими симптомами в виде ощущения неритмичных сердцебиений, часто коротких эпизодов учащенного сердцебиения, что сопровождалось разнообразными психоэмоциональными реакциями. Длительность выявленной и документированной на электрокардиограмме (ЭКГ) ЖА составляла не менее 1 года, хотя точный срок существования аритмии оценке не подлежал. Ни у кого из пациентов не было указаний на внезапную смерть у родственников, анамнестических указаний на синкопальные состояния. В анализ не включали пациентов с выявленной в результате контрольных холтеровских мониторных наблюдений устойчивой желудочковой тахикардией (ЖТ) (более 30 с), полиморфной ЖТ или мономорфной ЖТ, приобретающей хотя бы на короткий период времени непрерывно-рецидивирующий характер.
У 46 пациентов (18 мужчин) в возрасте 38±10 (от 17 до 53) лет физикальное, электрокардиографическое, рентгенологическое и эхокардиографическое исследования не выявляли патологии сердца, и ЖА расценена как идиопатическая (ИЖА). У 27 пациентов (12 мужчин) в возрасте 35±10 (от 17 до 49) лет при эхокардиографии (ЭхоКГ) выявляли пролапс митрального клапана (ПМК). При этом отсутствовали признаки миксоматозного поражения створок клапана и митральной регургитации выше II степени. Для включения в анализ допускали данные пациентов с ПМК и неспецифическими изменениями конечной части желудочкового комплекса на ЭКГ в виде отрицательных волн Т в нижних стандартных и левых грудных отведениях.
По данным ЭхоКГ, конечный диастолический размер (КДР) левого желудочка (ЛЖ) не превышал 55 мм, а фракция выброса ЛЖ была выше 60% (ΔS не менее 0,3). Тест с физической нагрузкой на велоэргометре, в обязательном порядке выполнявшийся лицам старше 35 лет, не выявлял ишемии миокарда. У 17 пациентов первое появление ЖА следовало по времени за острой респираторной вирусной инфекцией.
У всех больных имелись ЭКГ в 12 отведениях с зарегистрированной ЖЭ. Анализ локализации источника патологической импульсации проводили по алгоритму F. Zhang и соавт. [8], останавливая его на этапе детализации положения источника в выносящем тракте правого желудочка (ПЖ). Таким образом, выделяли 3 варианта желудочковой эктопической активности (ЖЭА): 1) из выносящего тракта ПЖ с признаками на ЭКГ блокады левой ножки пучка Гиса (БЛНПГ) и отклонением электрической оси сердца вниз, переходной зоной не ранее отведения V4 или, если последнее не выполнялось, индексом длительности зубца R менее 0,5 или амплитудным индексом R/S менее 0,3 в отведениях V1 или V2; 2) из выносящего тракта ЛЖ с признаками БЛНПГ на ЭКГ и отклонением электрической оси вниз при переходной зоне в V2—V3 и индексом длительности зубца R более 0,5 или амплитудным индексом R/S более 0,3 в отведениях V1 или V2; 3) из ЛЖ с признаками блокады правой ножки пучка Гиса на ЭКГ и отклонением электрической оси сердца влево.
Методом количественной оценки ЖЭА служило холтеровское мониторирование (ХМ) ЭКГ, которое выполняли с использованием аппаратуры Del Mar Avionics (регистраторы модели 447 и анализатор аритмий модели 9020А). Регистрацию ЭКГ проводили в двух биполярных отведениях, близких к V1 и V5. Выявленную ЖЭА классифицировали в соответствии с градациями Lown и Wolff [9]. При этом градацию III не рассматривали, если основная морфологическая форма экстрасистол превышала по численности 90% от общего числа желудочковых эктопических сокращений (ЖЭС). Общее число ЖЭС помимо абсолютных значений выражали в виде процентного отношения к общему числу сердечных сокращений, обозначая этот показатель термином «бремя ЖЭА». Под антиаритмическим эффектом аллапинина понимали снижение общего числа ЖЭС более чем на 70% от исходного, снижение числа парных ЖЭС на 90% и более при полном устранении пробежек ЖТ [10]. Проаритмическим эффектом аллапинина считали более чем четырехкратное увеличение общего числа ЖЭС и (или) десятикратное увеличение ЖЭС градации IV или появление новой, более высокой градации ЖЭА [11].
Влияние аллапинина на длительность интервалов ЭКГ оценивали по результатам ХМ, производя измерения через 1 ч после очередного приема препарата по распечатанному на бумаге со скоростью 50 мм/с фрагменту ЭКГ.
Перед назначением аллапинина отменяли любые лекарственные препараты на время, соответствующее не менее 6 периодам их полувыведения, и проводили контрольное ХМ ЭКГ. Аллапинин изначально назначали в фиксированной дозе (75 или 100 мг/сут), определяемой условиями исследовательского протокола, в который включали конкретного пациента. По завершении исследования дозу индивидуально корректировали, наращивая при необходимости для достижения антиаритмического эффекта (критериями невозможности увеличения дозы служили удлинение комплекса QRS на 25% от исходного или наличие побочных действий препарата), либо снижая для устранения побочных действий. Таким образом, для настоящего анализа использованы результаты лечения на фоне индивидуально подобранных доз аллапинина. Контроль действия аллапинина осуществляли на 5—7-е сутки приема препарата в неизменной суточной дозе.
Для длительного лечения отбирали пациентов, у которых в коротком курсе лечений достигали антиаритмический эффект и которые имели возможность регулярно являться в клинику для повторных обследований. Их повторяли каждые 3 мес на протяжении 1-го года лечения, контролируя действие препарата с помощью ХМ ЭКГ. В случае исчезновения эффекта аллапинин отменяли и оценивали уровень ЖЭА на безмедикаментозном фоне. Эту процедуру проводили также в случае длительного отсутствия ЖЭА на фоне лечения аллапинином. Если после пробной отмены аллапинина при ХМ ЭКГ не наблюдали возобновления ЖА или она проявлялась градацией I, лечение не возобновляли вплоть до нового появления жалоб, указывающих на рецидив аритмии.

При сравнении параметрических показателей в случае нормального распределения использовали t-тест Стьюдента для непарных и парных сравнений и, соответственно, ранговые тесты Манна—Уитни или Вилкоксона для распределения, отличного от нормального. При сравнении непараметрических показателей использовали точный критерий Фишера. Нулевую гипотезу отвергали при p<0,05.
Результаты
У пациентов с ИЖА электрокардиографический вариант 1 ЖЭС (рис. 1, А) был представлен в 29 случаях, вариант 2 (рис. 1, Б) — в 14 и вариант 3 (рис. 1, В) в 3 случаях. У пациентов с ПМК — в 13, 11 и 3 случаях соответственно (p>0,36). Таким образом, в целом по группе вариант 1 наблюдали в 58% случаев, вариант 2 — в 34% и вариант 3 — в 8% случаев. На безмедикаментозном фоне общее количество ЖЭС в среднем составило 926±510/ч. «Бремя ЖЭА» — 21,5±11,8%, при этом у 15 пациентов оно не превышало 10%, у 30 было больше 10%, но не превышало 24%, и у 28 было больше 24%. У 23 (32%) пациентов наивысшей была градация ЖЭА IVА, у 28 (38%) — градация IVБ. У остальных 22 (30%) пациентов имелась ЖЭА градации II. В соответствии с принятыми для настоящего анализа критериями ЖЭА во всех случаях была монофокусной.
 В условиях короткого курса лечения действие аллапинина оценивали при дозах от 75 до 150 мг/сут, что в среднем составило 111,6±26 мг/сут. У 4 пациентов (по 2 с ИЖА и ПМК) антиаритмическое действие препарата оценить не удалось из-за необходимости его отмены в связи с неприемлемыми побочными действиями. У остальных 69 пациентов аллапинин значительно снижал число как одиночных, так и групповых ЖЭС. Изменения средних для группы показателей ЖЭА представлены в таблице. Различий по степени снижения общего числа ЖЭС, а также степени снижения числа ЖЭС градации IV, при разных электрокардиографических вариантах ЖЭС не выявлено.
В условиях короткого курса лечения действие аллапинина оценивали при дозах от 75 до 150 мг/сут, что в среднем составило 111,6±26 мг/сут. У 4 пациентов (по 2 с ИЖА и ПМК) антиаритмическое действие препарата оценить не удалось из-за необходимости его отмены в связи с неприемлемыми побочными действиями. У остальных 69 пациентов аллапинин значительно снижал число как одиночных, так и групповых ЖЭС. Изменения средних для группы показателей ЖЭА представлены в таблице. Различий по степени снижения общего числа ЖЭС, а также степени снижения числа ЖЭС градации IV, при разных электрокардиографических вариантах ЖЭС не выявлено.
При индивидуальном рассмотрении антиаритмический эффект достигнут у 51 (74%) из 69 пациентов: у 33 (75%) из 44 с ИЖА и у 18 (72%) из 25 с ПМК (р=0,8). При оценке в общей группе у 17 (24,6%) пациентов отмечено полное подавление ЖЭА, у 15 (21,7%) оно составляло 90% и более. Таким образом, снижение числа ЖЭС на 90% и более произошло у 46,4% пациентов. Проаритмическое действие аллапинина проявилось у 1 пациента с ПМК в виде увеличения общего числа ЖЭС на 143% и появления отсутствовавшего в контроле одиночного эпизода ЖТ из 3 комплексов QRS. Зависимости эффективности аллапинина от электрокардиографических вариантов ЖЭС не выявлено.
Под действием аллапинина происходило удлинение интервалов PQ и QRS, но длительность интервала QTс не претерпевала значимых изменений. Средняя за сутки частота ритма сердца значимо увеличивалась под влиянием препарата (см. таблицу). Только в 3 случаях прекращение наращивания дозы аллапинина было обусловлено достижением предельно допустимого удлинения интервалов ЭКГ. Развития нарушений предсердно-желудочкового проведения не наблюдали.
У 36 (49,3%) пациентов на фоне лечения аллапинином отмечены побочные действия. В 4 (5,5%) случаях они потребовали прекращения лечения до оценки его результатов, проявившись в виде устойчивого повышения артериального давления (2 случая), упорной синусовой тахикардии (1 случай) и аллергической реакции в виде крапивницы (1 случай). У других 32 (43,8%) больных они не требовали отмены препарата и проявлялись головокружением в 31 (42,5%) случае, которое в 3 случаях сопровождалось нарушением фиксации взгляда, в 1 — чувством оглушенности, и в 3 случаях — общей слабостью и сердцебиением. У 1 (1,4%) пациента имелись жалобы на постоянное учащенное сердцебиение.
Среди 19 пациентов, у которых антиаритмический эффект аллапинина проявлялся подавлением общего числа ЖЭС менее 90%, у 10 (53%) имелись внекардиальные побочные действия препарата, в то время как из 32 пациентов с подавлением ЖЭА более 90% побочные действия отмечены у 11 (34,4%) (р=0,25).
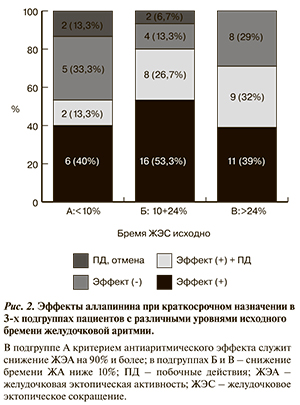
 Для дополнительной оценки действия аллапинина пациенты разделены на 3 подгруппы в зависимости от исходной величины «бремени ЖЭА»: подгруппа А с «бременем ЖЭА» ниже 10% (n=15), подгруппа Б — от 10 до 24% (n=30), и подгруппа В с «бременем ЖЭА» более 24% (n=28). На фоне приема аллапинина общее число ЖЭС в этих подгруппах снизилось соответственно на 73,7, 71,4 и 76,7% (р=0,9). В подгруппе А у 8 (53,3%) пациентов снижение числа ЖЭС превысило 90%, но у 2 сопровождалось переносимыми побочными эффектами (рис. 2).
Для дополнительной оценки действия аллапинина пациенты разделены на 3 подгруппы в зависимости от исходной величины «бремени ЖЭА»: подгруппа А с «бременем ЖЭА» ниже 10% (n=15), подгруппа Б — от 10 до 24% (n=30), и подгруппа В с «бременем ЖЭА» более 24% (n=28). На фоне приема аллапинина общее число ЖЭС в этих подгруппах снизилось соответственно на 73,7, 71,4 и 76,7% (р=0,9). В подгруппе А у 8 (53,3%) пациентов снижение числа ЖЭС превысило 90%, но у 2 сопровождалось переносимыми побочными эффектами (рис. 2).
У 2 пациентов имелись непереносимые побочные эффекты. В подгруппе Б снижение «бремени ЖЭА» ниже 10% отмечено у 24 (80%) пациентов, и у 7 из них имелись переносимые побочные эффекты препарата. У этих 24 пациентов «бремя ЖЭА» снизилось с 16,9±4,2 до 3,1±3,1% (p<0,0001). Кроме того, в 2 случаях отмечена непереносимость аллапинина в начальных дозах (см. рис. 2). В подгруппе В снижение «бремени ЖЭА» ниже 10% отмечено в 20 (71%) случаях и в 9 из них имелись переносимые побочные эффекты препарата (см. рис. 2). У этих 20 пациентов «бремя ЖЭА» снизилось с 34,6±8,9 до 2,1±2,7% (p<0,0001). В целом в подгруппах Б и В снижение «бремени ЖЭА» ниже 10% произошло у 44 из 58 (75,9%) пациентов.
Длительное лечение аллапинином продолжили 26 больных, из них у 13 в коротком курсе имелись побочные эффекты препарата. В 2 случаях они стали причиной прекращения лечения на 3 и 4 мес наблюдения. Еще 5 больных в сроки от 3 до 12 мес предпринимали попытки уменьшения дозы препарата для устранения побочных действий, что приводило к исчезновению антиаритмического эффекта препарата и вынуждало восстановить прежнюю эффективную дозу. Один пациент умер на 2-м месяце наблюдения из-за несчастного случая, обстоятельства которого исключали связь с заболеванием и лечением. Один пациент выбыл из-под наблюдения после 9 мес, и еще у 1 пациентки лечение прекращено на 10-м месяце по причине спонтанной ремиссии ЖА (см. ниже). Остальные 16 пациентов продолжали наблюдаться в сроки от 12 до 66 мес (мода 36 мес), принимая аллапинин непрерывно в неизменной дозе, подобранной в коротком курсе. При этом в контрольных исследованиях не обнаружено случаев исчезновения антиаритмического эффекта или появления новых побочных действий препарата.
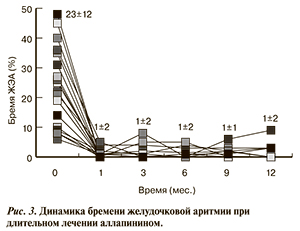
При регулярных ХМ ЭКГ, проводимых на протяжении 1-го года наблюдения, отмечалось стойкое снижение уровня ЖЭА. Исходно «бремя ЖЭА» составило у 25 пациентов (исключая умершего) 23±12%. Начиная с 1-го месяца наблюдения, этот показатель оставался сниженным до уровня 1±2% на протяжении всех 12 мес (рис. 3). Если исходно у 11 пациентов «бремя ЖЭА» превышало 24%, у 9 находилось в пределах от 10 до 24% и у 5 было ниже 10%, то на фоне лечения аллапинином на протяжении всего периода наблюдения ни у одного пациента оно не превышало этого последнего уровня (см. рис. 3).
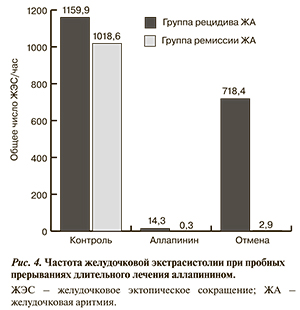
В сроки от 6-го до 36-го месяца наблюдения 18 больным (3 повторно) производили пробную отмену аллапинина. При этом у 10 аритмия возобновлялась, и число ЖЭС значимо не отличалось от контрольного перед началом лечения (рис. 4). У 8 пациентов в сроки до 1 нед после отмены препарата ЖА не возобновлялась или проявлялась ЖЭ градации I. При этом средние значения общего числа ЖЭС не отличались значимо от значений на фоне лечения аллапинином (см. рис. 4). У 2 из этих больных в сроки до 1 мес после пробной отмены аритмия рецидивировала, и лечение аллапинином возобновлено с прежним успехом. У 6 пациентов (24% от общего числа длительно наблюдавшихся) имелась стойкая спонтанная ремиссия ЖА.
Обсуждение
ЖЭ у лиц без признаков ОЗС не сопряжена с развитием опасных ЖА и не несет в себе повышенного риска тяжелых сердечно-сосудистых осложнений, таких как инфаркт миокарда, внезапная сердечная смерть (ВСС) и сердечная недостаточность [13, 14]. Это же относится к ЖЭ, которая сопровождает ПМК, если последний не приводит к выраженной митральной регургитации и отсутствует миксоматозная дегенерация клапанов [15]. На этом основании утвердилось мнение о доброкачественном характере этих ЖА и об отсутствии необходимости специального анти-аритмического лечения таких больных, до тех пор, пока не возникнут новые отягчающие обстоятельства [2, 3, 12].
 В случаях, когда эти ЖА вызывают выраженные болезненные ощущения и приводят к снижению качества жизни, на фоне рациональной психотерапии прибегают к назначению лекарственных ААП, среди которых препаратами первого ряда являются β-адреноблокаторы [16]. При необходимости возможно применение других ААП, прежде всего класса IС [2, 3, 12, 17]. Они высокоэффективны в устранении ЖА у пациентов с различной патологией сердца, но рекомендации их использования у пациентов с ЖА при нормальном сердце не основываются на специальных исследованиях и носят характер экстраполяции результатов, полученных в общей группе больных. При этом полагают, что отсутствие ОЗС и сердечной недостаточности определит минимальный риск проаритмических реакций, а это в сочетании с низким потенциалом внекардиальных побочных эффектов указанных препаратов создаст благоприятное соотношение пользы и риска лечения. Сопоставление результатов настоящего исследования с результатами изучения эффективности аллапинина в смешанной группе [5] (эффективность в 74% случаев против 74,2% соответственно) подтверждает справедливость таких предположений.
В случаях, когда эти ЖА вызывают выраженные болезненные ощущения и приводят к снижению качества жизни, на фоне рациональной психотерапии прибегают к назначению лекарственных ААП, среди которых препаратами первого ряда являются β-адреноблокаторы [16]. При необходимости возможно применение других ААП, прежде всего класса IС [2, 3, 12, 17]. Они высокоэффективны в устранении ЖА у пациентов с различной патологией сердца, но рекомендации их использования у пациентов с ЖА при нормальном сердце не основываются на специальных исследованиях и носят характер экстраполяции результатов, полученных в общей группе больных. При этом полагают, что отсутствие ОЗС и сердечной недостаточности определит минимальный риск проаритмических реакций, а это в сочетании с низким потенциалом внекардиальных побочных эффектов указанных препаратов создаст благоприятное соотношение пользы и риска лечения. Сопоставление результатов настоящего исследования с результатами изучения эффективности аллапинина в смешанной группе [5] (эффективность в 74% случаев против 74,2% соответственно) подтверждает справедливость таких предположений.
Реальные данные о применении ААП класса IC у таких пациентов крайне скудны. В единственном, вероятно, в настоящее время исследовании, в котором целенаправленно изучали эффективность препарата класса IC (пропафенон) при ЖА у пациентов без ОЗС [18], показано, что он эффективен в коротком курсе лечения не более чем у 42% пациентов с проявлениями аритмогенности и непереносимости в 2% случаев и необходимостью прекращения лечения в последующем из-за побочных действий у 17% пациентов. Столь низкие показатели эффективности обусловлены жесткими критериями антиаритмического действия, требующими 90% и более снижения числа ЖЭС. Это кажется вполне оправданным, поскольку задачей лечения являлось устранение клинических симптомов аритмии. Сравнение этих данных с нашими результатами показывает, что аллапинин при указанных критериях обладает сопоставимыми показателями эффективности и безопасности: 46% эффективность в сочетании с 11% переносимых побочных эффектов, и 5% непереносимых побочных эффектов. В сопоставлении с эффективностью альтернативного метода лечения таких больных — радиочастотной катетерной абляцией (РЧА) аритмогенных очагов, непосредственная эффективность которой составляет 70—90% [17], результат вполне соответствует устоявшемуся мнению об ограниченных возможностях лекарственной терапии данной аритмии. Однако для окончательных суждений о возможностях лекарственной антиаритмической терапии (ААТ) более внимательного рассмотрения требует вопрос о конечных целях лечения и соответствующих им критериях эффективности.
Прежде всего, следует отметить, что не только болезненные субъективные ощущения определяют необходимость лечения, направленного на устранение ЖЭА. У пациентов с нормальным сердцем ЖА при доброкачественном течении с точки зрения развития тяжелых аритмических осложнений и ВСС имеет, тем не менее, неблагоприятные последствия, связанные с развитием особой формы кардио-миопатии (КМП), проявляющейся расширением полости ЛЖ и развитием его дисфункции вплоть до клинических проявлений сердечной недостаточности [19—22]. Природа ее до конца не установлена, но показано, что в развитии этой КМП важнейшую роль играет число ЖЭС, т.е. «бремя ЖЭА» [22—24]. Риск развития КМП при «бремени ЖЭА» ниже 10% практически отсутствует, в то время как при «бремени ЖЭА» 24% и выше развитие этого осложнения прогнозируется с высокой точностью [23]. Важно, что устранение ЖЭА с помощью РЧА приводит к нормализации размеров ЛЖ и нормализации его фракции выброса [17, 21—23]. Еще раньше показано, что у больных дилатационной КМП спонтанное или связанное с назначением ААП (амиодарон) уменьшение числа ЖЭС приводит к уменьшению КДР ЛЖ и к увеличению фракции выброса ЛЖ [19, 20]. Степень выраженности снижения числа ЖЭС, достаточного для обеспечения обратного развития КМП, никогда не подлежала точному определению, но в одной из указанных работ минимальная степень снижения ЖЭС составила 65%, а в другой среднее снижение составило 74% на 3-м месяце лечения амиодароном и 83% через 6 мес. В то же время из анализа наиболее важных исследований по использованию РЧА для устранения ЖЭА с целью обратного развития КМП [17] следует, что положительный результат в отношении восстановления нормальной сократительной функции миокарда достигался при снижении ЖЭС с «бремени ЖЭА» в среднем от 22—34 до 0,2—2,6%. Эти последние значения «бремени ЖЭА» вполне сопоставимы с нашими результатами лечения аллапинином у тех пациентов, у которых под влиянием препарата происходило снижение «бремени ЖЭА» ниже 10% (подгруппы Б и В). Сопоставляя эти данные, можно сделать предположение, что снижение частоты ЖЭА до величин «бремени ЖЭА» 10% и ниже может предотвратить развитие КМП. Эту же величину можно использовать в качестве более уместного с точки зрения целей лечения критерия эффективности ААТ у тех пациентов, у которых аритмия протекает мало- или бессимптомно.
Такой подход существенно расширяет рамки понятия эффективности ААП и, напротив, суживает понятие не-эффективности ААТ, являющееся одним из основополагающих в определении показаний к РЧА [3]. Ограничением настоящего исследования является неспособность его доказательно утвердить данное предположение. Безусловно, вопрос требует дальнейшего изучения, но наши результаты длительного лечения аллапинином, хотя и ограниченные числом пациентов, указывают на правомерность данного подхода. Ни у одного из пациентов на фоне лечения аллапинином сроком не менее 1 года не наблюдалось развития симптомов сердечной недостаточности, при том что «бремя ЖЭА» на протяжении всего периода наблюдения не только не превышало 10%, а реально находилось на очень низком уровне. Большим упущением работы, однако, было отсутствие систематического контроля показателей функции ЛЖ с помощью ЭхоКГ.
Возвращаясь к показаниям по использованию РЧА для лечения больных с ЖА в отсутствие ОЗС [3], следует отметить, что при всей очевидности преимуществ этого метода в плане эффективного устранения ЖЭС общим направлением является выжидательная тактика с использованием лекарственной ААТ и относительно длительным наблюдением за пациентом [13, 14].
В качестве объяснения можно выделить две основные причины. Первая — риск развития тяжелых осложнений вмешательства, оцениваемый частотой около 3% [17]. Такой риск абсолютно недопустим у пациентов, отнесенных в нашем исследовании к подгруппе А (показание класса III в отсутствие симптоматики), а на успех лечения аллапинином у них можно рассчитывать более чем в 50% случаев. У пациентов с высокой частотой ЖЭА и риском развития КМП (подгруппы Б и, особенно, В) соотношение риска и пользы РЧА в отсутствие симптоматики определяет показания на уровне класса IIb. Рассчитывать на успех лечения аллапинином у этой категории больных, имея в виду новые предлагаемые критерии эффекта, можно почти в 76% случаев. Исключение составят пациенты, у которых развилась КМП. Диагностика КМП, вызванной ЖЭА, основывается на ее полной обратимости на фоне устранения ЖА. До этого момента нет никакой возможности дифференцировать ее от других форм КМП, назначение аллапинина при которых противопоказано [2, 3].
Второй причиной, оправдывающей выжидательную тактику в отношении РЧА, служит частое развитие спонтанной ремиссии ЖА, которая оценивается частотой около 25% [13, 14], как и в нашем исследовании. Природа ее не установлена, и одно из направлений поиска нацеливает на изучение роли воспалительных и иммунных, в частности, аутоиммунных факторов [25—27]. Аллапинин, проявляя устойчивое сохранение антиаритмической активности и не выявляя новых побочных действий, может рассматриваться в качестве важного средства длительного лечения больных с доброкачественной ЖА, позволяя путем периодических перерывов в лечении выявлять наступление спонтанной ее ремиссии.
Существенным недостатком аллапинина является высокая частота развития переносимых внекардиальных побочных действий, что, безусловно, затрудняет его клиническое использование. Клинический опыт подсказывает, что меры, направленные на замедление всасывания препарата из желудочно-кишечного тракта, приводят к снижению частоты и степени выраженности этих побочных действий. В этом плане требуются усилия по совершенствованию лекарственной формы препарата.
Заключение
Антиаритмический препарат аллапинин высокоэффективен в лечении больных с желудочковой экстрасистолией в отсутствие органических заболеваний сердца и может рассматриваться как важный элемент комплексной терапии у таких больных.



