Сахарный диабет (СД) 2-го типа является одним из важнейших факторов риска (ФР) развития сердечно-сосудистых заболеваний [1]. В настоящее время СД 2-го типа рассматривается как эквивалент ишемической болезни сердца (ИБС) в отношении риска развития сердечно-сосудистых осложнений (ССО) [2]. Значительное число больных с СД 2-го типа и ИБС подвергаются операции коронарного шунтирования (КШ), которая признана оптимальным методом реваскуляризации у больных данной категории [2—4]. Доля больных СД 2-го типа составляет от 15 до 40% от общего числа прооперированных [5]. Очевидно, что наличие СД влияет на прогноз исходов вмешательств. Однако этот фактор не всегда учитывается при оценке риска. Так, заболевание не было включено в первую версию шкалы риска смерти при КШ EuroSCORE, а во второй ее версии учтен только инсулинозависимый СД [6, 7].
КШ на работающем сердце обеспечивает низкую летальность и небольшое количество осложнений [8]. Ранние ССО после КШ на работающем сердце у больных ИБС с СД 2-го типа и ФР их развития мало изучены. Все это и обусловило цель данной работы: определить ФР развития ранних ССО после КШ на работающем сердце у больных ИБС и СД 2-го типа.
Материал и методы
В исследование включали больных ИБС с сопутствующим СД 2-го типа, которым выполнена операция КШ без искусственного кровообращения на работающем сердце. Критерии включения: мужчина или женщина в возрасте от 45 до 70 лет, наличие СД 2-го типа с уровнем гликированного гемоглобина (HbA1c) <13%, стабильной стенокардии напряжения III или IV функционального класса (ФК), изолированного поражения ствола левой коронарной артерии (ЛКА) >50% или проксимального поражения передней нисходящей артерии (ПНА), или трехсосудистого поражения коронарных артерий (КА) без проксимального стеноза ПНА и ствола ЛКА и высоким риском по шкале SYNTAX [4], гипогликемическая терапия пероральными сахароснижающими препаратами (ПССП) или инсулином, наличие синусового ритма в предоперационном периоде. Критерии исключения: нестабильная стенокардия, клапанные пороки сердца, СД 1-го типа, кетоацидоз, уровень HbAlc ≥13%, операция КШ по экстренным показаниям, реваскуляризация миокарда в предшествующие 12 мес. Набор материала осуществлялся в 2010—2013 гг.
Анализировали частоту развития ССО в течение 7 сут после операции. При этом учитывали случаи острого послеоперационного инфаркта миокарда (ИМ) по критериям Европейского общества кардиологов (2012) [9], ишемического инсульта/транзиторной ишемической атаки [10], фибрилляции предсердий (ФП) по электрокардиограмме. Всего за период наблюдения зарегистрировано 47 ССО. В конт-рольную группу методом случай—контроль включили 141 пациента без ССО, сопоставимых по полу, возрасту и соответствующих критериям включения, из расчета 1:3. Таким образом, в исследование включены 188 больных, средний возраст которых составил 59,0 (55—63,5) года, из них 160 (85,1%) мужчин.
Всем пациентам проводили электрокардиографию покоя при поступлении и мониторирование электрокардиограммы во время операции и в блоке интенсивной терапии. Рассчитывали индекс массы тела (ИМТ). Учитывали уровень артериального давления (АД) при поступлении. Осуществляли допплер-эхокардиографию с оценкой фракции выброса (ФВ) левого желудочка по Симпсону. Рассчитывали скорость клубочковой фильтрации (CКФ) по MDRD. Проводили дуплексную ультрасонографию брахиоцефальных и периферических артерий. Атеросклероз артерий нижних конечностей (АСНК) диагностировали по Фонтену [11], атеросклероз брациоцефальных артерий (АСБЦА) — при наличии бляшки или утолщении интимы—медии более 1,3 мм [11]. Учитывали перенесенный ранее ИМ по данным анамнеза и эхокардиографии, характер поражения КА по данным коронарографии, количество шунтов, длительность операции, объем интраоперационной кровопотери, прогнозируемую летальность по шкале EuroSCORE II [7].
Из 188 пациентов 78 (41,5%) принимали метформин, 86 (45,7%) — препараты сульфонилмочевины (глимепирид — 7, гликлазид — 28, глибенкламид — 51), 24 (12,8%) пациента находились на инсулинотерапии. В периоперационном периоде 43 пациента продолжали принимать ПССП до начала операции, 121 — на 2-й день пребывания в стационаре переведены на терапию инсулином короткого действия в начальной дозе 18 ед/сут с последующей коррекцией по уровню глюкозы в крови [12] и 24 продолжали получать инсулин.
При поступлении определяли уровень HbA1c. Измеряли концентрацию глюкозы в плазме крови глюкозооксидазным методом в 8:00, 11:00, 13:00, 15:00, 18:00, 21:00 в первый день госпитализации, в течение суток перед операцией и однократно во время операции. Таким образом, у каждого больного осуществлялось 13 измерений глюкозы. Рассчитывали индивидуальный средний уровень глюкозы и ее вариабельность (путем вычисления среднеквадратического отклонения) за указанные суточные периоды. Определяли долю значений уровня глюкозы, ниже рекомендуемого для периоперационного периода целевого диапазона [13]. С этой целью вычисляли процент измерений глюкозы <6,1 ммоль/л от всех измерений глюкозы за сутки наблюдения. Учитывали случаи гипогликемии <2,8 ммоль/л [13].
В изучаемых группах сравнивали медианы перечисленных показателей. Для выявления ФР развития ССО проводили пошаговый логистический регрессионный анализ. В уравнение регрессии в качестве независимых включали признаки, медиана или доля которых статистически значимо различались в изучаемых группах. Рассчитывали отношение шансов (ОШ) и 95% доверительные интервалы (ДИ) развития ССО при наличии каждого из выявленных ФР.
Статистическую обработку данных выполняли с помощью пакета программ Statistica 6.1 for Windows, IBM SPSS Statistics 22.0. Для каждой выборки проверяли гипотезу о нормальности распределения по Колмогорову—Смирнову, Шапиро—Вилку. Поскольку был выявлен непараметрический характер распределения, средние значения представляли в виде медианы (Ме) и интерквартильного интервала (25-й процентиль; 75-й процентиль). Статистическую значимость различий средних оценивали по критерию Манна—Уитни (U), относительных показателей — по χ².
Результаты
Послеоперационный ИМ зарегистрирован у 18 (9,6%), острое нарушение мозгового кровообращения (ОНМК)/транзиторная ишемическая атака (ТИА) — у 2 (1,1%) и ФП — у 27 (14,4%) больных. В 1-е сутки после операции ИМ выявлен у 11 больных (у 6 — крупноочаговый переднеперегородочный, у 5 — задней стенки), на 2-е сутки — у 5 (мелкоочаговый переднебоковой), на 3-и и 4-е сутки — у 2 (крупноочаговый высоких боковых отделов). Зафиксирован один летальный случай в 1-е сутки после операции на фоне крупноочагового переднеперегородочного ИМ вследствие тромбоза шунта ПНА. Нефатальное ОНМК в виде ишемического инсульта в вертебробазилярном бассейне развилось у одного пациента на 3-и сутки после операции, ТИА — у одного пациента на 2-е сутки после операции. ФП обнаружена у 6 больных сразу после основного этапа операции, что потребовало выполнения электрической кардиоверсии. У 21 больного эпизоды ФП возникли в сроки от 12 до 36 ч после операции и были купированы медикаментозно.
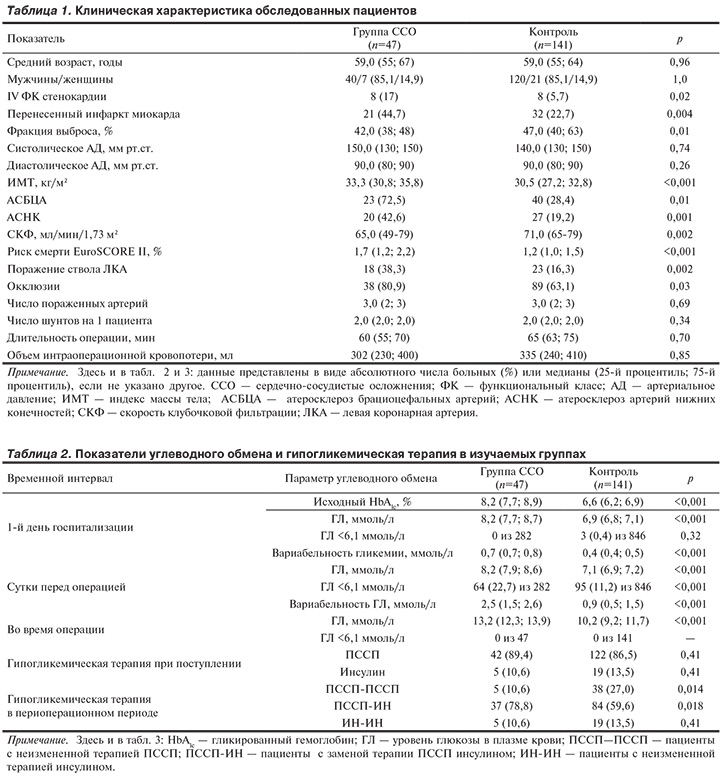
В табл. 1 представлена клиническая характеристика изучаемых групп.
Согласно представленным данным, группа с ССО имела более тяжелое течение стенокардии, большее число больных с перенесенным ИМ, АСНК и АСБЦА, больший ИМТ, более низкие ФВ левого желудочка и уровень СКФ, более высокий риск смерти по шкале EuroSCORE II, а также более тяжелое поражение КА.
В табл. 2 представлены параметры контроля уровня глюкозы в крови в изучаемых группах.
Таким образом, в группе ССО были выше исходный уровень HbAlc, средние уровни глюкозы и ее суточной вариабельности на всех изученных этапах периоперационного периода, большее число случаев уровня глюкозы <6,1 ммоль/л накануне операции. Случаев гипогликемии <2,8 ммоль/л не выявлено. Соотношение используемых видов терапии при поступлении в группах не различалось, тогда как в периоперационном периоде в группе ССО доля больных со сменой терапии ПССП на инсулин была больше.
После пошагового включения в логистическую регрессионную модель переменных, средние значения или доля которых статистически значимо различались по результатам сравнительного межгруппового анализа (см. табл. 1, 2), получена совокупность предикторов развития ССО, обеспечивающая наибольшую точность их прогнозирования (табл. 3).

Таким образом, независимыми ФР развития ССО при операции КШ на работающем сердце у больных СД 2-го типа явились наличие АСНК, вариабельность уровня глюкозы в крови при поступлении и накануне операции, замена гипогликемической терапии с ПССП инсулином.
Обсуждение
В последние годы отмечается рост числа операций КШ у больных СД 2-го типа, что связано как с увеличением заболеваемости СД 2-го типа, так и с тем, что КШ признано предпочтительным методом реваскуляризации миокарда именно у больных СД [3, 4]. Сведения о ближайших результатах КШ у больных ИБС с СД 2-го типа ограничены и противоречивы [5]. В ряде работ проводилось сравнение ближайших результатов КШ в неоднородной группе, у отдельных больных операция проведена с искусственным кровообращением, у других — на работающем сердце [5]. В настоящем исследовании были проанализированы клинические и ангиографические данные, а также состояние углеводного обмена на различных этапах периоперационного периода с целью выявления предикторов развития ранних ССО при КШ на работающем сердце у пациентов с ИБС и СД 2-го типа.
Результаты показали, что среди ССО преобладает послеоперационная ФП (14,4%), нередко встречается ИМ (9,6%), реже всего — ОНМК (1,1%). При этом у пациентов с ССО были закономерно большими тяжесть стенокардии и степень поражения КА, ниже СКФ и, соответственно, выше расчетный риск смерти по шкале EuroSCORE II. Наши данные соответствуют результатам других работ, посвященных КШ у больных СД 2-го типа [5].
Связь состояния гликемического контроля и периоперационных сердечно-сосудистых исходов является предметом активного изучения в последние годы. По нашим данным, у пациентов с периоперационными ССО параметры углеводного обмена свидетельствовали в целом о более тяжелом течении СД 2-го типа, что подтвердило ранее опубликованные сведения [3, 5].
Нами впервые установлены ФР развития ССО при КШ на работающем сердце у больных СД 2-го типа. Оказалось, что вероятность ранних осложнений увеличивается у пациентов с распространенным атеросклерозом, нестабильным периоперационным уровнем глюкозы в крови и при переводе с ПССП на инсулинотерапию перед операцией. В то же время на исходы КШ практически не влияли объем хирургического вмешательства и величина кровопотери.
Атеросклероз периферических артерий является, с одной стороны, маркером диабетической макроангиопатии, а с другой – указывает на высокий риск смерти больных СД от ССО [14]. После операции КШ, по данным исследования CASS [15], у пациентов с АСНК риск смерти, развития неврологических осложнений, почечной недостаточности в течение 30 дней были выше, чем в отсутствие АСНК [16]. Таким образом, периферический атеросклероз является признанным предиктором неблагоприятного прогноза реваскуляризации миокарда, в том числе, как показали наши данные, у больных СД 2-го типа при операции на работающем сердце.
Следует подчеркнуть, что риск развития ССО в изученной нами выборке больных СД 2-го типа в большей степени зависел не от абсолютного уровня глюкозы в крови, но от размаха его колебаний. Ранее было показано, что вариабельность уровня глюкозы в крови является самостоятельным предиктором поздних осложнений СД. По-видимому, высокая вариабельность уровня глюкозы в крови увеличивает вероятность развития гипогликемии. Это, в свою очередь, является ФР развития ССО, вероятно, вследствие компенсаторной симпатико-адреналовой активации [17, 18]. Аналогичные данные были недавно получены у больных, перенесших КШ c искусственным кровообращением [19]. Можно предположить, что даже незначительные, но частые эпизоды снижения уровня глюкозы в крови <6,1 ммоль/л увеличивают вероятность осложнений операции. Повышение риска развития ССО при переводе находящихся в стабильном состоянии пациентов с ПССП на инсулин, по нашему мнению, также связано с увеличением амплитуды колебаний уровня глюкозы в крови при многократном введении инсулина короткого действия, что выявлено нами впервые у больных данной категории.
Полученные результаты указывают на необходимость обязательного учета состояния периферических артерий и суточной вариабельности уровня глюкозы в крови при оценке прогноза КШ на работающем сердце. Кроме того, полученные нами данные указывают на необходимость обсуждения вопроса о целесообразности и безопасности перевода всех пациентов перед операцией КШ на инсулинотерапию.
Заключение
Среди ранних сердечно-сосудистых осложнений коронарного шунтирования на работающем сердце у больных ишемической болезнью сердца и сахарным диабетом 2-го типа чаще всего регистрируются фибрилляция предсердий и инфаркт миокарда. Факторами риска развития сердечно-сосудистых осложнений явились клинически значимый атеросклероз сосудов нижних конечностей, суточная вариабельность уровня глюкозы в крови при поступлении и накануне операции, перевод перед операцией больных с контролируемым углеводным обменом с пероральных сахароснижающих препаратов на инсулин короткого действия.



