Введение
Филаггрин (ФЛГ) представляет собой структурный кальций, связывающий белок кожного покрова. Он практически нерастворим и содержит массу гистидина. ФЛГ принимает участие в процессах формирования рогового слоя. Продукты распада ФЛГ являются компонентом натурального увлажняющего фактора, который способствует формированию защитного барьера кожного покрова, препятствуя избыточной трансэпидермальной потере воды, колонизации патогенами, проникновению аллергенов и токсических веществ [1, 2].
Известно, что ФЛГ образуется из более крупного белка – профилаггрина. Профилаггрин является одним из основных компонентов кератогиалиновых гранул [1]. Профилаггрин не способен взаимодействовать с кератиновым цитоскелетом, тогда как ФЛГ и его более мелкие пептидные производные легко связывают кератин. Переход от гранулярного предшественника, профилаггрина, к диффузно распределенному белку, ФЛГ, происходит в ответ на инициирующий сигнал, который до сих пор неизвестен [3].
Согласно данным литературы, экспрессия ФЛГ и его локализация в клетке претерпевают последовательные изменения. На ранних этапах дифференцировки кератиноцитов происходит свободная диффузия образующегося профилаггрина в цитоплазму. Ряд ферментов, таких как фурин [4], каспаза-14 [5], матриптаза и простазин [6], оказывают влияние на профилаггрин. В результате протеолиза и дефосфорилирования профилаггрин распадается на молекулы ФЛГ [1]. Этот механизм позволяет активировать усиление экспрессии ФЛГ, вызванной положительной обратной связью. Однако диффузия профилаггрина уменьшается, когда его локальная концентрация достигает порога, необходимого для образования кератогиалиновых гранул [7]. Такая динамика должна сопровождаться активным контролирующим механизмом для поддержания «безопасного» внутриклеточного уровня ФЛГ, на котором клетка может выжить, т.е. ниже определенного «порога апоптоза» [8].
Продукты, полученные из профилаггрина/ФЛГ, эффективно удаляются из цитозоля кератиноцитов посредством захвата и экспорта внеклеточными везикулами/экзосомами. Этот механизм позволяет клеткам поддерживать безопасные цитоплазматические уровни мономеров ФЛГ в процессе интенсификации синтеза профилаггрина, что обеспечивает образование кератогиалиновых гранул. Экзосомы, содержащие ФЛГ, обнаруживаются в кровотоке, что свидетельствует о транспорте внеклеточными везикулами белка ФЛГ. Примечательно, что содержание ФЛГ в везикулах остается относительно неизменным, однако у пациентов с АтД увеличивается количество экзосом с данным белком в крови [7].
Получается, что накопление белка ФЛГ в мономерной форме может инициировать преждевременную гибель кератиноцитов, а небольшие внеклеточные везикулы, секретируемые кератиноцитами, могут захватывать ФЛГ и транспортировать из кератиноцитов. Таким образом, удаление избытка ФЛГ из кератиноцитов предотвращает их преждевременную гибель и дисфункцию эпидермального барьера [7].
На сегодняшний день существует множество экспериментальных работ по изучению мутаций гена ФЛГ, немного реже встречаются исследования по уровню ФЛГ в коже, однако крайне мало работ, посвященных изучению содержания ФЛГ в сыворотке крови.
В 2018 г. Z. Rasheed et al. провели исследование уровня ФЛГ в сыворотке крови у 810 пациентов детского возраста, 395 (48,7%) из которых имели аллергические заболевания, такие как АтД, бронхиальная астма и аллергический ринит. В результате исследования выявлено, что уровни ФЛГ чрезвычайно высоки у детей с АтД. Более низкие значения определены в группе с бронхиальной астмой и аллергическим ринитом. Полученные данные позволили предположить, что оценка уровня ФЛГ в сыворотке крови может быть полезной для оценки прогрессирования АтД и для выяснения механизмов, участвующих в патогенезе данного заболевания [9].
Вторым более масштабным исследованием при участии той же группы авторов было изучение уровня ФЛГ в сыворотке крови у 1246 взрослых пациентов с различными атопическими заболеваниями. АтД был представлен в 216 (17,33%) случаях, 360 (28,89%) человек имели смешанную патологию, включая и АтД. В качестве контрольной группы были исследованы 410 образцов сыворотки крови здоровых людей. В результате исследования выявлено значительное повышение уровня ФЛГ в группах с атопией по сравнению с контрольной группой. Наибольшие средние значения уровня ФЛГ в сыворотке крови наблюдались в группе с АтД. Эти результаты показали, что белок ФЛГ явно связан почти со всеми атопическими расстройствами, особенно выраженные изменения отмечаются при АтД [10].
В последние годы отмечается тенденция к росту заболеваемости АтД среди беременных женщин. В 50% случаев течение АтД на фоне беременности ухудшается, в 25% улучшается и в 25% не изменяется [11]. Механизмы развития обострения АтД на фоне беременности до конца не изучены. Известно, что важную роль играет сочетание дисфункций иммунной системы и кожного барьера [12]. В связи с этим интерес представляет изучение роли ФЛГ как биомаркера дисфункции кожного барьера при обострении АтД у беременных женщин.
Цель исследования: оценить уровень ФЛГ в сыворотке крови у беременных женщин с АтД.
Методы
Исследование проводилось на клинических базах кафедры аллергологии и иммунологии с курсом дерматовенерологии и косметологии ПИУВ – филиала ФГБОУ ДПО РМАНПО Минздрава РФ – с 2020 по 2022 г. Проведение исследования одобрено на заседании Локального этического комитета при ПИУВ – филиала ФГБОУ ДПО РМАНПО Минздрава РФ (протокол № 13 от 20.11.2020). Дизайн исследования: простой открытый клинический сравнительный проспективный рандомизированный контролируе-мый.
Обследованы 139 женщин. На первом этапе были сформированы четыре группы. Основную группу составили 76 беременных женщин с обострением АтД, первую группу сравнения – 23 небеременные женщины с обострением АтД, вторую группу сравнения– 20 беременных женщин без АтД, контрольную группу– 20 небеременных женщин без АтД.
Средний возраст беременных женщин с обострением АтД, включенных в исследование, составил 29,27±0,57 года, небеременных женщин с обострением АтД – 28,95±1,00 год, беременных женщин без АтД – 28,65±1,50 года, небеременных без АтД – 28,4±1,37 года. Статистически значимых различий по возрасту выявлено не было (p>0, 05).
Критерии включения в исследование: обострение АтД, информированное добровольное согласие.
Критерии исключения: крайне тяжелая степень тяжести АтД, психические заболевания, туберкулез любой локализации в активной фазе и в анамнезе, тяжелые и декомпенсированные заболевания печени и почек, сердечно-сосудистой системы; тяжелое и декомпенсированное течение эндокринных заболеваний, включая сахарный диабет, аутоиммунные и онкологические заболевания, нежелание участвовать в исследовании.
Диагноз «АтД, обострение» устанавливали на основании совокупности соответствующих критериев, изложенных в клинических рекомендациях по АтД 2023 г. [13].
На втором этапе были проведены клиническое и лабораторно-иммунологическое исследования. Клиническое исследование включило осмотр, сбор анамнеза, определение степени тяжести по индексу SCORAD (Scoring of Atopic Dermatitis) [13]. Значение индекса SCORAD до 25 баллов соответствовало легкой степени тяжести, 25–50 – средней и более 50 баллов – тяжелой степени тяжести.
В качестве биологического материала для проведения иммунологического исследования были приняты образцы крови, полученные от пациенток. Уровень ФЛГ определялся в сыворотке крови методом иммуноферментного анализа коммерческими наборами Cloud–Clone Corp. (CCC, США) Elisa Kit for Filaggrin.
На третьем этапе проводили статистическую обработку с помощью пакета прикладных программ IBM SPSS Statistics 23.0 на персональном компьютере. Данные представлены в виде медианы (Ме) и квартилей [25%; 75%]. Качественные признаки оценивали и сравнивали с помощью χ2-критерия Пирсона. При статистическом анализе был использован тест Манна–Уитни для двух независимых выборок. Результаты считали статистически значимыми при р<0,05. Для определения статистической взаимосвязи применяли метод корреляционного анализа по Спирмену. Силу корреляционной связи оценивали по коэффициенту корреляции (R): при значении меньше 0,30 – слабая связь, 0,30–0,69 – умеренная, 0,70–1,00 – сильная связь.
Результаты
В результате исследования получены следующие данные: индекс SCORAD при первом осмотре у беременных женщин с обострением АтД составил 28,2 [19,30; 36,20] балла, у небеременных женщин с обострением АтД – 32,20 [25,45; 46,35] балла. Различия были статистически не значимыми (тест Манна–Уитни; р>0,05).
По значению индекса SCORAD выявлено: легкая степень тяжести в 23 (30,3%) случаях у беременных женщин, средняя степень тяжести – в 39 (51,3%), тяжелая степень тяжести – в 14 (18,4%). У небеременных женщин: в 7 (30,4%) случаях легкая степень тяжести, в 10 (43,5%) – средняя, в 6 (26,1%) – тяжелая степень тяжести. Статистически значимого различия между группами не обнаружено (χ2-критерий; р>0,05).
Значения ФЛГ существенно разнились в группах. Уровень ФЛГ в сыворотке крови у беременных женщин с АтД составил 9,72 [8,31; 14,77] нг/мл, у небеременных женщин с АтД – 7,65 [5,65; 8,29] нг/мл (рис. 1), у беременных женщин без АтД – 5,50 [3,91; 6,84] нг/мл (рис. 2), у небеременных женщин без АтД – 3,03 [2,22; 3,96] нг/мл (рис. 3).
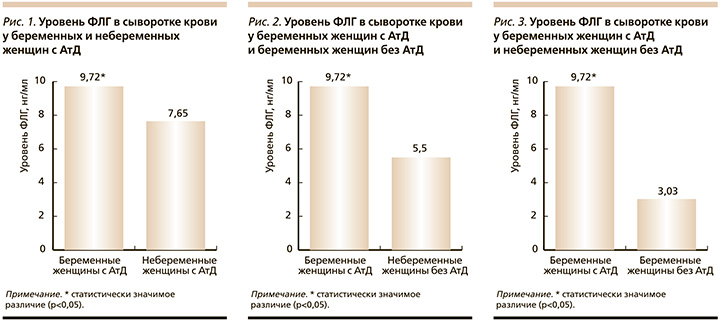
В группе беременных женщин с обострением АтД уровень ФЛГ был статистически значимо выше, чем в группах небеременных женщин с АтД, беременных и небеременных женщин без АтД (тест Манна–Уитни; р<0,05). Кроме того, у небеременных женщин с АтД уровень ФЛГ был достоверно выше, чем в группе небеременных женщин без АтД (тест Манна–Уитни; р=0,001). Уровень ФЛГ у беременных женщин без АтД был статистически значимо выше, чем у небеременных без АтД (тест Манна–Уитни; р=0,001), что свидетельствует об изменениях в функционировании кожного барьера при беременности и требует дальнейшего углубленного изучения.
Мы предположили, что содержание ФЛГ в сыворотке крови увеличивается с утяжелением кожного воспалительного процесса при АтД. Для подтверждения данной теории был проведен корреляционный анализ, который показал наличие умеренной связи уровня ФЛГ в сыворотке крови и индекса SCORAD (R=0,653; р=0,001, прямая связь).
При распределении уровня ФЛГ в сыворотке крови по степени тяжести АтД были получены следующие значения (см. таблицу).

Уровень ФЛГ в сыворотке крови при тяжелой степени АтД был достоверно выше, чем при средней и легкой степенях тяжести (тест Манна–Уитни; р=0,001). Между средней и легкой степенями тяжести АтД статистически значимого различия не выявлено (тест Манна–Уитни; р=0,264).
При легкой степени тяжести АтД уровень ФЛГ между группами беременных и небеременных женщин с АтД достоверно не различался (тест Манна–Уитни; р=0,180). При средней и тяжелой степенях тяжести уровень ФЛГ у небеременных женщин статистически был значимо ниже, чем у беременных (тест Манна–Уитни; р<0,05).
Обсуждение
В ходе исследования установлено, что беременные и небеременные женщины с АтД имеют более высокие значения ФЛГ в сыворотке крови, чем беременные и небеременные женщины без АтД. Полученные данные сопоставимы с результатами зарубежных исследований уровней ФЛГ в сыворотке крови [9, 10], что свидетельствует о наличии изменений в кожном покрове и гиперактивации защитного механизма кератиноцитов у пациентов с АтД. Однако у беременных женщин c АтД данные процессы протекают наиболее выраженно, что подтверждается статистически значимым увеличением уровня ФЛГ в сыворотке крови по сравнению с небеременными женщинами с АтД. Вероятнее всего, за счет нарушения процессов распада ФЛГ происходит накопление мономеров ФЛГ в кератиноцитах, в результате чего активируется защитный механизм в клетках с захватом белка экзосомами и транспортом из клеток кожи в кровоток [7].
Утяжеление течения АтД сопровождается повышением уровня ФЛГ в сыворотке крови. Следовательно, определение ФЛГ в сыворотке крови можно рассматривать как биомаркер тяжести течения обострения АтД при беременности.
Заключение
На сегодняшний день изучение роли ФЛГ в патогенезе АтД при беременности представляется актуальным. Беременные женщины с обострением АтД имеют высокие значения уровня ФЛГ в сыворотке крови, поэтому ФЛГ можно рассматривать как важный биомаркер обострения АтД при беременности. Более детальное исследование роли ФЛГ при АтД, в т.ч. оценка мутаций гена ФЛГ, определение ФЛГ в коже и в сыворотке крови у беременных в корреляции, могло бы поспособствовать формированию более полноценной картины механизмов развития обострения АтД на фоне гестации, а также разработке специфического лечения для пациентов данной группы.
Вклад авторов. Е.А. Орлова – концепция и дизайн исследования, редактирование. Ю.А. Кандрашкина, О.А. Левашова – сбор и обработка материала. Е.М. Костина – статистическая обработка данных. Ю.А. Кандрашкина – написание текста.
Дополнительная информация
Публикация статьи осуществляется в рамках диссертационной работы: «Особенности течения атопического дерматита у беременных с учетом нейроиммунологических нарушений и оптимизация терапии».



