Термин «идиопатические» аритмии (ИА) подразумевает нарушения ритма и проводимости у больных (как правило, моложе 60 лет) без структурных заболеваний сердца или, что точнее, с неустановленной причиной. Вместе с тем наличие аритмии свидетельствует об изменении электрических свойств сердца, в основе которого могут лежать такие латентные и трудно диагностируемые состояния, как хронический миокардит, различные генетические кардиомиопатии, миокардио-дистрофии (МКД), амилоидоз и пр. Поэтому термин ИА мы берем в кавычки и ставим цель по возможности выявить этиологию аритмии. В предшествующих наших публикациях отражены результаты эндомиокардиальной биопсии (ЭМБ) у больных с ИА, которая при определенном отборе оказалась высокоинформативной и позволила разработать критерии неинвазивной нозологической диагностики [1—3]. Данная работа является продолжением исследования с использованием установленных критериев у широкого круга больных.
Цель исследования: установить нозологическую природу ИА с помощью комплексного клинико-морфологического обследования и оценить эффективность дифференцированного этиотропного и патогенетического лечения.
Материал и методы
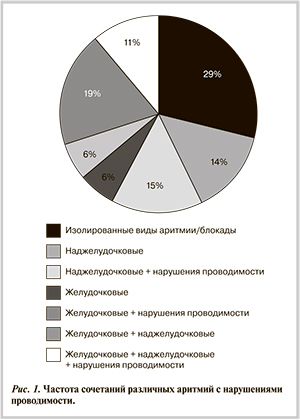
В исследование включены 190 больных 16—76 лет (средний возраст 45,3±14,8 года, 117 женщин) с различными аритмиями (табл. 1), главным образом, наджелудочковой и желудочковой экстрасистолией (НЖЭ/ЖЭ) и мерцательной аритмией (МА); более чем у 2/3 пациентов аритмии сочетались между собой и/или с нарушениями проводимости (рис. 1).
Критериями исключения были дилатация левого желудочка (ЛЖ) (конечный диастолический размер (КДР) ≥5,5 см), гипертрофия ЛЖ >14 мм, фракция выброса (ФВ) ЛЖ<50%, инфаркт миокарда, инфекционный эндокардит, операции на открытом сердце в анамнезе, пороки сердца, гипертрофическая и рестриктивная кардиомиопатия (КМП), верифицированные диффузные болезни соединительной ткани, системные васкулиты, тиреотоксическое сердце.
 Средний возраст, в котором начиналась аритмия, составил 40,5±14,6 года — 47,2±13,2 года у больных с МА, 20,4±3,1 года у больных с атриовентрикулярной (АВ) блокадой; давность аритмии составила 30,0 (10,0; 84,0) мес. У каждого больного было в среднем использовано 3 (от 1 до 8) антиаритмических препарата (ААП). Медиана числа НЖЭ составила 946 (250; 5050) в сутки, ЖЭ — 5404 (1184; 14778) в сутки. МА расценена как пароксизмальная, персистирующая и постоянная у 79,7, 14,9 и 5,4% больных соответственно. Стенокардия имелась у 23,2% больных и не отражала наличие ишемической болезни сердца — ИБС (см. ниже); ожирение отмечено у 35,3% (в основном 1-й степени), артериальная гипертония (АГ) — у 41,6% (у 16,8% 3-й степени, но в отсутствие признаков гипертрофии ЛЖ, его диастолической дисфункции, а также анамнестической связи АГ и аритмии); минимальные симптомы сердечной недостаточности (СН) — у 14,2%, в том числе у пациентов с МА. Данные факторы ни в одном случае не могли рассматриваться как ведущая причина аритмии.
Средний возраст, в котором начиналась аритмия, составил 40,5±14,6 года — 47,2±13,2 года у больных с МА, 20,4±3,1 года у больных с атриовентрикулярной (АВ) блокадой; давность аритмии составила 30,0 (10,0; 84,0) мес. У каждого больного было в среднем использовано 3 (от 1 до 8) антиаритмических препарата (ААП). Медиана числа НЖЭ составила 946 (250; 5050) в сутки, ЖЭ — 5404 (1184; 14778) в сутки. МА расценена как пароксизмальная, персистирующая и постоянная у 79,7, 14,9 и 5,4% больных соответственно. Стенокардия имелась у 23,2% больных и не отражала наличие ишемической болезни сердца — ИБС (см. ниже); ожирение отмечено у 35,3% (в основном 1-й степени), артериальная гипертония (АГ) — у 41,6% (у 16,8% 3-й степени, но в отсутствие признаков гипертрофии ЛЖ, его диастолической дисфункции, а также анамнестической связи АГ и аритмии); минимальные симптомы сердечной недостаточности (СН) — у 14,2%, в том числе у пациентов с МА. Данные факторы ни в одном случае не могли рассматриваться как ведущая причина аритмии.
Помимо стандартного обследования (в том числе определения уровня гормонов щитовидной железы) абсолютному большинству пациентов проведено определение:
1) IgG к вирусам герпетической группы, Коксаки В и ДНК вирусов герпеса 1, 2 и 6-го типов, вируса Эпштейна—Барр (ВЭБ), varicellae-zoster virus, цитомегаловируса в крови методом полимеразной цепной реакции (лаборатория «ДНК-технология», центр молекулярной диагностики НИИ эпидемиологии);
2) антикардиальных антител (АТ) в 3 лабораториях: «МедБиоСпектр» (IgM и IgG к миокардиальному антигену, в норме 1:100); «Иммункулус» (естественные аутоантитела (аутоАТ) класса IgG к цитоплазматическому белку кардиомиоцитов (КМЦ) CoS05—40 и белку мембран CoM015—15; NO-синтетазе; β1-адренорецепторам, в норме от –30 до +20); лаборатории иммуногистохимии Федерального научного центра трансплантологии и искусственных органов им. акад. В.И. Шумакова: АТ к антигенам эндотелия, КМЦ, гладкой мускулатуры, волокон проводящей системы сердца (в норме 1:40), антинуклеарный фактор (АНФ) с антигеном сердца быка (в норме нет); использовали чистые АТ против IgG человека, меченные флюоресцеинизотиоцианатом, а также люминесцирующие сыворотки против IgG человека; учет проводили на микроскопах Leica («Laborlux», DM4000В) при увеличении 400 и 600.
Прочие инструментальные исследования выполняли индивидуально (табл. 2). Показания к ЭМБ и ее результаты представлены в нашей предшествующей публикации [3].
 В зависимости от диагноза проводилась базисная терапия.
В зависимости от диагноза проводилась базисная терапия.
В контрольную группу включен 51 человек (средний возраст 50,0±14,1 года, 31 женщина) — здоровые добровольцы, пациенты гастроэнтерологического профиля без заболеваний сердца, а также больные с ИБС, гипертрофической КМП, пороками сердца: уровень антикардиальных АТ определялся у 36 из них, вирусный геном в крови — у всех.
Проведение исследования (в том числе формы информированного согласия на ЭМБ и отдельные виды лечения) одобрено Межвузовским комитетом по этике.
Статистическая обработка результатов исследования осуществлялась с помощью программы SPSS 11.5.
Методы статистического анализа включали параметрические и непараметрические методы сравнения, данные представлены как М±d (среднее ± одно стандартное отклонение) в случае нормального распределения или в виде медианы с указанием интерквартильного диапазона. Различия считали статистически значимыми при p<0,05.
Результаты
Диагностика ИА. Дифференциально-диагностическое значение в нозологической диагностике имели следующие клинико-инструментальные данные:
1. Анамнез. Отягощенный семейный анамнез (случаи внезапной смерти, имплантации электрокардиостимулятора (ЭКС) в возрасте моложе 40 лет) выявлен в 4,2% случаев, ангины и хронический тонзиллит — в 37,9%, клинические проявления герпетической инфекции — в 20,5%. У 24 (12,6%) больных имелись системные иммунные проявления: бронхиальная астма, аллергическая риносинусопатия, аутоиммунный тиреоидит, псориаз, хронический гломерулонефрит и др. Из заболеваний и синдромов с возможной или доказанной генетической природой выявлены марфаноподобный фенотип, минимальные признаки миопатии и др. (4,7%).
Синдром апноэ во время сна легкой и средней степени определен у 3 (1,6%) больных без ожирения. Тиреотоксикоз имелся в анамнезе у 5 больных (полностью компенсирован) и развился в ходе исследования еще у 5 (5,3%). Гинекологические заболевания у 25,6% женщин были представлены миомой матки, эндометриозом, мастопатией и пр. Средний уровень употребления алкоголя был низким — 0,29 балла (медиана 0 (0; 1)) по шкале от 0 до 3; не выявлено корреляции с видом аритмии. Злоупотреблявших алкоголем не было.
У 29,5% больных давность появления аритмии составила меньше года, у 37,9% она развилась остро, у 36,3% отмечена связь дебюта/обострений аритмии с инфекцией (респираторные вирусные инфекции, ангина, герпес, пневмония, рожа и др.). Эти признаки составили полную анамнестическую триаду, которая выявлена в 10,5% случаев. У 4,3% пациенток имелась связь дебюта/обострения ЖЭ с беременностью и родами, в том числе в результате полной отмены ААП.
2. Лабораторные данные. Небольшие общевоспалительные изменения в крови, преимущественно одного из показателей, выявлены у 5,8—15,8% больных (табл. 3), изолированные изменения иммунологических маркеров — у 7,9%, повышение уровня АТ к различным стрептококкам — у 39,5% (при посеве отделяемого с миндалин получен рост стрептококков и стафилококков в диагностически значимых титрах).
3. Данные инструментальных исследований. В результате целенаправленного поиска в ряде случаев удалось выявить специфичные признаки. Так, при анализе стандартной электрокардиограммы (ЭКГ) отмечены эпсилон-волна (n=3), Бругада-паттерн I типа (при назначении ААП I класса, n=2), синдром ранней реполяризации (n=18, 9,5%; мужчины составили 88,9%, были достоверно моложе остальных и чаще страдали АВ блокадой II—III cтепени), интервал PQ ≤0,12 с (n=9, 4,7%; исключительно женщины; при чреспищеводной стимуляции предсердий в 1 случае индуцирована МА), патологические зубцы Q в III отведении (n=5, 2,6%). Изменения зубцов Т выявлены в 32,6% случаев.
По данным эхокардиографии (ЭхоКГ) у отдельных больных выявлены увеличение левого (23,2%; 79,1±29,7 мл), правого (11,6%; 79,4±18,5 мл) или обоих (8,4%) предсердий, которое слабо коррелировало с наличием МА (преимущественно пароксизмальной); минимальная гипертрофия ЛЖ (n=9, 4,7%), субклиническая митральная (n=64, 33,7%) и трикуспидальная (n=54, 28,4%) регургитация, пролапс/прогиб митрального клапана (n=48, 25,3%), дополнительные хорды (n=28, 14,7%), минимальный выпот в перикарде (n=5, 2,6%) и некомпактный миокард ЛЖ у 2 пациентов (подтвержден при мультиспиральной компьютерной томографии — МСКТ).
Исследование коронарных артерий (коронарография/МСКТ) выполнено 56 (29,5%) больным: стенозы ≥50% выявлены у 6 (10,7% обследованных); в одном случае проведено стентирование передней межжелудочковой артерии. В целом отсутствовала корреляция стенокардии с наличием стенозов, видом аритмии, уровнем липидов, но выявлялась ишемическая депрессия сегмента ST: стенокардия, по-видимому, в значительной степени отражала поражение мелких (интрамиокардиальных) коронарных артерий. При МСКТ субэпикардиальное отсроченное накопление отмечено в 9,5% случаев, жировые включения в миокарде правого желудочка (ПЖ) или обоих желудочков — у 3 больных.
Магнитно-резонансная томография (МРТ) с гадолинием выполнялась в основном при подозрении на аритмогенную дисплазию ПЖ (АДПЖ; 26,8% случаев): жировые включения в ПЖ выявлены в 29,3% случаев, его истончение — в 39%, дис-/гипокинезия — в 61/34,1%, микроаневризма — в 2,4%, расширение выходного отдела — в 51,2%, увеличение КДР — в 48,8%, снижение ФВ — в 12,2%; отсроченное накопление в ЛЖ отмечено у 7 (63,6%) из 11 больных, уплотнение и спайки листков перикарда — у 51,2%. По 1 пациенту имели признаки некомпактного миокарда и липоматозной гипертрофии межпредсердной перегородки.
При сцинтиграфии миокарда в покое диффузное неравномерное распределение выявлено в 36,5% случаев, очаговое нарушение перфузии — в 5,8%, их сочетание — в 3,6%. Ни у одного из больных с очаговым поражением и/или стресс-индуцированной ишемией значимых коронарных стенозов не выявлено, но у 2/3 имелись «рубцовые» изменения на ЭКГ.
Кроме того, проводилась серодиагностика возможного миокардита. Вирусный геном в крови выявлен достоверно чаще, чем в контрольной группе (24,4 и 13,7% соответственно; p<0,001). Определялись ВЭБ (n=19), вирус герпеса человека 6-го типа (HHV6, n=3), сочетание этих вирусов (n=2), цитомегаловирус (n=2), вирусы гепатита В (n=2) и гепатита С (n=1), в контрольной группе — только ВЭБ и HHV6. Титры IgG к вирусам герпеса были повышены в 3—4 раза у большинства больных, IgG к парвовирусу В19 — у 71,2%; реже отмечались IgG к HHV6 (50,2%) и 10-кратное повышение IgG к цитомегаловирусу (13,8%); титры IgG к вирусам Коксаки повышены в 2 раза у 43,9% обследованных.
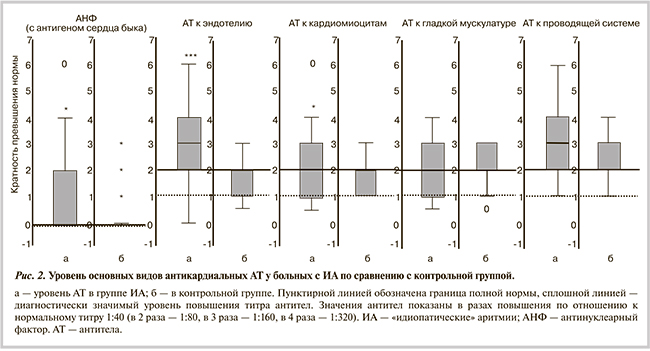
У пациентов с ИА оказался достоверно выше, чем в контрольной группе, уровень всех антикардиальных АТ, за исключением АТ к антигенам гладкой мускулатуры (рис. 2). Специфический АНФ выявлен в 41,5% (в том числе в титре 1:160—1:320 в 20%) случаев, в наибольшей степени повышались титры АТ к эндотелию и проводящей системе сердца. Для удобства анализа все комбинации АТ были разбиты на кластеры (табл.4). Наличие вируса в крови сопровождалось достоверно большим титром АНФ (среднее повышение в 1,7 раза по сравнению с нормальным средним титром 1:40 у больных без вирусного генома в крови; p<0,01), что доказывало роль вирусов в индукции иммунного ответа и позволило выделить этих больных в отдельный (5-й) кластер. Средняя частота пароксизмов МА по 8-балльной шкале при наличии АНФ/без него составила 5,6/3,3 (p<0,05): иммунная активность коррелировала с тяжестью аритмии.

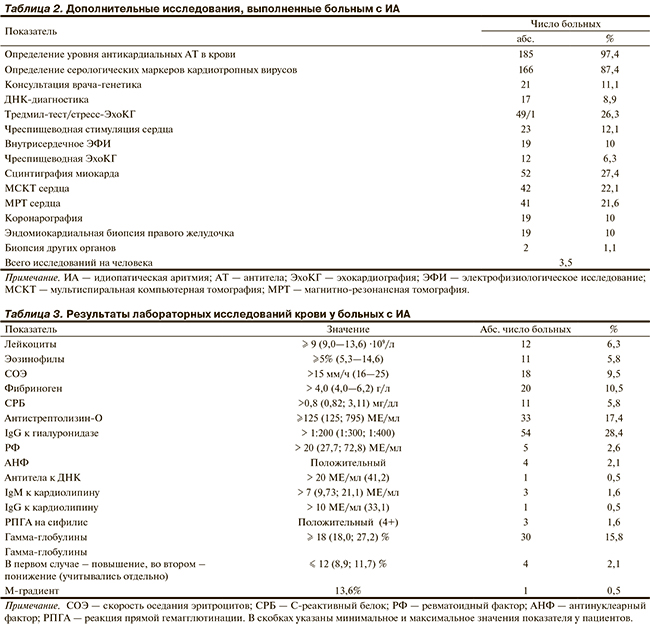
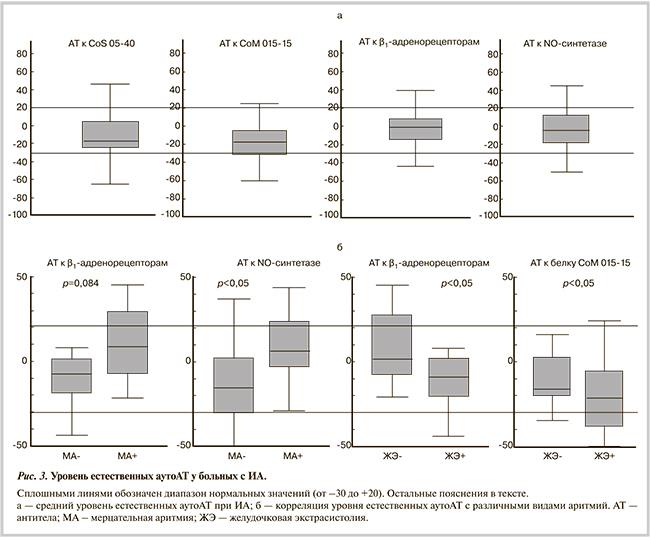
У большинства пациентов был повышен также титр IgG к миокардиальному антигену (1:300 у 41,6% и 1:400 у 39%). В единичных случаях выявлены IgM. Уровень естественных аутоАТ (в том числе к β1-рецепторам) оказался в пределах нормы (рис. 3). Однако отмечена корреляция отдельных видов АТ с наличием МА и ЖЭ, что доказывает возможную роль аутоАТ в патогенезе конкретных аритмий.
Наконец, 19 пациентам с высокой вероятностью миокардита (или необходимостью дифференцировать его от генетических заболеваний) была выполнена биопсия ПЖ, по данным которой, нормальной гистологической картины не получено ни в одном случае: у 14 больных диагностированы иммуновоспалительные заболевания (миокардит, эндомиокардит, миокардиальный и системный васкулит), у 4 — генетическая КМП (АДПЖ, болезнь Фабри, неуточненная).
ДНК-диагностика не завершена (проводится в лаборатории РНЦХ РАМН), к настоящему времени диагноз подтвержден генетически у 3 больных с АДПЖ (выявлены мутации в гене плакофиллина-2 PKP2, десмоглеина DSG2 и десмина DES) и у пациента с болезнью Фабри (мутация в гене галактозидазы X-GAL).
На основании сопоставления данных ЭМБ и результатов неинвазивного обследования был разработан алгоритм нозологической диагностики. По совокупности клинико-лабораторно-инструментальных данных диагноз миокардита мог рассматриваться как определенный или вероятный, в случае морфологического подтверждения он становился достоверным. Базовыми для диагноза миокардита у больных с ИА являются следующие признаки: 1) наличие полной анамнестической триады; 2) повышенные в 3—4 раза титры антикардиальных АТ; 3) наличие в крови генома кардиотропных вирусов, IgM или (что менее значимо) 5—10-кратного повышения уровня IgG к кардиотропным вирусам.
Чем выше кластер АТ, тем более вероятен диагноз миокардита; в то же время отсутствие вирусов, компонентов анамнестической триады ни в коей мере не исключает миокардита. Диагноз устанавливается по сочетанию основных и определенного количества дополнительных критериев (см. табл. 4). Последние распределены по 3 основным группам:
1) острое начало; связь дебюта/обострений аритмии с инфекцией; давность менее года; системные иммунные проявления; ангины в анамнезе; герпес в анамнезе; иммунодефицит (частые инфекции); сочетание различных нарушений ритма и проводимости; эффект от противовоспалительной (стероидной) терапии в анамнезе;
2) повышение уровня антистрептолизина-О; острофазовые показатели в крови (особенно в сочетании с субфебрилитетом); повышение содержания неспецифических иммунных маркеров (РФ, АТ к ДНК, кардиолипину), снижение уровня комплемента;
3) лабильные/отрицательные зубцы Т, патологические зубцы Q, комплексы QS в различных отведениях (II, III, aVF, V1—V6); атриомегалия; стенокардия/положительные нагрузочные тесты при неизмененных коронарных артериях; диффузное неравномерное распределение радиофармпрепарата при сцинтиграфии; субэпикардиальное отсроченное накопление контрастного препарата (КТ/МРТ); выпот в полости перикарда/ спайки.
Диагноз генетической КМП мы расценивали как достоверный при выявлении патогенной мутации либо специфичных биохимических признаков (при болезнях накопления), как определенный — при наличии критериев конкретных КМП (АДПЖ, синдрома Бругады и пр.), отягощенного семейного анамнеза, признаков периферической миопатии или иных генетических маркеров, некомпактного миокарда, как вероятный — при изолированном характере аритмии (особенно ЖЭ и АВ-блокады), возрасте моложе 40 лет, наличии ранней реполяризации, отдельных критериев (нейтропения, повышение уровня креатинфосфокиназы/лактата в крови, малые критерии АДПЖ и пр.).
Для верификации диагноза может использоваться биопсия скелетных мышц, кожи и других органов. Любая генетическая КМП может сочетаться с миокардитом, поэтому ее диагностика проводится независимо. В то же время отсутствие признаков миокардита расценивается в пользу первичной КМП.
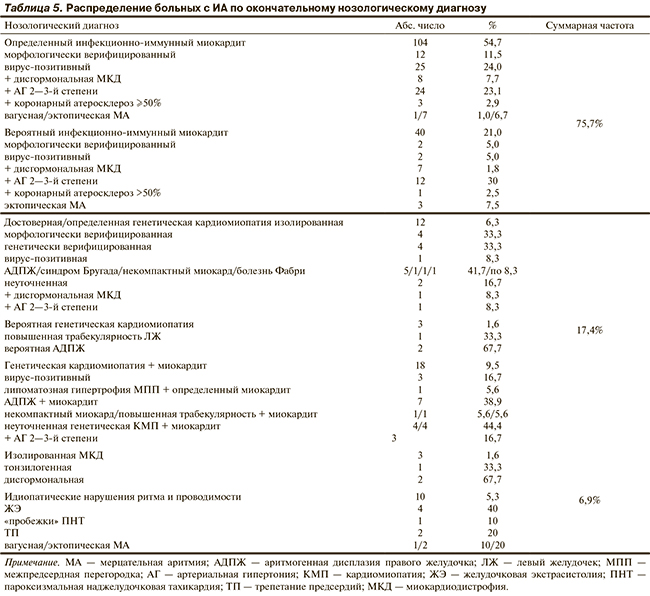
Применение этого алгоритма позволило с той или иной степенью достоверности установить нозологический диагноз абсолютному большинству пациентов с ИА (табл. 5). Собственно идиопатическими остались 5,3% из них. Диагноз МКД (изолированной, но чаще в сочетании с другими причинами аритмии) устанавливали при наличии указаний на гинекологические заболевания, хронический тонзиллит (в отсутствие данных, подтверждающих миокардит), связь аритмии с этими заболеваниями, изменений зубца Т преимущественно в правых грудных отведениях.
Доля миокардита, определенного и вероятного, была наибольшей в этиологической структуре НЖЭ и МА (85,9 и 82,4% соответственно), доля генетических КМП — у больных с устойчивой и неустойчивой желудочковой тахикардией (83,3 и 40% соответственно) и АВ-блокадой II и III степени (50 и 80% соответственно). Наиболее часто (в 19% случаев) не удавалось установить причину трепетания предсердий. Первично хроническое течение миокардита отмечено у 59,9% больных, сочетание 2 причин аритмии и более, в том числе воспалительных и генетических, — у 25%. Среди 12 пациентов с эктопической МА (непрерывно рецидивирующие, устойчивые к ААП пароксизмы в сочетании с ранней НЖЭ) у 10 диагностирован миокардит и у 2 идиопатическая МА; при ваготонической МА соотношение составило 1/1: очевидно, что электрофизиологические варианты МА не являются отдельной нозологической формой.
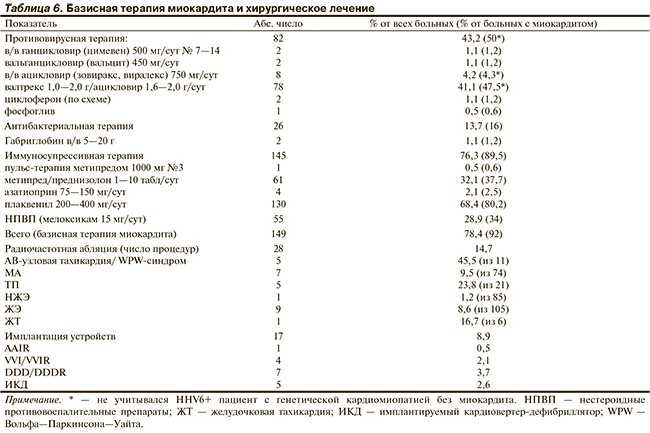
Лечение ИА. В соответствии с поставленным диагнозом лечение носило дифференцированный характер: большинству пациентов с миокардитом помимо кардиотропных и ААП была назначена базисная терапия (табл. 6). При наличии признаков активной вирусной инфекции лечение начинали с противовирусной терапии (ацикловир, ганцикловир, внутривенный иммуноглобулин): элиминация вируса из крови достигнута в 84,6% случаев, наибольшей устойчивостью к лечению (67,7%) отличался вирус HHV6. Антибактериальная терапия назначена отдельным пациентам с хроническим тонзиллитом при положительном результате посева отделяемого с миндалин. Побочных реакций не было.
Затем с учетом тяжести аритмий, их резистентности к лечению, активности миокардита, наличия вирусного генома в крови/миокарде, генетической КМП, противопоказаний к иммуносупрессивной терапии (ИСТ) выбирали один из режимов лечения: 1 — без ИСТ (17,3%), 2 — гидроксихлорохин (плаквенил, 46,3%), 3 — средние дозы метилпреднизолона (метипред, 4—28 мг/сут), в том числе в сочетании с плаквенилом (24,7%), 4 — метипред 32—48 мг/сут, в том числе с плаквенилом или азатиоприном (11,7%). Нестероидные противовоспалительные средства (мелоксикам 15 мг/сут и др.) назначали в течение 14—60 дней в сочетании с плаквенилом.
В 32,4% случаев ИСТ была комбинированной. Средняя доза и продолжительность приема составили для плаквенила 200 мг/сут и 6 (6; 12) мес соответственно, для метипреда 16 (16; 32) мг/сут и 6 (4; 13) мес, для азатиоприна 118,8±37,5 мг/сут и 10,5 (3,8; 33,0) мес. После назначения стартовой дозы стероидов в течение 1—2 мес ее снижали на 1/4—1/2 таблетки в неделю до поддерживающей дозы в среднем 4 мг/сут (от 2 до 8 мг/сут). Плаквенил в разные сроки был отменен из-за побочных эффектов у 7 (5,4%) больных. Доза азатиоприна снижена у 2 больных из-за нейтропении, временная отмена из-за инфекций потребовалась всем пациентам. Обусловившие необходимость увеличения темпа снижения дозы побочные эффекты стероидов развились у 13 больных, четко зависели от дозы и были полностью обратимы.
ИСТ приводила к достоверному снижению титра антикардиальных АТ, максимально выраженному в первые 6 мес и при использовании наиболее агрессивного режима. При снижении доз/отмене препаратов отмечалось некоторое возрастание титров без полной утраты эффекта. Адекватная исходной тяжести ситуации терапия позволила получить примерно одинаковый конечный результат во всех группах, сгладив исходные различия. Агрессивная ИСТ, назначенная при наихудших исходных данных, оказалась эффективна у отдельных больных с устойчивой аритмией. Так, средняя частота пароксизмов МА (по 8-балльной системе) снизилась недостоверно при 1-м режиме терапии; с 3,5 до 1,0 при 2-м режиме, с 6,0 до 3,0 при 3-м режиме и с 8,0 до 4,0 при 4-м режиме (p<0,005), т.е. с ежедневных пароксизмов до ежемесячных. Средняя эффективность ААП достоверно увеличилась в 3-й и 4-й группах (p<0,01), но существенно не изменилась в 1-й и 2-й группах. Распределение больных по наиболее эффективному ААП отражено на рис. 4. Случаев проаритмии, несмотря на высокую частоту миокардита и использование ААП I класса, не отмечено.
В целом у больных с воспалительной этиологией аритмий ИСТ позволила улучшить общий антиаритмический эффект лечения (табл. 7, рис. 5): только в группе миокардита удалось в 16,7% случаев при полном антиаритмическом эффекте отменить ААП, суммарно в 45,8% достигнут полный антиаритмический эффект (при генетических КМП в 24,2%, при ИА/МКД — в 46,2%), полная неэффективность лечения отмечена в 10,4% (в сравнении с 9,1 и 23,1%), потребность в хирургическом лечении — в 16% (в сравнении 39,4 и 53,8%). У больных с миокардитом также наиболее часто встречалось волнообразное течение (для изолированных генетических форм не характерно): отчетливая смена ремиссий и обострений отмечена в 15,3—22,2% случаев. Развитие хотя бы одного обострения зафиксировано у 29,7% больных с миокардитом.
Причинами обострений были интеркуррентные инфекции, отмена или быстрое снижение доз иммунодепрессантов, амиодарон-индуцированный тиреотоксикоз. Такое течение болезни делает необходимой длительную и непрерывную поддерживающую базисную терапию с периодическим увеличением доз препаратов во время обострений. Больные с истинными ИА отличались либо хорошим антиаритмическим эффектом терапии, либо его полным отсутствием, чем и обусловлена высокая частота выполнения радиочастотной абляции (РЧА) в этой нозологической подгруппе.
Результаты РЧА у пациентов с миокардитом (преимущественно по поводу МА) не отличались от результатов в других нозологических подгруппах: процедура выполнялась на фоне максимально возможного подавления активности воспалительного процесса и поддерживающей ИСТ. В 2 случаях (в том числе при идиопатической МА) потребовалась повторная процедура. У 1 пациента с МА/ТП процедура РЧА осложнилась развитием полной АВ-блокады, имплантирован постоянный ЭКС.
У 1 пациента с признаками некомпактного миокарда после успешной РЧА по поводу политопной ЖЭ отмечено развитие пароксизмов МА/трепетания предсердий. В остальных случаях эффект был удовлетворительным.
Средняя длительность наблюдения составила 14 (6; 36,5) мес, максимальный срок превысил 10 лет. Причина смерти единственной пациентки 46 лет с миокардитом осталась неясной (больная умерла вне клиники). Все тромбоэмболические осложнения (5 инсультов, транзиторная ишемическая атака) развились у больных с МА различной этиологии еще до включения в исследование. В целом не отмечено развития СН, значимой динамики параметров ЭхоКГ: у пациентов с миокардитом это позволяет констатировать стабильный аритмический вариант болезни.
Обсуждение
В литературе практически отсутствуют сообщения о комплексном обследовании и лечении пациентов с ИА: обычно анализ касается лишь отдельных аспектов проблемы. Наибольшее число работ посвящено изучению маркеров системного воспаления, в частности, С-реактивного белка (СРБ): показано его повышение у больных с идиопатической МА [4—6], однако причинно-следственные связи неясны: установлены как бóльшая частота МА у больных с увеличением уровня СРБ [7], так и обратная зависимость уровня СРБ от индукции МА [8, 9]. Повышение уровня других медиаторов воспаления (интерлейкина-6, α-фактора некроза опухоли и пр.) выявлено не только при ИА [6, 10—14], но и при аритмиях вследствие других различных заболеваний [15, 16], что может свидетельствовать о глобальной роли воспаления в патогенезе аритмий либо отражать вторичное воспаление. Во всяком случае опираться только на определение воспалительных маркеров при постановке диагноза и выборе лечения у больных с ИА не представляется возможным.

Изучение роли отдельных видов аутоАТ расширило представления о патогенезе ИА, но не дало ключа к определению их нозологической природы и, тем более, к лечению. В частности, уровень АТ к β1-адренорецепторам, имитирующих эффекты β-миметиков [17], был повышен по сравнению с таковым в контроле при наджелудочковых ИА [18, 19], нарушениях проводимости [20]; «неадекватной» синусовой тахикардии [21], доказано их неблагоприятное влияние на прогноз [22]. Блокада действия этих аутоАТ может быть одним из механизмов антифибрилляторного эффекта β-адреноблокаторов. Тем не менее профилактическое действие β-адреноблокаторов при большинстве ИА оказывается недостаточным.
Кроме того, остается неясной причина выявления титров АТ к β1-рецепторам у больных с ИА, сопоставимых с таковыми у больных с миокардитом, дилатационной КМП: естественно предположить, что и при аритмиях имеется латентный (аритмический) вариант миокардита. В единственной работе 2012 г. эта гипотеза получила подтверждение [23]: не только отмечена достоверно бóльшая по сравнению с контролем (15,7%) частота обнаружения АТ к β1-рецепторам у больных с желудочковыми (64,2%) и с наджелудочковыми (44%) аритмиями, но и при ЭМБ у 11 больных в 81% случаев диагностирован миокардит. Однако использование АТ к β1-рецепторам в диагностике миокардита распространения по-прежнему не получило.
В настоящем исследовании показаны не только статистически значимое по сравнению с контрольной группой повышение уровня серологических маркеров миокардита (вирусного генома в крови, АТ к ядрам, антигенам кардиомиоцитов, эндотелия и проводящей системы) у пациентов с ИА, но и прямая связь этих маркеров с морфологическими признаками миокардита (одновременная высокая чувствительность и специфичность [3]). В то же время уровень СРБ при высокой специфичности обладал очень низкой чувствительностью (14,3%), что свойственно и большинству других признаков, включенных нами в диагностический алгоритм. Это делает целесообразным наряду с опорой на уровень антикардиальных АТ выявление максимального числа дополнительных признаков.
Применение алгоритма у 190 больных показало практически то же соотношение иммуновоспалительных, генетических и иных причин ИА, что и по данным ЭМБ, при наличии определенных особенностей при разных аритмиях. Необходимо еще раз подчеркнуть, что ни отсутствие компонентов анамнестической триады, ни наличие у пациента коронарного атеросклероза или АГ не исключают возможности латентного миокардита как причины аритмий. В то же время достаточно высока частота смешанных форм. К примеру, пролапс/прогиб митрального клапана был выявлен у 40% пациентов с ЖЭ; оценить вклад мезенхимальной дисплазии в развитие аритмии у конкретного больного очень сложно. Синдром обструктивного апноэ во время сна нетяжелого течения имелся у 3 пациентов с МА и ЖЭ, страдавших миокардитом. Устанавливая нозологический диагноз, мы нередко определяем лишь ведущую причину аритмии.
В литературе сообщается о единичных попытках патогенетического лечения ИА. Показана эффективность стероидов у больных с идиопатической МА и другими аритмиями при верифицированном миокардите [24, 25], в том числе у детей [26, 27]; уровень антикардиальных АТ, а также маркеры вирусной инфекции в этих работах не оценивались. Обычно применяют высокие дозы стероидов (1 мг/кг), которые заимствованы из «большой» ревматологии. Вместе с тем отечественные авторы [28, 29] традиционно использовали в лечении миокардита, не только ревматического, меньшие дозы преднизолона (20—40 мг), эффективность которых у больных с аритмиями практически не изучалась.
В невысоких дозах преднизолон проявляет не столько иммуносупрессивные, сколько противовоспалительные свойства: снижает проницаемость капилляров и подавляет миграцию лейкоцитов. В одной из работ показано, что терапия малыми дозами метипреда (16 мг/сут) в сравнении с плацебо приводила к снижению частоты рецидивов МА (9,6 и 50% соответственно) и ее перехода в постоянную форму (2 и 29% соответственно) при наблюдении около 2 лет [30], однако критерием включения в исследование было лишь повышение уровня СРБ. Верификация диагноза миокардита не проводилась. Кроме того, из ревматологии пришло в лечение миокардитов использование аминохинолиновых препаратов, оказывающих иммунодепрессивный эффект: обычно их применяют в дополнение к кортикостероидам с целью снижения поддерживающей дозы последних.
Данное исследование показало целесообразность применения преимущественно мягкой ИСТ у пациентов с воспалительной этиологией ИА. Предпринята попытка выделить предикторы эффективности комплексной терапии у больных с миокардитом. Так, с высокой эффективностью лечения ассоциировались изолированный характер миокардита, наличие высокой вирусной и иммунной активности, анамнестической триады, системных иммунных проявлений, с низкой эффективностью — наличие мелкоочагового кардиосклероза и субэндокардиального липоматоза по данным ЭМБ, высокий исходный индекс сложности аритмии (более 3 видов аритмий, их высокая частота, давность более 5 лет, резистентность к 4 ААП и более в анамнезе, включая амиодарон). Отмечено, что «легкое» подавление иммунной активности заболевания коррелирует с отличным клиническим эффектом: такой ответ на лечение как раз и может отражать отсутствие необратимых структурных изменений в миокарде.
Заключение
При использовании комплексного дифференцированного диагностического алгоритма нозологическая природа «идиопатических» аритмий может быть с различной степенью достоверности установлена у 94,7% больных: в 75,7% случаев это миокардит (определенный или вероятный), в 17,4% — генетическая кардиомиопатия (изолированная или в сочетании с миокардитом), в 1,6% — изолированная миокардиодистрофия (дисгормональная, тонзилогенная). Смешанная этиология отмечена у 25% больных, первично хроническое течение миокардита — у 59,9%. Наиболее информативным методом неинвазивной диагностики миокардита является определение спектра антикардиальных антител (в том числе к ядрам кардиомиоцитов). Уровень антител к β-адренорецепторам коррелирует с видом аритмии, но не с ее этиологией. Этиотропная и патогенетическая терапия (в сочетании с антиаритмической) при аритмиях иммуновоспалительной этиологии позволяет повысить антиаритмический эффект лечения (в том числе у резистентных больных), в ряде случаев полностью отменить антиаритмический препарат и должна проводиться длительно и непрерывно с учетом хронического течения заболевания и склонности к обострениям.



