Антропометрические характеристики плода являются важным показателем исхода беременности и напрямую зависят от нормального процесса плацентации [1]. Нарушение развития плаценты будет приводить к плацентарной недостаточности и развитию таких осложнений беременности, как задержка роста плода (ЗРП) и преэклампсия [2–4].
Новорожденные с высокими/низкими значениями роста, массы тела характеризуются повышенным риском развития нарушений здоровья (в том числе смертности) в течение жизни по сравнению с новорожденными со средними значениями данных параметров [5, 6].
Важную роль в развитии плода и плаценты играет метаболизм фолиевой кислоты, так как она необходима для осуществления процессов метилирования, связанного с биосинтезом ДНК, РНК, регуляцией экспрессии генов для обеспечения роста, пролиферации и дифференцировки клеток [7]. Нарушения активности ферментов, играющих основную роль в цикле фолатов и метионина, могут приводить к дефициту фолиевой кислоты и гипергомоцистеинемии [8]. Повышенный уровень гомоцистеина способствует усилению апоптоза в плаценте и снижению секреции хорионического гонадотропина человека, что может привести к развитию плацентарной недостаточности и ЗРП [8–11].
Недавние молекулярно-генетические исследования показали, что полиморфизмы генов, связанные с ферментами фолатного цикла и цикла метионина, могут быть ассоциированы с ЗРП и/или низким весом новорожденного [12–15]. Так, в японской популяции полиморфизмы C677T и A1298C метилентетрагидрофолатредуктазы (MTHFR) были ассоциированы с низким весом ребенка при рождении у курящих женщин [12]. В двух работах, проведенных на индийской популяции, полиморфный локус C677T MTHFR также продемонстрировал связь с более низкими показателями веса ребенка [13, 15]. Вместе с этим в метаанализе, проведенном Wu H. et al. [16], не было выявлено ассоциаций C677T MTHFR с весом новорожденного. Также в недавнем исследовании в популяции женщин Китая, в котором изучалась взаимосвязь между пятью полиморфизмами генов фолатного обмена (C677T и A1298C MTHFR, A66G MTRR, A2756G MTR, rs3819102 TYMS) и низким весом ребенка при рождении, достоверных результатов получено не было [17].
Неоднозначность результатов молекулярно-генетических исследований роли полиморфизма генов фолатного цикла и цикла метионина в формировании веса новорожденного диктует необходимость дальнейшего проведения таких работ, т.к. позволит установить генетические факторы матери, связанные (влияющие) с весом новорожденного, и в последующем, после получения убедительных доказательств этих связей и их направленности, рекомендовать их для использования в практической медицине.
Поэтому целью нашего исследования стало изучение взаимосвязи между полиморфизмами генов, участвующих в метаболизме фолиевой кислоты/метионина, с весом новорожденных у беременных Центрально-Черноземного региона России.
Материалы и методы
В исследование были включены 317 беременных, проходивших обследование в Перинатальном центре Белгородской областной клинической больницы в период с 2008 по 2015 гг. Все женщины предоставили информированное согласие на включение в исследование. Комитет по этике медицинского института НИУ БелГУ одобрил дизайн этого исследования (протокол №2 от 13.02.2008 г.). При формировании выборки использовались следующие критерии включения: одноплодная беременность, закончившаяся живорождением; русская национальность; место рождения и проживания – Центрально-Черноземный регион России. Критерии исключения: многоплодная беременность, врожденные порки развития плода/новорожденного, врожденные аномалии матки.
Для молекулярно-генетического тестирования было отобрано 5 полиморфных локусов генов фолатного цикла и цикла метионина: rs699517 TYMS, rs2790 TYMS, rs1979277 SHMT1, rs1805087 MTR, rs1801394 MTRR. Данные локусы являются функционально значимыми, т.к. связаны с эпигенетическими изменениями и транскрипцией в соответствующих генах (данные получены in silico с помощью онлайн-ресурса Haploreg v.4.2, https://pubs.broadinstitute.org/mammals/haploreg/haploreg.php).
ДНК экстрагировали из венозной крови стандартным методом фенол-хлороформной экстракции. Генотипирование образцов осуществлялось методом ПЦР-синтеза ДНК на амплификаторе СFX96 (Bio-Rad) с использованием стандартных олигонуклеотидных праймеров и зондов с последующим анализом полиморфных локусов методом дискриминации аллелей [18].
Статистический анализ
Ассоциации между SNP материнского организма и весом новорожденного оценивались методом лог-линейного регрессионного анализа с помощью программного обеспечения gPLink [19]. Для данного анализа использовались трансформированные значения веса новорожденного, так как его распределение в исследуемой выборке (оценивалось на основе критерия Шапиро–Уилка) не соответствовало нормальному. Для оценки направленности ассоциативной связи были использованы коэффициент регрессии (β) и его ошибка (SE) (описывают изменение трансформированного показателя веса новорожденного на минорный аллель). Оценка индивидуальных эффектов SNP проводилась с учетом четырех генетических моделей (аллельной, аддитивной, доминантной, рецессивной) с коррекцией на ковариаты (возраст, индекс массы тела матери до беременности) и множественные сравнения (использовались адаптивные пермутационные процедуры с расчетом показателя pperm).
Неравновесие по сцеплению между парами SNP оценивалось с помощью коэффициента D’ и коэффициента корреляции r2 Пирсона. Гаплоблоки конструировались на основе алгоритма «Confidence intervals» (при D’>0,8), имплементированного в программу gPLINK. Анализ ассоциаций гаплотипов с весом новорожденного проводился методом лог-линейной регрессии с коррекцией на ковариаты (возраст, индекс массы тела матери до беременности) и пермутационными процедурами (выполнялось 1000 пермутаций). Показатель pperm<0,05 принимался за статистически значимый.
С помощью современных биоинформатических онлайн-ресурсов мы изучили связь SNP, показавших значимые ассоциации с весом новорожденного, с несинонимическими заменами (PolyPhen-2, http://genetics.bwh.harvard.edu/pph2/), эпигенетическими эффектами (HaploReg (v4.2), https://pubs.broadinstitute.org/mammals/haploreg/haploreg.php), экспрессией и альтернативным сплайсингом генов (GTEx portal, https://www.gtexportal.org/home/).
Результаты и обсуждение
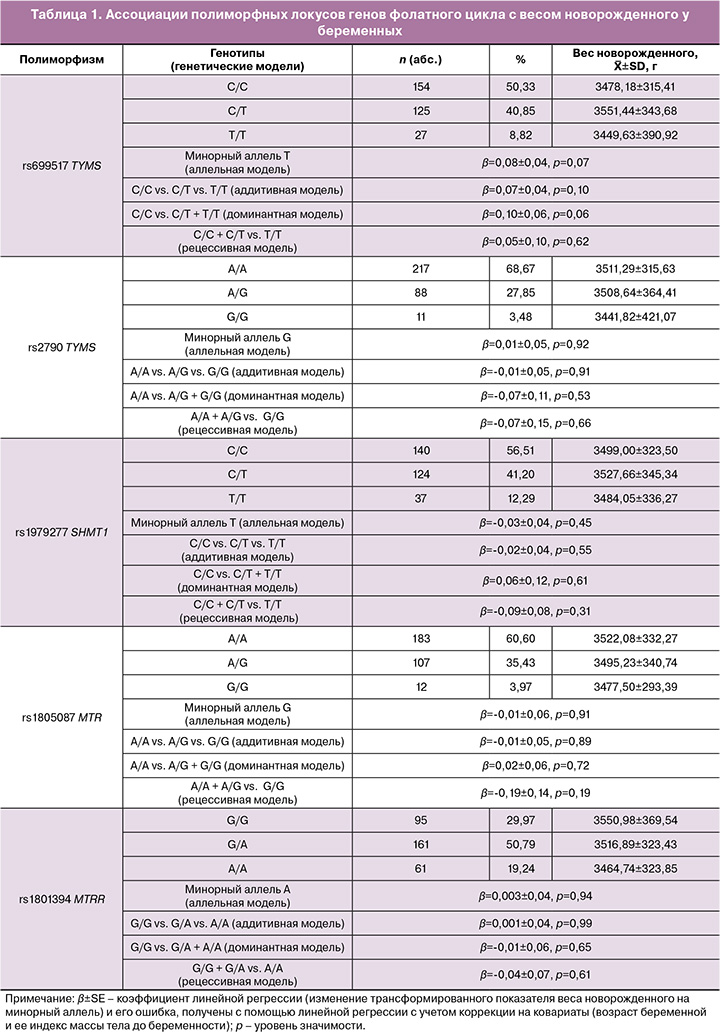
При анализе ассоциаций полиморфизма генов фолатного цикла с весом новорожденного у беременных статистически значимых различий выявлено не было (табл. 1).
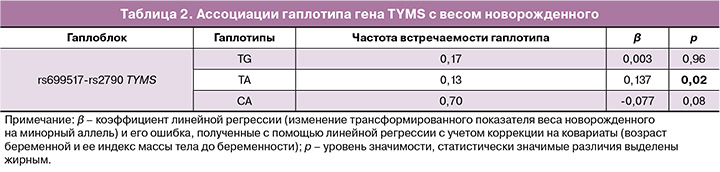
Изучено неравновесие по сцеплению для полиморфных локусов, расположенных на одной хромосоме в исследуемой группе женщин. С помощью алгоритма «Confidence intervals» c уровнем коэффициента сцепления D´>0,8 определены гаплоблоки по изучаемым SNP. В итоге был установлен один гаплоблок, включающий полиморфные локусы rs699517 и rs2790 гена TYMS (18 хромосома). При анализе ассоциаций гаплотипов в рамках выявленного гаплоблока установлено, что гаплотип TА rs699517–rs2790 TYMS ассоциирован с весом новорожденного у женщин (β=0,14, p=0,0195) (табл. 2).
По данным онлайн-ресурса HaploReg (v4.2) rs699517 и rs2790 TYMS обладают важным регуляторным потенциалом. Данные полиморфные маркеры расположены в сайте гиперчувствительности к ДНКазе в цельной крови, а rs699517 TYMS локализован в области регуляторного паттерна, являющегося сайтом связывания для фактора транскрипции NRSF. Для данного фактора различия между оценками логарифмов шансов (logarithm of the odds (LOD) scores) аллельных вариантов Т и С составляют ΔLOD scores = 2,4. Таким образом, аллель Т rs699517 TYMS, связанный с более высоким весом новорожденного, повышает аффинность к данному транскрипционному фактору.
Данные онлайн-ресурса GTEx Portal указывают на связь rs699517 и rs2790 TYMS с уровнем экспрессии генов в различных органах и тканях, связанных с весом новорожденного. Аллель С полиморфного локуса rs699517 TYMS ассоциирован с экспрессией гена ENOSF1 в скелетной мускулатуре (β=-0,40, р=1,1*10-25, pFDR≤0,05), культуре клеток фибробластов (β=0,24, р=1,6*10-15, pFDR≤0,05), надпочечниках (β=0,38, р=1,6*10-9, pFDR≤0,05), подкожной жировой ткани (β=-0,19, р=1,1*10-8, pFDR≤0,05); гена RP11-806L2.6 в щитовидной железе (β=0,38, р=1,8*10-13, pFDR≤0,05), подкожной жировой ткани (β=0,38, р=1,8*10-13, pFDR≤0,05); надпочечниках (β=0,51, р=1,2*10-8, pFDR≤0,05), культуре клеток фибробластов (β=0,23, р=7,7*10-5, pFDR≤0,05).
Аллель А полиморфного локуса rs2790 TYMS ассоциирован с экспрессией гена ENOSF1 в скелетной мускулатуре (β=-0,49, р=2,3*10-29, pFDR≤0,05), культуре клеток фибробластов (β=0,29, р=1,7*10-15, pFDR≤0,05), надпочечниках (β=0,43, р=5,5*10-9, pFDR≤0,05), подкожной жировой ткани (β=-0,26, р=8,1*10-11, pFDR≤0,05); гена RP11-806L2.6 в щитовидной железе (β=0,40, р=4,0*10-11, pFDR≤0,05), подкожной жировой ткани (β=0,35, р=1,7*10-8, pFDR≤0,05), надпочечниках (β=0,51, р=1,6*10-6, pFDR≤0,05).
Установлено, что аллель С rs699517 TYMS и аллель А rs2790 TYMS связаны с уровнем альтернативного сплайсинга гена ENOSF1 в щитовидной железе (β=-0,54, р=1,1*10-21, pFDR≤0,05 и β=-0,90, р=4,5*10-47, pFDR≤0,05 соответственно), подкожной жировой ткани (β=0,46, р=2,1*10-15, pFDR≤0,05 и β=0,41, р=3,2*10-9, pFDR≤0,05 соответственно), висцеральной жировой ткани (β=-0,41, р=1,4*10-15, pFDR≤0,05 и β=-0,56, р=2,8*10-23, pFDR≤0,05 соответственно), культуре клеток фибробластов (β=-0,23, р=2,7*10-7, pFDR≤0,05 и β=-0,40, р=3,6*10-7, pFDR≤0,05 соответственно). Также аллель С rs699517 TYMS влияет на уровень альтернативного сплайсинга гена ENOSF1 в надпочечниках (β=0,60, р=2,2*10-15, pFDR≤0,05).
В итоге rs699517 и rs2790 TYMS, ассоциированные с весом новорожденного, обладают важными функциональными эффектами: локализованы в регионе гиперчувствительности к ДНКазе в цельной крови, связаны с уровнем экспрессии мРНК гена ENOSF1 и гена RP11-806L2.6 в скелетной мускулатуре, жировой ткани, надпочечниках, щитовидной железе, культуре клеток фибробластов. Помимо этого, данные SNP влияют на уровень альтернативного сплайсинга гена ENOSF1 в жировой ткани, надпочечниках, щитовидной железе, культуре клеток фибробластов. Также rs699517 TYMS определяет чувствительность ДНК для фактора транскрипции NRSF.
Согласно информации из базы данных GeneCards (https://www.genecards.org), ген TYMS кодирует фермент тимидилатсинтазу, участвующую в так называемом фолатном цикле. Фолатный цикл связан с каскадом превращений фолиевой кислоты в тетрагидрофолаты, являющиеся донорами метильных групп, используемых в процессах биосинтеза пуринов [7]. Собственно, тимидилатсинтаза катализирует превращение дезоксиуридинмонофосфата (дУМФ) в дезокситиминмонофосфат (дТМФ), который необходим для биосинтеза дезоксинуклеотидов и имеет решающее значение для репликации ДНК [7]. Для осуществления данной реакции в качестве кофактора также используется 10-метилентетрагидрофолат (метилен-ТГФ). Ингибирование тимидилатсинтазы под действием различных факторов приводит к снижению в клетках дТМФ и накоплению дУМФ. В конечном итоге отсутствие дТМФ приводит к торможению синтеза ДНК, неправильному включению дУМФ в ДНК и ее повреждению (двойные и одноцепочечные разрывы) с последующим клеточным апоптозом, потенциально приводя к нарушениям в эндотелиальных клетках сосудов плаценты и развитию плацентарной недостаточности [11, 20]. Поэтому логичной является идентификация генетических маркеров гена TYMS, связанных с течением беременности и возникающими при этом нарушениями. Однако изучение роли полиморфизма генов TYMS в формировании веса новорожденного остается в значительной степени неисследованным. В молекулярно-генетических работах на разных популяциях изучалась связь полиморфных локусов rs699517 и rs2790 TYMS с риском развития ряда заболеваний: ишемический инсульт [21, 22], дефект межжелудочковой перегородки [23], лимфобластный лейкоз [24], колоректальный рак [25] и др. При этом обращают на себя внимание неоднозначность и противоречивость результатов таких исследований.
Разнонаправленность выявленных ассоциаций rs699517 и rs2790 TYMS с формированием различных заболеваний может быть обусловлена выраженными различиями в частотах аллелей данных полиморфных локусов в разных этнических группах по всему миру [24, 26].
Заключение
Таким образом, гаплотип TА rs699517–rs2790 TYMS у беременных может быть связан с более высоким весом новорожденного. Данные полиморфные локусы обладают важными функциональными эффектами. Они локализованы в регионе гиперчувствительности к ДНКазе в цельной крови, связаны с уровнем экспрессии мРНК гена ENOSF1 и гена RP11-806L2.6 в скелетной мускулатуре, жировой ткани, надпочечниках, щитовидной железе, культуре клеток фибробластов; влияют на уровень альтернативного сплайсинга гена ENOSF1 в жировой ткани, надпочечниках, щитовидной железе, культуре клеток фибробластов; rs699517 TYMS определяет чувствительность ДНК к фактору транскрипции NRSF.



