Введение
С каждым годом в мире и в Российской Федерации растет число пациентов с фибрилляцией предсердий (ФП) [1]. В настоящий момент она является одной из самых распространенных наджелудочковых тахиаритмий [1]. Одним из главных направлений лечения пациентов с ФП является профилактика тромбоэмболических осложнений (ТЭО) посредством применения антикоагулянтной терапии [2]. Однако прием антикоагулянтов в силу их механизма действия сопряжен с повышением риска развития кровотечений [3].
В настоящий момент не прекращаются попытки поиска новых факторов риска развития геморрагических осложнений, ассоциированных с антикоагулянтной терапией. Постепенно появляется все больше и больше шкал расчета риска кровотечений при применении антитромботических препаратов, так, например, в шкале АВС (Age – возраст, Biomarkers – биомаркеры, Clinical history – история заболевания) впервые учитываются такие биомаркеры повышенного риска развития кровотечений, как уровни высокочувствительного тропонина и фактора роста и дифференциации‐15 в крови [4]. В шкале HEMORR2HAGES учитывается наличие полиморфных вариантов гена CYP2C9. Необходимо отметить, что во всех шкалах расчета риска кровотечений обязательно учитывается наличие почечной недостаточности.
Хроническая болезнь почек (ХБП), которая часто сопровождает ФП, влияет на систему гемостаза, приводя к увеличению риска как ТЭО [5], так и кровотечений [6] По данным исследования ROCKET AF (Rivaroxaban Once Daily Oral Direct Factor Xa Inhibition Compared with Vitamin K Antagonism for Prevention of Stroke and EmbolismTrial in Atrial Fibrillation), «большие» и клинически значимые небольшие кровотечения развились у 1475 пациентов в группе ривароксабана и у 1449 – в группе варфарина (14,9%) [7]. При этом пациенты с «большими» кровотечениями имели более высокий уровень креатинина в крови по сравнению с пациентами без «больших» кровотечений [8].
Ривароксабан метаболизируется в организме следующими способами: 6% выводятся через почки с помощью клубочковой фильтрации, 30% – через активную секрецию с использованием Р-гликопротеина (Р-gp) и белка BCRP (ABCG2), 14% подвергаются гидролизу амидных связей, а оставшаяся часть метаболизируется в печени ферментами цитохрома Р-450: CYP 3A4/5, CYP2J2 (кодируются соответствующими генами) [9–10]. Образующиеся метаболиты выводятся как почками, так и через желчные протоки [9–10].
Существуют данные о влиянии носительства различных полиморфных вариантов генов, кодирующих белки системы цитохрома Р-450 (CYP3A4, CYP3A5), на метаболизм, биодоступность и индивидуальную вариабельность концентрации и терапевтического эффекта ривароксабана [11–12], однако их результаты противоречивы. В 2016 г. K. Lorenzini et al. опубликовали клинический случай развития анемии тяжелой степени на фоне приема ривароксабана. Авторы предположили, что причиной эпизода кровотечения является нарушение метаболизма ривароксабана из-за носительства двух полиморфных вариантов: c.2677 G>T (rs2032582) и c.3435 C>T (rs1045642), гена АВСВ1 в гомозиготном состоянии, а также из-за сниженной активности ферментов CYP3A4/5.Однако в доступной научной литературе отсутствуют данные о влиянии носительства различных аллелей и генотипов по полиморфным маркерам генов CYP3A4, CYP3A5 на развитие кровотечений у пациентов с ФП с различными стадиями ХБП.
Цель исследования: изучить возможную связь между наличием полиморфных вариантов генов CYP3A5 (rs776746), CYP3A4 (rs35599367), метаболической активностью CYP 3A4/5, минимальной остаточной концентрацией ривароксабана и развитием кровотечений у пациентов с неклапанной ФП и сопутствующей ХБП 3-й и 4-й стадий.
Методы
Протокол исследования рассмотрен и одобрен Этическим комитетом ФГБОУ ДПО РМАНПО Минздрава РФ (Протокол № 15 от 25.10.2021). Исследование проводилось с ноября 2021 по июнь 2023 г. на базе отделений терапевтического профиля ГБУЗ «ГВВ № 2» ДЗМ.
Проведено проспективное исследование, продолжительность периода наблюдения – 16 недель, исследование включило 5 визитов (каждые 4 недели).
На первом визите проводились забор биоматериала (кровь, моча), сбор анамнеза, объективный осмотр. Дальнейшие визиты осуществлялись с помощью телефонных звонков – проводили опрос пациентов на предмет наличия кровотечений и ТЭО за период наблюдения..Критерии включения: пациенты обоего пола 18 лет и старше с ФП неклапанной этиологии с риском по шкале CHA2DS2-VASc ≥1 балла для мужчин и ≥2 баллов для женщин, принимающих ривароксабан, в сочетании с ХБП 3а-, 3б- и 4-стадиями в соответствии с определением KDIGO 2012 г. [14]; наличие подписанного информированного согласия. Критерии невключения в исследуемую группу: возраст<18 лет, беременность, лактация, пациенты с протезированными клапанами или митральным стенозом средней/тяжелой степени, скорость клубочковой фильтрации <15 мл/мин/1,73 м² по CKD-EPI, клиренс креатинина по формуле Кокрофта–Голта<15 мл/мин, обратимые причины ФП (оперативные вмешательства на сердце, тиреотоксикоз, злоупотребление алкоголем), клинически значимое активное кровотечение на момент включения, состояния, сопровождающиеся существенным повышением риска геморрагических событий (хирургические операции высокого риска, травмы головного и спинного мозга, переломы в течение предыдущих 3 месяцев), постоянный прием антиагрегантных препаратов, обильное кровотечение любой локализации, состояние после перенесенного геморрагического инсульта (или ишемический инсульт с геморрагической трансформацией), внутричерепное кровотечение в анамнезе, анемия (гемоглобин – Hb≤100 г/л) или тромбоцитопения (тромбоциты ≤90×109/л) любой этиологии, пациенты с известными артериовенозными мальформациями, аневризмами сосудов, наличие некоторых сопутствующих заболеваний (системные заболевания соединительной ткани, заболевания крови, влияющие на гемостаз, онкологические заболевания, выраженная печеночная недостаточность (класс В и С по Чайлд–Пью), тяжелые психические расстройства), длительный прием препаратов, обладающих доказанным нефротоксическим действием, ожидаемая низкая приверженность лечению.
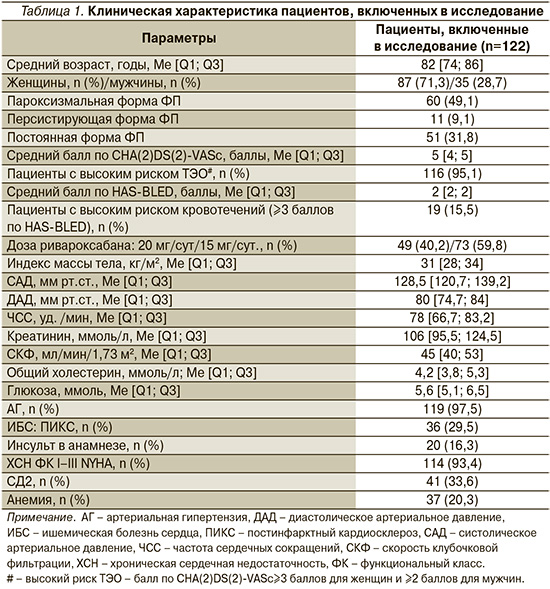
Всего в исследование были включены 122 пациента в возрасте от 52 до 97 лет, в т.ч. 62 пациента с ФП в сочетании с ХБП-С3а, медиана возраста – 82 [73,7; 85,2] года, из них женщин 45 (72,5%) и 60 пациентов с ФП в сочетании с ХБП-С3б и -С4, медиана возраста – 82 [74; 88] года, 42 (70,0%) женщины. Пациенты принимали ривароксабан в дозе 15 мг/сут и 20 мг/сут в зависимости от клиренса креатинина, согласно инструкции по медицинскому применению препарата [15]. Клиническая характеристика пациентов представлена в табл. 1.
Для определения остаточной равновесной концентрации ривароксабана проводили забор 4 мл крови в вакуумные пробирки с литий-гепарином Improvacuter (Guangzhou Improve Medical Instruments Co.Ltd, Китай) емкостью 6 мл через 13–15 часов после последнего приема ривароксабана. С целью получения плазмы образцы крови центрифугировали при 3000 об/мин в течение 15 минут. Выделенная плазма аликвотировалась в пробирки типа Эппендорф и замораживалась. Материал хранили при температуре -28°С до момента проведения тестирования. С помощью жидкостного хроматографа Agilent 1200, совмещенного с масс-спектрометром Agilent 6410, определялась остаточная равновесная концентрация ривароксабана.
При расчете суточной концентрации ривароксабана в связи с тем, что пациенты получали препарат в различных дозах (15 и 20 мг) остаточная равновесная концентрация (Сmin,ss) ривароксабана была скорректирована относительно суточной дозы лекарственного средства (Сmin,ss/D).
Фармакогенетическое исследование было проведено с помощью полимеразной цепной реакции (ПЦР) в реальном времени. Для генотипирования производили забор 4 мл крови в вакуумные пробирки VACUETTE (GreinerBio-One, Австрия) с К3 ЭДТА (этилендиаминтетраацетат). Материал хранили при температуре -28°С до момента проведения тестирования. Используя ДНК-амплификатор CFX96 Touch Real Time System, с помощью наборов «SNP-Скрин» проводили анализ полиморфных вариантов rs776746 гена CYP3A5, rs35599367 гена CYP3A4, rs890293 гена CYP2J2.
Активность изоферментной группы CYP3A оценивали по отношению концентрации 6-β-гидроксикортизола к концентрации кортизола в моче пациентов. Низкое соотношение 6-β-гидроксикортизол/кортизол соответствует низкой активности CYP3A, а высокое соотношение 6-β-гидрокси-кортизол/кортизол соответствует высокой активности CYP3A [16].
Фармакогенетические, фармакокинетические и фармакометаболомные исследования проводили на базе Научно-исследовательского института молекулярной и персонализированной медицины ФГБОУ ДПО РМАНПО Минздрава РФ.
На протяжении 16 недель все пациенты оценивались на предмет возникновения кровотечений с помощью специального опросника [17].
Статистический анализ данных выполнен с использованием программы IBM SPSS StatisticsBase 22.0. Нормальность распределения данных оценивали с помощью критерия Шапиро–Уилка. Для непрерывных переменных с нормальным распределением рассчитывали среднее арифметическое (M) и стандартное отклонение среднего (SD). При отклонении распределения параметров от нормы данные представляли в виде медианы с указанием 25-го и 75-го процентилей. Для сравнения количественных показателей использовали t-критерий Стьюдента либо критерий Манна–Уитни (в зависимости от характера распределения данных). Статистически значимыми считали различия при р<0,05.
Результаты
По окончании периода наблюдения (16 недель) все пациенты были разделены на 2 группы: пациенты, у которых зарегистрированы кровотечения (n=48), из них женщин 36 (79,1%), медиана возраста – 82 [74,0; 87,0] года, и пациенты без кровотечений за период наблюдения (n=74), 51 (68,9%) женщина, медиана возраста – 83 [74,0;85,0] года. Принимали ривароксабана в дозе 20 мг/сут 19 (39,5%) пациентов в группе с наличием кровотечений за период наблюдения и 34 (45,9%) пациента в группе без кровотечений. Также 7 (14,5%) пациентов в группе с наличием кровотечений за период наблюдения принимали необоснованно высокую дозу ривароксабана (20 мг вместо 15 мг, согласно инструкции по медицинскому применению [15]), в группе без кровотечений таких пациентов было 21 (28,3%).
Группы пациентов с наличием/отсутствием кровотечений были сопоставимыми по полу, возрасту, клиническим характеристикам (возраст, статус курения, уровни АД, ЧСС, индекс массы тела и др.), спектру сопутствующих заболеваний, медикаментозной терапии, лабораторных параметрам (уровни Hb, общего белка, альбумина, активность печеночных ферментов, число эритроцитов, тромбоцитов в крови и др.).
Уровень креатинина и СКФ также были сопоставимыми в группах пациентов с наличием и отсутствием кровотечений за период наблюдения: 104,0 [93,0; 127,25] и 106,0 [97; 130,0] ммоль/л соответственно; 47 [40; 53] и 44 [41;53] мл/мин/1,73 м2 соответственно.
Среди кровотечений на первом месте были синяки – 39 (31,9%) пациентов, на втором месте – кровотечения из мелких ран – 17 (13,9%) пациентов, на третьем месте – носовые кровотечения – 14 1(1,4%) пациентов; далее по частоте встречаемости следовали кровотечения из полости рта – 9 (7,3%) пациентов, геморроидальные кровотечения – 8 (6,5%) и на последнем месте оказались мышечные гематомы – 2 (1,6%) пациента.
При сравнении распределения генотипов среди пациентов с наличием/отсутствием кровотечений статистической значимой разницы не выявлено (p>0,05): 38 (79,1%) пациентов в группе кровотечений имели генотип GG по полиморфизму rs776746 гена CYP3A5, соответственно, носителей генотипа AG в данной группе – 10 (20,8%) пациентов, в группе без кровотечений носителей генотипа AG – 66 (84,6%), носителей генотипа GG – 8 (10,4%) человек; различия оказались статистически незначимыми (табл. 2).

Также не было выявлено статистически значимой разницы в распределении генотипов по полиморфизму CYP3A4*22 (rs35599367) C>T у пациентов с ФП и ХБП-С3 и -С4: в группе с кровотечениями были 43 (89,5%) носителя генотипа СС, соответственно, 5 (10,6%) носителей генотипа СТ, в группе без кровотечений – 71 (91,1%) носитель генотипа СС и 3 (3,8%) носителя генотипа СТ (табл. 3).

При сравнении Сmin,ss и Сmin,ss/D ривароксабана не было выявлено статистически значимых различий в группах обследованных нами пациентов с наличием/отсутствием кровотечений за период наблюдения (табл. 3).
Однако при сравнении метаболической активности CYP3A выявлено, что у пациентов с кровотечениями за период наблюдения метаболическая активность СYР3А (соотношение 6-β-гидроксикортизол/кортизол) была статистически значимо выше по сравнению с таковой у пациентов без кровотечений: 0,8 [0,6; 1,6] и 0,7 [0,5; 1,6] нг/мл соответственно (р=0,046).
Исходя из полученных данных, далее мы оценили метаболическую активность CYP3A в зависимости от генотипа по полиморфным вариантам CYP3A4*22 rs35599367 C>T и CYP3A5*3 rs776746 A6986G (табл. 4) и обнаружили, что у пациентов с генотипом СТ по полиморфному варианту CYP3A4*22 rs35599367 C>T метаболическая активность CYP3A была статистически значимо выше, чем у пациентов с генотипом СС: 1,9 [1,4; 2,32] и 0,79 [0,48; 1,58] нг/мл соответственно (р=0,009) (табл. 4). При этом метаболическая активность CYP3A у пациентов с различными генотипами (GA и GG) по полиморфному варианту CYP3A5*3 rs776746 A6986G была сопоставимой (табл. 4).
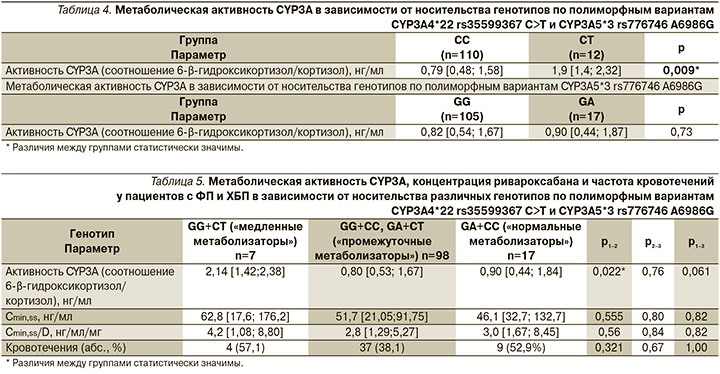
Учтя полученные результаты, в качестве дополнительного анализа мы сгруппировали пациентов в зависимости от объединенных результатов генотипирования по анализируемым полиморфным вариантам генов CYP3A4 и CYP3A5: 1-я группа «медленные метаболизаторы» по CYP3A (пациенты, у которых сочетаются генотип GG по полиморфному варианту CYP3A5*3 с генотипом CT по полиморфному варианту CYP3A4*22); 2-я группа «промежуточные метаболизаторы» по CYP3A (пациенты, у которых сочетаются генотип GG по CYP3A5*3 с генотипом CC по CYP3A4*22, а также пациенты, у которых сочетаются генотип GA по CYP3A5*3 с генотипом CT по CYP3A4*22); 3-я группа «нормальные метаболизаторы» по CYP3A (пациенты, у которых сочетаются генотип GA по CYP3A5*3 с генотипом CС по CYP3A4*22) [18]. Согласно результатам анализа (табл. 5), метаболическая активность CYP3A в группе «медленных метаболизаторов» была статистически значимо выше по сравнению с группой «промежуточных метаболизаторов»: 2,14 [1,42; 2,38] и 0,80 [0,53; 1,67] нг/мл соответственно (р=0,022), и выше таковой в группе «нормальных метаболизаторов» (р=0,061). При сравнении Сmin,ss/D ривароксабана и частоты эпизодов кровотечений статистически значимых различий между группами не выявлено (р>0,05).
Обсуждение
В ранее проведенных исследованиях было установлено, что у пациентов с ФП даже на фоне приема прямых пероральных антикоагулянтов (ПОАК) риск кровотечений увеличивается [7, 19], особенно при наличии сопутствующей ХБП, причем риск кровотечений нарастает параллельно снижению СКФ [20–21]. В связи с этим не прекращается поиск маркеров, наличие которых ассоциируется с повышенным риском кровотечения в данной группе полиморбидных пациентов с ФП.
В последние годы активно изучается влияние носительства различных полиморфных вариантов генов, кодирующих систему цитохромов печени Р-450, участвующих в метаболизме ПОАК, в частности ривароксабана, на эффективность и безопасность антикоагулянтной терапии.
Как известно, подсемейство CYP3A состоит из четырех функциональных изоферментов – CYP3A4, CYP3A5, CYP3A7 и CYP3A43, а в метаболизме ривароксабана участвуют CYP3A4 и CYP3A5, кодируемые одноименными генами [9–10]. По результатам нашего исследования не было выявлено связи между носительством различных генотипов по полиморфизмам rs776746 CYP3A5*3 и rs35599367 CYP3A4*22. Полученные нами результаты совпадают с таковыми других авторов. Так, H. Y. Yoon et al. [22] в своем исследовании также не нашли связи между носительством различных генотипов по полиморфному варианту rs776746 CYP3A5*3 и возникновением кровотечений на фоне приема ПОАК (апиксабан, дабигатран, эндоксабан, ривароксабан), что совпадает с результатами нашего исследования.
В исследование H.Y. Yoo et al. [22] были включены 50 пациентов с кровотечениями, из них 14 пациентов с «большими» кровотечениями (желудочно-кишечное кровотечение, внутримозговое кровоизлияние, анемия тяжелой степени) и 36 пациентов с клинически незначимыми кровотечениями (всего 16 пациентов в группе кровотечений, принимавших ривароксабан – 32% от всех пациентов с кровотечениями), группу сравнения составили 418 пациентов (из них 58 пациентов – 13,9% от числа пациентов контрольной группы, принимавших ривароксабан с ФП), принимавшихПОАК более 3 месяцев.
A.M. Campos-Staffico et al. [23] также не обнаружили связи между носительством различных генотипов по полиморфным вариантам CYP3A4 (rs35599367, c.15389C>T) и CYP3A5 (rs776746, c.6981A>G) и возникновением кровотечений. В свое исследование авторы включили 2364 пациента, принимавших апиксабан или ривароксабан: 802 (33,9%) участника получали лечение исключительно ривароксабаном, 1324 (56,0%) участника лечились исключительно апиксабаном, а 238 (10,1%) начали антикоагулянтную терапию одним из двух указанных ПОАК, а затем в процессе лечения были переведены на другой ПОАК. Анализ возникновения кровотечений проводился ретроспективно – с момента инициации терапии ПОАК. «Большие» кровотечения (желудочно-кишечное, внутримозговое кровоизлияние, анемия тяжелой степени) и клинически значимые кровотечения (не соответствуют критериям «большого» кровотечения, но требуют хотя бы одного из следующих критериев: медицинское вмешательство медицинского работника и/или госпитализация, или повышенный уровень ухода, и/или консультация медицинского работника) развились у 412 пациентов. В цитируемом исследовании период наблюдения (2,3±2,0 года – 828,2±739,8 дня) был значительно больше, чем в нашем исследовании (16 недель) [23].
Наконец, Д.А. Сычев и соавт. [24] не выявили влияния носительства различных генотипов по полиморфному варианту CYP3A5 (rs776746, c.6981A>G) на протромбиновое время при приеме ривароксабана на пациентов после эндопротезирования тазобедренного сустава.
В то же время в публикации K. Lorenzini et al. [13] описан клинический случай, когда у пациента на фоне высокой концентрации ривароксабана из-за, как предположили авторы, носительства двух полиморфных вариантов: c.2677 G>T (rs2032582) и c.3435 C>T (rs1045642), гена АВСВ1 в гомозиготном состоянии, а также из-за сниженной активности ферментов CYP3A4/5 возникло кровотечение. Стоит отметить, что в данном исследовании был оценен единственный эпизод «большого» кровотечения у одного пациента, в то время как в нашем исследовании у включенных пациентов за период наблюдения развились преимущественно т.н. малые кровотечения (синяки – 31,9%, кровотечения из мелких ран – 13,9%, носовые кровотечения – 11,4%, кровотечения из полости рта – 7,3%, геморроидальные кровотечения – 6,5%, мышечные гематомы – 1,6%).
В нашем исследовании также не выявлена связь между Cmin,ss ривароксабана и возникновением кровотечений. Подобную взаимосвязь ранее изучали в ряде исследований, однако их результаты противоречивы. Так, C.F. Sin et al. [25] у пациентов с ФП и ХБП обнаружили прямую корреляционную связь между Cmin,ss риварокабана и возникновением кровотечений («больших» и «малых»; «большое» кровотечение определялось как уровень Hb ниже 8 г/дл или падение Hb более чем на 2 г/дл от исходного уровня, угрожающее жизни кровотечение, все остальные эпизоды кровотечения были определены как «малые»). В исследование были включены 92 пациента, из них 10 пациентов с ХБП-С1, 53 – с ХБП-С2 и 29 пациентов – с ХБП-С3 соответственно; 68 (73,9%) пациентов получали дозу ривароксабана 20 мг/сут и 24 (26,1%) – 15 мг/сут (из них 18 пациентам дозировка 15 мг назначена из-за нарушения функции почек и 6 – из-за «легких» симптомов кровотечения на момент начала приема ривароксабана). При этом при оценке клиренса креатинина по уравнению Кокрофта–Голта 22 (32,4%) из 68 пациентов, получавших ривароксабан в дозе 20 мг/сут, фактически вместо этого должны были получать 15 мг/сут. Преставляется важным тот факт, что, по данным C.F. Sin et al. [25], Сmin,ss ривароксабана коррелировал с СКФ только в группе пациентов, получавших ривароксабан в дозе 20 мг/сут. В наше исследование были включены пациенты с более тяжелой ХБП (ХБП-С3–4), у всех них СКФ была снижена; также в нашем исследовании число пациентов, принимавших ривароксабана в дозе 15 мг/сут, было больше, чем пациентов, принимавших препарат в дозе 20 мг/сут: 73 (59,8%) и 49 (40,2%) человек соответственно. Также необходимо отметить, что в исследовании C.F. Sin et al. [25] среднее время от момента определения уровня ривароксабана в плазме крови до возникновения кровотечений составило 399,5 дня, тогда как в нашем исследовании длительность периода наблюдения составила всего 16 недель.
S. Testa et al. [26] наблюдали 172 пациента, которым была впервые назначена терапия ривароксабаном. По результатам исследования выявлена связь между максимальной концентрацией ривароксабана в плазме крови и возникновением кровотечений, тогда как связь между минимальной концентрацией ривароксабана и кровотечениями отсутствовала. Необходимо также отметить тот факт, что пациенты в этом исследовании наблюдались в течение года и только 20% кровотечений произошли в течение первых 3 месяцев лечения.
A.L. Sennesael et al. [27] опубликовали данные о 10 госпитализированных пациентах в связи с развитием кровотечения, ассоциированного с приемом ривароксабана, среди которых у 4 пациентов отмечены высокие показатели Cmin,ss ривароксабана, у остальных 6 пациентов Cmin,ss ривароксана сохранялась в пределах референсных значений. Стоит отметить, что такие кровотечения следует рассматривать как «клинически значимые», т.к. они потребовали госпитализации пациентов (у 4 пациентов – желудочно-кишечное кровотечение, у 2 – внутримозговое кровоизлияние, у 3 – макрогематурия и у 1 – сильное носовое кровотечение), в то время как в нашем исследовании у включенных пациентов зарегистрированы клинически незначимые кровотечения.D. Bozic et al. [28] обнаружили, что из 39 пациентов, получающих ривароксабан, госпитализированных с желудочно-кишечными кровотечениями, Сmin,ss и Cmax,ss выше референсных значений зарегистрирован в 25,6% случаев.
В 2023 г. А.А. Кудрявцева и соавт. [29] опубликовали клинический случай о возникновении рецидивирующего кровотечения у пациентки с ФП. При анализе Cmin,ss ривароксабана установлено, что она составляла 111 нг/мл, т.е. находилась в пределах референсных значений. Дополнительно выполнен тест «Тромбодинамика», по результатам которого на фоне остаточной равновесной концентрации препарата (непосредственно перед приемом очередной дозы ривароксабана) отмечалась умеренная гипокоагуляция, а на пике концентрации препарата (через 2 часа после приема) имела место выраженная гипокоагуляция. Пациентке также было проведено фармакогенетическое исследование, которое не выявило наличия значимых для развития кровотечений полиморфизмов генов АВСB1 (rs1045642 C3435T, rs2032582), CYP2J2 (rs890293 A>C), CYP3A4 (CYP3A4*22 rs35599367 C>T), CYP3A5 (rs776746 CYP3A5*3 A6986G). Авторы предположили, что возможная причина возникновения кровотечений заключается я в межлекарственном взаимодействии – предположительно ривароксабана и амиодарона.
Мы также изучили метаболическую активность CYP3A у пациентов с ФП и ХБП и обнаружили парадоксальный факт: наибольшая метаболическая активность зарегистрирована у т.н. медленных метаболизаторов (носители генотипа GG по полиморфизму CYP3A5*3+носители генотипа CT по полиморфизму CYP3A4*22).
Полиморфизм СYР3А5*3 характеризуется изменением в 3-м интроне, которое ведет к аберрации сплайсинга и нарушению синтеза фермента СYР3А5 [30]. Генотип GG характеризуется отсутствием экспрессии фермента СУР3А, а генотип AG – снижением его экспрессии [31]. У людей, гомозиготных по аллели CYP3A5*3 («медленные метаболизаторы»), наблюдается более низкий клиренс субстратов CYP3A5, таких как такролимус [32–33], цилостазол [34] и верапамил [34]. В нашем исследовании носительство гомозиготных аллелей также ассоциировано с более низкой метаболической активностью данного фермента.
В 2011 г. D. Wang et al. [35] сообщили, что полиморфный вариант CYP3A4*22 (генотипы СТ, ТТ) характеризуется заменой С>T в 6-м интроне (rs35599367) и ассоциируется со снижением выработки матричной рибонуклеиновой кислоты (мРНК) CYP3A4 (без каких-либо вариантов сплайсинга) и ограниченной активностью 6-β-гидроксилирования тестостерона в печени человека. Согласно исследованию M. Okubo et al. [36], носительство полиморфизма CYP3A4*22 было ассоциировано со снижением уровня экспрессии белка CYP3A4, а также со снижением ферментативной активности, опосредованной CYP3A4. По данным исследований, носительство полиморфного варианта CYP3A4*22 ассоциировано с меньшей метаболической активностью, а также с более высокой концентрацией ряда лекарственных средств в крови [37–39]
Такие противоречивые результаты, на наш взгляд, можно объяснить феноменом феноконверсии, при котором генотипически «быстрые метаболизаторы» превращаются в фенотипически «медленных метаболизаторов» лекарственных средств. Так, ранее в доступной научной литературе сообщалось о феноконверсии нескольких ферментов, метаболизирующих различные медикаменты. Феноконверсия CYP2D6 чаще встречалась у пациентов с такими заболеваниями, как инфекция, вызванная вирусом иммунодефицита человека [40–41], хронический гепатит С [42] и депрессия [41]. Согласно имеющимся литературным данным, при почечной недостаточности активность СYР3А снижается [43]. Подавлять активность CYP3A при почечной недостаточности могут такие сигнальные молекулы, как уремические токсины, паратиреоидный гормон и воспалительные цитокины (интерлейкин-6 и фактор некроза опухоли-α) [45–48], соответственно, потенциально они могут участвовать в феноконверсии CYP3A у пациентов с ХБП. Y. Suzuki et al. [49] в своем исследовании выяснили, что феноконверсия у пациентов с ХБП может быть следствием накопления индоксилсульфата (растворимый, связанный с белками уремический токсин, образующийся в результате метаболизма поступающего с пищей триптофана в индол при участии бактерий). C. Lenoir еt al. [50] обнаружили, что площадь под фармакинетической прямой (AUC) выше в группе «промежуточных метаболизаторов» СУР3А по сравнению с «нормальными метаболизаторами», авторы также интерпретировали свои результаты явлением феноконверсии.
Согласно результатам нашего исследования, у пациентов, у которых наблюдались эпизоды кровотечения за период наблюдения, метаболическая активность CYP3A была статистически значимо выше, чем у больных без кровотечений за период наблюдения. К сожалению, в доступной научной литературе нами не найдено исследований, в которых бы изучалась связь метаболической активности CYP3A с возникновением кровотечений на фоне приема ривароксабана или апиксабана. Несколько противоречивую на первый взгляд связь высокой метаболической активности с развитием кровотечений мы можем объяснить несколькими факторами. C. Lenoir et al. [50] в своем исследовании изучали фенотипическую активность СYР3А и P-gp и не обнаружили связи между фенонтипической активностью СYР3А и кровотечениями, однако выявили связь между фенотипической активностью P-gp и кровотечениями. Необходимо отметить, что в данном исследовании среднее значение клиренса креатинина у включенных пациентов составило 77,7±28,0 мл/мин/1,73 м2, тогда как в нашем исследовании медиана СКФ была 45 [40; 53] мл/мин/1,73 м2. Мы не анализировали активность Р-gp, однако у пациентов с сопутствующей ХБП активность Р-gp может быть снижена, а высокая метаболическая активность СУР3А может быть отражением компенсаторного увеличения активности данного фермента.
Большинство пациентов, вошедших в наше исследование, имеют коморбидную патологию (медиана индекса коморбидности Чарлсон составляет 5 баллов [4, 6]), что ассоциируется с одновременным назначением множества лекарственных средств. Как известно, фермент СYР3А метаболизирует массу лекарственных препаратов, в т.ч. статины, антиаритмические средства, противогрибковые препараты, антибиотики [51]. Поэтому рассчитанная нами метаболическая активность СYР3А, по-видимому, отражает общую метаболическую активность данного фермента и может быть ассоциирована с повышенным метаболизмом других лекарственных препаратов. Возникновение же кровотечений может быть обусловлено межлекарственным взаимодействием.
Заключение
При сравнении распределения генотипов по полиморфизму rs776746 гена CYP3A5 и по полиморфизму CYP3A4*22 (rs35599367) C>T среди пациентов с наличием/отсутствием кровотечений статистической значимой различий выявлено не было (p>0,05). При сравнении Сmin,ss и Сmin,ss/D ривароксабана также не было отмечено статистически значимых различий в группах обследованных нами пациентов с наличием/отсутствием кровотечений за период наблюдения. Однако при сравнении метаболической активности CYP3A выявлено, что у пациентов с кровотечениями за период наблюдения метаболическая активность СYР3А (соотношение 6-β-гидроксикортизол/кортизол) была статистически значимо выше по сравнению с таковой у пациентов без кровотечений.
Исходя из полученных данных, далее мы оценили метаболическую активность CYP3A в зависимости от генотипа по полиморфным вариантам CYP3A4*22 rs35599367 C>T и CYP3A5*3 rs776746 A6986G и обнаружили, что у пациентов с генотипом СТ по полиморфному варианту CYP3A4*22 rs35599367 C>T метаболическая активность CYP3A была статистически значимо выше, чем у пациентов с генотипом СС, при этом метаболическая активность CYP3A у пациентов с различными генотипами (GA и GG) по полиморфному варианту CYP3A5*3 rs776746 A6986G была сопоставимой.
Метаболическая активность CYP3A4/5 в группе «медленных метаболизаторов» была статистически значимо выше по сравнению с группой «промежуточных метаболизаторов» и выше таковой в группе «нормальных метаболизаторов» (р=0,061), что по-видимому, является следствием феномена феноконверсии.
Результаты нашего исследование демонстрируют необходимость дальнейшего изучения влияния метаболизма ривароксабана на возникновение кровотечений.
Финансирование. Работа поддержана грантом РНФ № 22–15–00251 «Персонализированное применение прямых оральных антикоагулянтов на основе фармакогеномного подхода».
Дополнительная информация
Публикация статьи осуществляется в рамках диссертационной работы Шаталовой Н.А.: «Факторы риска кровотечений у пациентов с фибрилляцией предсердий неклапанной этиологии в сочетании с хронической болезнью почек, получающих ривароксабан».



