Среди сердечно-сосудистых заболеваний, ассоциированных с атеросклерозом, остается высокой доля цереброваскулярных заболеваний, в первую очередь патологии экстракраниальных артерий, приводящей к хронической и/или острой ишемии головного мозга. Экстракраниальные отделы брахиоцефальных артерий (БЦА) поражаются атеросклерозом в 2—5 раз чаще, чем интракраниальные. Классическим местом локализации стенотических атеросклеротических бляшек является бифуркация общей сонной артерии, где возникают вихревые потоки крови, поражающие сосудистый эндотелий [1—4]. Показано, что стеноз внутренней сонной артерии (ВСА) более 60% свидетельствует о нарушении нормальных математических связей между геометрическими параметрами артерий и поступательным движением крови в области каротидной бифуркации, приводя к значимому снижению мозгового кровотока.
Клинически выделяют 4 степени хронического нарушения мозгового кровообращения (ХНМК) [5]. I степень — бессимптомное течение или отсутствие признаков ишемии мозга на фоне доказанного клинически значимого поражения сосудов головного мозга; II степень — преходящие нарушения мозгового кро- вообращения, или транзиторная ишемическая атака; III степень — так называемое хроническое течение сосудисто-мозговой недостаточности, т.е. наличие общемозговой неврологической симптоматики без перенесенного очагового дефицита в анамнезе или его последствий; IV — перенесенный завершенный или полный инсульт. Данная классификация отражает прогрессирование нарушения перфузии мозга от I к IV степени и, соответственно, снижение обеспечения кислородом головного мозга.
В большинстве исследований ограничиваются в основном степенью стеноза артерий и выраженностью клинических проявлений ХНМК [6]. Между тем оценка рисков и показаний к хирургическому лечению у пациентов с патологией БЦА должна основываться не только на степени стеноза артерии и клинических признаках ишемии мозга, но и на исходном состоянии кислородного статуса головного мозга, а также на объективной оценке компенсаторных резервных возможностей церебрального кровообращения. Сопоставление клинической классификации ХНМК с количественными параметрами кислородного статуса является актуальным также с точки зрения прогнозирования течения заболевания и оценки интра- и послеоперационного риска.
Целью настоящего исследования являлась оценка кислородного обеспечения головного мозга у пациентов с патологией БЦА в зависимости от выраженности сосудисто-мозговой недостаточности.
Материал и методы
В исследование включены 469 пациентов с мультифокальным атеросклерозом, гемодинамически значимым поражением БЦА, поступившие в ННИИПК им. акад. Е.Н. Мешалкина для хирургической реваскуляризации артерий брахиоцефального бассейна в объеме каротидной эндартерэктомии. Группу включенных в исследование составили 361 (77%) мужчина и 108 (23%) женщин. Средний возраст больных составлял 62,0±8,4 года.

Критериями исключения из исследования являлись: наличие сахарного диабета, системных аутоиммунных заболеваний, а также гемодинамически значимых стенозов подключичных артерий.
В предоперационный период пациентам не проводилась медикаментозная терапия сосудистыми, метаболическими, а также ноотропными препаратами. Пациенты получали по показаниям гипотензивную терапию: препараты из групп β-адреноблокаторов, диуретиков, антагонистов кальция, ингибиторов ангиотензинпревращающего фермента. С целью коррекции липидного состава крови назначались статины.
Диагноз верифицирован на основании клинико-инструментальных данных. Всем пациентам проводили дуплексное сканирование БЦА и мультиспиральную компьютерную ангиографию ветвей дуги аорты. Степень стеноза ВСА оценивали согласно рекомендациям NASCET и ECST [7, 8].
 Оценку кислородного статуса головного мозга выполняли с помощью транскраниальной спектроскопии прибором INVOS-5100 («Somanetics», США) с билатеральным измерением церебральной оксигенации (ЦО, %) в лобно-височных областях головного мозга. На основе полученных данных рассчитывали индекс гемодинамического соответствия (ИГС, усл. ед.) как отношение ЦО к системному артериальному давлению, коэффициент экстракции кислорода (КЭК, %). Толерантность головного мозга к гипоксии оценивали по длительности пробы с задержкой дыхания. Длительность пробы Штанге менее 30 с расценивали как значительное снижение толерантности к гипоксии, от 30 до 60 с — как умеренное снижение толерантности к гипоксии, более 60 с — как высокую толерантность к гипоксии.
Оценку кислородного статуса головного мозга выполняли с помощью транскраниальной спектроскопии прибором INVOS-5100 («Somanetics», США) с билатеральным измерением церебральной оксигенации (ЦО, %) в лобно-височных областях головного мозга. На основе полученных данных рассчитывали индекс гемодинамического соответствия (ИГС, усл. ед.) как отношение ЦО к системному артериальному давлению, коэффициент экстракции кислорода (КЭК, %). Толерантность головного мозга к гипоксии оценивали по длительности пробы с задержкой дыхания. Длительность пробы Штанге менее 30 с расценивали как значительное снижение толерантности к гипоксии, от 30 до 60 с — как умеренное снижение толерантности к гипоксии, более 60 с — как высокую толерантность к гипоксии.
Для оценки вклада системной гемодинамики в кислородное обеспечение головного мозга всем пациентам проводили эхокардиографию. Анализировали структурно-функциональные параметры левого желудочка (ЛЖ): конечный диастолический размер (КДР, см), конечный диастолический объем (КДО, мл) ЛЖ, фракцию выброса (ФВ, %) ЛЖ, массу миокарда (ММ, г) ЛЖ и сердечный индекс (СИ, л/мин/м2).
Статистическую обработку данных проводили с помощью пакета программ Statistica 6.0 (США). Результаты представлены в виде среднего значения и стандартного отклонения (M±σ). Сравнение параметров нескольких независимых групп выполняли по методу Крускала—Уоллиса. Парное сравнение проводили с использованием критерия Манна—Уитни. Различия считали статистически значимыми при p<0,05.
Результаты
В зависимости от степени ХНМК (по классификации А.В. Покровского) пациенты с патологией БЦА распределились следующим образом: ХНМК I степени — 15 (3%), II степени — 45 (10%), III степени — 299 (64%), IV степени — 110 (23%). Анализ параметров внутрисердечной и системной гемодинамики показал, что вклад данного фактора в эффективность мозговой перфузии во всех группах пациентов одинаков (см. таблицу).
Степень стеноза ВСА с оперируемой (ипсилатеральной) стороны составила в среднем 72,0±10,7%. Среди обследованных пациентов у 15% зарегистрировано одностороннее гемодинамически значимое поражение ВСА, у 70% — двустороннее поражение ВСА, у 15% — значимый стеноз ВСА ипсилатеральной стороны с контралатеральной окклюзией.
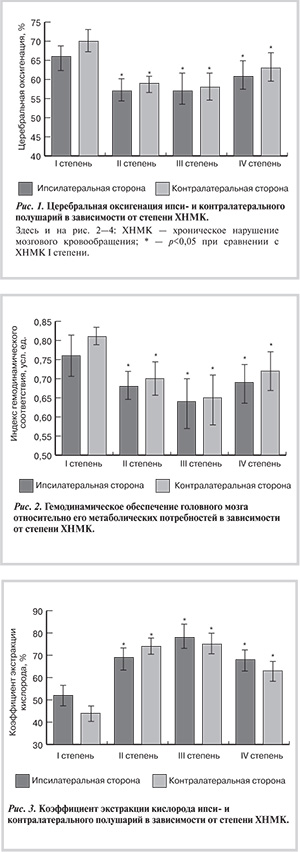
Хроническая сосудисто-мозговая недостаточность характеризуется изменениями в кислородном обеспечении головного мозга. Прогрессирование ХНМК у пациентов с патологией БЦА сопровождается снижением эффективности кислородного обеспечения головного мозга (рис. 1—3).
Согласно представленным данным, ХНМК I степени характеризуется практически нормальными значениями ЦО, что обеспечивается повышением потребления кислорода тканями мозга (КЭК 40—50% при норме <30%). Компенсацию кислородного дефицита берет на себя в том числе контралатеральное полушарие, экстракция кислорода которым на 15% выше, чем ипсилатеральным полушарием мозга.
При ХНМК II степени уровень экстракции кислорода из крови повышается в 2—2,5 раза по сравнению с нормой, однако это не обеспечивает эффективного кислородного обеспечения головного мозга пациентов — ЦО в среднем на 10% по сравнению с пациентами с патологией БЦА и ХНМК I степени.
При ХНМК III степени кислородный статус головного мозга еще более ухудшается, что наиболее четко отражает уровень ЦО, отнесенный к системному артериальному давлению, т.е. ИГС. При этом отмечено еще большее по сравнению с ХНМК II степени повышение КЭК ипсилатерального полушария мозга. Компенсаторные возможности кровотока контралатерального полушария при ХНМК III степени, по-видимому, исчерпаны.
Состояние кислородного статуса головного мозга при ХНМК IV степени, т. е. после перенесенного инсульта, характеризуется декомпенсацией механизмов повышения потребления кислорода, о чем свидетельствует снижение КЭК в данной группе пациентов.
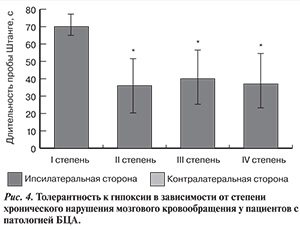
Показатели пробы на устойчивость головного мозга к гипоксии также различаются в зависимости от степени сосудисто-мозговой недостаточности (рис. 4).
Таким образом, степени выраженности ХНМК соотносятся со стадийным снижением эффективности кислородного обеспечения головного мозга и уровнем толерантности мозга к гипоксии.
Обсуждение
ХНМК — патологическое состояние, основным патогенетическим звеном которого является хроническая гипоперфузия головного мозга. Механизмы компенсации нарушения кровоснабжения при прогрессировании ХНМК могут истощаться, энергетическое обеспечение мозга становится недостаточным, в результате чего сначала развиваются функциональные расстройства, а затем его необратимое морфологическое повреждение [9].
Головной мозг характеризуется высокой чувствительностью к недостатку кислорода, что связано с недостаточностью запасов энергоресурсов в мозговой ткани и аэробным типом обменных процессов [10]. Одну из основных групп риска по ишемии головного мозга представляют собой больные с окклюзирующими заболеваниями БЦА. Особенно высок риск ишемического повреждения головного мозга у этих больных в ходе хирургической реваскуляризации [11]. Поэтому дооперационное определение состояния кислородного статуса головного мозга, сопоставление клинической классификации ХНМК и объективных данных представляется актуальным для определения факторов прогноза неблагоприятного исхода заболевания и риска, связанного с хирургическим лечением.
 Для оценки кислородного обеспечения головного мозга нами анализировались данные ЦО, которые сопоставлялись со степенью ХНМК по классификации А.В. Покровского.
Для оценки кислородного обеспечения головного мозга нами анализировались данные ЦО, которые сопоставлялись со степенью ХНМК по классификации А.В. Покровского.
При сопоставлении клинической классификации ХНМК с объективными показателями кислородного статуса головного мозга выявлено следующее. ХНМК I степени характеризуется нормальными ЦО и толерантностью к гипоксии, что обеспечивается за счет повышения экстракции кислорода тканями головного мозга относительно нормальных значений, в том числе контралатеральным полушарием. При II степени ХНМК уровень кислородного обеспечения головного мозга и его толерантность к гипоксии снижаются, несмотря на увеличение КЭК в 2—2,5 раза выше нормы. На этой стадии значительно задействованы резервные возможности контралатерального полушария, экстракция кислорода которым выше, чем ипсилатеральным. У пациентов с ХНМК III степени происходит наибольшее расходование резервных возможностей обеспечения мозга кислородом (повышение КЭК), однако резервы контралатерального полушария, вероятно, на данной стадии истощены, о чем свидетельствует более высокий КЭК ипсилатерального полушария. Повышение экстракции кислорода тканями мозга у пациентов с ХНМК III степени не обеспечивает адекватного кислородного обеспечения головного мозга, ЦО и толерантность головного мозга к гипоксии снижены. ХНМК IV степени сопровождается декомпенсацией механизмов повышения потребления кислорода тканями мозга, о чем свидетельствует значительное снижение КЭК относительно такового при III степени. При этом уровень ЦО и толерантности к гипоксии остается сниженным.
Необходимо подчеркнуть, что в условиях покоя, даже при выраженном стенозе ВСА, ЦО может быть в пределах нормы. Однако, если в ответ на функциональные пробы уровень ЦО оказывается ниже нормы, имеются все основания предполагать декомпенсацию кровообращения в пораженном полушарии [12, 13]. Так, по данным исследования, проведенного при участии 398 пациентов с атеросклеротическим поражением экстракраниальных артерий [14], показано, что у пациентов с нарушением мозгового кровообращения устойчивость к гипоксии соответствовала низкой толерантности. При первой стадии нарушения мозгового кровообращения устойчивость к гипоксии соответствовала умеренно сниженной толерантности. Самая низкая толерантность к гипоксии выявлена при II стадии. При III стадии толерантность к гипоксии оставалась низкой, но немного повышалась относительно II стадии [14], что сопоставимо и с нашими данными.
По мнению ряда авторов, изменение толерантности к гипоксии при разной степени сосудисто-мозговой недостаточности соотносится с фазами общего адаптационного синдрома по Г. Селье [15]. I степень ХНМК соответствует фазе активации общего адаптационного синдрома, при этом сохранена достаточная чувствительность центральных и периферических хеморецепторов и повышена активность симпатико-адреналовой системы. Это обеспечивает повышение активности лимфоцитарного звена, фагоцитарной активности, незначительное повышение лейкоцитарного коэффициента и некоторое снижение толерантности к гипоксии. При II степени ХНМК адаптационный процесс переходит в фазу резистентности с наибольшей активностью гипофизарно-надпочечниковой оси, проявляющейся возрастанием лейкоцитарного коэффициента, повышением фагоцитарной активности и высокой сенситивностью центральных и периферических хеморецепторов, что приводит к резкому снижению толерантности к гипоксии. При III степени ХНМК происходит истощение адаптационных механизмов, снижается реактивность рецепторного и рефлекторного аппарата, в связи с чем длительность пробы с задержкой дыхания увеличивается по сравнению с таковой при II стадии. При этом усугубляется стрессовая реакция лейкоцитов периферической крови, отмечаются элементы аутоиммунных реакций. Эти изменения свидетельствуют о выраженном снижении неспецифической резистентности организма [14].
Заключение
Оценка церебральной оксигенации и толерантности головного мозга к гипоксии у пациентов с атеросклеротическим поражением брахиоцефальных артерий позволяет охарактеризовать патофизиологические звенья кислородного метаболизма головного мозга, что, вероятно, имеет большое значение при определении риска хирургического лечения и послеоперационного прогноза.



