Актуальность
Изучение микробиома кожи человека при различных заболеваниях и у здоровых пациентов является актуальной темой большинства исследований современной медицины. Под термином «микробиом» принято понимать совокупность микроорганизмов, населяющих определенные анатомические локусы, включая бактерии, вирусы и грибы, а также их гены, метаболиты и факторы окружающей среды, оказывающие влияние на их видовой состав и жизнедеятельность. Термин «микробиота» ограничен описанием структуры группы комменсалов, симбиотических и патогенных микроорганизмов, обнаруженных в фиксированной среде. Количество микробных клеток, колонизирующих организм человека, в 10 раз больше человеческих. Помимо детального изучения уровня контаминации и состава микробиоты кожи и кишечника в многочисленных исследованиях были получены данные о существенном влиянии комменсалов и патогенов на активность иммунологических, гормональных и метаболических процессов [1, 2].
Стабильность и индивидуальность микробиома кожи здорового человека находятся в тонко настроенном равновесии, нарушение которого может приводить к различным воспалительным заболеваниям кожи. На ее поверхности и непосредственно в сальных железах наиболее часто выявляются представители трех основных бактериальных родов: Corynebacteria, Propionibacteria и Staphylococci [3].
Propionibacterium acnes является одним из патогенетических факторов развития рака предстательной железы, саркоидоза, инфекционного эндокардита, инфицирования протезов суставов, желудочковых шунтов центральной нервной системы и сердечных имплантов [4–7]. Наиболее глубоко изучена роль данных бактерий в патофизиологии акне, а филотипы, участвующие в развитии данного заболевания, теперь принято выделять в отдельные виды, которые идентифицируют как Cutibacterium acnes. С учетом знаний о ключевой роли C. acnes в формировании угрей очевидным является, что комплексная терапия акне должна проводиться с использованием средств с антибактериальной активностью. Однако в связи с высоким удельным весом антибиотикорезистентности среди пациентов с данной патологией в современных клинических рекомендациях антибиотики для местной и системной терапии являются препаратами второй линии и часто вопрос об их использовании рассматривается специалистами только в отсутствие эффекта от применения топических ретиноидов, бензоила пероксида или азелаиновой кислоты [8].
Цель исследования: обоснование применения системных антибиотиков в качестве стартовой терапииу пациентов со среднетяжелым течением акне. Провести сравнительную оценку клинической эффективности раннего применения системной антибиотикотерапии в комплексной терапии при среднетяжелом течении акне. Оценить влияние комплексной терапии со стартовым назначением системных антибиотиков на приверженность лечению пациентов со среднетяжелым течением акне.
Методы
Под наблюдением находились 60 больных (28/46,67% мужчин и 32/53,33% женщин) со средне тяжелым течением акне в возрасте от 18 до 50 лет (средний возраст – 29,28±3,17 года). Преобладающим клиническим проявлением акне у всех больных являлось наличие пустулезных элементов и папул (более 20) на фоне выраженной себореи, а также наличие открытых и закрытых комедонов. У большинства пациентов отмечались явления постакне, представленных атрофическими рубцами различной конфигурации и поствоспалительными пятнами. Основным критерием включения в исследование помимо наличия акне являлось отсутствие наружной или системной терапии заболевания, включая косметические процедуры и аппаратные методики, в течение последних 6 месяцев. Процедуры исследования проводились в соответствии с Хельсинкской декларацией. Информированное согласие было получено от всех субъектов до начала исследования. Все испытуемые подписали форму согласия на публикацию результатов исследования. Данные конфиденциальности и неприкосновенности частной жизни участников строго соблюдались, а субъекты были проинформированы о том, что у них есть право выйти из исследования в любое время.
Оценка степени тяжести акне проводилась у всех больных на этапе до начала терапии каждые 4 недели и через 4 месяца лечения с использованием индекса GAGS (Global Acne Grading System), который был разработан в 1997 г. A. Doshi et al. [9]. Согласно первичным данным, при оценке степени тяжести акне с использованием данного индекса необходимо разделить участки кожи пациента на условные 6 областей: лоб, правая щека, левая щека, нос, подбородок, грудь и спина. К каждой области применяется свой коэффициент: лоб, правая щека, левая щека по 2, нос, подбородок по 1, грудь и верх спины по 2+2. Оценка выраженности и тяжести проявлений акне проводилась по 4-балльной шкале (чистая кожа – 0, один комедон –1, одна папула – 2, одна пустула – 3, один узел – 4). Балл для каждой области представляет собой произведение наиболее тяжелых проявлений и коэффициента площади. Затем эти баллы суммируются для получения общего числа индекса. Результаты оценивали по следующим критериям: 1–18 – легкая степень тяжести акне, 19–30 – среднетяжелая степень тяжести акне, 31–38 – тяжелая степень тяжести акне, >38 баллов – очень тяжелая степень тяжести акне. Максимальное числоо баллов – 52.
По окончании терапии проводилась глобальная оценка терапевтического эффекта с определением числа и соотношения пациентов с достижением ремиссии, отличным (снижение GAGS на 90%), хорошим (снижением GAGS на 75%) и удовлетворительным (снижение GAGS на 50%) результатами и оценка приверженности больных лечению по шкале Мориски–Грина [10]. Приверженными считались больные, ответившие на вопросы тестирования «нет» более 3 раз.
Вопросы к тесту Мориски–Грина:
- Забывали ли Вы когда-либо принимать (наносить) препараты?
- Не относитесь ли Вы иногда невнимательно к часам приема (нанесения) лекарств?
- Не пропускаете ли Вы прием (нанесение) препаратов, если чувствуете себя хорошо?
- Если Вы чувствуете себя плохо после приема (нанесения) лекарств, не пропускаете ли Вы следующий прием?
Помимо этого регистрировали побочные эффекты в процессе лечения. Статистические исследования проводили с использованием программы StatSoft Statistica.
Больные были рандомизированы в 2 сравниваемые терапевтические группы. Группу I составили 30 пациентов (12 мужчин и 18 женщин), которым была проведена монотерапия с использованием геля, действующим веществом которого являлась фиксированная комбинация адапалена 1 мг/г и бензоила пероксида 25 мг/г 1 раз в сутки в течение 28 недель.
В группу II были включены 30 больных (16 мужчин и 14 женщин), которым была назначена комплексная терапия с использованием фиксированной комбинации адапалена 1 мг/г и бензоила пероксида 25 мг/г 1 раз в сутки в течение 28 недель и диспергируемые таблетки доксициклина моногидрата 100 мг 2 раза в сутки в течение первых 4 недель. Всем больным было рекомендовано использование специализированных косметических средств для ухода за проблемной кожей в течение всего курса лечения.
Результаты
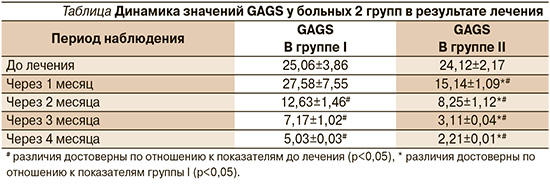
В результате сравнительного анализа динамики индекса тяжести акне GAGS в двух терапевтических группах установлено, что включение в комплексную терапию антибиотиков способствовало достоверной регрессии средних значений индекса уже через месяц от начала терапии, когда в группе I наблюдалась тенденция к увеличению данного показателя, хотя различия не были достоверными по отношению к показателям до лечения. Дальнейшая динамика индекса GAGS в группах также значительно и достоверно различалась, что характеризовалось более быстрым снижением данного показателя в группе II и более низкими значениями по отношению к средним показателям индекса в группе I (см. таблицу).
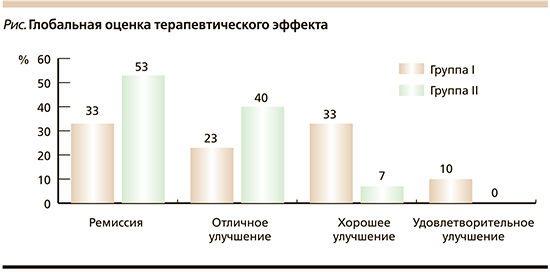
С целью определения наиболее эффективного метода терапии среди сравниваемых групп проведена глобальная оценка терапевтического эффекта (см. рисунок). Установлено, что стартовая терапия с включением антибиотика позволила повысить эффективность лечения. После окончания курса терапии число пациентов с ремиссией акне или отличным улучшением в группе II было больше на 20 и 17% соответственно, чем в группе, где проводилась монотерапия с использованием топического препарата.
На окончательном этапе наблюдения проводилось тестирование больных с целью определения влияния метода лечения на приверженность пациентов терапии. В группе I приверженных пациентов было 14 (46,67%), в группе II – 24 (80%), р<0,05, что было обусловлено более быстрым наступлением клинического эффекта. Побочные эффекты характеризовались развитием ретиноевого дерматита различной интенсивности у всех субъектов, антибиотикассоциированной диареи у одной пациентки и признаков повышения внутричерепной гипертензии (головные боли, шум и заложенность в ушах) у 2 больных. Все побочные эффекты были легкой степени и не требовали отмены или смены режима терапии.
Обсуждение
Среди основных патофизиологических факторов развития акне ключевым звеном считается реакция кожи на активизацию C. acnes, которая проявляется формированием субклинического и явно выраженного перифолликулярного воспаления. Данные бактерии при определенных условиях проявляют выраженную ферментативную активность с выделением липазы, протеазы, фосфатазы, гиалуронатлиазы, эндогликоцерамидазы и нейраминидазы. Продуцируемые C. acnes ферменты расщепляют кожное сало до свободных жирных кислот, которые через активацию Toll-подобных рецепторов индуцируют воспалительные реакции с поражением волосяных фолликулов, сальных желез и дермального внеклеточного матрикса, что в конечном итоге усугубляет воспаление и способствует формированию рубцов. Также C. acnes способствуют комедогенезу путем образования окисленного сквалена и свободных жирных кислот, что приводит к качественному изменению кожного сала [11, 12]. C. acnes активируют сигнальный путь рецептора IGF-1/IGF-1 и регуляцию экспрессии филаггрина, увеличивая уровни интегринов-α3, -α6 и vβ6, тем самым повышая пролиферацию кератиноцитов и их дифференцировку, что является еще одним механизмом образования комедонов [13, 14]. Иммуногенное влияние C. acnes доказано в различных исследованиях. Установлено, что данные бактерии обладают митогенной активностью в отношении Т-клеток, результатом чего является возбуждение процессов в адаптивном иммунитете с экспрессией Th1 и Th17. C. acnes провоцируют индукцию мононуклеарных клеток периферической крови с экспрессией интерлейкина-6 (ИЛ-6), ИЛ-1β, трансформирующего фактора роста-β и интерферона-γ. Таким образом, современные знания о многофакторной роли C. acnes в патофизиологии акне обусловливают необходимость проведения терапевтических мероприятий, направленных на подавление ее активности на ранних этапах лечения [15].
Несмотря на то что в исследованиях не была установлена корреляция степени тяжести акне, контаминации кожи и сальных желез бактериальной биотой, абсолютно точно доказано, что при антибактериальной терапии снижение микробной колонизации кожи способствует подавлению активности воспалительного процесса при акне. Неантибактериальные действия антибиотиков обусловлены ингибирующим действием в отношении липаз бактерий, а также противовоспалительным и иммуномодулирующим воздействиями [16]. Так, установлено прямое дозозависимое подавляющее действие антибиотиков на активность митоза лимфоцитов и фагоцитоза, снижение секреции провоспалительных цитокинов ФНО-a, ИЛ-1 и-6 и индукцию секреции противовоспалительного цитокина ИЛ-10; ингибирование лейкотаксиса и снижение активации комплемента C3 (только у тетрациклинов); модуляцию альфа-меланоцитстимулирующего гормона (α-MSH) и ингибирование генерации активных форм кислорода. Сегодня одним из главных вопросов, касающихся эффективности антибиотиков при акне, является задача в определении, какой из эффектов (антибактериальный или противовоспалительный) оказывает основное терапевтическое действие. Так, например, до настоящего времени нет полного объяснения эффективности субантибактериальных доз антибиотиков при акне или розацеа [17].
В последние годы, согласно зарубежным и Российским клиническим рекомендациям, антибиотики должны быть использованы как лекарственные средства второй линии в лечении акне. Указано, что они не должны применяться в качестве монотерапии и их не следует комбинировать с топическими антибиотиками [18, 19]. Однако рассмотрение вопроса раннего применения препаратов данного класса при среднетяжелом течении акне является обоснованным и рациональным, с учетом современных сведений о противовоспалительной и антилипазной активности антибактериальных средств, в частности тетрациклинов.
В настоящем исследовании установлено, что применение системных антибиотиков на старте лечения пациентов со среднетяжелой степенью течения акне в комплексе с топической терапией способствует снижению вероятности экзацербации дерматоза при применении ретиноидов, а также более быстрому снижению активности клинических симптомов заболевания, формированию ремиссии и выраженному улучшению течения дерматоза у достоверно большего числа пациентов. Быстрая регрессия высыпаний в группе комплексной терапии способствовала повышению приверженности пациентов проводимому лечению, а низкий уровень побочных эффектов при достаточно краткосрочном применении доксициклина моногидрата позволяет расширять показания к его назначению при акне.
Выводы
В результате проведенного исследования установлено, что терапия акне среднетяжелой степени тяжести с использованием системных антибиотиков на начальных этапах лечения с последующим применением средств наружной терапии способствует достоверно более быстрой динамике клинических симптомов дерматоза и увеличению числа пациентов с достижением клинической ремиссии на 20%. Более быстрое снижение активности симптомов среднетяжелого течения акне при поэтапном применении системной антибиотикотерапии и наружного лечения способствует повышению приверженности пациентов проводимой терапии.



