После опубликования результатов международного многоцентрового рандомизированного клинического испытания (РКИ) POISE [1] вопрос о периоперационном использовании β-адреноблокаторов у 8351 больных, подвергаемых так называемым некардиальным хирургическим вмешательствам (хирургия аорты, магистральных артерий), стал предметом активной дискуссии. Действительно, не могло не остаться незамеченным достоверное снижение частоты развития первичной конечной точки (сочетание таких исходов, как смерть по сердечно‑сосудистой причине, нефатальный инфаркт миокарда или нефатальная остановка сердца в пределах 30 дней после рандомизации) при применении β-адреноблокатора метопролола сукцината, с одной стороны, и повышение риска смерти от всех причин и развития инсультов в этой группе пациентов, с другой. Поэтому неслучайным оказались призывы к комитетам по рекомендациям пересмотреть позицию в отношении поддержки использования β-адреноблокаторов у пациентов, подвергаемых некардиальным хирургическим вмешательствам. В качестве одного из таких призывов можно привести выводы мета‑анализа, выполненного S. Bangalore и соавт. [2], которые объединили результаты 33 исследований РКИ (всего 12 306 больных), в том числе и РКИ POISE [1]. Тем не менее до настоящего времени рекомендации остались неизменными [3, 4], а противоречивые результаты ряда РКИ стали
ассоциировать с особенностями их дизайна.
В свою очередь периоперационное применение β-адреноблокаторов у больных ишемической болезнью сердца (ИБС), подвергаемых реваскуляризации миокарда — транслюминальной баллонной ангиопластике (ТБКА) и коронарному шунтированию (КШ) рассматривается в качестве важного компонента защиты миокарда, обеспечивающей снижение летальности у пациентов данной категории [5–10]. Кроме того, терапия β-адреноблокаторами ассоциируется с более низкой
частотой развития фибрилляции предсердий в раннем постоперационном периоде [11]. Вместе с тем ряд авторов указывают на недостаточно частое применение данных лекарственных средств у больных ИБС, подвергнутых реваскуляризации миокарда [12]. Более того, при оценке долгосрочных эффектов β‑адреноблокаторов в отношении предупреждения и лечения ишемических осложнений у больных ИБС после КШ были получены неоднозначные результаты [13, 14].
В свете изложенного целью настоящего исследования стало проведение клинико-фармакоэкономического анализа длительного применения 3 β-адреноблокаторов
(бисопролола, атенолола и метопролола тартрата) у пациентов с ИБС, подвергнутых КШ.
Материал и методы
В открытое проспективное, рандомизированное исследование были включены 294 пациента с ИБС
(272 мужчины, 22 женщины) в возрасте от 33 до 70 лет (в среднем 54,4±0,4 года), проходившие стационарное лечение в кардиохирургическом и кардиологическом отделениях Волгоградского областного кардиологического центра (ВОКЦ), а затем наблюдающиеся в реабилитационном отделении поликлиники этого же учреждения. Показаниями к проведению КШ у пациентов с ИБС, включенных в исследование, явились сохраняющиеся приступы стенокардии на фоне комбинированной антиангинальной терапии, многососудистое поражение коронарного русла, гемодинамически значимое поражение ствола левой коронарной артерии (ЛКА). Средний функциональный класс
(ФК) тяжести стабильной стенокардии по классификации Канадской ассоциации кардиологов составил
2,9±0,2, а средний ФК хронической сердечной недостаточности (ХСН) по классификации Нью-Йоркской ассоциации сердца — 2,2±0,1.
Больные ИБС, подвергнутые КШ, были рандомизированы в 3 группы (рандомизация осуществлялась методом конвертов). В 1‑ю группу были включены 98 больных (87 мужчин и 11 женщин, средний возраст 55±0,1 года и давность заболевания в среднем 4,4±0,04 года), получающих бисопролол (конкор, Merck KgaA, Германия) в начальной дозе 2,5–5 мг с повышением до 10 мг через 1 мес в течение 2 нед до операции, затем продолжившие прием препарата в послеоперационном периоде и на протяжении последующих 3 лет. Во 2-ю группу вошли 98 больных ИБС (97 мужчин и 1 женщина, средний возраст 53,2±0,1 года, давность заболевания 5,5±0,6 года), которые получали атенолол (атенолол, Синтез, Россия) в начальной дозе 12,5–25 мг с повышением до 50 мг через 1 мес в течение 2 нед до операции, затем продолжившие прием препарата в послеоперационном периоде и на протяжении последующих 3 лет. В 3-ю группу объединили 98 пациентов с ИБС (93 мужчины и 6 женщин, средний возраст 54,8±0,1 года, давность заболевания 5,9±0,5 года), которые получали метопролола тартрат в начальной дозе 25–50 мг с повышением до 200 мг через 1 мес в течение
2 нед до операции, затем продолжившие прием препарата в послеоперационном периоде и на протяжении последующих 3 лет. Пациенты с ИБС, включенные в исследование, принимали базисную терапию по поводу основного заболевания, при этом выбор лекарственных препаратов и их дозировок осуществляли в соответствии с утвержденными внутрибольничными стандартами ведения больных данной категории. Регистрировали сведения о дозе и кратности назначения этих препаратов.
Продолжительность наблюдения за больными ИБС, включенными в исследование, составила 3 года, в течение которых осуществлялось динамическое наблюдение за их клинико‑инструментальными параметрами.
Затраты на лечение больных рассчитывали на основании стоимости койко-дня, лабораторного и инструментального обследования, хирургических вмешательств, амбулаторных визитов (данные определяли по базовому тарифу цен по данным Волгоградского Территориального фонда обязательного медицинского страхования и по ценам на платные услуги ВОКЦ, утвержденным
Областным комитетом здравоохранения при администрации Волгоградской области на момент окончания каждого года с учетом коэффициента дефлятора в соответствии с Приказами Минэкономразвития РФ от 19.11.2007 № 401; от 03.11.2006 № 359; от 27.10.2005 № 277;
от 09.11.2004 № 298; от 11.11.2003 № 337; Федеральный закон от 31.12.2002 № 191-ФЗ). Затраты на лечение пациентов с использованием таких групп препаратов как β‑адреноблокаторов, ингибиторов ангиотензинпревращающего фермента, нитратов, антагонистов кальция, аспирина, нефракционированного гепарина, низкомолекулярных гепаринов, триметазидина при условии проведения КШ определяли на конец каждого года исследования (по данным прайс‑листа компании «Протек» и розничным ценам на лекарственные средства в аптечной сети (аптека «Волгофарм», «Пересвет», «Аптека 36,6»).
Для определения эффективности затрат в периоперационном периоде использовался коэффициент затраты/эффективность Ксе=С/Е. Анализ затраты/полезность выполняли с применением критерия QALY (Quality adjusted life years)— числа сохраненных лет жизни с поправкой на ее качество.
Ангиографию коронарных артерий (КА) выполняли на установке BICOR (Siemens, Германия). При
анализе коронарограммы оценивали локализацию и степень поражения КА, гемодинамически значимыми считали сужение просвета КА на 50% и более. Структурно‑функциональные параметры сердца оценивали с помощью эхокардиографии на аппарате Acuson 128 XP/10 m (США). Помимо стандартных показателей систолической и диастолической функций левого желудочка (ЛЖ), рассчитывали величину миокардиального стресса ЛЖ (МСЛЖ) по формуле: МСЛЖ = САД × КСР/(4 × ТЗСЛЖс) × (1+ТЗСЛЖс/КСР), где САД — систолическое АД, КСР — конечный систолический размер
ЛЖ, ТЗСЛЖс — толщина задней стенки ЛЖ в систолу. Пробу с физической нагрузкой проводили на велоэргометре фирмы Marquette Hellige (Германия) по стандартному протоколу «Французский стандарт».
Статистическую обработку данных исследования проводили с использованием пакета статистических
программ Microsoft XP, StatSoft Statistica 6.0, программы BIOSTAT. Выполняли дисперсионный анализ повторных измерений. Для определения значимости переменной в отношении непрерывных показателей использовали t‑критерий Стьюдента с поправкой Бонферрони, для дискретных показателей — критерий χ2. Изменения считали статистически значимыми при р<0,05.
Результаты и обсуждение
Клинико‑демографические характеристики больных ИБС, включенных в исследование, приведены
в табл. 1. По большинству анализируемых параметров достоверных различий между больными, принимающими бисопролол (1‑я группа), атенолол (2‑я группа) и метопролол (3‑я группа) обнаружено не было. У большинства пациентов имелись указания в анамнезе на перенесенный инфаркт миокарда (ИМ), кроме того, у 11,2% (в группе метопролола), 12,2% (в группе бисопролола) и 15,3% (в группе атенолола) больных была выявлена аневризма ЛЖ. Следует заметить, что в каждой исследуемой группе пациентов с ИБС достаточно часто встречались такие состояния, как сахарный диабет, ожирение и хроническая обструктивная болезнь легких (достоверных различий по частоте выявления
этих состояний в 3 группах больных не отмечено).
Таблица 1. Клинико-демографические характеристики больных ИБС, включенных в исследование.
Таблица 2. Характеристики поражения коронарного русла у больных ИБС, подвергшихся КШ, в группах бисопролола, атенолола и метопролола.
По данным коронарографии не было выявлено достоверных различий по степени и характеру поражения коронарного русла в сравниваемых группах больных. Так, многососудистое поражение КА выявлено у 84 (85,7%) больных ИБС, принимавших бисопролол, в группах атенолола и метопролола — у 90 (91,8%) больных; однососудистое поражение отмечалось соответственно в 14 (14,3%), 8 (8,2%), и 8 (8,2%) случаях. Характер поражения коронарного русла у пациентов в исследуе-
мых группах представлен в табл. 2.
Структура проведенных больным ИБС хирургических вмешательств, включенным в исследование, представлена в табл. 3. Большинству пациентов была проведена полная реваскуляризация миокарда (в 1‑й группе в 84,7%, во 2‑й группе — в 77,5%, в 3‑й группе — в 81,6% случаев). Следует подчеркнуть, что у 12 (12,2%) больных 1-й группы, у 15 (15,3%) во 2‑й группе и у 11 (11,2%) в 3‑й группе КШ сочеталось с резекцией аневризмы ЛЖ. Достоверных различий по частоте выполнения отдельных видов хирургических вмешательств в 3 сравниваемых группах пациентов с ИБС обнаружено не было.
Исключение составила лишь меньшая частота КШ без искусственного кровообращения и эндартерэктомии из КА в 1-й группе (группа бисопролола).
Динамика снижения ФК стенокардии и ХСН у больных ИБС, включенных в исследование, приведена
в табл. 4. Уменьшение ФК стенокардии носило высоко достоверный характер (p<0,001): в 1‑й группе (бисопролол) с 2,8±0,05 до 0,01±0,001 к 1-му месяцу наблюдения и до 0,2±0,03 к концу периода наблюдения; во 2‑й группе (атенолол) — с 2,9±0,05 до 0,2±0,02 к 1‑му месяцу и до 0,6±0,05 к концу периода наблюдения; в 3‑й группе (метопролол) — с 3±0,05 до 0,2±0,02 к 1‑му месяцу и до 0,5±0,05 к концу периода наблюдения.
Таблица 3. Характеристика хирургических вмешательств у больных ИБС, включенных в исследование.
Таблица 4. Динамика ФК стенокардии и ФК ХСН у больных ИБС, включенных в исследование.
Таблица 5. Динамика АД, ЧСС у больных ИБС, подвергшихся КШ, в группах наблюдения за весь период наблюдения.
В группе больных ИБС, принимавших бисопролол, было отмечено достоверное снижение ФК ХСН
с 2,2±0,04 до 1,57±0,06 (p<0,01) к концу периода наблюдения, в то время как в группах атенолола и метопролола отмечалась лишь тенденция к уменьшению ФК ХСН (за период наблюдения — с 2,1±0,03 до 1,9±0,03 и с 2,1±0,03 до 1,8±0,04 соответственно). Заметим, что последние данные еще раз подчеркивают целесообразность назначения тех β-адреноблокаторов, эффективность которых доказана при лечении больных с ХСН.
Динамика средних значений артериального давления (АД) и частоты сердечных сокращений (ЧСС), а также средние дозы принимаемых β‑адреноблокаторов в 3 сравниваемых группах больных ИБС приведена в табл. 5. В целом бисопролол, атенолол и метопролол оказывали сопоставимое влияние на АД и ЧСС (достоверных различий по этим показателям между сравниваемыми группами пациентов не обнаружено). Следует заметить, что особенно во 2‑й (атенолол) и 3‑й (метопролол) группах отчетливо прослеживалась тенденция к увеличению суточной дозы β‑адреноблокаторов за весь период наблюдения.
Изменения большинства структурно‑функциональных параметров сердца в группах больных ИБС, принимавших участие в исследовании, не носили статистически значимого характера. Было отмечено, что фракция выброса (ФВ) ЛЖ в группе пациентов, принимавших бисопролол и атенолол, увеличилась за период наблюдения на 4% (с 51,7±1,1% до 54,6±0,7% к 1‑му месяцу и до 53,85±0,8% к концу периода наблюдения; с 49,3±1,07 до 52,2±0,7 к 1‑му месяцу и до 51,3±0,9% к концу наблюдения соответственно). В группе метопролола динамика ФВ ЛЖ носила еще менее значимый характер — всего 2,1%.
Конечный диастолический объем ЛЖ достоверно уменьшился в группе пациентов, принимавших атенолол и метопролол: в группе атенолола на 8,3% — с 155±4,6 мл к 1‑му месяцу до 147,1±3,2% и к концу периода наблюдения до 146,1±3,7%, в группе метопролола на 12,8% — с 153,6±4,4 до 143,3±3,14 мл к 1‑му месяцу и 143,4±3,7 мл к концу наблюдения. В группе бисопролола конечный диастолический объем ЛЖ остался практически неизменным: с 137,7±3,6 до 139,6±3,4 мл к окончанию исследования.
Кроме того, была обнаружена отчетливая тенденция к уменьшению МСЛЖ. Так, величина МСЛЖ в группе бисопролола до хирургического вмешательства составила с 120,5±3,7 ед, а через 1 мес и затем 1, 2 и 3 года терапии — соответственно 128,37±4,2, 127,2±3,9, 127,2±3,9 и 118,4±3,2 ед, причем к 3‑му году лечения различия носили достоверный характер (p<0,05 по сравнению с исходным значением показателя). В группе атенолола отмечалось снижение МСЛЖ с 119,1±3,3 до 115,4±2,9 ед, а затем — увеличение до 120,2±3,8, 122,2±3,8 и 126,4±4,4 ед к концу 1, 2 и 3‑го года соответственно, в группе метопролола — с 123,9±3,5 до 118,7±3,3 ед к моменту выписки, до 125,3±4,3 ед — к концу 1‑го года, до 126,8±4,1 ед — к концу 2‑го года и до 133±4,4 ед — к концу 3‑го года.
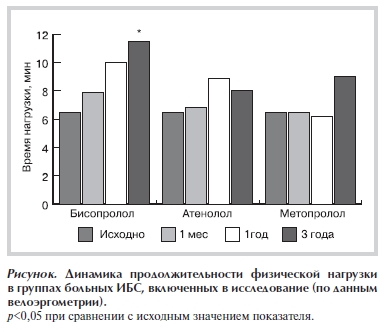
Отчетливое увеличение продолжительности нагрузочной пробы у больных ИБС, включенных в исследование, было отмечено, прежде всего, только в группе бисопролола (с 7±0,03 до 12±0,06 мин; p<0,05), в группах атенолола и метопролола изменения данного параметра носили недостоверный характер (см. рисунок). При анализе общих затрат в исследуемых группах средняя сумма общих прямых медицинских затрат в периоперационном периоде у пациентов 1‑й группы, принимавших бисопролол, составила 215 582,9±5246 руб., в группе атенолола — 228 471,9±7700 руб., в группе метопролола — 225 973,4±7940 руб. Из них затраты на медикаментозную терапию в 1-й группе составили 44 718,9±1877 руб., во 2‑й группе — 37 781,7±3115 руб., а в 3‑й группе — 41 549,2±2982,6 руб.
В 1-й группе средняя длительность пребывания больных в стационаре в периоперационном периоде
составила 33,2±1,01 дня (во 2-й группе — 35,8±1,4 дня, в 3‑й группе — 36,2±1,6 дня), в реанимационном отделении — 1,8±0,1 сут (во 2‑й группе — 2,6±0,2 сут; в 3‑й группе — 3,2±0,3 сут), а в послеоперационный период — 19,3±0,6 дня (во 2‑й группе —23,2±0,9 дня, в 3‑й группе — 22±0,98 дня).
Дополнительные расходы во время проведения хирургического вмешательства в 1-й группе (бисопролол) составили 216±25,5 руб.: реторакотомия проводилась у 2 (2,04%) больных, решунтирование — у 2 (2,04%), постановка внутриаортального баллонного контрпульсатора — у одного (1,02%). Во 2‑й группе (атенолол) дополнительные расходы равнялись 128,3±15,8 руб.: реторакотомия проводилась у 3 (3,1%) больных, постановка внутриаортального баллонного контрпульсатора — у 4 (4,1%). В 3‑й группе (метопролол) дополнительные расходы достигали 192,4±23,8 руб.: реторакотомия проводилась у 7 (7,1%) больных, решунтирование — у одного (1,02%), постановка внутриаортального баллонного контрпульсатора — у 3 (3,1%).
Причины повторных госпитализаций больных ИБС, подвергшихся КШ, за весь период наблюдения приведены в табл. 6.
В 1-й группе (бисопролол) в течение 3 лет наблюдения госпитализация потребовалась в 11 случаях,
средняя длительность пребывания больных в стационаре составила 7,5±0,6 дня. За период наблюдения одному (1,02%) пациенту выполнялась шунтография и одному (1,02%) — каротидная эндартерэктомия. Госпитализация по поводу острых коронарных синдромов осуществлена в 4 (4,1%) случаях. За 3 года число амбулаторных визитов равнялось 12,6±0,3 дня.
Во 2-й группе (атенолол) в течение 3 лет наблюдения госпитализация потребовалась в 14 случаях, средняя длительность пребывания больных в стационаре составила 12,8±1,1 дня. Всего за период наблюдения одному (1,02%) больному была проведена шунтография. Повторное вмешательство на коронарных артериях (транслюминальная баллонная ангиопластика ТЛБАП со стентированием) выполнено одному (1,05%) пациенту в течение 3‑го года после КШ. За 3 года число амбулаторных визитов достигло 12,3±0,4.
В 3-й группе (метопролол) в течение 3 лет наблюдения госпитализация потребовалась в 19 случаях, средняя длительность пребывания больных в стационаре составила 21,2±1,4 дня. Всего за время наблюдения 3 (3,1%) больным была проведена шунтография. У одного (1,02%) пациента выполнена ТЛБАП со стентированием в течение 3‑го года наблюдения и у одного (1,02%) имплантирован электрокардиостимулятор. За 3 года число амбулаторных визитов составило 12,7±0,4.
Таблица 6. Причины повторных госпитализаций больных ИБС, включенных в исследование, за весь период наблюдения.
Таблица 7. Средние прямые медицинские затраты у больных ИБС, подвергшихся КШ, в исследуемых группах за весь период наблюдения.
Следует отметить, что во всех 3 сравниваемых группах больных ИБС была отмечена разная частота возобновления стенокардии: наименьшая — в 1-й группе (бисопролол) — у 13 (13,3%) пациентов, в то время как во 2‑й (атенолол) и 3‑й (метопролол) группах — у 27 (27,5%) и 30 (30,6%) больных соответственно. Более низкая частота развития стенокардии в 1‑й группе сочеталась и с меньшей частотой повторных госпитализаций (см. табл. 6). Подчеркнем, что и наиболее высокая толерантность
к физической нагрузке была зафиксирована в группе больных ИБС, получавших бисопролол. В целом бисопролол выглядел более предпочтительным, чем два других сравниваемых β‑адреноблокатора (атенолол, метопролол).
Полученные нами данные несколько отличаются от результатов 2 других плацебо‑контролируемых
РКИ [13, 14], в которых не удалось продемонстрировать преимущество длительной терапии (2 года)
β‑адреноблокаторов в отношении частоты развития таких событий, как инфаркт миокарда, нестабильная стенокардия, потребность в повторных процедурах по реваскуляризации миокарда или частоты возникновения и степени тяжести стенокардии напряжения. Однако в качестве ограничения этих РКИ следует рассматривать низкую частоту развития анализируемых событий, различия в исходных характеристиках сравниваемых групп (β‑адреноблокаторов или плацебо), а также высокий процент больных, перешедших из «слепой» в «открытую» фазу исследования. Заметим, что в нашем исследовании также редко наблюдали случаи острых коронарных синдромов и выполнение ТЛБАП. Все это указывает на необходимость дальнейшего проведения крупных, двойных слепых РКИ.
Средние прямые медицинские затраты за весь период наблюдения за больными ИБС, включенных в исследование, приведены в табл. 7. Установлено, что пациенты c ИБС, находящиеся на терапии бисопрололом достоверно реже госпитализировались в стационар, что выразилось в более низких затратах на госпитализацию и проведение повторных хирургических вмешательств.
Стоимость лечения на амбулаторном этапе наблюдения у пациентов в 1‑й гру ппе в течение 3 лет составила 47 113,7±1656,9 руб. (во 2‑й группе — 36 989,3±2220,3 руб., в 3‑й группе — 39 146,3±1951,9 руб.). Структура затрат на медикаментозную терапию представлена в табл. 8.
Таблица 8. Стоимость базисной терапии у больных ИБС, в исследуемых группах за период наблюдения.
При проведении сравнительного анализа эффективности затрат в исследуемых группах (в качестве положительных результатов рассматривалось отсутствие летальных исходов, острых коронарных синдромов, повторных хирургических вмешательств, возобновление стенокардии), было установлено, что в периоперационном периоде у пациентов группы бисопролола отмечалось увеличение положительных результатов по сравнению с таковыми в группе атенолола на 10,4% при снижении
общих затрат на 10 136,6 руб. и по сравнению с группой метопролола — увеличение положительных результатов на 12,5% при снижении общих затрат на 9345 руб. В периоперационном периоде для получения единицы результата в группе пациентов, принимавших бисопролол, было необходимо затратить 2547,1 руб., в группе атенолола — 2911,1 руб., в группе метопролола — 2980,7 руб. Таким образом, для получения результата в периоперационном периоде затраты в группе бисопролола оказались меньше, чем в группе атенолола, на 454 руб. и в группе метопролола – на 523,6 руб.
Через 3 года наблюдения у пациентов группы бисопролола отмечалось увеличение положительных результатов по сравнению с таковыми в группе атенолола на 12,2% при снижении общих затрат
на 810,2 руб., по сравнению с группой метопролола — на 19,3% при снижении общих затрат на 11 986,7 руб. В периоперационном периоде для получения единицы результата в группе бисопролола необходимо было затратить 3462 руб., в группе атенолола — 4073,4 руб., в группе метопролола — 4706,9 руб. Таким образом, для получения результата за период наблюдения затраты в группе бисопролола оказались меньше, чем в группе атенолола на 611,4 руб., и в группе метопролола — на 1244,9 руб.
В качестве меры результата эффекта терапии также проанализирован такой показатель, как полезность, или QALY. В группе бисопролола результат за период наблюдения составляет (3,9–0,6)=3,3 QALY при стоимости курса 285 961,9 руб., коэффициент затраты/полезность — 86 655,1 руб./QALY (см. табл. 7), в группе атенолола — (3,76–0,6)=3,16 QALY при стоимости курса 286 772,7 руб., коэффициент затраты/полезность — 90.750,85 руб./QALY, в группе метопролола — (3,8–0,6)=3,2 QALY при стоимости курса 297 948,6 руб., коэффициент затраты/полезность — 93 108,9 руб./QALY. Заметим, что наименьшие затраты на год жизни с учетом показателя «полезность» отмечены в группе пациентов, принимавших бисопролол.
В современных условиях перед практикующими врачами стоит достаточно непростая задача: при закономерной экономии материальных затрат выбрать то лекарственное средство, а чаще комбинацию препаратов, которые позволяют достичь максимального положительного эффекта. По нашим данным, назначение β-адреноблокатора бисопролола больным ИБС, подвергнутым КШ, максимально отвечает поставленной задаче, поскольку терапия препаратом по сравнению с атенололом и метопрололом в большей степени улучшает клиническое течение заболевания, повышает толерантность к физической нагрузке, а также приводит к меньшим материальным затратам при 3-летнем ведении пациентов данной категории. Полученные нами результаты указывают
на необходимость дальнейшего изучения этого вопроса, в том числе в рамках крупных многоцентровых рандомизированных клинических испытаний.



