В течение последнего десятилетия каждая третья женщина репродуктивного возраста отдает предпочтение гормональным методам предохранения от нежелательной беременности [1]. В этой связи одним из направлений современной медицины является создание контрацептивных препаратов, обладающих высокой эффективностью и безопасностью, хорошей переносимостью, низким числом побочных реакций и наличием дополнительного лечебного действия на различные звенья репродуктивной системы [2]. Развитие фарминдустрии в линейке «репродуктивное здоровье» за последние 10 лет привело не только к изменению состава гормональных контрацептивов (ГК), но и разработке новых стероидных молекул и различных способов доставки препаратов в организм.
Одной из наиболее эффективных и часто используемых форм гормональной контрацепции являются комбинированные гормональные контрацептивы (КГК). Их применяют более 100 млн женщин во всем мире при планировании семьи [2]. Было проведено множество исследований, в которых изучалась безопасность пероральных контрацептивов. Однако почти половина женщин, использующих КГК, не полностью удовлетворены методом из-за возникающих побочных эффектов (межменструальные кровянистые выделения, диспептические расстройства, изменение настроения, снижение либидо и т.д.). Очевидно, что женщины, не полностью удовлетворенные применением КГК, с большей вероятностью могут допустить ошибки и прекратить использование контрацепции, что приводит к повышению риска наступления нежелательной беременности [3]. Таким образом, успех использования контрацепции в высокой степени связан с удовлетворенностью женщин.
В последние десятилетия женщины находились в ожидании новых достижений науки, одним из которых явилось создание нового контрацептива с натуральным селективным эстрогеном – эстетролом (Е4), имеющим характеристики, отличные от других эстрогенов. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (Food and Drug Administration, FDA) и Европейское агентство по лекарственным средствам (European Medicines Agency, EMA) одобрили использование Е4 в сочетании с дроспиреноном (ДРСП) в качестве КГК нового поколения. Препарат зарегистрирован и применяется в странах Европы, США, Канаде, Австралии. В России препарат зарегистрирован под названием «Эстеретта», содержит в своем составе Е4 15 мг и ДРСП 3 мг [4–10]. Впервые Е4 был выделен Egon Diczfalusy в 1965 г. и представляет собой нативный фетальный эстроген III поколения, вырабатываемый клетками печени плода во время беременности посредством экспрессируемых у плода гидроксилаз из эстрадиола (Е2) и эстриола (Е3). Установлено, что действие эстрогенов реализуется посредством активации эстрогеновых рецепторов типа α (ЭРα) [11, 12]. Активация данных рецепторов инициирует дальнейшие каскады передачи сигналов [13]. Согласно данным доклинических исследований, для Е4 характерна более низкая способность к связыванию (аффинитет) с ЭРα по сравнению с Е2 [13]. В настоящее время завершены все фазы клинических исследований нового КГК, содержащего 15 мг Е4 и 3 мг ДРСП (Е4/ДРСП). Высокая контрацептивная эффективность Е4/ДРСП показана в двух клинических исследованиях III фазы, проведенных в Северной Америке (NCT02817841) с участием женщин в возрасте от 16 до 35 лет (n=1674) в течение 13 циклов (индекс Перля 1,43–2,65, частота беременностей в течение 13 циклов 2,1%), в странах Европы и 10 Центрах России (NCT02817828), в число которых входили ФГБУ «НМИЦ АГП им. В.И. Кулакова», ФГБНУ «НИИ АГиР им. Д.О. Отта», ГБУЗ МО МОНИИАГ, с участием женщин в возрасте 18–50 лет (n=1353), использовавших Е4+ДРСП в течение 13 циклов (индекс Перля 0,47) [14, 15]. Основной принцип консультирования по применению методов ГК заключался в необходимости соблюдения безопасности при назначении комбинированных оральных контрацептивов (КОК) в соответствии с разработанными национальными критериями приемлемости применения препаратов с контрацептивным действием [16].
Согласно имеющимся в настоящее время данным по изучению метаболических эффектов ГК, содержащего Е4, выявлено его минимальное влияние на функцию печени, липидный профиль крови. Для оценки метаболических эффектов КГК Mawet M. et al. провели исследование по поиску безопасной схемы и дозы у здоровых женщин в возрасте 18–35 лет. В данном исследовании женщинами были использованы 6 различных по составу препаратов (5 мг Е4/3 мг ДРСП; 10 мг Е4/3 мг ДРСП; 5 мг Е4/0,15 мг левоноргестрела (ЛНГ); 10 мг Е4/0,15 мг ЛНГ; 20 мг Е4/0,15 мг ЛНГ; 0,02 мг этинилэстрадиола (ЕЕ)/3 мг ДРСП) в режиме 24/4 в течение 3 циклов. Было показано, что КГК, содержащие Е4, оказывали незначительное влияние на уровни липопротеинов и триглицеридов по сравнению с группой использующих ЕЕ/ДРСП [17]. Было также отмечено незначительное изменение концентрации С-реактивного белка, глобулина, связывающего кортизол, глобулина, связывающего тироксин, и церулоплазмина при приеме Е4/ДРСП. Аналогичные результаты получены в исследовании Klipping C. et al. (2021). Так, после 6 циклов применения препарата, содержащего 15 мг Е4/3 мг ДРСП, не выявлено его существенного влияния на липидный обмен по сравнению с содержащим ЕЕ/ДРСП [18]. При использовании Е4/ДРСП также не наблюдалось изменений уровня холестерина липопротеидов низкой плотности (ЛПНП), общего холестерина, соотношения холестерин липопротеидов высокой плотности (ЛПВП)/холестерин ЛПНП и липопротеина А. Влияние на углеводный обмен также был минимальным – инсулин натощак, глюкоза, С-пептид и HbA1c существенно не изменялись на фоне приема Е4/ДРСП [18]. В плацебо-контролируемом исследовании Relief (NCT02834312) у женщин в постменопаузе, получавших Е4 в дозе 2,5, 5, 10 или 15 мг ежедневно в течение 12 недель [19], изменения уровней глюкозы, триглицеридов, ЛПНП и общего холестерина по сравнению с исходным уровнем были статистически незначимыми, а уровень ЛПВП увеличился по сравнению с исходными данными, в группе плацебо увеличения не наблюдалось. Снижение резистентности к инсулину было отмечено в группах, принимавших дозу Е4 10 мг или 15 мг, что указывало на улучшение толерантности к глюкозе [20]. Таким образом, полученные данные свидетельствуют о минимальном влиянии Е4 на метаболизм липидов и углеводов.
Е4 обладает избирательным фармакологическим профилем при влиянии на параметры гемостаза по сравнению с другими эстрогенами. Для изучения метаболического эффекта Е4 было проведено профилирование метаболитов с помощью метода масс-спектрометрии с образцами, собранными во время исследования I фазы (получали Е4, меченный радиоактивным изотопом). Было показано, что Е4 подвергается метаболизму фазы II с образованием неактивных конъюгированных метаболитов, а ферменты цитохрома Р450 (CYP) не играют основной роли в метаболизме Е4, что подтверждает его минимальное влияние на параметры системы гемостаза по сравнению с другими эстрогенами [21, 22]. Анализ результатов многоцентровых исследований III фазы (n=3417 женщин) подтвердил безопасность применения Е4/ДРСП. Оценка влияния препаратов, содержащих Е4/ДРСП, ЕЕ/ЛНГ и ЕЕ/ДРСП, на параметры гемостаза (образование тромбина) исходно и через 6 месяцев применения контрацепции показала, что препарат, содержащий Е4/ДРСП, не вызывал образование тромбина в отличие от содержащих ЕЕ, при использовании которых повышался тромботический риск [23, 24]. Аналогичные данные были получены в исследовании Kluft C. et al., в котором также не обнаружено негативное влияние Е4 на показатели гемостаза (фибриноген, протромбин, D-димер, фактор VIII, протеин С, протеин S, антитромбин, ингибитор пути тканевого фактора) [25]. Согласно данным сравнительных клинических исследований, через 6 месяцев изменение чувствительности к активированному протеину С и эндогенный тромбиновый потенциал для Е4/ДРСП составил +30%, ЕЕ/ЛНГ +165% и ЕЕ/ДРСП +219% [14]. Таким образом, Е4 демонстрирует отсутствие негативного воздействия на параметры гемостаза.
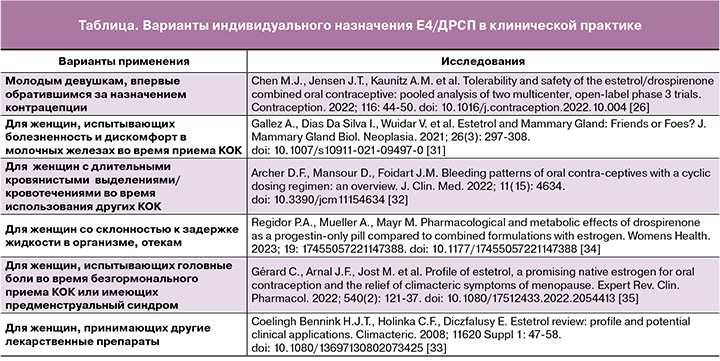
В настоящее время особенности фармакокинетики E4/ДРСП позволили представить возможные варианты его индивидуализированного назначения в клинической практике (таблица).Так, ввиду высокой контрацептивной эффективности и переносимости, его могут применять молодые женщины, впервые обратившиеся по поводу назначения оральных контрацептивов [26].
В научно-поликлиническом отделении ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России наблюдались 30 молодых женщин в возрасте от 18 до 25 лет, впервые обратившихся с целью подбора современных методов контрацепции. Оценивались противопоказания к назначению гормональных методов контрацепции в соответствии с разработанными национальными критериями приемлемости применения препаратов с контрацептивным действием [16].
Из анамнеза было установлено, что болезненные менструации с менархе (первичная дисменорея) отмечали 7 (23,3%) женщин, предменструальный синдром (психоневрологические симптомы) – 11 (36,6%), масталгию – 7 (23,3%). Всем 30 женщинам был назначен КОК, содержащий 15 мг Е4 и 3 мг ДРСП (режим приема 24+4) согласно медицинской инструкции по применению препарата [19]. Длительность наблюдения при применении КГК составила 6 месяцев (168 дней).
Пациенткам было предложено фиксировать любые нежелательные явления и изменения в менструальном цикле.
В течение периода наблюдения не было отмечено пропуска таблеток и нарушения схемы применения, ни у одной женщины беременность не возникла.
В первые 1–3 месяца использования препарата возникли нежелательные явления в виде мажущих выделений – у 2 (6,7%), головных болей – у 1 (3,4%), тошноты – у 2 (6,7%), которые проходили самопроизвольно и не явились причиной отмены препарата.
Следует отметить, что среднее число дней мажущих кровянистых выделений было минимальным, а у 28 (98%) женщин наблюдалась ожидаемая менструальноподобная реакция. Все пациентки указали на снижение интенсивности дисменореи. Также снижение интенсивности боли в молочных железах отметили 5 из 7 женщин с масталгией.
Нами были проанализированы исследования о влиянии Е4, в том числе в сочетании с ДРСП, на ткани молочной железы [27–31].
В исследовании Gerard C. et al. указано на антипролиферативное действие Е4 на эпителиальные клетки молочной железы [27]. Тканеспецифические свойства Е4 изучали на клеточных культурах у животных с индуцированным раком молочной железы (РМЖ) и практически не выявили влияния на пролиферацию нормальных и злокачественных клеток молочной железы. В экспериментальных исследованиях применение Е4 не способствовало усилению роста опухоли и не оказывало влияния на ее метастазирование. Результаты клинического исследования пациенток с прогрессирующим распространенным РМЖ (IB/IIA), резистентным к антиэстрогенам, показали, что Е4 в дозах 20–60 мг оказывает противоопухолевый эффект, который был выявлен у 5 из 9 пациенток после курса лечения [28].
Gallez A. et al. приводят данные об эстрогенных и антиэстрогенных свойствах Е4, а также о его влиянии в комбинации с ДРСП на риск развития и прогрессирования РМЖ [13, 29]. Было установлено нейтральное влияние Е4, в том числе в сочетании с ДРСП, на рост РМЖ. В исследовании на модели трансгенных мышей показано, что при применении Е4 в дозах, превышающих терапевтические, обнаружена его противоопухолевая активность [13, 29].
Gerard С. et al. указывают на антиэстрогенное действие Е4 в опухолевой ткани молочной железы. Так, Е4 является частичным антагонистом мембранных ЭРα, что приводит к предотвращению реализации мембранно-опосредованного сигнального пути стероидов (сигнальный путь MISS) и способствует устранению передачи сигналов в линии клеток РМЖ [30]. Таким образом, результаты исследований демонстрируют отсутствие негативного пролиферативного действия Е4 на молочные железы и отмечают его антипролиферативное действие в опухолевой ткани молочной железы при применении дозы, превышающей терапевтическую. Следовательно, ввиду отсутствия отрицательного воздействия Е4 на ткани молочных желез в клинической практике данный контрацептив можно рассматривать в качестве альтернативы для женщин, которых беспокоят болезненность и дискомфорт в молочных железах во время приема КОК [31].
Исследования также показали, что при использовании Е4/ДРСП частота встречаемости нерегулярного «кровомазания» или кровотечений не увеличивается и не связана с длительностью приема контрацептива. Как известно, данный эффект связан с длительным периодом полувыведения E4. В этой связи применение контрацептива, содержащего Е4/ДРСП, является более актуальным для женщин, имеющих более высокую частоту кровянистых выделений и кровотечений во время использования других контрацептивных таблеток [32].
Одним из интересных направлений в изучении свойств Е4 является его лекарственное взаимодействие. Отсутствие влияния эстетрола на метаболизм цитохрома С450 позволяет рассматривать данный КГК как метод выбора для женщин, принимающие другие препараты (антидепрессанты, антиретровирусные, противосудорожные) [33]. Фармакокинетика контрацептива E4/ДРСП предоставляет возможные варианты его индивидуального назначения в клинической практике. Так, ввиду высокой контрацептивной эффективности и хорошей переносимости, его могут применять молодые женщины, впервые обратившиеся по поводу назначения оральных контрацептивов [26].
Известно, что ДРСП является антагонистом альдостерона, что позволяет рассматривать назначение его комбинации с Е4 для женщин, имеющих склонность к задержке жидкости в организме [34], испытывающих головные боли во время безгормонального периода или имеющих симптомы предменструального синдрома [35]. Все эти возможные клинические варианты применения Е4/ДРСП, безусловно, должны быть подтверждены в исследованиях и клинической практике.
Таким образом, фармакокинетический профиль Е4/DRSP демонстрирует высокую приемлемость при отсутствии отрицательных метаболических эффектов и определяет его дополнительные преимущества для применения в клинической практике.
Заключение
В настоящее время в России и ряде стран зарегистрирован новый КГК, содержащий комбинацию E4/DRSP. Особенности фармакокинетики E4/DRSP позволяют рассматривать его в качестве препарата первого выбора для молодых женщин, впервые планирующих использование гормональной контрацепции, при нежелательных эффектах (длительные кровянистые выделения/кровотечения, боли в молочных железах, склонность к отекам) на фоне применения других КОК.



