Сердечная недостаточность (СН) — конечный исход многих заболеваний системы кровообращения. В прошлом веке под СН подразумевали недостаточность именно систолы, т.е. выброса из левого желудочка (ЛЖ), что обычно характеризуется сниженной фракцией выброса (ФВ) [1]. В нынешнем столетии выделена форма СН с нормальной ФВ, но нарушенным расслаблением и наполнением желудочка [2—5]. Данную форму предложено обозначать как диастолическая СН. Ее отличительными признаками являются замедленное расслабление, повышенное диастолическое давление в ЛЖ, сниженная скорость развития давления. Особенность данной формы заключается в том, что диастолическая дисфункция, являющаяся ведущим синдромом данной формы СН, может наблюдаться и без наличия систолической СН. Одно из самых простых определений этих форм предложил A. Katz [6] — «систолическая дисфункция характеризует желудочек, ударный объем которого уменьшен из-за нарушенного изгнания, а диастолическая дисфункция характеризует желудочек с нарушенным наполнением».
 Значение диастолической СН определяется тем, что ее доля в общем числе случаев хронической СН в настоящее время превышает 50% [7—10]. Существование этой формы породило оживленную дискуссию. Одни считают, что это две разные формы СН, другие — что диастолическая СН предшествует систолической СН. С физиологической точки зрения разделять систолу и диастолу нельзя, поскольку они регулируются одними и теми же внутриклеточными белками, определяющими транспорт Са2+ в кардиомиоцитах (КМЦ) [11—13]. Ключевым звеном системы ионного транспорта является саркоплазматическая сеть. Освобождение Са2+ из нее, вызванное входом внешнего Са2+ по медленным кальциевым каналам через воротный механизм — белок рианодинового рецептора RYR2, позволяет запустить процесс сокращения, а обратный транспорт Са2+ из миофибрилл через Са2+-АТФазу — белок SERCA2а — запускает процесс расслабления.
Значение диастолической СН определяется тем, что ее доля в общем числе случаев хронической СН в настоящее время превышает 50% [7—10]. Существование этой формы породило оживленную дискуссию. Одни считают, что это две разные формы СН, другие — что диастолическая СН предшествует систолической СН. С физиологической точки зрения разделять систолу и диастолу нельзя, поскольку они регулируются одними и теми же внутриклеточными белками, определяющими транспорт Са2+ в кардиомиоцитах (КМЦ) [11—13]. Ключевым звеном системы ионного транспорта является саркоплазматическая сеть. Освобождение Са2+ из нее, вызванное входом внешнего Са2+ по медленным кальциевым каналам через воротный механизм — белок рианодинового рецептора RYR2, позволяет запустить процесс сокращения, а обратный транспорт Са2+ из миофибрилл через Са2+-АТФазу — белок SERCA2а — запускает процесс расслабления.
Функциональная роль последнего чрезвычайно важна, потому что от его активности зависят содержание Са2+ в саркоплазматической сети и последующая сила сокращения. Такому представлению соответствуют результаты выполненных ранее экспериментов, показавшие, что процесс расслабления изменяется раньше и в большей степени, чем процесс сокращения под влиянием разнообразных физиологических факторов — действия катехоламинов при умеренном увеличении притока к сердцу, частоты сокращений или концентрации Са2+ в перфузате [1, 14].
Это позволяет предполагать, что именно изменения процесса удаления Са2+ из миоплазмы являются ведущими для определения сократимости миокарда.
При действии патологических факторов ситуация гораздо менее ясна. Данная тема служила предметом многих исследований, выполненных преимущественно в прошлом веке.
Хроническая СН характеризуется глубоким нарушением и сокращения, и расслабления миокарда. Однако последовательность нарушения этих процессов проследить удается редко, хотя важно выяснить какие белки и регулируемые ими процессы повреждаются прежде всего. Это позволило бы прицельно искать эффективные средства профилактики и терапии.
В настоящее время совершенствование традиционных и создание новых методов исследования позволяют получить новые данные о механизме саморегуляции сократительной функции сердца. Поскольку в физиологических условиях изменения процесса расслабления определяют последующие изменения сокращения миокарда, естественным выглядит предположение, что и в патологических условиях его роль может быть ведущей [15].
Эта гипотеза легла в основу данной работы. В работе в качестве повреждающего фактора мы использовали агонист β-рецепторов изопротеренол (ИЗО), действие которого сопровождается повреждением миокарда вследствие множественных микронекрозов [16] и дозозависимым нарушением гемодинамики [17].

Материал и методы
Опыты выполняли на наркотизированных кетамином (100 мг/кг) самцах крыс Вистар массой 400—450 г. Всего выполнено 4 серии экспериментов, в которых дозы ИЗО варьировались от 85 до 180 мг/кг, которые вводили дважды с суточным интервалом. Смертность в этих сериях колебалась от 15 до 40%. Выжившие животные и контрольные к ним были исследованы с применением различных неинвазивных и инвазивных методов, причем некоторые группы были исследованы всеми методами.
 Эхокардиография. Исследование функции сердца наркотизированных крыс выполняли на аппарате iE33 с использованием датчика S12-4 (12—4 MГц). Конечный диастолический размер (КДО) и конечный систолический размер (КСО) ЛЖ, а также толщину задней стенки ЛЖ измеряли в М-режиме из парастернального доступа в проекции длинной оси сердца; площадь поперечного сечения ЛЖ в конце диастолы (Sd, см2) и в конце систолы (Ss, см2) определяли из парастернального доступа в проекции по короткой оси сердца на уровне папиллярных мышц, рассчитывая процент изменения площади поперечного сечения ЛЖ в систолу по следующей формуле: ΔS%=(Sd–Ss)/Sd 100. Объемы ЛЖ (КДО, КСО) и ФВ определяли с использованием модифицированного алгоритма Симпсона из апикального доступа в трех проекциях (4- и 2-камерных и по длинной оси ЛЖ). Интеграл линейной скорости кровотока (VTI, см) — эквивалент ударного объема, а также ударный объем ЛЖ (УО, мл) и сердечный выброс (МО, мл/мин) определяли с помощью допплеровского исследования в импульсном режиме на уровне выходного тракта ЛЖ.
Эхокардиография. Исследование функции сердца наркотизированных крыс выполняли на аппарате iE33 с использованием датчика S12-4 (12—4 MГц). Конечный диастолический размер (КДО) и конечный систолический размер (КСО) ЛЖ, а также толщину задней стенки ЛЖ измеряли в М-режиме из парастернального доступа в проекции длинной оси сердца; площадь поперечного сечения ЛЖ в конце диастолы (Sd, см2) и в конце систолы (Ss, см2) определяли из парастернального доступа в проекции по короткой оси сердца на уровне папиллярных мышц, рассчитывая процент изменения площади поперечного сечения ЛЖ в систолу по следующей формуле: ΔS%=(Sd–Ss)/Sd 100. Объемы ЛЖ (КДО, КСО) и ФВ определяли с использованием модифицированного алгоритма Симпсона из апикального доступа в трех проекциях (4- и 2-камерных и по длинной оси ЛЖ). Интеграл линейной скорости кровотока (VTI, см) — эквивалент ударного объема, а также ударный объем ЛЖ (УО, мл) и сердечный выброс (МО, мл/мин) определяли с помощью допплеровского исследования в импульсном режиме на уровне выходного тракта ЛЖ.
Катетеризация. У наркотизированных кетамином (100 мг/кг) животных непрерывно регистрировали электрокардиограмму (ЭКГ) во II стандартном отведении, среднее артериальное давление (АД), давление в ЛЖ и тетраполярную импедансную кардиограмму (ИКГ).
В яремную вену вставляли катетер для введения веществ. Для регистрации давления в ЛЖ и аорте использовали Милларовский прецизионный микроманометр на конце тонкого (диаметр 0,53 мм) катетера, введенного через сонную артерию, и тензометрический усилитель.
АД через катетер в бедренной артерии измеряли с помощью электроманометра. Для регистрации ИКГ вводили подкожно токовые электроды-иглы в область нижней челюсти и одной из нижних конечностей, а сигнальные — по верхней и нижней границам грудины. Сигнал ИКГ (ΔZ) регистрировали с помощью модифицированного для работы с мелкими лабораторными животными реоплетизмографа РПКА-2-01 с расширенной полосой пропускания (от 0,1 до 150 Гц при несущей частоте 40 кГц и амплитуде импульсов тока 3,5 мА).
Сигналы ЭКГ, давления в ЛЖ и аорте подавали на Biograph-4. Измеряли традиционные показатели сократимости — максимальную скорость развития давления (dP/dtmax) и индекс Veragut & Krayenbuhl [18] (dP/dtmax/P — давление в момент достижения максимума dP/dt). Для характеристики процесса расслабления использовали максимальную скорость снижения давления (dP/dtmin), а также производный из нее индекс «расслабимости» по аналогии с индексом сократимости (ИС). Кроме того, вычисляли константы скорости снижения давления в изоволюмической [19] и ауксоволюмической [20] фазах.
Все сигналы оцифровывали с частотой 1 кГц с помощью аналого-цифрового преобразователя NI-USB-6210 и записывали на жесткий диск компьютера. Для записи и обработки физиологических сигналов были разработаны собственные программы (автор — Е.В.Л.). Величины всех параметров рассчитывали на основе анализа записей первичных сигналов, подвергнутых предварительной процедуре пульс-синхронного усреднения, которая обеспечивает автоматический расчет «усредненных форм» сигналов по 40 кардиоциклам каждые 5 с. Для этого сначала производили интерполяцию и переоцифровку сегментов сигнала ЭКГ, содержащих комплекс QRS, с шагом 0,2 мс, что необходимо для точного определения положения вершины зубца R в каждом кардиоцикле. Затем все фрагменты пульсовых волн исследуемых сигналов синхронизовали, совмещая во времени вершины зубцов R.
 Синхронизированные по зубцу R сигналы подвергали медианной фильтрации для удаления помех и сильно отличающихся по форме или амплитуде волн. Полученные семейства кривых усредняли и рассчитывали первые и вторые производные сигналов ΔZ и давления, применяя метод полиномиальной фильтрации-дифференцирования Савицкого—Голаи. Чтобы обеспечить аккуратность оценки амплитуд максимумов производных этих сигналов и необходимое разрешение при измерении соответствующих временны'х интервалов, снова применяли интерполяцию с переходом к дробному шагу 0,1 мс. В результате получали хорошо воспроизводимые кривые с минимумом помех и разрешением во времени до 0,1 мс, несмотря на сравнительно небольшую частоту аппаратной оцифровки (шаг 1 мс).
Синхронизированные по зубцу R сигналы подвергали медианной фильтрации для удаления помех и сильно отличающихся по форме или амплитуде волн. Полученные семейства кривых усредняли и рассчитывали первые и вторые производные сигналов ΔZ и давления, применяя метод полиномиальной фильтрации-дифференцирования Савицкого—Голаи. Чтобы обеспечить аккуратность оценки амплитуд максимумов производных этих сигналов и необходимое разрешение при измерении соответствующих временны'х интервалов, снова применяли интерполяцию с переходом к дробному шагу 0,1 мс. В результате получали хорошо воспроизводимые кривые с минимумом помех и разрешением во времени до 0,1 мс, несмотря на сравнительно небольшую частоту аппаратной оцифровки (шаг 1 мс).
Расчет частоты сердечных сокращений (ЧСС) производили каждые 5 с по средней длительности интервалов RR для каждого из наборов кардиоциклов. Для неинвазивной оценки сократимости ЛЖ использовали измерение длительности периода предизгнания (ДПП, в мс) по методу В.М. Хаютина [21]. Эту величину определяли по сигналу ИКГ — от вершины зубца R до максимума второй производной импедансного сигнала (d2Z/dt2)max, а при записи давления в ЛЖ величину ДПП измеряли от зубца R до максимума скорости повышения давления (dP/dtmax) (по Siegel [22]).
Изолированные кардиомиоциты. За 15 мин до выделения сердца крысе вводили гепарин (5 ед/г массы животного, внутрибрюшинно). После декапитации и вскрытия грудной клетки сердце иссекали и немедленно подвешивали на канюлю с перфузией по Лангендорфу, длительность перфузии бескальциевым раствором (содержание остаточного Са2+ не более 50 мкМ) составляла 30 мин. В течение этого этапа происходило вымывание Са2+ из межклеточных пространств. Затем перфузировали сердце раствором коллагеназы CLS2 (325 ед/мг) в замкнутом цикле 20 мин. После этого миокард измельчали, удаляли супернатант с коллагеназой, оставляя осадок с живыми КМЦ и добавляли раствор альбумина с 0,1 мМ Са2+. В зависимости от исходного количества миокарда, взятого для выделения клеток, получали 5—10 млн жизнеспособных КМЦ для исследований. Выделенные клетки инкубировали в камере экспериментальной установки в нормоксическом буфере Тироде, аэрированным карбогеном при температуре 37 °С в течение 1—2 ч, постоянно продувая пространство камеры над раствором карбогеном.

Для измерения внутриклеточного свободного Са2+ в изолированных КМЦ к клеткам добавляли 1 мкл раствора флуоресцентного Са2+ индикатора Fluo-4 и инкубировали в темноте в течение 20 мин при температуре 37 °С для насыщения клеток индикатором. После этого переносили около 50 КМЦ в камеру объемом 250 мкл с дном из покровного стекла и помещали ее на объектив ×63 инвертированного микроскопа. Клетки освещали светом ртутной лампы, используя минимальную интенсивность освещения клеток для снижения их фотоповреждения. Длительность одного сеанса освещения не превышала 20 с. Флуоресцентный сигнал регистрировали с помощью высокоскоростной цифровой камеры AxioCam HS со скоростью 50—200 кадров/с и записывали на жесткий диск компьютера. Для возбуждения клеток использовали электростимуляцию с частотой 1 Гц и напряжением 38 В течение 10 с.
Гистологическое исследование. В конце опыта из середины боковой стенки ЛЖ вырезали кусочек миокарда и фиксировали с последующим окрашиванием гематоксилином и эозином полутонких срезов. Образцы просматривали под световым микроскопом.
Результаты
Насосная функция. Всего выполнено 4 серии с применением различных дозировок ИЗО — 85, 120, 150 и 180 мг/мг, каждую дозу вводили дважды с интервалом 1 сут.
В первой серии эхокардиографическое исследование выполнено дважды — через 3 дня и 3 мес. Через 3 дня частота сокращений, диастолический объем, ФВ и степень уменьшения площади ЛЖ остались неизменными, но индекс VTI был достоверно снижен на 27% (табл.1). Отмечалась явная тенденция к снижению минутного объема (МО), при сопоставлении этой величины только в парных опытах (n=9) различия оказались статистически значимыми (p<0,05). В дальнейшем почти все эти крысы выжили и характеризовались повышенным МО при нормальной ФВ (см. табл. 1), Однако сравнение этих групп не вполне правомерно из-за отсутствия адекватного возрастного контроля.
Поскольку введение данной дозы не привело к развитию явной СН, в дальнейших сериях были применены более высокие дозировки. Исследование сердца крыс, получивших по 120 и 150 мг/кг дважды, было проведено через 2 нед (см. табл. 2). При кумулятивной дозе 240 мг/кг выявилась тенденция к увеличению КДО и КСО, снижению ФВ и МО. Эти изменения проявились более отчетливо при кумулятивной дозе 300 мг/кг. ФВ и МО были достоверно снижены на 14 и 25% соответственно, одновременно ФВ уменьшалась в такой же степени и площадь ЛЖ при систоле, при этом КДО увеличился на 31%. Толщина задней стенки ЛЖ в диастоле и систоле существенно не изменялась, но тенденция к уменьшению степени утолщения стенки при систоле была явной.
 Еще более значительные изменения наблюдали при использовании самой большой дозы ИЗО 360 мг/кг (табл. 2).
Еще более значительные изменения наблюдали при использовании самой большой дозы ИЗО 360 мг/кг (табл. 2).
Через 2 мес после введения КДО увеличился более чем в 2 раза, КСО был увеличен в несколько раз, ФВ и степень утолщения стенки уменьшились на 32—45%.
Тем не менее МО был снижен незначительно, что свидетельствует о хороших компенсаторных возможностях системы кровообращения.
Эти данные показали, что между объемом ЛЖ и ФВ существует обратная связь. Расчет корреляции между КДО и ФВ показал наличие относительно слабой связи в группе контроля и ИЗО-2 (r=-0,49 и r=-0,50), но эта связь усиливалась в группах ИЗО-3 и ИЗО-4 (r=-0,71 и r=-0,88 соответственно). В отличие от этого корреляция между КСО и ФВ была высокой во всех группах (r=-0,86—0,88), что отражает явную зависимость ФВ от степени сокращения волокон ЛЖ в систоле. Указанную связь иллюстрирует рис. 1 (данные по серии ИЗО-4 не приведены, так как они резко выходят за пределы шкалы).
Однонаправленные и близкие по степени изменения ФВ и степени уменьшения площади ЛЖ при систоле нашли свое отражение при расчете корреляции (r=0,6 в контроле и 0,80—0,85 в группах ИЗО-2 и ИЗО-3), а также на рис. 2.
Фазовый анализ насосной функции после введения 300—360 мг/кг, выполненный отдельно для каждого желудочка, показал, что при формировании СН происходит закономерное изменение структуры кардиоцикла — удлинение изоволюмических фаз на 24—28% за счет укорочения фазы наполнения на 14—20% (табл. 3).
 Кроме того, у животных, получивших 360 мг/кг, отмечено удлинение фазы изгнания на 11%, а также выявлена аналогичная перестройка структуры цикла для правого желудочка (ПЖ).
Кроме того, у животных, получивших 360 мг/кг, отмечено удлинение фазы изгнания на 11%, а также выявлена аналогичная перестройка структуры цикла для правого желудочка (ПЖ).
Укорочение фазы наполнения сердца за счет удлинения фаз систолы позволяет предполагать, что недостаточное наполнение ЛЖ может послужить одной из причин ослабления сократительной функции сердца под влиянием ИЗО. Действительно, расчет корреляции между ФВ и относительной длительностью диастолы позволил установить, что в контрольной группе никакой связи между ними нет, а в группах ИЗО-2, ИЗО-3 и ИЗО-4 прослеживается отчетливая связь (r=0, 64—0,69—0,69 соответственно, т.е. в каждой группе укорочение диастолы коррелирует с уменьшением ФВ).
Таким образом, основными функциональными признаками поражения миокарда под влиянием высоких доз ИЗО являются дилатация полости ЛЖ, уменьшение ФВ, удлинение изоволюмических фаз сокращения и расслабления, а также сокращение длительности фазы наполнения. В сердцах крыс, у которых введение ИЗО не сопровождалось дилатацией ЛЖ и снижением ФВ, единственным достоверным изменением было удлинение изоволюмических фаз на 19%. Принимая во внимание, что длительность изоволюмического расслабления заметно больше, чем сокращения, можно предполагать, что именно расслабление замедлено у животных без признаков СН.
Сократимость и «расслабимость». Через 2—3 нед после введения ИЗО (кумулятивная доза 170 мг/кг) 50% животных были подвергнуты инвазивному исследованию ЛЖ с применением Милларовского катетера в сочетании с импедансометрией. Результаты технически успешных опытов представлены в табл. 4.
Основные параметры гемодинамики были снижены у крыс, получавших ИЗО — частота сокращений на 10%, а систолическое давление в ЛЖ — на 20%. Снижались и скоростные показатели развития давления — максимальная скорость развития давления — на 30%, а ИС — на 20%. Изоволюмическое расслабление проявило тенденцию к замедлению, при этом ауксоволюмическое расслабление в начальном периоде наполнения было достоверно замедленным — константа скорости была снижена на 30%, а константа времени выше на 39%. Длительность периода предизгнания имела тенденцию к увеличению, а длительность систолы увеличивалась соответственно увеличению длительности цикла. Таким образом, при инвазивном исследовании крыс, получавших ИЗО, были выявлены явные признаки недостаточности миокарда — снижение сократимости и «расслабимости», причем снижение «расслабимости» было более выраженным, особенно в фазе начального наполнения ЛЖ.
 Результаты следующих серий, в которых были применены гораздо более высокие кумулятивные дозы ИЗО — 240 и 360 мг/кг, подтвердили это наблюдение (табл. 5). В этих сериях использованы обычные катетеры, поэтому максимальные скорости развития и снижения давления в контрольных опытах были значительно ниже, представленных в табл. 4. В обеих сериях опытов с ИЗО получены принципиально сходные результаты, но степень изменений была определенно больше в группе с наибольшей дозой ИЗО.
Результаты следующих серий, в которых были применены гораздо более высокие кумулятивные дозы ИЗО — 240 и 360 мг/кг, подтвердили это наблюдение (табл. 5). В этих сериях использованы обычные катетеры, поэтому максимальные скорости развития и снижения давления в контрольных опытах были значительно ниже, представленных в табл. 4. В обеих сериях опытов с ИЗО получены принципиально сходные результаты, но степень изменений была определенно больше в группе с наибольшей дозой ИЗО.
В группе, получившей 240 мг/кг, систолическое давление в ЛЖ и показатели сократимости не изменялись, но показатели, характеризующие процесс расслабления, были статистически достоверно снижены: индекс расслабимости — на 33%, константа скорости ауксоволюмического расслабления снижена в 2 раза, а константа времени ауксоволюмического расслабления повышена также почти в 2 раза. При этом показатели изоволюмического расслабления проявили лишь тенденцию к замедлению.
Сердца крыс, получивших 360 мг/кг ИЗО, характеризовались еще более глубокими изменениями расслабления миокарда — наряду со снижением показателей ауксоволюмического расслабления была также понижена константа скорости изоволюмического расслабления более чем в 2 раза. Эти изменения сочетались со снижением скоростных параметров развития и падения давления на 22—32%, а также их производных индексов на 24—35%. Следует отметить, что степень снижения показателей расслабления была больше, чем показателей сокращения. В результате ухудшения сократимости и расслабления миокарда конечное диастолическое давление (КДД) в ЛЖ было явно повышено, а длительность систолы увеличена на 16%.
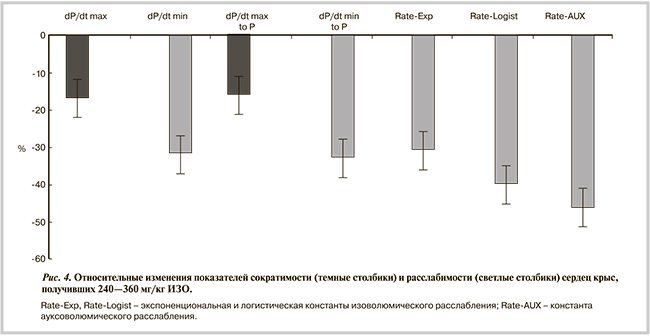
Корреляционный анализ по всему массиву представленных в табл. 5 данных показал, что между скоростными параметрами сокращения и расслабления существует прямая зависимость (r=0,74). Еще более высокий коэффициент (r=0,85) характерен для сердец из групп ИЗО. Для ИС во всем массиве данных характерна обратная корреляция с временем до пика скорости (r=-0,78) и КДД в ЛЖ (r=-0,83; рис. 3). Тесная корреляция отмечена также между КДД и показателями расслабления (r=-0,67—0,7). С остальными показателями ИС коррелировал слабо, исключением были только группы ИЗО, в которых отмечена тесная положительная корреляция с максимальной скоростью снижения давления и изоволюмической константой расслабления (r=0,83 и 0,72 соответственно).
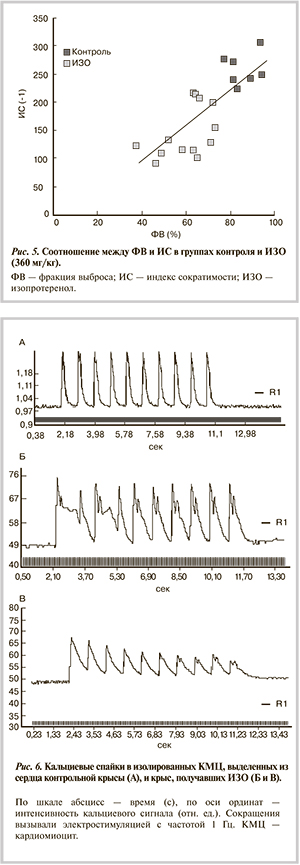
В каждой серии крыс, получавших ИЗО, показатели сократимости и расслабления миокарда были снижены по сравнению с контрольными величинами. Однако относительная степень снижения всех показателей процесса расслабления была приблизительно в 2 раза больше, чем показатели процесса сокращения (рис. 4).
По парному критерию Стьюдента различия были высоко статистически значимыми (p<0,01), а самая высокая степень статистической значимости (p<0,001) отмечена для ауксоволюмической константы расслабления.
Наряду с инвазивными показателями были также измерены некоторые неинвазивные показатели, полученные при анализе импедансного сигнала. Результаты, приведенные в табл. 6, свидетельствуют о том, что показатель, характеризующий длительность периода электромеханического сопряжения, — длительность периода предизгнания, как и время до пика dP/dt, остался неизменным при поражении ИЗО миокарда. В отличие от этого длительность механической систолы отчетливо увеличивалась соответственно замедлению частоты сокращений. Длительность систолы по отношению к общей длительности цикла в контрольной группе составляла 53%, а в группах, получавших ИЗО — 56%. Широко используемый импедансный показатель сократимости — максимальная скорость систолического изменения Z-сигнала (Z-Vmax) — отчетливо снижался в группе, получившей большую дозу ИЗО, на 31%, а ускорение (Z-Amax) — почти в 2 раза. Более чувствительными оказались два других показателя — амплитуда волны О в импедансном сигнале (Z-O-max) и отношение величины волн О и С, повышавшиеся в 2,5—3 раза и 3,5—4 раза соответственно.
Корреляция между инвазивными и эхокардиографическими показателями. Некоторые группы крыс были исследованы сначала эхокардиографическим, а затем инвазивным методами. Это дало возможность коррелировать отдельные показатели по каждому животному.
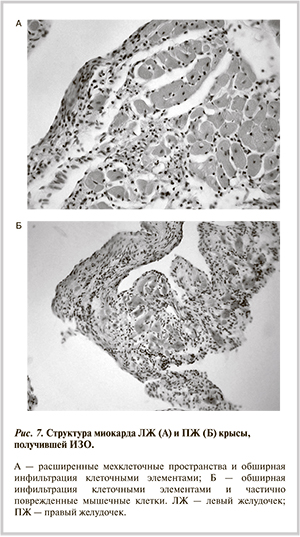
Основные эхокардиографические показатели сократимости миокарда — ФВ и степень уменьшения площади ЛЖ — проявили высокую степень корреляции (r=0,77—0,81) с основными инвазивными показателями сократимости миокарда — максимальной скоростью развития давления и ИС. Связь близка к линейной (рис. 5).
Представленные на рис. 5 данные показывают, что ИС ниже 200 с-1 характерен для СН. Несколько слабее коррелировало с показателями сократимости миокарда КДД (r=-0,61—0,66). Это соответствует представлению, что сократимость миокарда определяет скорость развития давления и степень изгнания крови из ЛЖ, а также отрицательно влияет на объем остающейся после систолы крови. Об этом свидетельствуют положительная корреляция между КСО и КДД (r=0,77), а также тесная отрицательная корреляция с инвазивными показателями сократимости (r=-0,74—0,84). Близкая к этому отрицательная корреляция найдена и для КСО, и диастолической площади ЛЖ (r=-0,77—0,89). Это согласуется с представлением об ухудшении сократимости миокарда при увеличении объема ЛЖ.
В работе особое внимание уделено измерению показателей расслабления миокарда. Корреляционный анализ этих данных показал, что с эхокардиографическими показателями сокращения ЛЖ наиболее тесно связана максимальная скорость снижения давления (r=-0,69—0,84).
Вероятной основой такой связи является зависимость обоих показателей от состояния кальциевого транспорта в КМЦ. Среди остальных показателей более высокие коэффициенты корреляции найдены для экспоненциальной константы изоволюмического расслабления.
 Она, как и показатели сократимости, отрицательно коррелировала с показателями диастолического объема ЛЖ (r=-0,70—0,77) и гораздо слабее — с показателями сократимости. Константа ауксоволюмического расслабления характеризовалась теми же соотношениями, но ее связь с показателями диастолического объема ЛЖ была выражена слабее.
Она, как и показатели сократимости, отрицательно коррелировала с показателями диастолического объема ЛЖ (r=-0,70—0,77) и гораздо слабее — с показателями сократимости. Константа ауксоволюмического расслабления характеризовалась теми же соотношениями, но ее связь с показателями диастолического объема ЛЖ была выражена слабее.
Изолированные КМЦ. Запись изменений концентрации свободного Са2+ в саркоплазме изолированных КМЦ позволила установить типичные нарушения кальциевого транспорта. Как видно из сравнения кривых на рис. 6, в контроле каждому электрическому стимулу соответствует один пик подъема концентрации Са2+. Все пики имеют одинаковую амплитуду и практически симметричную форму. Иногда нисходящее плечо пика несколько затянуто. Тем не менее при применяемой частоте стимуляции 1 Гц пики Са2+ хорошо разрешены, и между стимуляциями клеток уровень Са2+ в них опускается до базального. В КМЦ из сердец крыс, получивших ИЗО, наблюдается искажение кривой Са2+, в основном ее нисходящего плеча. Вместо него отмечается возникновение «купола» на половине высоты нисходящего плеча, отражающего замедление выведения Са2+ из саркоплазмы в саркоплазматическую сеть или появление дополнительного пика (см. рис. 6, Б). При этом восходящее плечо (возрастание уровня Са2+ в саркоплазме, отражающее работу кальциевых каналов) изменяется в меньшей степени, но амплитуда пиков падает примерно в 1,4 раза.
Затем кальциевые ответы в КМЦ из сердец крыс с СН теряют соответствие электрическим стимулам.
На приведенной записи (см. рис. 6, Б) видно, что на 10 электрических импульсов, стандартно подаваемых в камеру с КМЦ, происходит только 9 ответов Са2+, причем особенно страдают первые 2 пика: они сильно затянуты, и в конце каждого возникает спонтанный пик, нарушающий нормальный ритм сокращений. На рис. 6В представлен другой тип нарушения, при котором ритм сохраняется неизменным, но диастолический уровень Са2+ не достигает базального, а величина последующих пиков неуклонно понижается.
Таким образом, при функциональной нагрузке в КМЦ крыс с СН нарушается кальциевый транспорт, обеспечивающий сократительную активность. Судя по характеру кривых изменения концентрации Са2+, главным образом, страдает процесс удаления Са2+ из цитоплазмы, в то время как процесс его поступления в цитоплазму нарушен в меньшей степени.
Структура миокарда. В миокарде крыс, получивших ИЗО (85 мг/кг дважды), обнаружены серьезные изменения: расширенные межклеточные пространства, отражающие значительный отек, и мозаичные изменения КМЦ (рис. 7). Тинкториальные свойства были изменены: наряду с нормальными можно было видеть и поврежденные клетки (см. рис. 7, Б), что предшествует их распаду. На всех снимках видна обширная инфильтрация клеточными элементами и фибробластами — организаторами фиброза.
Обсуждение
Результаты, полученные в данной работе, можно кратко суммировать в виде трех основных положений: 1) во всех сериях независимо от дозы ИЗО расслабление миокарда страдает в большей степени, чем сократимость; 2) при использовании низких доз ИЗО возникает диастолическая СН, проявляющаяся замедлением расслабления и снижением максимальной скорости развития давления; 3) при использовании высоких доз ИЗО возникает систолическая СН, проявляющаяся в виде уменьшения ФВ и дилатации полости ЛЖ; она сочетается с нарушением транспорта Са2+ в КМЦ.
Повышенная реактивность процесса расслабления по сравнению с сокращением в норме основывается на том, что формирование фракции Са2+, активирующей процесс сокращения, происходит (в миокарде крыс в большей степени, чем у других млекопитающих) пропорционально содержанию Са2+ в саркоплазматической сети, а последнее определяется количеством Са2+, поглощенного в этой сети через Са2+-АТФазу. Этот энергозависимый процесс нарушается в условиях гипоксии или недостатка субстратов окисления, что, естественно, выражается и в замедлении расслабления, и в уменьшении сокращения. Окислительный стресс, возникающий в миокарде при продолжительном действии ИЗО, сопровождается нарушением функции митохондрий, снижением скорости синтеза АТФ.
Это создает ситуацию, близкую к той, которая возникает при направленном нарушении энергообразования [23, 24], что и выражается в снижении расслабления миокарда во всех сериях применения ИЗО. Одновременно снижается сократимость миокарда, но в меньшей степени.
Расслабление миокарда нарушается достаточно рано при введении даже небольших доз ИЗО крысам в течение 3—7 дней. Исследование функции изолированного сердца показало замедление расслабления при неизменном развиваемом давлении [25]. При этом авторы нашли значительное уменьшение экспрессии белков, участвующих в кальциевом транспорте — Са2+-АТФазы саркоплазматической сети, фосфоламбана, а также Na+/K+-АТФазы. Аналогично и при другой экспериментальной патологии сердца — перевязке коронарной артерии — изоволюмическое расслабление миокарда было замедлено во всех сердцах независимо от наличия или отсутствия СН [26], и это сочеталось со сниженной растяжимостью сердца [27].
Естественным следствием снижения расслабления и сократимости миокарда является неполное опорожнение камеры ЛЖ в систолу, что приводит к повышению КДД. Между величиной последнего и ИС зарегистрирована обратная связь (см. рис. 3) с высоким коэффициентом корреляции (r=-0,83). Другим фактором, способствующим повышению КДД, является закономерное повышение диастолической упругости миокарда (или снижение его растяжимости) вследствие отека и развивающегося фиброза, ограничивающих нормальное растяжение миокардиальных волокон. Эти изменения наиболее выражены в эндокарде, они сочетаются с двукратным ростом диастолической упругости при неизменной способности к развитию систолического давления [27]. В совокупности эти факторы способствуют повышению КДД — обязательному признаку диастолической СН. В свою очередь повышенная диастолическая упругость миокарда облегчает развитие силы в систолу [28, 29], что способствует поддержанию нормального систолического давления.
Однако дальнейшее ухудшение расслабления и закономерное снижение сократимости заставляют орган мобилизировать максимальные резервные ресурсы в виде дилатации полости ЛЖ. Это происходит при действии высоких доз ИЗО вследствие активации воспалительных цитокинов — интерлейкина (ИЛ)-1, ИЛ-6 и ИЛ-17, индуцирующих экспрессию матричных металлопротеиназ MMP-2 и MMP-9 [30]. Нарушение нормальной геометрической формы ЛЖ, естественно, снижает эффективность систолы — уменьшаются и ФВ, и степень уменьшения площади ЛЖ (см. табл. 2, серия ИЗО-4), развивается систолическая СН. Как показали наши данные, при этом происходит глубокое нарушение транспорта Са2+ в КМЦ — резко замедляется процесс поглощения Са2+ из миоплазмы, удаление Са2+ становится неполным, это может формировать субконтрактурные явления в миофибриллах, способствующие дальнейшему повышению КДД в ЛЖ. Снижение сократимости изолированных КМЦ желудочка и замедленный ритм спонтанных сокращений изолированных предсердий отмечается достаточно рано — через 1 нед после ежедневного введения малых доз ИЗО [31].
Следует отметить, что несмотря на глубокие изменения свойств миокарда, МО снижается гораздо в меньшей степени (см. табл. 2, серия ИЗО-4) благодаря включению компенсаторных возможностей системы кровообращения. Периферическое сопротивление снижается, что облегчает изгнание, а венозное давление повышается для обеспечения достаточного притока в условиях повышенного диастолического давления. Это позволяет поддержать кровоснабжение органов на приемлемом уровне. Недостаточная мобилизация компенсаторных факторов, определяющих необходимый приток или сопротивление, может сопровождаться преобладанием одной из форм, ограничивающих функцию недостаточного сердца. Поэтому А. Katz [6] рекомендует выделять СН с преобладанием нарушенного притока или сопротивления (backward or forward failure).
В современной кардиологической литературе оживленно дискутируется вопрос, являются ли диастолическая и систолическая СН самостоятельными формами заболевания или же они представляют разные стадии процесса. Наши данные свидетельствуют в пользу последней версии, а именно: 1) при использовании низких доз ИЗО возникает диастолическая СН, в то время как для развития систолической СН требуются высокие дозы ИЗО; 2) признаки диастолической СН проявляются рано, в то время как для развития систолической СН требуется, по крайней мере, 1—2 нед, что обусловлено синтезом матричных металлопротеиназ для последующей дилатации сердца; 3) нарушение расслабления и по времени, и по степени опережает нарушения сократимости миокарда. При этом в формировании одного из основных признаков СН — повышенного КДД — участвуют оба процесса: в результате неполного расслабления уменьшается объем камеры ЛЖ к началу наполнения, а в результате сниженного изгнания увеличивается остаточный объем крови в ЛЖ, что и демонстрирует достаточно высокая корреляция КДД с показателями сократимости и расслабления миокарда.
Представляется важным также преимущественное изменение показателей расслабления в ауксоволюмической фазе по сравнению с изоволюмической. Ауксоволюмическая фаза представляет заключительный этап снижения давления в ЛЖ, когда диастолическое давление становится меньше давления в левом предсердии и наступает фаза быстрого наполнения. Именно в этом периоде Са2+ удаляется из миоплазмы белками с высоким сродством к катиону, и только достаточно эффективное поглощение Са2+ обеспечивает возможность падения диастолического давления в ЛЖ ниже нуля. Рано возникающее нарушение этого процесса при повреждении миокарда, проявляющееся на эхокардиограмме снижением пика быстрого наполнения, позволяет полагать, что нарушение этого процесса может быть одним из первых признаков развивающейся СН.
Работа поддержана грантом РФФИ № 12-04-01104а.



