Результаты эпидемиологических исследований, выполненных в последние годы, свидетельствуют о высокой распространенности аортального стеноза (АС) в странах Европы и Северной Америки. В частности, в США около 5,2 млн человек страдают АС. Об актуальности этой проблемы свидетельствует и то, что с момента появления симптомов летальность при этом заболевании достигает 25% в год и 50% – в течение 2 лет. Большинство летальных исходов (50%) — это внезапная смерть [1]. Единственным методом лечения тяжелого АС по-прежнему остается протезирование аортального клапана (АК). Ежегодно в США больным АС проводится около 95 тыс. хирургических вмешательств [2, 3], тогда как в России число операций за 2011 г. не превысило 5850 [4].
Среди наиболее частых причин АС у лиц моложе 60 лет называют врожденную аномалию АК, бикуспидальный АК (БАК), который выявляется у 59% больных с данным пороком [5]. Врожденные мальформации АК могут быть причиной развития АС и у лиц старше 75 лет (в 35% случаев). Однако, как свидетельствует статистика, основной причиной развития АС, выявляемого у 43,1% больных с клапанной патологией сердца, служит дегенеративное поражение трикуспидального АК (ТАК), на долю которого приходится 81,9% всех случаев АС [6—8]. Известно, что дегенеративные изменения АК имеются примерно у 30% всех лиц в возрасте 65 лет и старше и у 3—9% лиц старшей возрастной группы выявляется АС [9]. В результате увеличения продолжительности жизни растущего населения планеты можно ожидать увеличения распространенности АС и потребности в хирургическом лечении пациентов старшей возрастной группы. Вместе с тем протезирование АК у пациентов старше 70 лет ассоциировано с ростом интраоперационной летальности (5—15%) по сравнению с таковой у более молодых пациентов (2—5%), а необходимость проведения сочетанных операций дополнительно увеличивает риск развития периоперационных осложнений на 5—7%. С учетом распространенности, высокой летальности и необходимости оказания высокотехнологичной медицинской помощи АС становится одной из важных медико-социальных и экономических проблем, что подчеркивает важность изучения механизмов развития дегенеративного АС с целью разработки оптимальных методов профилактики данного заболевания.
Механизмы, лежащие в основе кальцификации АК, до сих пор недостаточно изучены. Известно, что система остеопротегерин (ОПГ)/лиганд рецептора активатора фактора транскрипции κВ (RANKL)/рецептор активатора фактора транскрипции κВ (RANK) принимает активное участие в регуляции иммуновоспалительных процессов у больных атеросклерозом и кальцинозом АК. Оценка концентрации ОПГ и растворимого RANKL (sRANKL) в сыворотке крови у пациентов с различными морфологическими вариантами АС – ТАК и БАК послужила целью настоящей работы.
Материал и методы
 Исследование проводили на базе ФГБУ ФЦСКЭ им. В.А. Алмазова. В основную группу вошли 57 пациентов с тяжелым АС (табл. 1). Контрольную группу составили 16 практически здоровых доноров крови и 16 пациентов без заболеваний сердечно-сосудистой системы (средний возраст 55,6±0,6 года). Пациенты контрольной группы не имели клапанной патологии, признаков соединительнотканной дисплазии, артериальной гипертензии (АГ) и ишемической болезни сердца (ИБС) в анамнезе. Исследуемые группы были сопоставимы по полу и возрасту. Пациентов с инфекционным эндокардитом и ревматической болезнью сердца в исследование не включали. Тяжесть АС оценивали по стандартному протоколу трансторакальной эхокардиографии (ЭхоКГ) на аппарате аппаратае Vivid 7, согласно Европейским/Американским рекомендациям по эхокардиографии [10]. Наличие БАК у 21 пациента подтверждено на основании интраоперационной биопсии. По результатам гистологического исследования, причиной формирования АС у 16 пациентов с ТАК был дегенеративный процесс. Основным критерием отбора пациентов в исследование была пиковая скорость на АК (Vmax) более 3,0 м/с. В зависимости от анатомических особенностей АК пациенты были разделены на 2 подгруппы: 1-я — пациенты с ТАК, 2-я —пациенты с БАК. Для характеристики степени тяжести АГ использованы анамнестические значения максимального артериального давления (АД), а также офисное АД в момент взятия крови для определения биомаркеров. Клиническая характеристика пациентов представлена в табл. 1.
Исследование проводили на базе ФГБУ ФЦСКЭ им. В.А. Алмазова. В основную группу вошли 57 пациентов с тяжелым АС (табл. 1). Контрольную группу составили 16 практически здоровых доноров крови и 16 пациентов без заболеваний сердечно-сосудистой системы (средний возраст 55,6±0,6 года). Пациенты контрольной группы не имели клапанной патологии, признаков соединительнотканной дисплазии, артериальной гипертензии (АГ) и ишемической болезни сердца (ИБС) в анамнезе. Исследуемые группы были сопоставимы по полу и возрасту. Пациентов с инфекционным эндокардитом и ревматической болезнью сердца в исследование не включали. Тяжесть АС оценивали по стандартному протоколу трансторакальной эхокардиографии (ЭхоКГ) на аппарате аппаратае Vivid 7, согласно Европейским/Американским рекомендациям по эхокардиографии [10]. Наличие БАК у 21 пациента подтверждено на основании интраоперационной биопсии. По результатам гистологического исследования, причиной формирования АС у 16 пациентов с ТАК был дегенеративный процесс. Основным критерием отбора пациентов в исследование была пиковая скорость на АК (Vmax) более 3,0 м/с. В зависимости от анатомических особенностей АК пациенты были разделены на 2 подгруппы: 1-я — пациенты с ТАК, 2-я —пациенты с БАК. Для характеристики степени тяжести АГ использованы анамнестические значения максимального артериального давления (АД), а также офисное АД в момент взятия крови для определения биомаркеров. Клиническая характеристика пациентов представлена в табл. 1.
Концентрацию в сыворотке крови ОПГ и sRANKL определяли методом ручного планшетного иммуноферментного анализа с детекцией на планшетном ридере. Уровень C-реактивного белка (СРБ) в сыворотке крови оценивали на автоматическом биохимическом анализаторе Cobas Integra 400+ турбидиметрическим методом. Содержание общего холестерина (ОХС), триглицеридов (ТГ), холестерина (ХС) липопротеидов высокой плотности (ЛВП), ХС липопротеидов низкой плотности (ЛНП) в сыворотке крови определяли с использованием стандартных наборов реактивов фирмы «Abbott Clinical Chemistry». ОХС и ТГ определяли ферментативным методом, ХС ЛВП, ХС ЛНП — хромогенным методом.
Статистический анализ данных, полученных в ходе исследования, проведен с использованием прикладных статистических программ Statistica for Windows ver. 10.0. Для показателей, имеющих приближенно нормальное распределение, результаты представлены в виде среднего арифметического значения (М), средней арифметической ошибки (m) и числа признаков в группе (n). Критерий значимости устанавливали на уровне р<0,05. Корреляционные связи между парами количественных переменных оценивали, используя непараметрический критерий Спирмена. Для выявления независимого влияния на количественные показатели качественных факторов использована процедура однофакторного дисперсионного анализа (ANOVA).
Результаты
Среди включенных в исследование превалировали пациенты с БАК (50,8%). Подгруппы не различались по демографическим характеристикам и показателям липидного состава крови.
В анамнезе у 80,7% больных АС имелась АГ. Анамнестические максимальные уровни систолического АД (САД), а также офисного САД во время осмотра были значимо выше у пациентов с ТАК. Вместе с тем максимальные уровни диастолического АД (ДАД) у пациентов в подгруппах не различались (см. табл. 1). Подгруппы также не различались по эхокардиографическим показателям тяжести АС (табл. 2).
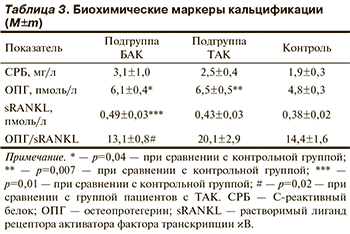
Сравнительный анализ уровней ОПГ, sRANКL и СРБ в сыворотке крови у пациентов с тяжелым АС не выявил различий в исследуемых подгруппах (табл. 3). Вместе с тем по сравнению с контрольной группой у больных АС концентрация ОПГ в сыворотке крови была повышена. Кроме того, в подгруппе пациентов с БАК по сравнению с контрольной группой отмечено увеличение уровня sRANKL в сыворотке крови. Увеличение уровня ОПГ было ассоциировано с повышенным содержанием СРБ (r=0,291; p=0,03) и увеличением возраста обследованных пациентов (r=0,448; p<0,001). Кроме того, высокий уровень СРБ был достоверно связан с ростом концентрации sRANKL в сыворотке крови (r=0,299; p=0,024). Не выявлено связи концентрации ОПГ и sRANKL с наличием в анамнезе сахарного диабета (СД) и никотиновой зависимости. Однако у пациентов с АС ТАК концентрация sRANKL была тесно связана с наличием АГ (r=0,4; p=0,02). У пациентов с ТАК также выявлено повышение соотношения ОПГ/sRANKL. Установлена прямая корреляция между возрастом обследованных больных АС и величиной отношения ОПГ/sRANKL (r=0,399; p<0,01).
Обсуждение
 Длительное время кальциноз АК рассматривался с позиции пассивного дегенеративного процесса, возникающего в ответ на гемодинамическую нагрузку под влиянием возраста. Однако отсутствие кальциноза АК у 30% больных старше 80 лет противоречит этой гипотезе. Сходство гистологической картины при АС и атеросклеротическом поражении сосудистой стенки указывает на общность механизмов, связанных с повреждением эндотелия, накоплением «атерогенных липопротеидов», активацией ренин-ангиотензиновой системы, развитием иммуновоспалительного процесса и кальцификации [11]. Общими являются и основные факторы риска: возраст, мужской пол, СД, АГ, избыточная масса тела, почечная недостаточность, гиперхолестеринемия и курение. Вместе с тем для клапанного поражения характерны ранняя и быстрая кальцификация, отсутствие гладких мышечных клеток, функцию которых выполняют миофибробласты, относительно редкое вовлечение в процесс коронарных артерий (только в 40% случаев) и низкая эффективность статинов в профилактике прогрессии АС [12], что указывает на различия в патогенезе атеросклеротических и дегенеративных поражений.
Длительное время кальциноз АК рассматривался с позиции пассивного дегенеративного процесса, возникающего в ответ на гемодинамическую нагрузку под влиянием возраста. Однако отсутствие кальциноза АК у 30% больных старше 80 лет противоречит этой гипотезе. Сходство гистологической картины при АС и атеросклеротическом поражении сосудистой стенки указывает на общность механизмов, связанных с повреждением эндотелия, накоплением «атерогенных липопротеидов», активацией ренин-ангиотензиновой системы, развитием иммуновоспалительного процесса и кальцификации [11]. Общими являются и основные факторы риска: возраст, мужской пол, СД, АГ, избыточная масса тела, почечная недостаточность, гиперхолестеринемия и курение. Вместе с тем для клапанного поражения характерны ранняя и быстрая кальцификация, отсутствие гладких мышечных клеток, функцию которых выполняют миофибробласты, относительно редкое вовлечение в процесс коронарных артерий (только в 40% случаев) и низкая эффективность статинов в профилактике прогрессии АС [12], что указывает на различия в патогенезе атеросклеротических и дегенеративных поражений.
Большинство гистологических и молекулярно-биологических исследований последнего десятилетия подтверждает гипотезу о развитии кальциноза АК в рамках иммуновоспалительного процесса. RANKL — трансмембранный гликопротеин, продуцируемый клетками остеобластного ряда и активироваными Т-лимфоцитами, принадлежит к семейству фактора некроза опухоли и является главным стимулом для созревания остеокластов. Остеобластными клетками, клетками стромы, эндотелиальными клетками сосудов и В-лимфоцитами синтезируется растворимый рецептор для RANKL, ОПГ, который действует как эндогенный рецептор для RANKL, блокируя его взаимодействие с собственным рецептором (RANK) и нарушая процесс остеокластогенеза. Наряду с ремоделированием костной ткани система RANKL/ОПГ/RANK принимает активное участие в формировании кальциноза клапанов сердца. Увеличение продукции провоспалительных цитокинов (RANKL, интерлейкина-1β и фактора некроза опухоли α), хемокинов, матриксных металлопротеиназ и факторов роста активированными макрофагами и Т-лимфоциами приводит к фенотипической трансформации фибробластов с образованием остеобластоподных клеток, способствующих формированию кальцинатов [13]. Сложный процесс кальцификации АК регулируется многочисленными генами, ответственными за функциональное состояние эндотелия, накопление атерогенных липопротеидов, развитие воспалительных реакций, ремоделирование экстрацеллюлярного матрикса, неоваскулогенез и эктопическое отложение кальция [14]. Поэтому существует гипотеза, что генетические факторы играют важную роль в патологической дифференцировке миофибробластов при АС.
Развитие кальциноза АК у 54% больных с БАК служит неопровержимым доказательством генетической предрасположенности к данному заболеванию [15].
 Наряду с выявлением генетических детерминант активно ведется поиск биомаркеров, позволяющих оценить степень тяжести АС, темпы его прогрессирования и прогноз. Еще C.R. Dhore и K.L. Tyson предположили, что ОПГ, будучи ингибитором кальцификации и резорбции костной ткани, может иметь большое значение в патогенезе кальцификации АК и сосудистой стенки [16, 17]. В проведенном нами исследовании выявлена более высокая концентрация ОПГ, чем в раннее опубликованных работах, в которых указанный показатель варьировался от 2,0 до 3,5 пмоль/л [18—20]. Полученные нами данные соответствуют результатам T. Adamczyk и W. Lieb [21, 22]. Вместе с тем T. Adamczyk и соавт. при обследовании 68 пациентов с умеренным и тяжелым АС не удалось выявить различий по концентрации ОПГ в основной и контрольных группах, а также установить связь между концентрацией ОПГ и тяжестью АС. В настоящей работе, как и в работе К. Akat и соавт., получены более высокие концентрации ОПГ у пациентов с тяжелым АС по сравнению с группой контроля. Возможно, высокое содержание ОПГ в сыворотке крови пациентов контрольной группы в исследовании T. Adamczyk обусловлено включением пациентов с ИБС [21, 23].
Наряду с выявлением генетических детерминант активно ведется поиск биомаркеров, позволяющих оценить степень тяжести АС, темпы его прогрессирования и прогноз. Еще C.R. Dhore и K.L. Tyson предположили, что ОПГ, будучи ингибитором кальцификации и резорбции костной ткани, может иметь большое значение в патогенезе кальцификации АК и сосудистой стенки [16, 17]. В проведенном нами исследовании выявлена более высокая концентрация ОПГ, чем в раннее опубликованных работах, в которых указанный показатель варьировался от 2,0 до 3,5 пмоль/л [18—20]. Полученные нами данные соответствуют результатам T. Adamczyk и W. Lieb [21, 22]. Вместе с тем T. Adamczyk и соавт. при обследовании 68 пациентов с умеренным и тяжелым АС не удалось выявить различий по концентрации ОПГ в основной и контрольных группах, а также установить связь между концентрацией ОПГ и тяжестью АС. В настоящей работе, как и в работе К. Akat и соавт., получены более высокие концентрации ОПГ у пациентов с тяжелым АС по сравнению с группой контроля. Возможно, высокое содержание ОПГ в сыворотке крови пациентов контрольной группы в исследовании T. Adamczyk обусловлено включением пациентов с ИБС [21, 23].
Повышение содержания sRANKL в сыворотке крови у больных БАК по сравнению с контрольной группой, продемонстрированное в нашем исследовании, служит дополнительным подтверждением роли системы RANKL/RANK в развитии кальциноза сосудистой стенки и АК, в том числе у пациентов с врожденной аномалией клапанов [24, 25].
В то же время у больных АС на фоне ТАК уровень sRANKL сопоставим с таковым в контрольной группе. Сходные результаты получены в исследовании M. Schoppet и соавт., в котором, несмотря на повышение уровня ОПГ, ассоциированного с увеличением частоты развития сердечно-сосудистых осложнений (ССО), концентрация sRANKL у 240 мужчин с доказанной ИБС была существенно ниже, чем у пациентов без данного заболевания; более того, она отрицательно коррелировала не только с ОПГ, но и с возрастом, липидным составом крови, уровнем АД, СД и индексом массы тела [26].
В другом, более крупном исследовании W. Lieb и соавт., проанализировав содержание ОПГ и sRANKL в сыворотке крови у 3250 пациентов, пришли к выводу, что ОПГ может служить маркером ССО, в то время как повышение концентрации sRANKL ассоциируется с благоприятным прогнозом в плане ССО [27]. Трактовка выявленного в настоящем исследовании изолированного повышения уровня sRANKL у пациентов с БАК с учетом ранее опубликованных исследований крайне затруднена и нуждается в дальнейшем изучении. Нельзя исключить модифицирующего влияния терапии статинами, которую в основном получали больные ТАК.
В рамках настоящего исследования не выявлено связи между эхокардиографическими показателями степени тяжести АС и уровнем СРБ, что, вероятно, обусловлено отсутствием достоверных отклонений содержания указанного биомаркера от нормы. Полученные данные также можно объяснить приемом лекарственных препаратов, в первую очередь статинов.
С учетом иммуновоспалительной теории патогенеза АС неоднократно предпринимались попытки доказать эффективность статинов в профилактике прогрессирования АС. Однако результаты исследований SEAS и ASTRONOMER показали, что статины лишь уменьшают риск развития ССО у пациентов данной категории, не влияя на течение основного заболевания [28—31]. Поэтому назначение статинов больным АС осуществляется в соответствии с принципами первичной и вторичной профилактики [32].
Наряду с терапией статинами 36,8% (n=21) пациентов принимали ингибиторы ангиотензинпревращающего фермента (АПФ)/антагонисты рецепторов к ангиотензину II (АРА).
Ранее из-за уменьшения сердечного выброса вследствие снижения преднагрузки назначения препаратов этого класса больным АС старательно избегали. Однако результаты последнего рандомизированного исследования показали, что ингибиторы АПФ и АРА способствуют уменьшению частоты развития ССО и увеличивают выживаемость пациентов с АС [33].
В заключение следует отметить, что несмотря на различия в патогенезе АС у пациентов с БАК и ТАК процесс кальцификации АК имеет общие механизмы. С учетом полученных данных наибольшее значение изменения в системе ОПГ/RANKL/RANK приобретают для развития и прогрессирования дегенеративного АС. Поиск лекарственных препаратов, способных оказывать модифицирующее действие на эту систему, откроет новые возможности для лечения и профилактики аортального стеноза.



