Введение
По мере старения населения увеличивается распространенность возрастных заболеваний мелких сосудов головного мозга (церебральная микроангиопатия). При нейровизуализации эти состояния характеризуются гиперинтенсивностью перивентрикулярного белого вещества, лакунами и церебральными микрокровоизлияниями, распространенность которых в популяции варьируется от 3,1 до 26,9% [1].
SARS-CoV2 как триггер церебральной микроангиопатии
Церебральная микроангиопатия (ЦМА) обычно протекает бессимптомно или может ассоциироваться с незначительными изменениями психических (например, замедление мышления, депрессивное настроение, апатия) и/или двигательных функций (например, замедление походки). Такие тонкие изменения часто воспринимаются как часть нормального процесса старения. ЦМА может прогрессировать медленно (например, в течение многих лет или десятилетий) и начинает отчетливо проявлять массивные когнитивные нарушения, когда достигается определенный порог поражения мозга или более драматично, когда происходят провоцирующие события (например, пневмония, гипотония). Исследования в период пандемии COVID-19 показали, что вирус SARS-CoV2 является важнейшим триггером прогрессирования ЦМА. Сегодня стало очевидным, что длительный COVID, сохранение симптомов более 12 недель после выздоровления от острой инфекции [2, 3] также могут иметь пагубные долговременные последствия для нервной и сосудистой систем [3]. Многочисленные исследования показали, что до 70% пациентов с длительным диагнозом COVID имеют когнитивную дисфункцию [4], включая нарушения исполнительных функций, скорости обработки информации, беглости категорий, кодирования памяти и воспроизведения [5]. Патофизиологические механизмы, запускающие клинически значимое поражение сосудов головного мозга мелкого и среднего калибров и появление когнитивных нарушений, в первую очередь обусловлены особенностями соединения вируса SARS-CoV2 с клеткой хозяина через ангиотензинпревращающий фермент-2 (АПФ-2). Прикрепление белка-шипа SARS-CoV2 к рецептору АПФ-2 на эндотелиальных клетках приводит к образованию тромбовоспалительной среды с избыточной продукцией активных форм кислорода [6], что вызывает нарушение регуляции функции эндотелия в макро- и микроциркуляторное русло у пациентов в острый и отдаленный периоды COVID-19 [7]. Конечно, инфекция SARS-CoV-2 в первую очередь поражает легочную систему, но накапливающиеся данные позволяют утверждать, что она также влияет на все сосуды внелегочных систем. Отдельные исследования демонстрируют, что вызванная COVID-19 системная макро- и микрососудистая эндотелиальная дисфункция персистирует после острого периода инфекции [8] и связана со снижением когнитивных функций у пациентов, выздоровевших от COVID-19 [9]. Об усилении воспаления эндотелия свидетельствует повышенная экспрессия различных биологических маркеров. Недавнее ретроспективное исследование показало, что воспалительные эндотелиальные маркеры были повышены у пациентов с COVID-19 и изменялись во время прогрессирования и регрессии заболевания, что повышает вероятность того, что эти воспалительные маркеры являются хорошим показателем воспаления и дисфункции эндотелия при COVID-19 [10]. Высвобождение воспалительных цитокинов представляет собой первый этап воспалительной реакции, инициирующей или усугубляющей развитие атеросклероза. Большой объем литературы подтверждает роль системного воспаления в развитии атеросклероза и повышенном риске деменции. Верификация основных механизмов патогенного влияния COVID-19 на церебральную микроциркуляцию и развитие когнитивной дисфункции определяет выбор нескольких категорий эндотелий-таргетной терапии, которая потенциально может уменьшать эндотелиальную дисфункцию у пациентов с COVID-19.
Фармакологическая коррекция
В настоящее время предпринимаются большие усилия по поиску противовоспалительных препаратов, которые можно использовать в течение длительного времени с минимальными побочными эффектами. Этому условию отвечает препарат винпоцетин, производное алкалоида винкамина, который применяется во многих странах для лечения цереброваскулярных расстройств, включая деменцию, на протяжении более 40 лет. Винпоцетин – ингибитор фосфодиэстеразы (ФДЭ), известный своими минимальными побочными эффектами [11, 12] и высоким потенциалом улучшения когнитивных функций [13, 14], также обладает мощным противовоспалительным действием [15]. Винпоцетин ингибирует внутриклеточный транскрипционный NF-κB, который контролирует очень большую группу генов, отвечающих за процесс воспаления, пролиферацию клеток и апоптоз, а также экспрессию фактора некроза опухоли α (ФНО-α) [16]. Винпоцетин также снижает индуцированную ФНО-α экспрессию мРНК провоспалительных молекул, таких как интерлейкин-1β, белок-хемоаттрактант моноцитов-1 (MCP-1) и молекула адгезии сосудистых клеток-1 (VCAM-1). В основе противовоспалительных свойств винпоцетина лежит ингибиция одного из сигнальных компонентов NF-κB, а именно киназы IκB (IKK), в результате чего нарушается транслокация NF-κB в ядро [15]. Важно, что этот механизм не зависит от действия винпоцетина на ФДЭ.
Одним из достижений современной фармакологии является создание комбинированных лекарственных препаратов, компоненты которых, действуя на различные мишени, клинически демонстрируют синергичный эффект. Примером такой удачной комбинации является препарат винпоцетин (5 мг)+пирацетам (400 мг), который широко используется при лечении пациентов с различными заболеваниями центральной нервной системы.
Механизм действия винпоцетина дополняется влиянием пирацетама на обмен веществ в нервной ткани и влиянием на гладкую мускулатуру мозговых сосудов.
Сегодня российскими исследователями накоплен достаточный клинический опыт применения комбинированного препарата винпоцетин+пирацетам у пациентов с различными формами расстройств мозгового кровообращения, в частности с ЦМА (хронической ишемией мозга) [17–19]. В то же время противовоспалительные и тропные к эндотелию эффекты позволяют использовать препарат для коррекции когнитивных нарушений в постковидный период. Мы представляем клинический случай, иллюстрирующий изложенные положения.
Клиническое наблюдение
С марта по декабрь 2021 г. мы наблюдали пациента С. 63 лет, работавшего преподавателем в техническом колледже, проживавшего в семье. В анамнезе имелись следующие факторы сосудистого риска: гипертоническую болезнь I стадии, степень 1, дислипидемию, ожирение I степени (индекс массы тела – 32), курение с 17 лет. В семейном анамнезе не было никаких психических и неврологических проблем.
Двенадцатого марта 2021 г. у пациента остро повысилась температура тела (максимально до 39,6оС), появились малопродуктивный кашель, одышка, выраженная слабость, 15 марта 2021 г. диагноз COVID-19 был подтвержден положительным результатом полимеразной цепной реакции на SARS-CoV-2 в мазках из носоглотки. Компьютерная томография – КТ (Siemens Somatom Sensation 40-срезовый) грудной клетки, проведенная 15 марта 2021 г., выявила двустороннюю полисегментарную вирусную пневмонию (полисегментарно в обоих легких, субплеврально и периорбитально визуализируются множественные очаги и зоны уплотнения легочной паренхимы по типу «матового стекла» округлой и неправильной формы с участками консолидации и интерстициальных изменений; паренхима легких вовлечена в патологический процесс на 40% справа, 25% слева), КТ-2. Пациент был госпитализирован с 16.03.2021 по 28.03.2021 для лечения осложнений коронавирусной инфекции: двусторонней полисегментарной пневмонии, интоксикационного синдрома. На момент поступления у него была пограничная лейкопения (число лейкоцитов – 3,5 тыс.), уровень С-реактивного белка был повышен до 89,7 мг/л (референтный диапазон <5 мг/л), D-димер оставался в пределах нормы – 413 нг/мл (референтный диапазон – 0,0–500,0 нг/мл). Пациенту проводилась кислородная поддержка без экстракорпоральной мембранной оксигенации, детоксикационная терапия и профилактика венозной тромбоэмболии. Был выписан из стационара 28.03.2021 в удовлетворительном состоянии с положительной динамикой, улучшением лабораторных показателей. В середине апреля 2021 г. пациент приступил к работе.
Визит 1. Пациент обратился 18.05.2021 к неврологу с жалобами на постоянное ощущение «несвежей головы», трудности концентрации внимания, периодические затруднения с подбором нужных слов в спонтанной речи, а также нарушение сна. Он рассказал, что ранее привычная профессиональная деятельность требует от него значительного напряжения, поэтому он постоянно ощущает усталость, ему кажется, что он утратил способность быстро усваивать новую информацию. Пациент высказывал беспокойство, что теряет память. Жена пациента сообщила, что в последнее время ее супруг изменился: стал раздражительным, более замкнутым, практически не занимался домашними делами.
Для оценки когнитивного статуса пациенту проведено тестирование с помощью Монреальской когнитивной шкалы (MoCA), версия 8.1 (URL: https://www.mocatest.org/). Общий счет MoCA составил 27 баллов, для более полной оценки когнитивного статуса использовались МоСА-индексы на основе методики P. Julayanont et al. [20]. Расчетные индексы (табл. 1) показали, что наиболее значимо у пациента были нарушены исполнительные функции и внимание, собственно функция памяти практически не пострадала (индекс памяти – 14 баллов). Паттерн когнитивных нарушений нашего пациента соответствовал паттерну поствирусных изменений когнитивных функций, при которых доминируют нарушения внимания, исполнительных функций и в меньшей степени – памяти [21, 22], при этом полимодальные изменения встречаются чаще, чем изменения в одном домене [21]. Поскольку когнитивная дисфункция у пациента была легкой степени, ему рекомендовано соблюдение баланса между активностью и отдыхом, включая профессиональную активность, разбиение профессиональных и бытовых задач на этапы, восстановительную когнитивную реабилитацию (упражнения на удержание внимания), расширение физической активности.
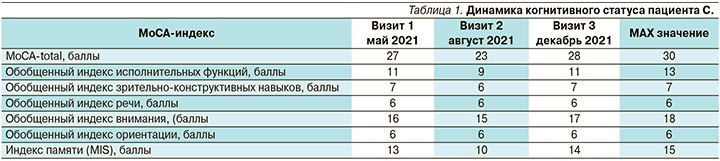
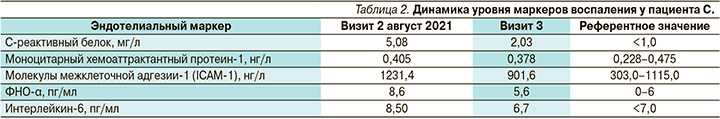
Визит 2. Однако спустя 3 месяца в августе 2021 г. пациент вновь обратился к неврологу. Супруга пациента объяснила, что она заметила у мужа тревожные когнитивные изменения, по ее мнению, проблемы с усвоением новой информации, забывчивость ограничивают не только его трудовую деятельность, но и мешают частной жизни. Повторное тестирование показало значительное ухудшение когнитивных функций. Общий счет MoCA составил 23 балла, индекс памяти – 12 баллов. Ускоренная потеря когнитивных способностей, по нашему мнению, может быть объяснена прогрессированием ЦМА до порогового уровня. Вероятно, триггером этого состояния послужило перенесенное вирусное заболевание COVID-19. Нашу гипотезу подтвердило дополнительное инструментальное обследование пациента. Магнитно-резонансная томография (МРТ) головного мозга от 23.08.2021: МРТ-картина очагового изменения белого вещества головного мозга как следствие микроангиопатии (2-я стадия по шкале Fazekas); атрофическое расширение наружных и ликворных пространств (ликвородинамика не нарушена). МРТ данных за объемное поражение и острое нарушение мозгового кровообращения в структурах головного мозга не выявлено. Методом иммуноферментного анализа (ELISA) определены уровни периферических маркеров эндотелиального воспаления. О воспалении эндотелия у пациента С. свидетельствовало повышение 4 из 5 проанализированных биологических маркеров периферической крови (табл. 2).
Исходя из концепции роли системного воспаления в развитии ЦМА и когнитивных нарушений, мы рекомендовали пациенту прием комбинированного препарата винпоцетин+пирацетам, один из компонентов которого, винпоцетин, обладает противовоспалительными свойствами. Дополнительно к препаратам, корректирующим сосудистые риски, пациент С. получал винпоцетин+пирацетам по 2 капсулы 3 раза в сутки начиная с 26.08.2021 в течение 3 месяцев. Также пациенту рекомендовано продолжить когнитивный тренинг.
Визит 3. При наблюдении 14 декабря 2021 г. общий счет MoCA улучшился до нормального уровня 28 баллов, при этом важно отметить, что индекс памяти улучшился до максимально достижимого уровня 15 баллов, наблюдалось значительное уменьшение дефицита внимания (индекс вырос до 17 баллов). Параллельно с улучшением когнитивных функций значительно снизились уровни воспалительных маркеров, 4 из 5 маркеров достигли нормативных значений (табл. 2). Снижение уровней маркеров воспаления в представленном клиническом наблюдении свидетельствует о пролонгированном противовоспалительном действии винпоцетина. О побочных эффектах не сообщалось. Наше наблюдение согласуется с теоретическими соображениями, предполагающими, что использование комбинированного препарата винпоцетин+пирацетам является многообещающим терапевтическим вмешательством при когнитивных нарушениях у пациентов, перенесших COVID-19.
Заключение
Доказательные терапевтические возможности лечения пациентов с когнитивными нарушениями, связанными с пост-COVID-19, еще не созданы. С учетом хорошей переносимости и низкого потенциала взаимодействия с другими лекарственными средствами применение комбинированного препарата винпоцетин+пирацетам в суточной дозе не менее 2400 мг пирацетама и 30 мг винпоцетина является оправданным терапевтическим вариантом, который следует рассматривать для пациентов с возрастзависимой ЦМА, перенесших COVID-19.



