Введение. На сегодняшний день лапароскопическая резекция почки (ЛРП) практически полностью вытеснила открытые вмешательства в лечении локализованного рака паренхимы почки, что привело к снижению количества осложнений, а также к длительности пребывания пациента в стационаре [1, 2]. С другой стороны, отсутствие тактильного контакта, зачастую ограниченная визуализация могут стать причиной повреждения сосудов или соседних органов, положительного хирургического края при резекции опухоли, особенно при сложных вариантах анатомии почки и резецируемой опухоли [3, 4]. В настоящее время с целью улучшения результатов и повышения эффективности минимально-инвазивных вмешательств разрабатываются различные методы интраоперационной визуализации, в частности технология дополненной реальности (Augmented reality, AR), позволяющая визуализировать наложение трехмерных реконструкций пораженного органа или смежных структур на операционное поле в реальном времени через специализированные устройства.
Цель исследования: оценить безопасность и полезность применения технологии AR с использованием очков HoloLens во время выполнения ЛРП.
Материалы и методы. В работу включены 5 пациентов (средний возраст – 64 [38–82] года) с локализованным раком почки (стадия – сТ1aN0M0), которым одним хирургом выполнена AR-ассистированная ЛРП. Справа опухоль локализовалась в трех наблюдениях, слева – в двух. Средний размер новообразования составил 3,9 (1–7) см.
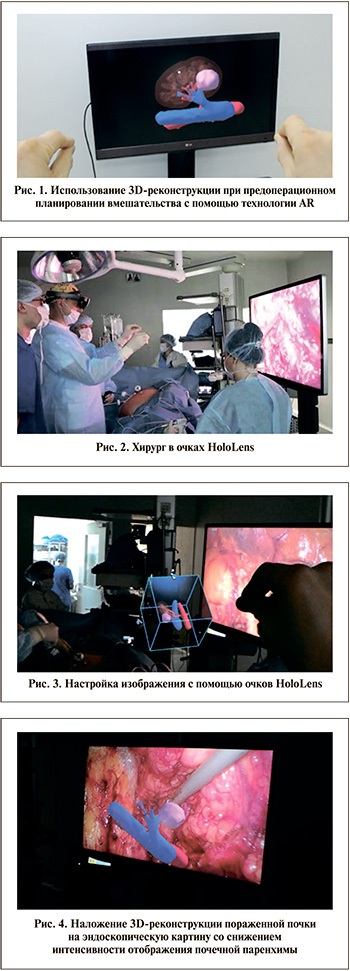 Всем пациентам перед операцией была проведена МСКТ брюшной полости с контрастным усилением. После этого исходный DICOM-файл с томограммой пациента загрузили в программу Инобитек DICOM-Просмотрщик Pro©. В программе были выделены данные о почке, опухоли, артериях и венах около почки, после чего сегментированные данные были экспортированы при помощи той же программы в полигональную сетку в виде STL-файла. Для стабильной работы очков HoloLens требуется до 200 тыс. треугольников на всех объектах в сцене, геометрию полигональных сеток оптимизировали вручную. Для разработки приложения HoloLens использовали платформу Unity© совместно со специальным набором инструментов разработчика для HoloLens, а именно Mixed Reality Toolkit for Unity. После загрузки оптимизированной трехмерной модели органов в приложение к моделям были добавлены материалы для отрисовки разными цветами, а также настроена прозрачность моделей. В ходе разработки настраивали взаимодействие с моделями – перемещение, поворот и масштабирование их в пространстве. В конце настройки отображения и взаимодействия были проведены тесты вне операционной (рис. 1). Время, затраченное на подготовку модели, складывалось из времени, необходимого на оптимизацию модели, и времени затраченного на настройку отображения модели и взаимодействия.
Всем пациентам перед операцией была проведена МСКТ брюшной полости с контрастным усилением. После этого исходный DICOM-файл с томограммой пациента загрузили в программу Инобитек DICOM-Просмотрщик Pro©. В программе были выделены данные о почке, опухоли, артериях и венах около почки, после чего сегментированные данные были экспортированы при помощи той же программы в полигональную сетку в виде STL-файла. Для стабильной работы очков HoloLens требуется до 200 тыс. треугольников на всех объектах в сцене, геометрию полигональных сеток оптимизировали вручную. Для разработки приложения HoloLens использовали платформу Unity© совместно со специальным набором инструментов разработчика для HoloLens, а именно Mixed Reality Toolkit for Unity. После загрузки оптимизированной трехмерной модели органов в приложение к моделям были добавлены материалы для отрисовки разными цветами, а также настроена прозрачность моделей. В ходе разработки настраивали взаимодействие с моделями – перемещение, поворот и масштабирование их в пространстве. В конце настройки отображения и взаимодействия были проведены тесты вне операционной (рис. 1). Время, затраченное на подготовку модели, складывалось из времени, необходимого на оптимизацию модели, и времени затраченного на настройку отображения модели и взаимодействия.
Для стандартизации описания анатомических характеристик опухолей почки использовали нефрометрическую шкалу RENAL, показатели которой коррелируют с результатами резекции почки. Средний показатель по RENAL составил 6 (5–8) баллов.
HoloLens (Microsoft corporation) – это легкие (579 г) автономные очки дополненной реальности на базе операционной системы Windows.10 (Microsoft corporation), отображающие виртуальные трехмерные голограммы в окружающей среде. HoloLens содержат специальную оптику и сенсоры, которые позволяют отображать голограммы внутри реального пространства. Интерфейс устройства основан на виртуальном курсоре, расположенном в центре экрана и перемещающемся при помощи поворота головы, на распознавании ограниченного набора жестов (рис. 2). После запуска приложения в HoloLens при помощи жестов осуществлена калибровка и настройка полученной модели вне операционного поля (рис. 3). Во время непосредственно операции после экспозиции крупных магистральных сосудов выполняли мануальное наложение хирургом полученной 3D-модели пораженной почки с опухолью и сегментированными сосудами на эндоскопическую картину. Таким образом, становилась понятной локализация реальной опухоли почки (рис. 4).
Оценивали время, затрачиваемое на подготовку устройства HoloLens и подготовку 3D-модели, длительность операции и тепловой ишемии, а также частоту и характер интраоперационных осложнений. Помимо этого оперирующий уролог оценивал полезность и эффективность применения AR-технологии по психометрической шкале Ликерта, в соответствии с которой ответ «не полезно» оценивался в 1 балл, «слабо полезно» – в 2, «трудно сказать» – в 3, «полезно» – в 4, «высоко полезно» – в 5 баллов. Статистический анализ выполняли, используя программу PAST XLStat (XLSTAT | Statistical Software for Excel).
Результаты. Среднее время, необходимое для полной настройки AR-оборудования, составило 7,8 (5–12) мин. На изготовление 3D-модели в среднем требовалось 10 (9–11) ч. Общая длительность операции и тепловой ишемии составила 108 (90–120) и 20 (15–25) мин соответственно, интраоперационная кровопотеря – 160 (110–250) мл. Осложнений – повреждение соседних органов, крупных сосудов, вскрытие полостной системы почки – в данной серии пациентов не возникло. Во всех случаях, по данным патоморфологического исследования, констатировали отрицательный хирургический край. Хирург, проводивший оперативное вмешательство, оценил использование AR-технологии с помощью устройства HoloLens во время ЛРП как высокополезную. Средний балл психометрического опросника Ликерта составил 4,7 (4–5).
Обсуждение. Малоинвазивная нефронсберегающая хирургия (nephrone-sparing technique) является «золотым» стандартом лечения пациентов с опухолями почек клинической стадии Т1a-1bN0M0 [5]. Однако сложная анатомия опухоли почки может приводить хирурга к удалению либо чрезмерного объема здоровой паренхимы почки в попытке провести радикальную операцию либо, что еще хуже, недостаточного объема с положительным хирургическим краем после оперативного вмешательства, что повышает вероятность рецидива опухоли и негативно влияет на скорректированную выживаемость (cancer-specific mortality) [6]. Резекция при эндофитно расположенной опухоли почки нередко является непростой задачей, требующей применения интраоперационного УЗИ, а в отсутствие необходимого оборудования способной превратиться в нефрэктомию.
Одним из методов повышения эффективности минимально-инвазивных операций может служить AR-технология. Накладывая трехмерные реконструкции органов на окружающую среду, хирург получает возможность сопоставлять информацию из оперативного поля с результатами инструментальных обследований (например, МСКТ с 3D-моделированием). Однако применение данной технологии во время операции на почке зачастую затруднительно, что связано с ее смещением относительно анатомических ориентиров [7–9]. В современной литературе имеется ряд работ, посвященных использованию интраоперационной технологии дополненной реальности для повышения эффективности ЛРП, однако в России данная технология применяется впервые.
Ю. Г. Аляев и соавт. [10] использовали результаты компьютерной томографии, на основании которых с помощью специального программного обеспечения получали 3D-модели, детально описывающие анатомию почки, взаимоотношение крупных сосудов и полостной системы по отношению к опухоли. Данная технология позволяет проводить виртуальное удаление опухоли почки. Однако применение данной технологии в операционной требует переключения внимания с операционного поля на дополнительный монитор с референсной моделью.
В 2008 г. O. Ukimura et al. [11] представили свой первый опыт применения AR-технологии с использованием КТ- и МРТ-изображений. Компьютер и специальный магнитный сенсор представляли собой основную установку, предназначенную для отслеживания положения хирургических инструментов. Сначала авторы изучили клиническую пользу данного подхода при выполнении радиочастотной абляции опухолей почки, затем проверили эту технологию уже во время лапароскопической радикальной простатэктомии. Авторы сообщили о повышении прецизионности по сравнению с контрольными группами.
T. Drewniak et al. [12] использовали 3D-лазерный сканер во время ЛРП на моделях животных. При сканировании и последующем наложении трехмерных реконструкций погрешность в соответствии с оперативным полем составила 2–9 мм. Авторы пришли к выводу, согласно которому благодаря такой методике можно обеспечить сохранность здоровой паренхимы почки при выполнении резекции опухоли без ущерба в отношении отдаленных результатов.
В работе [13] описано использование специального приложения, обрабатывающего КТ-изображения для создания трехмерных виртуальных моделей почечных сосудов, почки и окружающих органов с дальнейшим их наложением на оперативное поле через отдельный монитор. В результате выполнения трех лапароскопических радикальных нефрэктомий в среднем продолжительность операции и кровопотеря составляли 210 мин и 40 мл соответственно.
G. C. S. Ruppert et al. [14] изучали систему отслеживания рук и распознавания жестов, позволяющую хирургу просматривать КТ-данные во время операции через персональный компьютер с помощью программного обеспечения, которое сопоставляло движения хирурга с перемещением компьютерной мыши. Технология была использована при выполнении ЛРП трем пациентам с опухолью почки небольшого размера. В каждом случае не было ни интра-, ни послеоперационных осложнений. Хирургический край также был отрицательным.
В 2016 г. T. Simpfendörfer et al. [15] представили новую концепцию навигации во время лапароскопических вмешательств, основанную на интраоперационном конусно-лучевом КТ-сканировании, что позволило объединить рентгеновские 2D-изображения в реальном времени с результатами компьютерной томографии. Данная методика была апробирована во время ЛРП по поводу эндофитных опухолей высокого риска операционных осложнений (средний балл RENAL – 9). Данная методика обеспечила лучшее понимание пространственного расположения хирургических инструментов и границ опухоли. Длительность операции была на 15 мин больше, чем в контрольной группе. Среднее время ишемии и кровопотеря составили 11 мин и 50 мл соответственно.
Несмотря на многообещающие результаты, применение вышеописанных технологий зачастую затруднено. Это связано как с необходимостью специализированного оборудования, многоэтапностью его подготовки, так и с недостаточной автономностью AR-изображений.
Результаты нашего пилотного исследования свидетельствуют о том, что применение AR-технологий во время ЛРП не влияет на частоту интраоперационных осложнений, а оперирующим хирургом оценивается как высокополезное. Сама подготовка очков HoloLens не требует много времени. Легкость очков, высокое качество передаваемого изображения, а также многофункциональность и стабилизация в зависимости от направления взгляда хирурга позволяют выполнять хирургические вмешательства без переключения внимания с операционного поля на виртуальные модели. Однако определенным сдерживающим фактором на пути к рутинному использованию AR-технологий в оперативной урологии могут быть времязатратность, связанная с оптимизацией и настройкой отображения модели, а также их стоимость. Для повышения уровня доказательности требуется рандомизированное исследование с включением контрольной группы.
Заключение. В настоящее время во всем мире растет интерес к использованию дополненной реальности в хирургии, что может способствовать повышению безопасности и эффективности оперативного вмешательства, особенно при опухолях почек высокого риска операционных осложнений. Применение AR-технологии с помощью специализированного оптического устройства HoloLens во время лапароскопической резекции почки может приводить к улучшению результатов лечения.



