Введение. На сегодняшний день под простатитом подразумевают заболевание простаты, характеризующееся воспалением и отеком, составляющих ее тканей. Современная классификация подразделяет простатит на острый бактериальный простатит – тип I, хронический бактериальный простатит – тип II, хронический небактериальный простатит/синдром хронической тазовой боли (ХНП/СХТБ) с воспалительным компонентом – тип IIIa и без воспалительного компонента – тип IIIb, а также бессимптомный воспалительный простатит – тип IV. На долю III типа приходится около 90% [1]. По данным отечественных авторов, воспалительный процесс в простате выявляется у 19 % мужчин Российской Федерации [2]. В США распространенность ХНП/СХТБ в среднем составляет 8,2 % и колеблется в пределах от 2,2 до 12,8% [3]. В Российской Федерации в период с 2008 по 2017 г. выявляемость заболеваний простаты увеличилась более чем на 30%. Среди них ХНП/СХТБ занимают третье место, уступив первенство доброкачественной гиперплазии и раку простаты [4]. Большинство пациентов жалуются на значительное снижениие общего самочувствия из-за симптомов ХНП/СХТБ, таких как боли в половых органах, синдром тревожного ожидания, увеличение частоты мочеиспусканий, непродуктивные и болезненные позывы на мочеиспускание, задержка мочи, дриблинг, которые имеют катастрофические последствия как для здоровья, так и для качества жизни мужчины в целом [5]. Исследование R. Zhang и соавт. [6] не выявило зависимости между ХНП/СХТБ и дополнительными факторами риска: индексом массы тела (ИМТ), окружностью талии, соотношением талии и бедер, курением сигарет, гипертонической болезнью. Авторы отмечают, что, поскольку этиология ХНП/СХТБ остается неизвестной, необходимы дополнительные проспективные исследования для установления модифицируемых и немодифицируемых причин этого распространенного состояния [6]. Однако в ходе исследования обнаружено, что у пациентов с высоким уровнем физической активности значительно снижается вероятность развития ХНП/СХТБ. L. Gallo [7] выявил 13 потенциальных факторов риска развития ХНП/СХТБ, включивших нарушение диеты (алкоголь, кофе, перец и острая пища, нарушение функции кишечника), изменение сексуального поведения (задержка эякуляции, половое воздержание, чрезмерная половая активность, прерванный половой акт), образ жизни (гиподинамия, стресс), травмы промежности (тазового дна), миофасциальный синдром, длительное сидячее положение, ношение тесной или обтягивающей одежды. Подробное изучение компонентного состава тела мужчин с ХНП/СХТБ является перспективным. Так, у мужчин первого периода зрелого возраста, страдающих ХНП/СХТБ, выявлена недостаточность мышечной массы по сравнению с популяцией здоровых мужчин [8]. Ежегодный рост заболеваемости ХНП/СХТБ, часто рецидивирующее течение, обусловливают поиск новых методов диагностики, профилактики и подходов к лечению данного заболевания.
Современным неинвазивным доступным методом оценки компонентного состава является биоимпедансометрия. При помощи данного метода были выявлены значимые отклонения состава тела при многих хронических заболеваниях. Так, нарушения гидратации, отношения жировой и активной клеточной масс обнаружены при доброкачественной гиперплазии простаты в сочетании с ХП, соматических заболеваниях (сахарный диабет, варикозная болезнь нижних конечностей, гипертоническая болезнь, хроническая сердечная недостаточность, хроническая обструктивная болезнь легких), острых хирургических (мастит) и хронических воспалительных, в том числе инфекционных (парадонтит, гепатит), заболеваниях, асците. Динамика показателей гидробаланса являлась предиктором исхода воспалительных заболеваний, критерием эффективности терапии и профилактики [9–12]. Продолжаются исследования практического применения биоимпедансометрии в онкологии и отделениях интенсивной терапии [13, 14].
Исходя из вышеизложенного, целью нашего исследования стало выявление биоимпедансометрических и клинических особенностей у молодых мужчин с воспалительным синдромом хронической тазовой боли (ВСХТБ) в зависимости от соматотипа.
Материалы и методы. В период с 2018 по 2022 г. на базе дневного стационара КГБУЗ КМКБ № 4 обследованы 150 мужчин с ВСХТБ первого периода зрелого возраста от 22 до 35 лет. Медиана возраста пациентов составила 31 (28;34) год.
Категорирование простатита проводили согласно общепринятой классификации Национального института здоровья США (National Institutes of Health Prostatitis Syndrome Classification, 1999) [1].
Для объективизации и количественного выражения основных жалоб и проявлений заболевания у пациентов с ВСХТБ были использованы валидные опросники. Оценку болевого симптомокомплекса (локализация, частота и интенсивность), дизурических проявлений, а также их влияние на качество жизни и повседневную активность проводили с помощью анкеты суммарной оценки симптомов при ХП (СОС-ХП) [15]. Нарушения половой функции (расстройства либидо, эрекции, их длительность, качество жизни) оценивали по квантификационной шкале сексуальной функции мужчин (СФМ) [16].
Всем пациентам выполнено комплексное антропометрическое обследование с последующим соматотипированием по методу B. Heath–J. Carter. Соматотип устанавливали по наибольшему значению экто-, мезо- или эндоморфий [17].
Биоимпедансометрию проводили с использованием комплекса КМ-АР-01, комплектация «ДИАМАНТ-АИСТ-мини» (ООО «ДИАМАНТ», Россия, Санкт-Петербург). Метод исследования основан на измерении импеданса Z всего тела. Электрический импеданс биологических тканей имеет два компонента: активное R и реактивное сопротивление XC. Материальным субстратом активного сопротивления R в биологическом объекте являются жидкости (клеточная и внеклеточная), обладающие ионным механизмом проводимости. Субстратом реактивного сопротивления XC (диэлектрический компонент импеданса) являются клеточные мембраны [18].
Всем пациентам выполняли общий и биохимический анализы крови, общий анализ мочи, трансректальное ультразвуковое исследование (УЗИ) простаты, исследование отделяемого переднего отдела уретры и секрета простаты на инфекции передаваемые половым путем (ИППП) методом полимеразной цепной реакции на Trichomonas vaginalis, Mycoplasma hominis, Mycoplasma genitalium, Chlamydia trachomatis, Neisseria gonorrhea и Ureaplasma urealyticum, бактериологическое исследование средней порции мочи, постмассажной порции мочи, гормональное исследование крови (общий и свободный тестостерон, глобулин, связывающий половые гормоны [ГСПГ], эстрадиол). Уровень свободного тестостерона определяли с использованием калькулятора на веб-сайте Международного общества по изучению проблем пожилых мужчин ISSAM (референсный диапазон >0,250 нмоль/л), уровень общего тестостерона, эстрадиола и ГСПГ – на автоматическом иммунохемилюминесцентном анализаторе Immulite (Diagnostic Products Corporation, США). Метод детекции – ферментативно усиленная хемилюминесценция.
Статистический анализ проводили с использованием программы StatTech v. 3.0.9 (разработчик – ООО «Статтех», Россия). Количественные показатели оценивали на предмет соответствия нормальному распределению с помощью критерия Шапиро–Уилка (при числе исследуемых менее 50) или критерия Колмогорова–Смирнова (при числе исследуемых более 50). Количественные показатели, имевшие нормальное распределение, описывали с помощью средних арифметических величин (M) и стандартных отклонений (SD), границ 95% доверительного интервала (95% ДИ).
В случае отсутствия нормального распределения количественные данные описывали с помощью медианы (Me), нижнего и верхнего квартилей [Q1; Q3]. Категориальные показатели представляли в виде абсолютных значений и процентных долей. Сравнение групп по количественному показателю, имевшему нормальное распределение, выполняли с помощью однофакторного дисперсионного анализа, апостериорные сравнения проводили с помощью критерия Тьюки (при условии равенства дисперсий). Сравнение групп по количественному показателю, распределение которого отличалось от нормального, выполняли с помощью критерия Краскела–Уоллиса, апостериорные сравнения – с помощью критерия Данна с поправкой Холма. Процентные доли при анализе многопольных таблиц сопряженности выполняли с помощью критерия хи-квадрат Пирсона. Различия считали статистически значимыми при p<0,05.
Результаты. Длительность заболевания составила от 3 мес. до 12 лет, в среднем 2 (0,25;3) года. Среди 150 обследованных по результатам соматотипирования по B. Heath– J. Carter пациентов эктоморфного соматотипа было 40 (26,7%), мезоморфного – 64 (42,7%), эндоморфного – 46 (30,7%). Все группы были сопоставимыми по возрасту (р=0,119).
Анализ половой функции по шкале СФМ показал незначительные нарушения у мужчин мезо- и эктоморфов в отсутствие статистически значимых межгрупповых различий. Пациенты эндоморфы отметили более выраженные сексуальные нарушения (табл. 1).

По результатам анкетирования с использованием шкалы СОС-ХП установлены наиболее частые локализации болевого синдрома (рис. 1). Пациенты эндоморфного соматотипа чаще других жаловались на боли в мочеиспускательном канале (р=0,022) и промежности (р=0,027). При суммарном анализе доменов анкеты выявлено преобладание домена боли, при этом значимых различий между мезоморфами и эктоморфами выявлено не было, эндоморфы характеризовались статистически значимым преобладанием болевого синдрома (р<0,001). Простаторея встречалась редко и по частоте была равномерно распределена среди всех соматотипов.
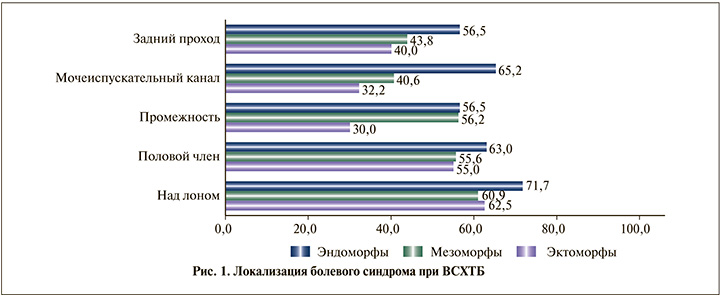
Домен расстройств мочеиспускания был выражен умеренно, соматотипические особенности соответствовали болевому синдрому. При оценке влияния симптомов ВСХТБ на качество жизни наименьшее влияние выявлено у эктоморфов, умеренное – у мезоморфов, выраженное – у эндоморфов. Индекс симптоматики (ИС) представляет собой сумму доменов боли, дизурии и простатореи, клинический индекс (КИ) – это сумма баллов ИС и домена качества жизни. В зависимости от количества баллов КИ ВСХТБ подразделяют на незначительный (0–10 баллов), умеренный (11–25 баллов) или значительный (26–50 баллов). Таким образом, пациенты эндоморфного соматотипа имели значительные проявления ВСХТБ (КИ – 29 [27; 32] баллов), эктоморфы и мезоморфы – умеренные (КИ –18 [15; 20] и 20 [18; 23] баллов соответственно) (табл. 2).

По данным антропометрии наибольшую масса тела и ИМТ имели пациенты-эндоморфы (83 [79; 95] кг и 28 [26; 30] кг/м2), затем располагались мезоморфы (80 [76; 88] кг и 25 [24; 27] кг/м2), наименьшие показатели наблюдались у эктоморфов (73 [65; 77] кг и 22 [20; 24] кг/м2).
Анализ компонентного состава тела выявил соматотипические особенности. При оценке суммарной жировой массы (ЖМ) наименьшее количество абсолютного и относительного жира наблюдалось у эктоморфов – 12 (8; 15) кг и 17 (13; 20)% соответственно, мезоморфы имели средние значения – 17 (14; 21) кг и 21 (19; 24)%, наибольшие показатели регистрировались у эндоморфов – 20 (15; 28) кг и 24 (19; 29)% (pмезоморфы–эктоморфы <0,001, pэндоморфы–эктоморфы <0,001, pэндоморфы–мезоморфы=0,037). Бесжировая масса (БЖМ) – часть массы тела, включающая все, что не является жиром: мышцы, внутренние органы, мозг, нервы, кости и все жидкости, находящиеся в организме. У эндоморфов значение этого показателя составило 66 (64; 68) кг, у мезоморфов – 65 (63; 66) кг, у эктоморфов – 60 (58; 61) кг. Мышцы, нервы, внутренние органы составляют суммарный показатель активной клеточной массы (АКМ). Эндоморфы и мезоморфы имели наибольшие показатели абсолютной АКМ – по 41 [(39; 43) кг, эктоморфы – значительно меньший – 38 (36; 40) кг (p<0,001).
Относительные значения АКМ демонстрировали обратную зависимость: эктоморфы имели наибольший показатель – 54 (51; 55)%, мезоморфы – среднее значение (50 [48; 51]%), наименьшие параметры регистрировали у эндоморфов – 45 (45; 51)%, различия статистически значимы (pмезоморфы–эктоморфы <0,001, pэндоморфы–мезоморфы=0,049).
Баланс жидкостных сред характеризовался наименьшим количеством абсолютных и относительных значений внеклеточной жидкости, наибольшим количеством внутриклеточной жидкости у эктоморфов по сравнению с мезоморфами и эндоморфами (р<0,001). Суммарные данные состава тела представлены на рис. 2.
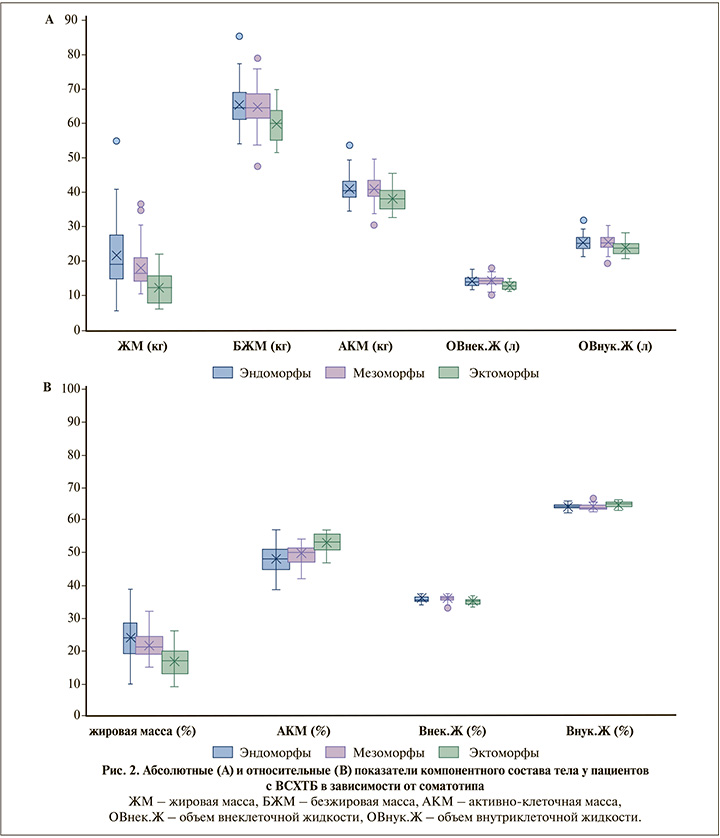
Показатель базового обмена веществ у мезоморфов составил 1888 (1808; 2018) ккал, у эндоморфов –1878 (1796; 2046) ккал, что было статистически значимо больше, чем у эктоморфов – 1752 (1665; 1807) ккал (р<0,001). В то же время уровень обмена веществ на 1 кг массы тела выявил наибольшие показатели у эктоморфов – 24,3±1,1 ккал/кг, промежуточные у мезоморфов 23,2±1,1 ккал/кг, наименьшие у эндоморфов 22,4±1,3 ккал/кг (pэктоморфы–мезоморфы< 0,001, pмезоморфы–эндоморфы=0,002).
При оценке гормонального статуса выявлено статистически значимое снижение уровня ГСПГ, общего и свободного тестостерона у эндоморфов. Содержание эстрадиола у данной группы пациентов было наибольшим. Эктоморфы имели максимальные значения общего и свободного тестостерона. Уровни ГСПГ и эстрадиола между экто- и мезоморфами достоверно не различались (табл. 3).

Показатели средней порции мочи у всех обследованных пациентов были в переделах нормы. При бактериологическом исследовании средней порции и постмассажной мочи роста патогенных микроорганизмов не выявлено. Результаты исследования отделяемого переднего отдела уретры и секрета простаты на ИППП были отрицательными.
Микроскопический анализ секрета простаты выявил статистически значимое повышение уровня лейкоцитов у пациентов эндоморфного соматотипа (pэктоморфы–эндоморфы=0,003, pмезоморфы–эндоморфы <0,001). Уровень лецитиновых зерен был значимо больше у эктоморфов, чем у эндоморфов (pэктоморфы–эндоморфы=0,004), различий с мезоморфами не установлено (рис. 3).
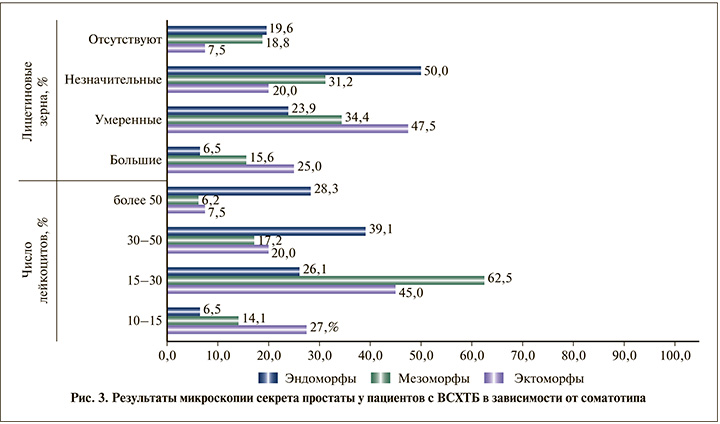

По данным УЗИ простаты наибольшие показатели длины, ширины, высоты и объема органа зарегистрированы у пациентов эндоморфного соматотипа. Эктоморфы имели промежуточное значение длины простаты – 41 (40; 41) мм, остальные параметры имели наименьшие значения. Пациенты мезоморфного соматотипа продемонстрировали средние размеры простаты, за исключением длины, которая была наименьшей среди всех соматотипов (p<0,001).
Обсуждение. Настоящее исследование показало, что вероятность возникновения, особенности клинических проявлений и течение ВСХТБ в зависимости от соматотипа мужчины различаются пациенты-эндоморфы имели наиболее выраженный дисбаланс компонентного состава тела. Выявленное статистически значимое повышение ИМТ, массы жировой ткани, снижение показателей активной клеточной массы сочетаются с увеличенными размерами простаты, более тяжелыми проявлениями ВСХТБ и статистически значимо меньшим уровнем общего и свободного тестостерона.
Данные нарушения могут быть обусловлены синтезом в жировой ткани физиологически активных молекул, в том числе цитокинов, оказывающих провоспалительный эффект, обусловливающих активацию и поддержание окислительного стресса, а также усиление процесса ароматизации [19, 20]. Ранее их роль была подтверждена в патогенезе ХНП/СХТБ категорий II–IV, а также доказана возможность их диагностического и прогностического использования [21]. Современные исследования выявили увеличение риска развития нарушений обмена андрогенов при ожирении, сахарном диабете 2 типа, аденоме простаты в сочетании с хроническим простатитом. Данная закономерность имеет достаточно высокую распространенность при других хронических заболеваниях [22]. Повышение уровня жировой массы коррелировало с повышением уровня свободного эстрадиола и снижением ГСПГ, общего и свободного тестостерона [20, 23]. Анализ работы репродуктивного центра «Международный центр репродуктивной медицины», Санкт-Петербург, проведенный И. А. Корнеевым [24], показал, что среди мужчин, состоявших в бесплодном браке и обратившихся за лечением, преобладали пациенты с избыточной массой тела и ожирением. Пациенты с метаболическими проблемами имеют системные изменения в кровоснабжении и иннервации органов, в том числе мочевого пузыря и простаты, которые могут вызывать симптомы нижних мочевыводящих путей [25]. Избыточное содержание жировой ткани ассоциировано с увеличением содержания в кровяном русле ионов натрия, альдостерона и инсулина, что обусловливает жесткость эндотелиальной коры, нарушение синтеза оксида азота и последующее развитие сосудистого фиброза за счет избыточной активации ионных каналов. Это впоследствии приводит к возникновению эректильной дисфункции органического генеза [26–28]. Более того, хроническое воспаление и дисбаланс половых гормонов, связанные с ожирением, могут создавать пролиферативную микротканевую среду, способную спровоцировать развитие рака простаты в будущем [29, 30].
Опираясь на данные литературы и собственные результаты, можно говорить о том, что установленные изменения компонентного состава тела и гормонального статуса могут способствовать поддержанию хронического воспаления в простате, ишемии, нарушению внутритканевого обмена веществ, рецидивирующему течению ВСХТБ, что значимо снижает качество жизни пациента и, вероятнее всего, увеличивает риск воспаления простаты с возрастом.
Заключение. Таким образом, нами выявлены особенности клинико-лабораторных и инструментальных изменений, а также компонентного состава тела пациентов первого периода зрелого возраста с ВСХТБ в зависимости от телосложения. Наиболее тяжелые клинические и лабораторные проявления ВСХТБ наблюдаются у пациентов эндоморфного соматотипа. С учетом выявленных закономерностей дисбаланса компонентного состава тела у мужчин биоимпедансометрия с успехом может применяться как перспективный метод в комплексной оценке статуса пациента с ВСХТБ для мониторинга течения заболевания и назначения рациональной терапии.



