В ХХI веке сердечно-сосудистые заболевания (ССЗ) по-прежнему сохраняют лидирующие позиции среди причин смертности населения во многих экономически развитых странах. Аналогичная тенденция прослеживается и в Российской Федерации, где в 55% случаев летальный исход обусловлен ССЗ. Согласно статистике последних лет, в структуре смертности от ССЗ в нашей стране на долю ишемической болезни сердца (ИБС) приходится 46,8% случаев [1].
Во многих крупных исследованиях доказана связь между ишемией миокарда и стенозирующим атеросклеротическим поражением коронарных артерий (КА), причем степень его выраженности определяет тяжесть течения ИБС и ее прогноз. На протяжении более 50 лет в поле зрения кардиологов все чаще попадают пациенты, у которых имеются классические ангинозные боли, положительные нагрузочные тесты, но при этом отсутствует атеросклеротическое поражение КА, по данным коронарографии (КГ). Следовательно, врач должен найти ответы на следующие вопросы: чем обусловлены загрудинные боли, действительно ли у больного имеется ИБС и какова должна быть тактика его ведения?
В 1973 г. Н. Kemp, описывая таких пациентов, использовал термин «кардиальный синдром Х» [2]. В последующем, основываясь на данных о том, что патологический процесс обусловлен структурными и функциональными изменениями коронарных микрососудов, S. Epstein и R.O. Cannon в 1988 г. первыми ввели понятие «микроваскулярная стенокардия» (МВС) [3].
В настоящее время классическое определение МВС включает триаду следующих признаков: типичные ангинозные боли, положительный тест с физической нагрузкой, подтверждающий ишемический генез болевого синдрома, и интактные КА, по данным КГ [4]. Некоторые авторы считают, что необходимо введение еще одного обязательного критерия для постановки диагноза МВС: наличие доказанной дисфункции коронарных микрососудов [3].
Эпидемиология МВС. По результатам многочисленных исследований, среди пациентов, которым выполнена КГ, существенную долю составляют лица с интактными КА. Согласно данным регистра CASS, из 25 тыс. обследованных пациентов у 50% имелись неизмененные КА: у 39% женщин и 11% мужчин соответственно [5].
Необходимо отметить, что в одном из крупнейших американских регистров NCDR (National Cardiovascular Data Registry, 375 886 больных ИБС, 2000—2002 гг.) прослеживается аналогичная тенденция: необструктивные поражения артерий сердца преобладают у женщин (51%), тогда как у мужчин их частота составляет лишь 32 % [6].
Более высокая заболеваемость МВС среди женщин также подтверждена в ходе исследования WISE (Women’s Ischemia Syndrome Evaluation), в котором у 62% пациенток при КГ не выявлено стенозирующего поражения КА [7].
Хотя у больных МВС отсутствуют значимые поражения КА, обследование и лечение таких больных сопряжены со значительными экономическими затратами. Например, в США ассигнования на ведение таких пациентов достигают 280 млн долларов в год. По данным исследования WISE, расходы на больных МВС могут иногда даже превышать таковые для лиц, страдающих ИБС, что обусловлено необходимостью частых госпитализаций (каждая пятая женщина в течение года была госпитализирована повторно с симптомами стенокардии), проведения углубленного обследования и сложностями подбора адекватной терапии. Предполагаемые суммарные затраты на одну женщину с МВС в течение жизни могут составить 767 288 долларов США, при однососудистом поражении КА — 1 001 000, при двухсосудистом — 1 051 000, при трехсосудистом — 1 009 000 долларов[3].
Этиология и патогенез МВС. Несмотря на возможности и достижения современной медицины, вопросы этиологии и патогенеза МВС остаются неясными и нуждаются в дальнейшем изучении. Полагают, что традиционные факторы риска (ФР) развития ИБС (курение, дислипидемия, гипертоническая болезнь — ГБ, ожирение) могут способствовать развитию МВС.
Установлено, что курение негативно действует на сосудистую стенку [8], у курящих лиц имеется дисфункция эндотелия (ДЭ) как на уровне крупных сосудов [9, 10], так и микроциркуляторного русла (МЦР), в том числе сердца. У здоровых курильщиков резерв коронарного кровотока (РКК) снижен на 21% по сравнению с некурящими, что свидетельствует о развитии дисфункции коронарных микрососудов [11].

Снижение РКК отмечается также у лиц с дислипидемией, у которых еще нет атеросклеротического поражения КА и классических приступов стенокардии [12, 13]. P.A. Kaufmann и соавт. показали, что чем выше уровень общего холестерина, тем ниже РКК, который может восстанавливаться на фоне гиполипидемической терапии [14].
Среди женщин, больных МВС, чаще, чем у здоровых того же возраста, встречается метаболический синдром (30 и 8% соответственно) [3], инсулинорезистентность [15—17] и гиперинсулинемия. По данным S.T. Jadhav, у пациенток с МВС индекс массы тела в среднем выше (28,6 кг/м2 против 25,1 кг/м2) [18].
Недавно проведенные исследования продемонстрировали наличие дисфункции МЦР у молодых больных (42±7 лет) с неосложненным сахарным диабетом (СД) [19]. Необходимо отметить, что самостоятельный вклад гипергликемии в развитие МВС оценить сложно, поскольку СД часто сочетается с другими ФР развития ССЗ (ожирение, дислипидемия, ГБ), которые негативно влияют на функцию эндотелия коронарных микрососудов.
К возможным ФР МВС относят негроидную расу, дефицит эстрогенов и гистерэктомию. По данным регистра NCDR, среди больных МВС в США преобладают представители негроидной расы (59%), тогда как среди испанцев их доля составляет 53%, белых — 50%, азиатов — 47% и коренных американцев — 45% [6].
В регистре CASS число афроамериканцев, страдающих МВС, составило 67% [20]. Однако, по данным других исследований, эта патология встречалось одинаково часто среди лиц негроидной и европеоидной рас [21].
Первые предположения о значимости дефицита эстрогенов и гистерэктомии в развитии МВС высказаны на основании результатов исследования G.M. Rosano и соавт., в которое вошли 107 женщин. У большинства пациенток заболевание дебютировало в период постменопаузы (66%), а у 34% — в период пременопаузы. Оказалось, что симптомы предменопаузы, связанные со снижением уровня эстрогенов (приливы, мигрень, нарушения сна), часто сопровождались эпизодами загрудинной боли. При изучении анамнестических данных обращало на себя внимание, что у больных МВС в 4 раза чаще выполнялась гистерэктомия, чем у здоровых женщин аналогичного возраста. У большинства пациенток клинические признаки болезни появились вскоре после удаления матки [22]. Аналогичная тенденция прослеживается и в исследовании WISE, в котором показано, что пациентки с МВС достоверно чаще имели гистерэктомию в анамнезе, чем больные ИБС со стенозирующим поражением КА [7].
В настоящее время имеются две альтернативные теории патогенеза развития МВС: ишемическая и неишемическая. Сторонники ишемической теории считают, что развитие заболевания происходит вследствие функциональных и структурных изменений коронарных микрососудов, которые появляются вследствие воздействия описанных ФР (курение, дислипидемия, ожирение и т.д.).
P.G. Camici и F. Crea [23] систематизировали все изменения коронарных микрососудов и обусловливающие их основные этиологические факторы (табл. 1).
Эти же авторы в 2007 г. объединили функциональные нарушения микрососудов у больных МВС в так называемую дисфункцию коронарных микрососудов (ДКМ) и выделили 4 ее типа: [23]:
1) ДКМ в отсутствие стенозирующего атеросклероза КА и болезней миокарда — функциональные нарушения микрососудов, которые возникают при воздействии ФР развития ССЗ (курение, АГ, дислипидемия, СД и инсулинорезистентность). В основе функциональных изменений лежит ДЭ;
2) ДКМ при наличии заболеваний миокарда (гипертрофическая и дилатационная кардиомиопатия, «гипертоническое сердце», патология клапанного аппарата сердца) характеризуется ремоделированием интрамуральных коронарных артериол и может быть достаточной для развития ишемии миокарда;
3) ДКМ при наличии стенозов КА (стабильная стенокардия, острый коронарный синдром). Считают, что в данном случае дисфункция микрососудов носит вторичный характер, когда из-за атеросклеротической обструкции КА в результате ишемии и последующей реперфузии миокарда происходит поражение МЦР с развитием дисфункции капилляров. Ранее показано, что у больных ИБС наряду с атеросклерозом КА имеются нарушения на уровне МЦР сердца [24]. Полагают, что данные изменения могут играть важную роль в прогрессировании ИБС [23];
4) ятрогенная ДКМ (вызванная реваскуляризацией). Ятрогенная ДКМ может быть вызвана вазоконстрикцией или эмболией дистальных микрососудов, которые возникают у больных после реваскуляризации. Показано, что у пациентов после реваскуляризации РКК снижен и восстанавливается самостоятельно спустя несколько недель [23].
Таким образом, в основе развития МВС лежит ДКМ, и если мы говорим о МВС в классическом ее понимании, то, вероятно, у таких пациентов имеется первый тип ДКМ, при котором отсутствуют стенозирующий атеросклероз КА и болезни миокарда. Вследствие дисфункции коронарных микрососудов миокард подвергается повторным эпизодам ишемии в зонах поражения МЦР, что приводит к дефициту кровоснабжения и появлению ангинозной симптоматики.
Необходимо отметить, что с развитием ДЭ патологический процесс в сосудистой стенке продолжает прогрессировать. Длительная гиперактивация вазоконстрикторных и проагрегантных систем, факторов роста и пролиферации, провоспалительных цитокинов способствуют апоптозу клеток эндотелия, кардиомиоцитов, гладких мышечных клеток (ГМК) [25].Это приводит к развитию гипертрофии и гиперплазии оставшихся ГМК, дезорганизации клеточных элементов, активации синтеза соединительнотканного матрикса в стенке сосуда, нарушению соотношения коллаген/эластин и утолщению медии артерий [25, 26]. Данные процессы являются основой ремоделирования сосудистой стенки на всех уровнях сосудистого русла [27]. Установлено, что структурные изменения коронарных микрососудов у больных МВС представлены преимущественно гипертрофией гладкомышечного слоя артериол [28, 29].
 Согласно альтернативной неишемической теории развития МВС основное значение придается нарушению болевой чувствительности. Показано, что у больных МВС снижен порог болевой чувствительности к электрическим и термическим раздражителям, воздействующим на кожу [30]. Кроме того, у пациентов с МВС отсутствует привыкание к повторным ноцицептивным раздражителям. В пользу данной теории также свидетельствует более частое развитие МВС у женщин в период постменопаузы, когда вследствие дефицита эстрогенов, оказывающих анальгезирующее действие через µ-опиодную систему, снижается порог болевой чувствительности [25].
Согласно альтернативной неишемической теории развития МВС основное значение придается нарушению болевой чувствительности. Показано, что у больных МВС снижен порог болевой чувствительности к электрическим и термическим раздражителям, воздействующим на кожу [30]. Кроме того, у пациентов с МВС отсутствует привыкание к повторным ноцицептивным раздражителям. В пользу данной теории также свидетельствует более частое развитие МВС у женщин в период постменопаузы, когда вследствие дефицита эстрогенов, оказывающих анальгезирующее действие через µ-опиодную систему, снижается порог болевой чувствительности [25].
Клинические формы МВС. В 2008 г. G.А. Lanza и F. Crea предложили выделить первичную и вторичную формы МВС. При первичной МВС отсутствует патология миокарда [23, 31, 32], при вторичной у больных имеется предшествующее заболевание сердца. Первичную МВС также разделяют на острую и хроническую.
Хроническая МВС — это стабильная МВС напряжения, как правило, возникающая при физических нагрузках, тогда как острая МВС — это нестабильная форма, которая клинически может протекать как острый коронарный синдром [33].
Диагностика нарушений коронарной микроциркуляции. Для постановки диагноза МВС необходимо сочетание следующих признаков: типичные ангинозные боли, положительный тест с физической нагрузкой и интактные КА, по данным КГ.
Необходимо помнить, что причинами кардиалгий могут быть не только болезни сердца и КА, но и патология других органов и систем. Следовательно, диагноз МВС может быть установлен только после исключения экстракардиальных причин кардиалгий, к которым относят поражение органов грудной клетки, желудочно-кишечного тракта, костно-мышечной системы, нервно-психические нарушения.
Ряд авторов считают, что для постановки диагноза МВС необходимо доказать наличие дисфункции коронарных микрососудов [3, 34]. Однако выявление ДКМ представляет собой непростую задачу, поскольку в настоящее время не существует методов, позволяющих визуализировать микрососуды сердца у человека in vivo. Имеющиеся в распоряжении врачей методы позволяют лишь косвенно оценить состояние коронарной микроциркуляции на основании определения суррогатных маркеров, к которым относятся параметры, отражающие состояние коронарного и миокардиального кровотока.
Коронарный кровоток характеризуется количеством крови, проходящей через коронарный сосуд за единицу времени. Данный параметр может быть оценен при помощи инвазивных и неинвазивных методов [35—40]. К инвазивным методам относят внутрисосудистое ультразвуковое исследование КА с допплерографией Данное исследование позволяет оценить среднюю и максимальную скорость кровотока в коронарных сосудах, что при наличии данных о ширине просвета КА (полученных в ходе КГ) позволяет рассчитать объемный коронарный кровоток. Миокардиальный кровоток — эта параметр, позволяющий оценивать кровоток на единицу массы ткани (мл/мин/г). Для его определения необходимо проведение позитронной эмиссионной томографии (ПЭТ), магнитной резонансной томографии (МРТ) или компьютерной томографии (КТ) сердца с контрастированием КА [41—42].
Судить о функциональном состоянии коронарных микрососудов при оценке коронарного или миокардиального кровотока возможно только в ходе проведения тестов на вазореактивность (внутривенное введение аденозина или дипиридомола).
Параметр, характеризующий вазореактивность, — РКК, который определяется как отношение коронарного кровотока после пробы к исходному кровотоку (в покое). Прирост РКК менее чем в 2 раза считается сниженным [23]. К неинвазивным методам оценки резерва коронарного кровотока относят трансторакальную допплер-эхокардиографию [40].
Основным недостатком перечисленных методов оценки дисфункции коронарных микрососудов является невозможность оценки РКК при наличии гемодинамически значимого стеноза КА [43—45]. Другими недостатками, приводящими к существенному ограничению применения способов в повседневной клинической практике, являются высокая стоимость оборудования, а также возможность развития тяжелых сердечно-сосудистых осложнений (ССО) в ходе проведения проб на вазореактивность.
В 1987 г. F. Sax и соавт. показали, что нарушения функции эндотелия микрососудов кожи у больных МВС коррелирует с таковыми в миокарде [46]. Это дало основание рассматривать ДЭ как системный процесс и послужило основой для разработки методов неинвазивной оценки дисфункции эндотелия сосудистого русла в доступных сосудистых ложах.
В настоящее время для оценки вазореактивности МЦР на периферии используют методы венооклюзионной плетизмографии (ВОП), лазерной допплерфлоуметрии (ЛДФ), фотоплетизмографии (ФПГ), периферической апплантационной тонометрии (ПАТ), которые выполняются на фоне окклюзионной пробы и фармакологических тестов с эндотелийзависимыми и эндотелийнезависимыми вазодилататорами.
ВОП — малоинвазивный метод, основанный оценке изменения кровотока в микрососудах предплечья после пробы с реактивной гиперемией. Метод позволяет определить функциональное состояние МЦР вне зависимости от влияния системных механизмов регуляции. Воспроизводимость ВОП относительно высока. Коэффициент вариации, по разным данным, составляет от 11 до 25% [47]. Однако инвазивность метода ограничивает его применение в крупных исследованиях. C помощью данного метода определена ДЭ у здоровых лиц с ФР развития CCЗ [48], больных ГБ [49], ИБС [50] и СД 2-го типа и выявлена корреляция показателей, характеризующих ДЭ на уровне периферических сосудов МЦР, с таковыми на уровне коронарных микрососудов при МВС [46].
ЛДФ основана на оптическом зондировании тканей монохроматическим сигналом и анализе его частотного спектра, отраженного от движущихся эритроцитов. ЛДФ позволяет выявить вклад различных механизмов, влияющих на вазореактивность (эндотелиальный, миогенный, нейрогенный, дыхательный). ДЭ сосудов МЦР кожи определяется в ходе проб с ионофорезом эндотелийзависимых (ацетилхолин) и эндотелийнезависимых (нитропруссид натрия) вазодилататоров кожи. Метод прост в применении, недорогой, широко применяется в исследованиях, в том числе для оценки ДЭ у здоровых лиц с ФР, больных СД 2-го типа [51–53].
В основе ПАТ лежит регистрация пульсового объема кровотока при помощи двухканального плетизмографа. Датчики регистрируют амплитуду пульсовой волны в состоянии покоя и после пробы с реактивной гиперемией. Функция эндотелия оценивается по приросту амплитуды пульсовой волны после пробы и выражается через параметр reactive hyperemia ratio (RH ratio) — отношение амплитуды пульсового объема кровотока после пробы к исходной амплитуде (в состоянии покоя). Снижение данного индекса менее 1,8 свидетельствует о наличии ДЭ. Снижение RH ratio у пациентов с ИБС коррелировало с ДЭ на уровне КА. При этом отмечено, что RH ratio менее 1,35 обладает 80% чувствительностью и 85% специфичностью в отношении диагностики ДЭ КА [24].
Методика запатентована как Endo PAT 2000 (EndoPAT; ItamarMedical, Caesarea, Israel) и одобрена Управлением США по контролю за качеством пищевых продуктов, лекарственных препаратов (FDA) для неинвазивной оценки ДЭ коронарных сосудов у пациентов с ИБС [54]. Метод отличается высокой точностью оценки ДЭ, воспроизводимостью, независим от оператора и не требует высокой квалификации исследователя, что дает возможность использовать его в крупных исследованиях.
Метод ФПГ также основан на регистрации амплитуды пульсового объема кровотока на уровне сосудов МЦР с помощью оптопары. Фотоплетизмографический сигнал регистрируется в покое и после пробы с реактивной гиперемией (окклюзионная проба). Функция эндотелия оценивается по приросту амплитуды пульсового объема кровотока, который определяется на основании параметра, именуемого «индекс окклюзии» (отношение амплитуды пульсового объема кровотока после пробы к исходной амплитуде в состоянии покоя).
 Оценка ДЭ при помощи приведенных методов может дать дополнительную информацию о функции эндотелия сосудов в организме человека и может быть рассмотрена в качестве дополнительного диагностического критерия МВС у пациентов, имеющих основные признаки заболевания.
Оценка ДЭ при помощи приведенных методов может дать дополнительную информацию о функции эндотелия сосудов в организме человека и может быть рассмотрена в качестве дополнительного диагностического критерия МВС у пациентов, имеющих основные признаки заболевания.
В последнее время появляются сообщения об изменениях капиллярного русла у больных сердечно- сосудистыми заболеваниями [55–57]. T.N. Antonios и соавт. с помощью компьютерной видеокапилляроскопии кожи пальца кисти выявили структурные нарушения капиллярной сети (снижение плотности капиллярной сети в покое, структурное капиллярное разряжение), которые не зависели от уровня артериального давления [58]. Однако для определения патогенетической и клинической значимости выявленных изменений капиллярной сети кожи требуется проведение дальнейших исследований у больных МВС.
В 2013 г. впервые в европейские рекомендации по ведению больных стабильными формами ИБС [59] включен раздел, посвященный МВС. Для верификации диагноза МВС в алгоритм обследования необходимо включить стресс-ЭхоКГ для выявления участков гипокинеза миокарда, трансторакальную или интракоронарную допплер-ЭхоКГ с фармакологическими пробами (аденозин, добутамин) для оценки РКК (табл. 2).
Лечение больных МВС. В связи с тем что в настоящее время механизмы МВС до конца неясны и не проводилось крупных рандомизированных исследований, оценивающих эффективность терапии, выбор оптимального лечения таких больных представляет собой сложную задачу. Очевидно, что при ведении таких больных врачу необходимо ориентироваться на достижение следующих целей: купирование болевого синдрома, профилактика прогрессирования заболевания, улучшение качества жизни пациента, снижение числа госпитализаций и предупреждение ССО.
Так как традиционные ФР играют важную роль [60] в развитии заболевания, в первую очередь необходимо проводить мероприятия, направленные на их выявление и коррекцию. Доказана эффективность дозированных физических нагрузок, которые снижали частоту ангинозных приступов [61]. Пациентам, страдающим МВС и имеющим дислипидемию, необходимо проводить лечение статинами (аторвастатин, розувастатин) [62]. Последние, помимо своего гиполипидемического действия, способны нормализовать функцию эндотелия за счет плейотропных эффектов (противовоспалительного и антиоксидантного) [63].
Для купирования и предупреждения прогрессирования симптомов заболевания больным МВС необходимо проводить антиишемическую терапию. Результаты клинических исследований антиангинальных препаратов противоречивы, однако в большинстве из них показана высокая эффективность β-адреноблокаторов. Полагают, что позитивное влияние β-адреноблокаторов обусловлено как их отрицательным хронотропным эффектом, так и положительным действием на функцию эндотелия [64—66].
R. Bugiardini и соавт. в ходе двойного слепого перекрестного исследования установили, что лечение β-адреноблокаторами (пропроналолом) в отличие от верапамила, в течение 7 дней достоверно снижает число эпизодов ишемии (депрессия сегмента ST, по данным суточного мониторирования электрокардиограмм) у больных МВС [66]. G. Fragasso и соавт. продемонстрировали, что терапия атенололом снижает частоту ангинозных приступов, эпизодов ишемии, по данным нагрузочных тестов (тредмил-тест) [65]. В другом небольшом двойном слепом исследовании (10 больных МВС) при сравнении антиишемического действия атенолола, амлодипина и изосорбида 5-динитрата оказалось, что терапия атенололом и амлодипином в течение 4 нед снижает число приступов стенокардии, при этом антиишемическое действие атенолола было достоверно выше, чем у амлодипина, в то время как нитраты такого действия не оказывали [64].
Необходимо обратить внимание, что ответ на терапию β-адреноблокаторами (уменьшение числа эпизодов ангинозных болей) варьируется в широких пределах (19—60%) [67], поэтому при лечении МВС часто возникает необходимость прибегать к комбинированной терапии, препаратами выбора при этом являются антагонисты кальция и нитраты.
Полагают, что не все β-адреноблокаторы могут быть одинаково эффективными при МВС. Среди прочих значительные преимущества может иметь высокоселективный β1-адреноблокатор небиволол, поскольку хорошо известно положительное действие препарата на функцию эндотелия за счет увеличения синтеза оксида азота. М. Togni оценил влияние небиволола на эндотелийзависимую функцию коронарных микрососудов (РКК). Препарат вводился интракоронарно больным ИБС, после чего отмечалось улучшение функции коронарных микрососудов (прирост РКК) [68]. В исследовании, выполненном в 2010 г. группой ученых из Турции, показано, что терапия небивололом в дозе 5 мг/сут в течение 4 нед способствует улучшению функции эндотелия крупных периферических сосудов [69]. N. Sen и соавт. в рандомизированном контролируемом исследовании изучали влияние небиволола на функцию эндотелия коронарных сосудов и оценивали число эпизодов нагрузочной ишемии у больных МВС, а также определяли плазменные уровни метаболитов оксида азота, L-аргинина и асимметричного диметиларгинина. Больные МВС (n=38) были разделены на две равные группы, одна из которых получала небиволол (5 мг), другая группа — метопролол (50 мг) в течение 12 нед. Лечение небивололом в отличие от метопролола ассоциировалось с улучшением функции эндотелия и снижением числа эпизодов ишемии в ходе нагрузочных тестов [70]. Таким образом, в настоящее время β-адреноблокаторы рекомендуется использовать как препараты первой линии в лечении МВС [59, 71].
Результаты клинических исследований по оценке эффективности терапии БКК у больных МВС неоднозначны.
В одних исследованиях выявлен их положительный антиишемический эффект [72], в других такой эффект отсутствовал [73]. R.O. Cannon и соавт. провели двойное слепое рандомизированное плацебо-контролируемое исследование, в котором 26 пациентов с МВС получали терапию верапамилом или нифедипином в течение 1 мес. В обеих группах отмечали уменьшение числа эпизодов загрудинной боли, повышение толерантности к физической нагрузке [72]. Однако, по данным G.A. Lanza и соавт., амлодипин оказался неэффективен в качестве монотерапии у больных МВС [64].
Имеющиеся данные о действии нитратов также противоречивы. В исследовании J.C. Kaski показано, что эффективность сублингвальных форм нитратов составила у больных МВС лишь 42% [67]. Другие авторы сообщали об отрицательном эффекте нитратов (изосорбид динитрат) у больных МВС, который проявлялся снижением толерантности к физической нагрузке [74]. Сублингвальные нитраты могут быть использованы для купирования ангинозных болей, в то время как применение пролонгированных форм (изосорбида-5-мононитрат) для предупреждения симптомов малоэффективно. Нитраты не рекомендуют использовать как препараты выбора, лучше комбинировать их с другими лекарственными средствами, в первую очередь с β-адреноблокаторами [64].
Ранее сообщалось о положительном влиянии ингибиторов ангиотензинпревращающего фермента (АПФ) на функцию эндотелия микрососудов. В небольшом плацебо-контролируемом исследовании было показано повышение толерантности к физической нагрузке в ходе проведения тредмил-теста на фоне терапии каптоприлом у больных МВС [75] и эналаприлом у больных МВС [76]. Полагают, что положительный эффект ингибиторов АПФ связан с увеличением уровня L-аргинина и снижением уровня ингибиторов NO (АДМА).
В пользу этого предположения свидетельствуют данные о приросте РКК у пациентов, получающих эналаприл [77].
Необходимо отметить, что не удалось достичь аналогичного эффекта при использовании блокатора рецепторов ангиотензина II ирбесартана [78]. В 2010 г. опубликованы результаты двойного слепого плацебо-контролируемого рандомизированного исследования, в которое были включены 20 женщин с МВС, получавшие терапию ранолазином в течение 28 дней. Препарат дал хороший антиишемический эффект: у больных снизилось число приступов стенокардии, повысилась толерантность к физической нагрузке, улучшилось качество жизни, кроме того, отмечался прирост РКК [79]. Ранолазин является относительно новым антиангинальным препаратом, который одобрен FDA для лечения стабильной стенокардии. Действие препарата основано на селективном ингибировании позднего натриевого потока, что способствует снижению индуцированной ишемией перегрузки клетки натрием и кальцием и улучшает перфузию, а также функциональные возможности миокарда. Уникальность ранолозина заключается в том, что он оказывает антиангинальное действие, не влияя на системную гемодинамику [80].
В апреле 2013 г. проведено сравнительное исследование по изучению антиишемической эффективности терапии раналозином (375 мг/сут) или ивабрадином (10 мг/сут) у больных МВС (n=46), у которых, несмотря на стандартную антиангинальную терапию, сохранялись боли за грудиной. Оказалось, что оба препарата оказывали положительный эффект (снижение числа болевых эпизодов, повышение толерантности к физической нагрузке, качества жизни) по сравнению с плацебо. При этом эффект ранолозина был достоверно выше, чем ивабрадина (опросник The Seattle Angina Questionnaire).Однако оба препарата не оказали существенного влияния на функцию коронарных микрососудов (отсутствовал прирост РКК). Результаты проведенного исследования позволили сделать заключение, что ранолозин и ивабрадин могут быть использованы в лечении пациентов МВС, у которых не удается достичь контроля симптомов на фоне адекватной антиишемической терапии [59, 81].
Перспективным в лечении рефрактерного к медикаментозной терапии болевого синдрома у пациентов с МВС является метод усиленной наружной контрпульсации (УНКП). Метод основан на последовательном нагнетании воздуха в манжеты, наложенные вокруг нижних конечностей пациента. Каждая манжета разделена на 3 секции, облегающие икры, нижнюю треть бедра и верхнюю треть бедра, в которые во время диастолы нагнетается воздух в быстрой последовательности от икр вверх. Это приводит к увеличению диастолического давления, коронарного перфузионного давления и усилению кровоснабжения миокарда. Поздними эффектами УНКП являются увеличение венозного возврата и усиление сердечного выброса. Все это ведет к увеличению доставки кислорода к миокарду. Увеличение давления в диастолу приводит к открытию и формированию коллатералей и усилению кровоснабжения гипоперфузируемого участка. K.D. Kronhaus и соавт. при проведении курсов УНКП 30 больным МВС продемонстрировали положительное воздействие данной терапии не только на ангинозную симптоматику, но и на функцию коронарных микрососудов [82].
Принимая во внимание роль гормонального дисбаланса в развитии МВС, а также корригирующее влияние эстрогенов на болевую чувствительность и ДЭ, можно предположить, что заместительная гормональная терапия (ЗГТ) будет эффективна в лечении заболевания. В перекрестном исследовании 25 больных МВС в постменопаузе принимали 17β-эстрадиол или плацебо в течение 4 нед. Снижение числа болевых эпизодов отмечалось у пациенток, находившихся на терапии эстрогенами [83]. В другом исследовании показано умеренное снижение болевых эпизодов и рост РКК [84] на фоне лечения комбинированным гормональным препаратом дроспиреноном (17β-эстрадиол+прогестин). Однако хорошо известно, что ЗГТ может приводить к развитию тяжелых осложнений ССЗ. До настоящего времени не проводили крупных рандомизированных клинических исследований, позволяющих оценить эффективность и безопасность данной терапии у больных МВС. Таким образом, ЗГТ может быть использована для лечения заболевания у женщин в постменопаузе, однако необходима профилактика развития ССО [3, 59].
У многих пациентов с МВС имеется инсулинорезистентность [85], которая потенцирует развитие ДЭ коронарных микрососудов и как следствие — ишемию миокарда. В рандомизированном плацебо-контролируемом исследовании показано, что метформин положительно влияет на функцию коронарных микрососудов у женщин с МВС и метаболическим синдромом (без СД) [86].
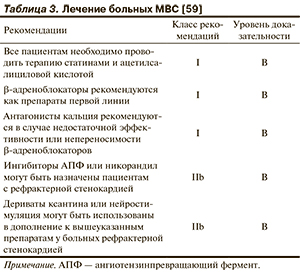
Все имеющиеся данные о лечении больных МВС проанализированы в последних европейских рекомендациях по ведению больных со стабильными формами ИБС (2013) [59] (табл. 3). Начинать терапию у больных МВС следует с β-адреноблокаторов, а при ее неэффективности — комбинировать с нитратами и антагонистами кальция, которые являются препаратами второй линии. Ингибиторы АПФ или никорандил целесообразно назначать больным рефрактерной стенокардией, особенно при сочетании с ГБ и СД. В отсутствие эффекта комбинаций препаратов первой и второй линий рекомендуется дополнительно назначать ранолазин или ивабрадин. В качестве средства дополнительной терапии можно рассматривать метформин у пациентов с нарушением толерантности к глюкозе [3]. В случае рефрактерности к терапии рекомендуют использовать УНКП, дериваты ксантина и нейростимуляцию (см. табл. 3).
Прогноз. До недавнего времени прогноз МВС считался благоприятным, что было подтверждено рядом небольших исследований случай-контроль, которые выполнялись, начиная с 60-х гг. XX века [87, 88]. Эти работы свидетельствовали о том, что МВС не вносит дополнительный риск в развитие инфаркта миокарда (ИМ) или рост летальности от ССЗ. Следует отметить, что эти исследования имели малую выборку, а срок наблюдения за пациентами был коротким, что снижает достоверность полученных данных при распространении их на всю популяцию больных МВС [2, 87, 88].
Результаты последних исследований изменили взгляд на роль МВС в развитии ССО. R. Bugiardini и соавт. установили, что при МВС ежегодный риск развития ССО (смерть, нефатальный ИМ, нефатальный инсульт и хроническая сердечная недостаточность) составляет 2,5% [60]. Кроме того, в течение десятилетнего наблюдения за женщинами с МВС у 30% из них впоследствии развился атеросклероз КА [89].
В ходе другого 15-летнего исследования, в которое были включены 40 пациентов с интактными артериями сердца и доказанным поражением микрососудистого русла (по данным биопсии эндомиокарда), ИМ развился у 7,5%, мозговой инсульт — у 10%, стойкие нарушения ритма сердца — у 15,45%, внезапная сердечная смерть — у 17,5%. Признаки коронарного атеросклероза разной степени тяжести выявлены у 17,5% обследованных пациентов. При этом у 82,5% пациентов КА оставались интактными, но имелся атеросклероз периферических артерий [29].
Согласно результатам исследования WISE, пациентки с МВС, у которых диагностировали дисфункцию коронарных микрососудов, имели худший прогноз заболевания (нефатальный ИМ и инсульт, декомпенсацию хронической сердечной недостаточности) [90]. Аналогичные данные получены в ранее выполненном исследовании M. Bottcher [91, 92].
Таким образом, очевидно, что МВС не является доброкачественным заболеванием и вносит существенный вклад в развитие нефатальных и фатальных ССО. Следовательно, ранняя диагностика, выявление ФР и признаков прогрессирования заболевания, оптимальная терапия и профилактика осложнений данной патологии представляются чрезвычайно важной задачей [93—96].



