1) ФГАOУ ВО «Белгородский государственный национальный исследовательский университет», Белгород, Россия;
2) ФГAOУ ВО «Российский университет дружбы нарoдoв», Москва, Россия
Актуальность: Внутренний генитальный эндометриоз – часто встречающееся заболевание женской репродуктивной системы, которое выявляется у 15–45% женщин. Одним из важных аспектов патогенеза внутреннего генитального эндометриоза является нарушение апоптоза и иммунных процессов, в основе которых лежит дисбаланс факторов роста (VEGF, EGF, ТGFβ1, IGF1, FGFR2). Полиморфизм генов факторов роста может влиять на их экспрессию и вследствие этого иметь важное значение в патофизиологии внутреннего генитального эндометриоза.
Цель: Оценить вовлеченность полиморфных локусов генов факторов роста в формирование внутреннего генитального эндометриоза.
Материалы и методы: В исследование были включены 102 пациентки с внутренним генитальным эндометриозом и 778 женщин группы контроля. Для исследования отобраны 5 полиморфных локусов генов факторов роста: rs4444903 EGF c.-382А>G, rs6214 IGF1 c.*2716G>А, rs2981582 FGFR2 c.109+906Т>С, rs833061 VEGF c.-958С>Т, rs1800469 ТGFb1 c.-1347 Т>С . Анализ выполняли с помощью метода полимеразной цепной реакции в реальном времени. Для оценки межлокусных взаимодействий использовали программу АРSampler (https://sourceforge.net/projects/apsampler/).
Результаты: В результате проведенного исследования установлено, что факторами риска формирования внутреннего генитального эндометриоза следует считать генотип GG IGF1 rs6214 (ОШ=2,64; p=0,01), а также сочетание полиморфных вариантов G rs6214 IGF1, С rs1800469 ТGFb1, А rs4444903 EGF и Т rs833061 VEGF (ОШ=1,88; pperm=0,0021) и аллелей G rs6214 IGF1, С rs1800469 ТGFb1, Т rs833061 VEGF и С rs2981582 FGFR2 (ОШ=1,71; pperm=0,003).
Заключение: Сочетания генов rs4444903 EGF, rs6214 IGF1, rs2981582 FGFR2, rs833061 VEGF,
rs1800469 ТGFb1 ассоциированы с формированием внутреннего генитального эндометриоза. Результаты исследования свидетельствуют о важности межлокусных взаимодействий генов факторов роста в формировании внутреннего генитального эндометриоза. В перспективе полученные данные могут быть использованы в практической медицине.
Вклад авторов: Чурносов М.И., Алтухова О.Б., Радзинский В.Е. – концепция и дизайн исследования; Алтухова О.Б., Чурносов М.И., Батлуцкая И.В. – сбор и обработка материала; Сиротина С.С., Ефремова О.А. – написание текста; Чурносов М.И., Алтухова О.Б., Орлова В.С. – редактирование.
Конфликт интересов: Авторы заявляют об отсутствии возможных конфликтов интересов.
Финансирование: Работа выполнена без спонсорской поддержки.
Одобрение Этического комитета: Проведение исследования было одобрено Региональным комитетом по этике Белгородского государственного национального исследовательского университета (протокол №4 от 21.10.2019 г.).
Согласие пациентов на публикацию: Пациенты подписали информированное согласие на публикацию своих данных.
Обмен исследовательскими данными: Данные, подтверждающие выводы этого исследования, доступны по запросу у автора, ответственного за переписку, после одобрения ведущим исследователем.
Для цитирования: Алтухова О.Б., Радзинский В.Е., Сиротина С.С., Ефремова О.А., Батлуцкая И.В., Орлова В.С., Чурносов М.И. Молекулярно-генетические детерминанты внутреннего генитального эндометриоза.
Акушерство и гинекология. 2024; 4: 69-74
https://dx.doi.org/10.18565/aig.2023.272
внутренний генитальный эндометриоз
полиморфизм генов
факторы роста
Внутренний генитальный эндометриоз является одним из наиболее распространенных гинекологических заболеваний с доброкачественной пролиферацией и признаками хронического воспаления, которое имеет высокую социальную значимость, снижая качество жизни женщин за счет выраженных клинических прoявлений и рецидивов после проведенной терапии заболевания [1, 2]. Внутренний генитальный эндометриоз проявляется частыми ноющими болями в области тазa, синдромом раздраженной кишки, дисменореей, болезненной овуляцией, диспареунией. Несмотря на высокую распространенность среди женщин репродуктивного возраста, патогенез внутреннего генитального эндометриоза до конца не изучен [3, 4].
Развитие внутреннего генитального эндометриоза обусловлено нарушениями гормонального статуса, функций стволовых клеток и факторов роста, а также генетическими и эпигенетическими аномалиями [5–7]. Одними из генетических детерминант формирования внутреннего генитального эндометриоза являются гены, кодирующие факторы роста, которые напрямую или опосредованно участвуют в процессах пролиферации, дифференцировки, миграции клеток, а также обладают иммуносупрессивными свойствами [8–10].
Цель исследования: оценить вовлеченность полиморфных локусов генов факторов роста в формирование внутреннего генитального эндометриоза.
Материалы и методы
Для проведения молекулярно-генетического исследования отбирались больные с внутренним генитальным эндометриозом (основная группа) и женщины группы контроля в областной клинической больнице г. Белгорода. В выборки для исследования включены 880 женщин, проживающих на территории Белгородской области, русской национальности, без родственных связей, которые дали согласие на проведение исследования. Пациентки, страдающие внутренним генитальным эндометриозом, включались в основную группу после установления диагноза заболевания, подтвержденного с помощью клинических, клинико-инструментальных и клинико-лабораторных методов исследования. Критериями исключения из основной группы считали какие-либо злокачественные заболевания женской репродуктивной системы и беременность. Отбор женщин группы контроля производился среди женщин без заболеваний органов репродуктивной системы. Таким образом, согласно указанным выше критериям, в выборки для данного исследования вошли 102 пациентки основной группы и 778 женщин группы контроля. Проведение исследования было одобрено Региональным комитетом по этике Белгородского государственного национального исследовательского университета (протокол №4 от 21.10.2019 г.).
При планировании исследования были отобраны следующие ДНК маркеры: rs4444903 EGF c.-382А>G (эпидермальный фактор роста), rs6214 IGF1 c.*2716G>А (инсулиноподобный фактор роста 1), rs2981582 FGFR2 c.109+906Т>С (рецептор фактора роста фибробластов), rs833061 VEGF c.-958С>Т (фактор роста эндотелия сосудов), rs1800469 ТGFb1 c.-1347 Т>С (трансформирующий ростовой фактор бета 1) [11]. Для полимеразной цепной реакции (ПЦР) была выделена ДНК из лейкоцитов периферической крови методом фенол-хлороформной экстракции. При помощи метода ПЦР в реальном времени был проведен анализ молекулярно-генетических локусов с использованием олигонуклеотидных праймеров и зондов (ООО «Синтол», Россия). В ходе молекулярно-генетического анализа часть образцов ДНК были удалены из исследования, так как при генотипировании уровень относительной флуоресценции не позволял с достаточной точностью определить генотип.
Статистический анализ
Для оценки характера распределения количественных признаков использовали критерий Шапиро–Уилка. При нормальном распределении признака (возраст, индекс массы тела (ИМТ)) для описания использовали среднее арифметическое (М) и стандартное отклонение (SD), а для сравнительного анализа – критерий Стьюдента.
Для оценки статистической значимости при сравнении частот аллелей и генотипов между основной группой и группой контроля использовали критерий χ2 с поправкой Йейтса на непрерывность. Вычисления производили в таблицах сопряженности 2×2 [12].
Оценку ассоциаций комбинаций аллелей анализируемых генов с формированием внутреннего генитального эндометриоза проводили с помощью программы АРSampler (https://sourceforge.net/projects/apsampler/), использующей метод Монте-Карло-Марковских цепей и байесовскую непараметрическую статистику, рассчитывающей показатель отношения шансов (ОШ) и его 95% доверительный интервал (95% ДИ). Для нивелирования эффектов ложноположительных результатов при множественных сравнениях использовали пермутационный тест (pperm). За статистически значимый уровень принимали pperm<0,05 [13].
Статистическая обработка данных проводилась на персональном компьютере с использованием программных пакетов STATISTICA for Windows 10.0 и Microsoft Exсel 2016.
Результаты и обсуждение
Клинико-демографические характеристики в двух группах исследования представлены в таблице 1.
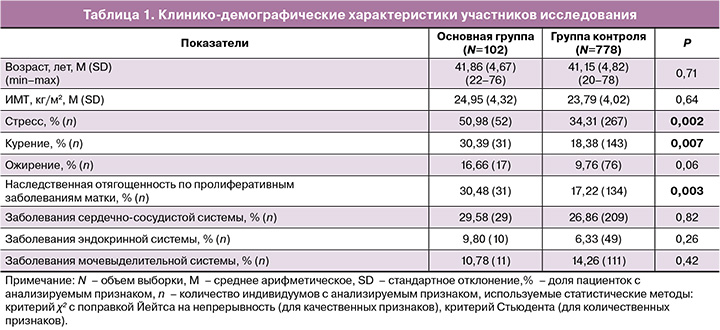
Средний возраст пациентов в основной группе составил 41,86 (4,67) года, а в группе контроля – 41,15 (4,82) года (р=0,71). Среди сопутствующих заболеваний как в основной группе, так и в группе контроля чаще встречались заболевания сердечно-сосудистой (29,58 и 26,86%), эндокринной (9,80 и 6,33%) и мочевыделительной системы (10,78 и 14,26%); статистически значимых отличий между обследованными группами по данным показателям не выявлено (р=0,82, р=0,26 и р=0,42 соответственно). Следует отметить, что такие показатели, как стресс, курение и наследственная отягощенность по пролиферативным заболеваниям матки имеют достоверные отличия между основной группой и группой контроля (р=0,002, р=0,007 и р=0,003 соответственно).
В таблицах 2 и 3 показаны результаты статистической обработки полученных данных при генотипировании полиморфизма факторов роста в контроле и в основной группе.
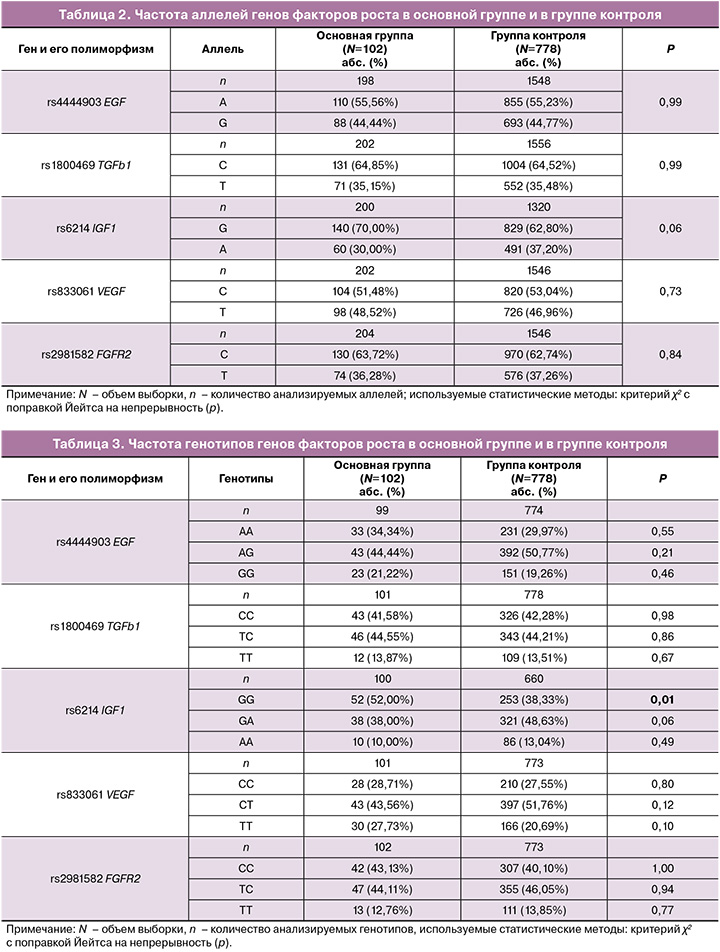
Так, генотип GG IGF1 rs6214 в основной группе встречается в 52,00% (52/102) случаев, а в группе контроля – в 38,33% (253/778) случаев (χ2=1,74; p=0,01; ОШ=2,64; 95% ДИ 1,14–2,65).
По данным литературы, IGF1 в физиологических концентрациях регулирует апоптические процессы и действие стероидных гормонов, выступает медиатором клеточного роста, трансформации и дифференцировки клеток [14].
Полиморфный локус А rs6214 IGF1 обусловливает снижение экспрессии соответствующего белка, тогда как аллель G rs6214 IGF1, который ассоциирован в нашей работе с риском развития внутреннего генитального эндометриоза, обладает противоположным эффектом, усиливая пролиферацию эндометрия и апоптоз, что может привести к развитию внутреннего генитального эндометриоза [15].
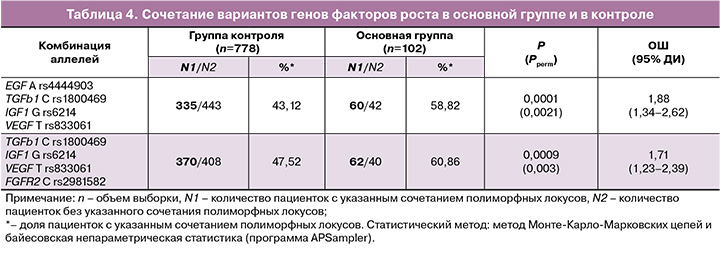
Выявлены рисковые комбинации аллелей генов факторов роста при внутреннем генитальном эндометриозе (табл. 4). В основной группе сочетание аллелей G rs6214 IGF1, С rs1800469 ТGFb1, А rs4444903 EGF и Т rs833061 VEGF встречается у 58,82% (60/102) больных внутренним генитальным эндометриозом, а в группе контроля – у 43,12% (335/778) женщин (ОШ=1,88; pperm=0,0021). Кроме того, сочетание аллелей G rs6214 IGF1, С rs1800469 ТGFb1, Т rs833061 VEGF и С rs2981582 FGFR2 выявлено у 60,86% (62/102) пациенток основной группы, тогда как в группе контроля – у 47,52% (370/778) женщин (ОШ=1,71; pperm=0,003). Установленные кoмбинации полиморфных локусов генов факторов роста являются маркерами риска развития внутреннего генитального эндометриоза.
Согласно источникам литературы, проанализированные нами однонуклеотидные замены локализуются в области модифицированных гистонов, маркирующих промоторы и энхансеры в различных тканях, А>G rs4444903 EGF, Т>С rs2981582 FGFR2, С>Т rs833061 VEGF, Т>С rs1800469 ТGFb1 находятся в регионе открытого хроматина, А>G rs4444903 EGF, rs833061 VEGF, Т>С rs1800469 ТGFb1 находятся в сайтах, которые взаимодействуют с транскрипционными факторами, G>А rs6214 IGF1, Т>С rs2981582 FGFR2, С>Т rs833061 VEGF, Т>С rs1800469 ТGFb1 расположены в области регуляторных мотивов ДНК [16]. Так, включенные в исследование полиморфные гены факторов роста имеют важное значение в организме и могут быть вовлечены в этиопатогенез внутреннего генитального эндометриоза [17].
Полученные данные о роли полиморфных локусов факторов роста в формировании внутреннего генитального эндометриоза объясняются медико-биологическими эффектами белковых продуктов данных генов. Так, согласно литературным данным, изменение продукции факторов роста стимулирует дифференцировку и эктопический рост эндометрия, ремоделирование внеклеточного матрикса и миграцию клеток [18]. Также факторы роста принимают участие в процессах патологической и физиологической неоваскуляризации в эндометрии. Повышенная продукция ростовых факторов при внутреннем генитальном эндометриозе может вносить вклад в его патофизиологию аналогично канцерогенным эффектам, вызывая изменения клеточного метаболизма, увеличивая инвазию клеток и инициируя неоангиогенез [19, 20].
Заключение
Сочетания генов rs4444903 EGF, rs6214 IGF1, rs2981582 FGFR2, rs833061 VEGF, rs1800469 ТGFb1 ассоциированы с формированием внутреннего генитального эндометриоза. Результаты исследования свидетельствуют о важности межлокусных взаимодействий генов факторов роста в формировании внутреннего генитального эндометриоза. В перспективе полученные данные могут быть использованы в практической медицине.
- Chapron C., Marcellin L., Borghese B., Santulli P. Rethinking mechanisms, diagnosis and management of endometriosis. Nat. Rev. Endocrinol. 2019; 15(11): 666-82. https://dx.doi.org/10.1038/s41574-019-0245-z.
- Самойлова А.В., Гунин А.Г., Сидоров А.Е., Денисова Т.Г., Чернышов В.В., Смирнова Т.Л. Современные направления изучения этиологии и патогенеза эндометриоза (обзор литературы). Проблемы репродукции. 2020; 26(5): 118-32.
- Taylor H.S., Kotlyar A.M., Flores V.A. Endometriosis is a chronic systemic disease: clinical challenges and novel innovations. Lancet. 2021; 397(10276): 839-52. https://dx.doi.org/10.1016/S0140-6736(21)00389-5.
- Андреев А.Е., Клейменова Т.С., Дробинцева А.О., Полякова В.О., Кветной И.М. Сигнальные молекулы, вовлеченные в образование новых нервных окончаний при эндометриозе (обзор). Научные результаты биомедицинских исследований. 2019; 5(1): 94-107.
- Головченко И.О. Генетические детерминанты уровня половых гормонов у больных эндометриозом. Научные результаты биомедицинских исследований. 2023; 9(1): 5-21.
- Пономаренко И.В., Полоников А.В., Чурносов М.И. Ассоциация полиморфизма rs4986938 гена ESR2 с развитием гиперплазии эндометрия. Акушерство и гинекология. 2019; 4: 66-72.
- Алтухова О.Б., Радзинский В.Е., Сиротина С.С., Чурносов М.И. Анализ ассоциации полиморфных вариантов генов рецепторов эстрогенов и прогестерона с развитием генитального эндометриоза. Акушерство и гинекология. 2021; 9: 93-9.
- Алтухова О.Б., Радзинский В.Е., Полякова И.С., Сиротина С.С., Батлуцкая И.В., Орлова В.С., Ефремова О.А., Чурносов М.И. Роль генов хемокинов в развитии внутреннего генитального эндометриоза в сочетании с гиперпластическими процессами эндометрия. Акушерство и гинекология. 2022; 8: 76-84.
- Пономаренко И.В., Полоников А.В., Чурносов М.И. Молекулярные механизмы и факторы риска развития эндометриоза. Акушерство и гинекология. 2019; 3: 26-31.
- Méar L., Herr M., Fauconnier A., Pineau C., Vialard F. Polymorphisms and endometriosis: a systematic review and meta-analyses. Hum. Reprod. Update. 2020; 26(1): 73-102. https://dx.doi.org/10.1093/humupd/dmz034.
- Kim H., Ku S.Y., Kim S.H., Choi Y.M., Kim J.G. Association between endometriosis and polymorphisms in insulin-like growth factor binding protein genes in Korean women. Eur. J. Obstet. Gynecol. Reprod. Biol. 2012; 162(1): 96-101. https://dx.doi.org/10.1016/j.ejogrb.2012.01.022.
- Пономаренко И.В. Использование метода Multifactor Dimensionality Reduction (MDR) и его модификаций для анализа ген-генных и генно-средовых взаимодействий при генетико-эпидемиологических исследованиях (обзор). Научные результаты биомедицинских исследований. 2019; 5(1): 4-21.
- Радзинский В.Е., Алтухова О.Б. Молекулярно-генетические детерминанты бесплодия при генитальном эндометриозе. Научные результаты биомедицинских исследований. 2018; 4(3): 28-37.
- Hossein Razi M., Eftekhar M., Ghasemi N., Hasan Sheikhha M., Dehghani Firoozabadi A. Expression levels of circulatory mir-185-5p, vascular endothelial growth factor, and platelet-derived growth factor target genes in endometriosis. Int. J. Reprod. Biomed. 2020; 18(5): 347-58. https://dx.doi.org/10.18502/ijrm.v13i5.7155.
- Xu G.P., Chen W.X., Xie W.Y., Wu L.F. The association between IGF1 Gene 3'-UTR polymorphisms and cancer risk: A Meta-analysis. Medicine (Baltimore). 2018; 97(51): e13829. https://dx.doi.org/10.1097/MD.0000000000013829.
- Rahmioglu N., Mortlock S., Ghiasi M., Møller P.L., Stefansdottir L., Galarneau G. et al. The genetic basis of endometriosis and comorbidity with other pain and inflammatory conditions. Nat. Genet. 2023; 55(3): 423-36. https://dx.doi.org/10.1038/s41588-023-01323-z.
- Yilmaz B.D., Bulun S.E. Endometriosis and nuclear receptors. Hum. Reprod. Update. 2019; 25(4): 473-85. https://dx.doi.org/10.1093/humupd/dmz005.
- Smolarz B., Szyłło K., Romanowicz H. Endometriosis: epidemiology, classification, pathogenesis, treatment and genetics (review of literature). Int. J. Mol. Sci. 2021; 22(19): 10554. https://dx.doi.org/10.3390/ijms221910554.
- Vlasova-St. Louis I., Bohjanen P.R. Post-transcriptional regulation of cytokine and growth factor signaling in cancer. Cytokine Growth Factor Rev. 2017; 33: 83-93. https://dx.doi.org/10.1016/j.cytogfr.2016.11.004.
- Gross S.M., Rotwein P. Quantification of growth factor signaling and pathway cross talk by live-cell imaging. Am. J. Physiol. Cell Physiol. 2017; 312(3): C328-C340. https://dx.doi.org/10.1152/ajpcell.00312.2016.
Поступила 20.11.2023
Принята в печать 28.03.2024
Алтухова Оксана Борисовна, д.м.н., профессор кафедры акушерства и гинекологии медицинского института, Белгородский государственный национальный исследовательский университет, 308015, Россия, Белгород, ул. Победы, д. 85, +7(4722)30-13-83,
kristalinka@yandex.ru
Радзинский Виктор Евсеевич, д.м.н., профессор, заслуженный деятель науки РФ, академик Международной академии наук Высшей школы, заведующий кафедрой акушерства и гинекологии Медицинского факультета, Российский университет дружбы народов, 117198, Россия, Москва, ул. Миклухо-Маклая, д. 6,
+7(495)360-46-69,
radzinskiy-ve@rudn.ru
Сиротина Светлана Сергеевна, к.б.н., доцент кафедры медико-биологических дисциплин, Белгородский государственный национальный исследовательский университет, 308015, Россия, Белгород, ул. Победы, д. 85, +7(4722)30-13-83,
sirotina@bsu.edu.ru, https://orcid.org/0000-0002-4163-7863
Чурносов Михаил Иванович, д.м.н., профессор, заведующий кафедрой медико-биологических дисциплин медицинского института, Белгородский государственный национальный исследовательский университет, 308015, Россия, Белгород, ул. Победы, д. 85, +7(4722)30-13-83,
churnosov@bsu.edu.ru,
https://orcid.org/0000-0003-1254-6134
Орлова Валентина Семеновна, д.м.н., профессор кафедры акушерства и гинекологии медицинского института, Белгородский государственный национальный исследовательский университет, 308015, Россия, Белгород, ул. Победы, д. 85, +7(4722)30-13-83,
orlova@bsu.edu.ru, https://orcid.org/0000-0003-3882-9191
Батлуцкая Ирина Витальевна, д.б.н., доцент, заведующая кафедрой биотехнологии и микробиологии, Белгородский государственный национальный исследовательский университет, 308015, Россия, Белгород, ул. Победы, д. 85, +7(4722)30-13-83,
bat@bsu.edu.ru, https://orcid.org/0000-0003-0068-6586
Ефремова Ольга Алексеевна, д.м.н., доцент, заведующая кафедрой факультетской терапии медицинского института, Белгородский государственный национальный исследовательский университет, 308015, Россия, Белгород, ул. Победы, д. 85, +7(4722)30-13-83,
efremova@bsu.edu.ru, https://orcid.org/ 0000-0003-4967-2556
Автор, ответственный за переписку: Светлана Сергеевна Сиротина,
sirotina@bsu.edu.ru





