Согласно клинической классификации, острый коронарный синдром (ОКС) включает в себя различные формы ишемической болезни сердца — нестабильную стенокардию (НС) и острый инфаркт миокарда (ОИМ). Наиболее ранняя диагностика ОКС базируется на электрокардиографии и определении уровня кардиоспецифичных маркеров в сыворотке крови, в частности, кардиоспецифичного тропонина I. Первые признаки ишемического повреждения миокарда на электрокардиограмме (ЭКГ) характеризуются подъемом или депрессией сегмента ST, инверсией зубца T (ОКС с подъемом сегмента ST или ОКС без подъема сегмента ST). В течение последующих 2—3 дней от момента сердечного приступа на ЭКГ возможно появление зубца Q — маркера крупноочагового некроза миокарда. В зависимости от результатов ЭКГ и концентрации кардиоспецифичного тропонина I в сыворотке крови определяют прогноз и тактику лечения [1—4].
Морфологическая классификация предусматривает деление острых форм ишемической болезни сердца на острую коронарную недостаточность и ОИМ. Для их посмертной диагностики наряду с гистологическим методом применяют определение активности аспартатаминотрансферазы, лактатдегидрогеназы и содержания кардиоспецифичного тропонина I в перикардиальной жидкости, которая представляет собой ультрафильтрат крови и межклеточной жидкости [5—9], определяют концентрацию ионов калия, натрия и кальция в миокарде [10—13].
Таким образом, клинические данные свидетельствуют, что уже в первые 3 сут от момента сердечного приступа ОИМ представляет собой различные варианты течения заболевания. Морфологические критерии, позволяющие на секционном материале дифференцировать различные формы ОИМ, отсутствуют.
Цель настоящего исследования — выявить морфологические изменения миокарда, различия в содержании глюкозы и электролитов в перикардиальной жидкости в зависимости от объема ишемического повреждения левого желудочка (ЛЖ) при ОИМ в донекротической стадии (ОИМДС) у скончавшихся на догоспитальном этапе.
Материал и методы
Работа выполнена на материале 38 случаев смерти от ОИМДС с трансмуральным (n=23) и субэндокардиальным или субэпикардиальным (n=15) поражением стенки ЛЖ. Среди умерших от трансмурального ОИМДС было 17 мужчин и 6 женщин, средний возраст которых составил 50,1±2,8 года. В крови у 10 человек был обнаружен этиловый спирт в концентрации менее 3‰. От субэндо- или субэпикардиального ОИМДС скончались 11 мужчин и 4 женщины, средний возраст которых достигал 51,6±2,7 года (p>0,05). У 6 человек в крови был обнаружен этиловый спирт в концентрации менее 3‰. Случаев одновременного сочетания субэндо- и субэпикардиального ОИМДС у одного больного мы не наблюдали. Во всех без исключения наблюдениях медицинская помощь не оказывалась.
С момента наступления смерти до исследования трупа проходило не более 1 сут. В связи с тем что донекротическая стадия ОИМ длится первые 24 ч от момента сердечного приступа и в миокарде отсутствует сформировавшийся очаг некроза, для гистологического исследования приводили забор образцов сердца по унифицированной методике. Вырезали 5 кусочков ЛЖ на середине расстояния между верхушкой и митральным клапаном из передней, боковой, задней стенки и межжелудочковой перегородки, а также из верхушки [14]. Материал фиксировали в растворе 10% нейтрального формалина, заливали в парафин. Срезы окрашивали гематоксилином и эозином, хромотропом 2В водным голубым. Неокрашенные микропрепараты изучали в поляризованном свете. Статистический анализ микроскопических данных проводили с использованием процента положительных значений изучаемого признака, выраженного в долях единицы (Р), аргумента нормального распределения и углового преобразования Фишера [15].
Перикардиальную жидкость получали в процессе аутопсии до эвисцерации органокомплекса и центрифугировали при 1500 об/мин в течение 15 мин. В полученном материале определяли содержание калия, натрия и кальция с помощью атомно-абсорбционного спектрометра «Квант-2А» с компьютерным программным обеспечением. Глюкозу определяли стандартным набором реактивов для глюкозооксидазного метода (набор «Фотоглюкоза»).
Результаты и обсуждение
При макроскопическом исследовании в группах с трансмуральным и субэндо- или субэпикардиальным ишемическим поражением масса сердца составила 352,93±12,23 г. Толщина стенки ЛЖ достигала 1,54±0,02 см, что незначительно превышало норму (1,1—1,4 см; p>0,05).
Топографический анализ позволил выявить, что при ОИМДС ишемический процесс локализуется в 1—2 соседних областях миокарда, независимо от глубины поражения стенки ЛЖ и содержания этилового спирта в крови умерших. Наиболее часто поражаются передняя и задняя стенки, в меньшей степени верхушка и межжелудочковая перегородка (табл. 1).
Таблица1. Частота (%) локализации ишемического процесса в ЛЖ сердца
Примечание. ЛЖ — левый желудочек. Здесь и в табл. 2—4: ОИМДС — острый инфаркт миокарда, донекротическая стадия.
Гистологическое исследование микропрепаратов, окрашенных гематоксилином и эозином, хромотропом 2В водным голубым (световая микроскопия), позволило оценить изменения в артериальной системе сердца, венозного и микроциркуляторного русла, нарушения реологических свойств крови. Ишемические повреждения кардиомиоцитов выявляли с помощью световой и поляризационной микроскопии (табл. 2).
Таблица 2. Патоморфологические микроскопические признаки (Р)
Примечание. Здесь и в табл. 4 * — p<0,05; ** — p<0,01.
Во всех исследованных группах спазм коронарных артерий преобладал над дистонией и обычным просветом сосудов. Одновременно было обнаружено, что при трансмуральном поражении стенки ЛЖ имеется статистически значимое трансформирование вытянутой формы клеток эндотелия в округлую. При субэндо- или субэпикардиальной локализации ишемического процесса чаще встречались интрамуральные артерии с обычным просветом. Для трансмурального поражения стенки ЛЖ были характерны гиперхромная окраска клеток эндотелия интрамуральных артерий и спазм артериол. Полученные данные согласуются с мнением, что тонус артерий зависит от состояния эндотелия, которому принадлежит важная роль в возникновении спазма и ишемии миокарда [16, 17].
При оценке венозного и микроциркуляторного русла обнаружено полнокровие сосудов с явлениями стаза крови и сладж-феномена, образование микротромбов без достоверных различий между сравниваемыми группами. Важным показателем нарушения реологических свойств крови был феномен образования «плазматических сосудов», который встречался более чем в 59% случаев (p>0,05) при любой локализации ишемического процесса в стенке ЛЖ.
Отмечались утолщение, волнообразная деформация и фрагментация сердечных мышечных волокон, как в очагах ишемии, так и вне их. Случаи трансмуральной ишемии миокарда достоверно отличались от субэндо- или субэпикардиальной локализации по слабо различимой сарколемме — морфологическому показателю повышенной проницаемости стенки кардиомиоцитов.
Поляризационная микроскопия независимо от локализации ОИМДС характеризовалась сочетанием контрактурных повреждений кардиомиоцитов III степени, внутриклеточного миоцитолиза и первичного глыбчатого распада миофибрилл. Указанные признаки являются морфологическими маркерами ишемического повреждения кардиомиоцитов с формированием зон коагуляционного и колликвационного некроза с одновременной потерей сократительной способности миокарда [6, 9, 18, 19].
Однако при трансмуральном поражении стенки ЛЖ количество контрактурных повреждений кардиомиоцитов II степени (участков гиперсокращения) было достоверно больше, чем при субэндо- или субэпикардиальном ОИМДС. Для последних характерны контрактурные повреждения кардиомиоцитов I степени, носящие обратимый характер. В то же время отсутствовали достоверные различия между сравниваемыми группами по количеству участков с трещинами и диссоциацией мышечных волокон, которые являются маркерами фибрилляции желудочков сердца [7, 20]. Таким образом, при ОИМДС с трансмуральным поражением стенки ЛЖ дегенеративные изменения кардиомиоцитов были более выражены.
В подгруппах с наличием этанола как при трансмуральной, так при субэндо- или субэпикардиальной ишемии достоверно чаще встречались микротромбы в микроциркуляторном русле, что совпадает с результатами ранее проведенных исследований [21, 22]. Небольшое увеличение толщины стенки ЛЖ на первый взгляд можно интерпретировать как незначительную гипертрофию миокарда. Однако при одновременном наличии в микропрепаратах периваскулярного и межмышечного отека, утолщения кардиомиоцитов, острых ишемических повреждений сердечных мышечных волокон (см. табл. 2) описанное изменение следует рассматривать как морфологический признак отека миокарда [23].
В перикардиальной жидкости выявлены достоверные различия концентрации кальция и глюкозы в зависимости от локализации ОИМДС. Для трансмурального поражения были характерны снижение уровня глюкозы и повышенное содержания кальция (табл. 3). Наличие этилового спирта в крови умерших вызвало некоторое повышение концентрации калия, кальция и снижение содержания глюкозы, которое было статистически незначимо (табл. 4).
Таблица 3. Показатели перикардиальной жидкости (M±m)
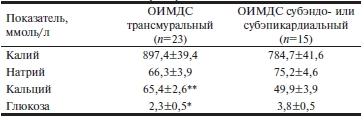
Таблица 4. Показатели перикардиальной жидкости взависимости от содержания этилового спирта в крови умерших(M±m)
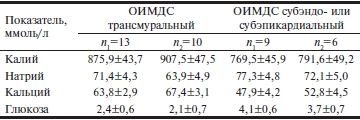
Примечание. n1 — подгруппы без содержания этилового спирта, n2 — подгруппы с содержанием этилового спирта.
Выявленные морфологические изменения кардиомиоцитов и показателей перикардиальной жидкости можно объяснить особенностью строения сердечного мышечного волокна, а также различным объемом ишемического повреждения ЛЖ. Структурной единицей кардиомиоцитов является саркомер, в состав которого входит тропониновый комплекс (I, Т, С). Тропонин С (cTnC) выполняет роль депо кальция, в котором каждая молекула белка связывает 4 иона кальция [24]. Появление контрактурных повреждений кардиомиоцитов III степени, участков внутриклеточного миоцитолиза и первичного глыбчатого распада миофибрилл свидетельствует о распаде тропонинового комплекса [9] с высвобождением свободного кальция из него в цитоплазму кардиомиоцита. Одновременно за счет повышенной проницаемости сарколеммы сердечных мышечных волокон кальций переходит из цитоплазмы клетки в перикардиальную жидкость [7, 12, 13, 25, 26], а возникновение дополнительных участков гиперсокращения мышечных волокон в виде контрактурных повреждений кардиомиоцитов II степени при трансмуральной ишемии миокарда свидетельствует о перегрузке кальцием цитоплазмы кардиомиоцитов. Следствием этих структурных изменений кардиомиоцитов является потеря сократительной способности миокарда.
При трансмуральной ишемии, захватывающей все слои стенки с локализацией в 1—2 соседних топографических областях (см. табл. 1), объем повреждения миокарда ЛЖ значительно больше, чем при субэндо- или субэпикардиальной ишемии с аналогичной топографической локализацией. Поэтому больший объем ишемического повреждения обусловливает резкое уменьшение запасов гликогена в миокарде и потерю его сократительной способности на большем участке. Следовательно, повышение концентрации кальция и снижение содержания глюкозы в перикардиальной жидкости отражают объем ишемического поражения миокарда ЛЖ.
Таким образом, острый инфаркт миокарда в донекротической стадии на догоспитальном этапе может протекать в двух морфологических формах — либо с трансмуральной, либо с субэндо- или субэпикардиальной локализацией ишемического процесса в стенки ЛЖ. Трансмуральное распространение характеризуется большим объемом ишемического поражения сердечной мышцы, генерализованным спазмом артериальной системы сердца с изменением формы и окраски клеток эндотелия, тромбозом микроциркуляторного русла, выраженными дегенеративными изменениями кардиомиоцитов с нарушением их энергетического обмена и сократительной способности.
При субэндо- или субэпикардиальной локализации очаги ишемического повреждения перемежаются с участками нормального кровоснабжения, менее выражены нарушения энергетического обмена и потеря сократительной способности миокарда. Вместе с тем независимо от объема поражения левого желудочка между двумя формами острого инфаркта миокарда в донекротической стадии имеется сходство по характеру нарушения реологических свойств крови с тромбозом микроциркуляторного русла и количеству маркеров фибрилляции желудочков сердца, что в итоге создает предпосылки для увеличения зоны некроза в миокарде и обусловливает высокий риск нарушения ритма.
Наличие этилового спирта в крови умерших от острого инфаркта миокарда в донекротической стадии как при трансмуральной, так при субэндо- или субэпикардиальной ишемии повышает микротромбообразование в микроциркуляторном русле. Однако это не приводит к дополнительному увеличению объема ишемического поражения миокарда левого желудочка.



