Введение
Простатит – распространенное заболевание предстательной железы (ПЖ) с гетерогенной этиологией и клиническими проявлениями, включающими тазовую боль, расстройства мочеиспускания и эякуляции [1–4].
В настоящее время используется классификация простатита, предложенная Национальным институтом здоровья США (NIH) в 1995 г., которая выделяет четыре категории заболевания в зависимости от наличия или отсутствия бактериального агента, лейкоцитов в секрете ПЖ, клинических проявлений. Согласно этой классификации, выделяют следующие категории простатита: острый бактериальный простатит (категория I), хронический бактериальный простатит (ХБП) (категория II), хронический простатит/синдром хронической тазовой боли (ХП/СХТБ; категория III), бессимптомный простатит (категория IV). ХП/СХТБ (простатит категории III) дополнительно подразделяется на воспалительный (IIIA) и невоспалительный (IIIB) подтипы, которые различаются в зависимости от наличия или отсутствия повышенного количества лейкоцитов в секрете ПЖ, образце мочи после массажа простаты. Каждая из этих категорий имеет свои клинические особенности [5].
Необходимо отметить, что патоген при ХБП обнаруживается классическим бактериологическим методом лишь в 5–10% случаев. Основными возбудителями ХБП являются различные бактерии порядка Enterobacterales, а также фекальные энтерококки.
В качестве источника и резервуара уропатогенных бактерий все чаще рассматривается кишечная микробиота (КМ). Ряд микроорганизмов, способствующих развитию воспалительных процессов в ПЖ, труднокультивируемы (например, анаэробы), что ограничивает возможности стандартных диагностических тестов. Известно, что при применении современных лабораторных методов инфекционная природа простатита, связанная с такими возбудителями, установлена в ряде случаев, а антимикробная терапия нередко оказывается эффективной для устранения воспалительного процесса при ХП/СХТБ категории IIIA [6–11].
ХП/СХТБ является наиболее распространенной формой (около 90% случаев ХП) и отличается трудностями в диагностике и лечении в связи с многофакторным и до конца не изученным патогенезом [12–14].
На сегодняшний день активно обсуждается роль состояния КМ при различных заболеваниях [15]. Новые подходы к идентификации бактерий с использованием не зависимых от культуры методов позволяют выявлять изменения в КМ. Изучение корреляций изменения КМ с наличием тех или иных патологических состояний представляет особый интерес. В ряде исследований предложена концепция «осей» кишечника и органов, предполагающая наличие межорганной связи и взаимного влияния [16]. В 2005 г. впервые была предложена концепция «ось простата–кишечник», указывающая на тесную связь между ПЖ и кишечником [17]. Известно, что КМ может оказывать влияние на состояние мочеполовой системы [18–22]. К сожалению, до настоящего времени патофизиологические взаимосвязи между состоянием КМ и развитием ХП остаются малоизученными, а в исследованиях, посвященных вопросам влияния микробиома на ПЖ, недостаточно внимания уделено роли кишечника [23].
Особенности кишечной микробиоты у пациентов с хроническим простатитом
D. A. Shoskes et al. провели комплексную оценку изменений в КМ у мужчин с ХП/СХТБ, сопоставив результаты с клиническими проявлениями заболевания. Тяжесть симптомов оценивали с помощью индекса симптомов хронического простатита (NIH-CPSI), а клинический фенотип с помощью системы UPOINT. Исследование КМ проводили при помощи секвенирования 16S рРНК. Всего в исследовании приняли участие 25 пациентов, а 25 мужчин составили контрольную группу. У пациентов с ХП/СХТБ различались результаты кластерного анализа относительно контрольной группы, также было выявлено более низкое среднее альфа-разнообразие КМ со значительными различиями в таксонах между группами. Наиболее значимым отличием являлась недостаточная представленность у пациентов с ХП/СХТБ бактерий рода Prevotella, которые, как известно, колонизируют желудочно-кишечный тракт и играют определенную роль в подавлении избыточной воспалительной реакции. При этом не было установлено значимых корреляций с показателями NIH-CPSI/UPOINT. Исследователи предположили, что различия в количестве Prevotella в КМ могут стать основой для новой диагностической модели ХП/СХТБ [24].
B. Holland et al. исследовали образцы фекалий 30 мужчин с симптомами нижних мочевыводящих путей, оцененными по Международной шкале оценки простатических симптомов (IPSS). Установлено, что 48 фекальных OTU (операционные таксономические единицы) продемонстрировали значительную корреляцию с одним или несколькими показателями шкалы IPSS. Наиболее существенная отрицательная корреляция обнаружена между Lachnospiraceae Blautia, которая увеличивает доступность короткоцепочечных жирных кислот (КЦЖК) в кишечнике и выраженностью беспокойства по поводу заболевания (r=0,702; p=0,001) [25].
При исследовании крыс с абактериальным хроническим воспалением ПЖ было определено значительное увеличение в КМ следующих представителей: Rikenellaceae, Odoribacter, Clostridiaceae, Allobaculum и Peptococcaceae по сравнению со здоровыми крысами. И наоборот, уровни Bacteroides Uniformis, Lactobacillus и Lachnospiraceae, а также концентрация КЦЖК были снижены у крыс с ХП [26].
В другой работе с использованием крыс также был установлен измененный профиль КМ при ХП/СХТБ. При сравнении относительной численности представителей КМ обнаружено уменьшение количества Muribaculum и увеличение некультивируемых бактерий Desulfovibrionaceae у крыс с ХП/СХТБ. В этом исследовании также было обнаружено, что относительная численность Lactobacillus снизилась с 4,0 до 3,2% у крыс с ХП/СХТБ. При сравнении относительного содержания мРНК обнаружено, что экспрессия 185 генов эпителия кишечника значительно изменилась в группе ХП/СХТБ. Среди этих генов 107 были подавлены, а активность 78 генов была повышена [16]. Известно, что КМ может воздействовать на экспрессию генов в эпителиальных клетках толстой кишки, контролируя гомеостаз и воспалительные процессы [27].
С помощью классификации KEGG было установлено, что эти гены участвуют в ряде клеточных процессов, в пищеварении (переваривании и всасывании белков, всасывании минералов, а также в метаболизме фруктозы и маннозы), в работе иммунной системы (сигнальные пути PPAR, p53, ИЛ-17). Полученные результаты могут свидетельствовать о возможной взаимосвязи ХП/СХТБ с функцией кишечника [16]. Рассматривая возможное значение бактерий семейства Desulfovibrionaceae, следует отметить, что увеличение их численности в кишечнике ассоциировано с употреблением продуктов с высоким содержанием жиров, а также длительностью полиаутоиммунитета [28, 29].
B. White et al. исследовали фекалии пациентов с ХП/СХТБ с помощью секвенирования 16S рРНК. Определено, что в КМ пациентов наблюдается повышенное количество бактерий типа Firmicutes по сравнению с микробиотой контрольных пациентов. Также отмечается, что в КМ в когорте ХП/СХТБ наблюдалось общее увеличение биоразнообразия, что отличается от данных других исследователей, в которых дисбиоз был связан преимущественно со снижением биоразно-образия КМ у больных. Исследователи считают, что такой результат мог быть получен из-за различий в когортах исследования, размере выборки, возрасте и диете [30].
В работе S. Wang et al., включившей 41 пациента с ХП/СХТБ и 43 участников контрольной группы, были установлены значимые различия в структуре КМ. У пациентов с ХП/СХТБ отмечено увеличение количества Bacteroides, Romboutsia, Escherichia-Shigella, Ruminococcus, Enterobacter, Pseudomonas, Clostridium, Lachnoclostridium. И наоборот, имело место снижение количества таких представителей КМ, как Blautia, Faecalibacterium, Bifidobacterium, Prevotella, Alistipes, Dialister [31].
Иммунологические аспекты оси «кишечник–простата»
На сегодняшний день определена важная роль иммунологического дисбаланса в патогенезе ХП/СХТБ. Установлено, что воспаление и аутоиммунитет вносят определенный вклад в развитие ХП/СХТБ. При данном заболевании в крови и сперме пациентов повышаются концентрации ряда провоспалительных факторов (ФНО-α, ИЛ-6, ЦОГ-2 и других) [32–36]. R.D. Motrich et al. определили, что иммунный ответ Th17-клеток связан с ХП, который может индуцировать и усугублять признаки тазовой боли. Кроме того, воспалительный процесс может обусловливать снижение качества спермы (снижение концентрации, подвижности и жизнеспособности сперматозоидов) [37]. Th17-клетки представляют собой одну из подгрупп CD4+ Т-клеток, обусловливающих высвобождение цитокина ИЛ-17. Определено, что Th17-клетки принимают участие в патогенезе аутоиммунных заболеваний [38].
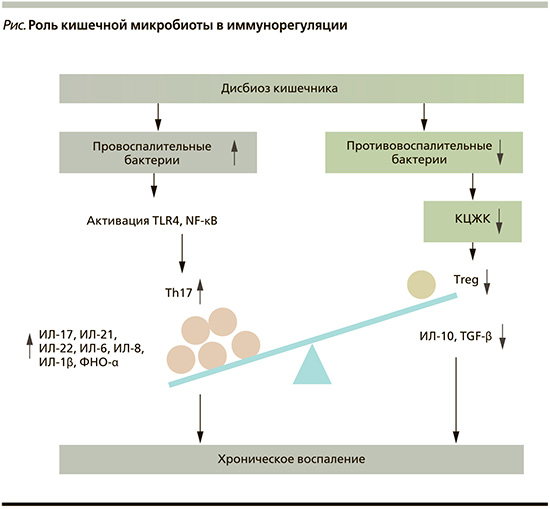
КМ оказывает несколько иммуномодулирующих функций и играет важную роль в модуляции иммунных/воспалительных реакций человека (см. рисунок) [37, 39, 40]. Исследователи связывают дисбиоз кишечника с развитием ряда аутоиммунных заболеваний, таких как системная красная волчанка и аутоиммунный тиреоидит [41, 42]. Установлено, что системные функции КМ, в т.ч. иммуномодуляция, в значительной степени связаны с микробным метаболомом, в особенности с КЦЖК. КЦЖК бактериального происхождения могут попадать в кровоток и принимать участие в регулировании иммунной системы, включая соотношение клеток Th17 и Treg во внекишечных органах, а также способствовать проникновению иммунных клеток кишечника в кровоток [43, 44].
С помощью экспериментальной модели аутоиммунного простатита проанализировано процентное содержание клеток Th17 и Treg в селезенке мышей с ХП и без такового. В результате доля Th17 в группе ХП оказалась значительно выше, чем в контрольной группе, тогда как содержание Treg было значительно ниже, что указывает на выраженный дисбаланс Th17/Treg в селезенке мышей с ХП. По сравнению с контрольной группой концентрации сывороточных противовоспалительных цитокинов TGF-β и ИЛ-10 были значительно снижены, в то время как уровни сывороточных провоспалительных цитокинов ИЛ-17, GM-CSF и IFNγ повышены [45]. Отмечено также значительное снижение альфа-разнообразия КМ у мышей с ХП. На уровне типа мыши с ХП имели меньшую относительную численность Firmicutes, Nitrospirae, Gemmatimonadetes и Fusobacteria. При этом обнаружено увеличение количества Bacteroidetes, Cyanobacteria и Patescibacteria. Установлено, что на уровне рода у мышей с ХП было заметно увеличено количество Lactobacillus [45]. В ходе исследования определено снижение концентрации пропионовой кислоты в фекалиях мышей с ХП относительно контрольной группы. Добавление пропионовой кислоты в воду значительно уменьшило признаки воспалительного процесса в ПЖ у мышей, а также снизило количество Th17-клеток в селезенке мышей, при этом способствуя дифференцировке Treg-клеток. Кроме того, пероральный прием пропионовой кислоты снижал выработку ИЛ-17 и GM-CSF, одновременно увеличивая секрецию TGF-β и ИЛ-10. Аналогичные результаты по уровням ИЛ-17, TGF-β и ИЛ-10 наблюдались в тканях ПЖ. Сообщается, что трансплантация фекальной микробиоты (ТФМ) от доноров с ХП здоровым реципиентам вызывала у них снижение дифференцировки Treg-клеток [45].
Коррекция кишечной микробиоты у пациентов с хроническим простатитом
Пациенты с ХП часто получают длительные курсы пероральных антимикробных препаратов, которые относят к одним из ведущих факторов нарушения состояния КМ [46, 47]. С учетом также высокой распространенности антибиотикорезистентности следует разрабатывать терапевтические подходы, позволяющие снижать повреждающее действие антимикробных препаратов на КМ или восстанавливать ее структуру и функции. На сегодняшний день изучению данной проблемы посвящены единичные исследования.
Одним из таких подходов может оказаться терапия с использованием пыльцы рапса, признанной одним из средств лечения ХП, способной также модулировать КМ. Определено, что такая терапия приводила к снижению массы простаты и отношения массы ПЖ к общей массе тела примерно на 32 и 36% соответственно, практически достигая показателей контрольной группы. Данное лечение также значительно уменьшило экспрессию провоспалительных цитокинов (ИЛ-6, -8, -1β и ФНО-α), подавляя патогенные бактерии и усиливая действие пробиотиков, особенно в соотношении Firmicutes-Bacteroidetes (F/B) и численности Prevotella [48].
В другом исследовании установлено, что полисахариды Poria cocos у крыс с ХП способствуют снижению массы ПЖ и ее отношения к общей массе тела, а также уровня С-реактивного белка и провоспалительных цитокинов (ФНО-α и ИЛ-1β) [49]. Poria cocos – широко известный древесный гриб, традиционно используемый в Китае в качестве пищевой и лекарственной добавки с антиоксидантной и противовоспалительной активностью. Одним из главных его компонентов являются полисахариды, ферментируемые в кишечнике человека микроорганизмами. В экспериментальной модели показано, что после ферментации Poria cocos фекальной микробиотой, полученной от здорового человека, значительный рост наблюдается у Parabacteroides, Fusicatenibacter и Parasutterella. Галоперидол-глюкуро-нид и 7-кетодеоксихолевая кислота, вырабатываемые этими бактериями, могут быть ответственными за повышенную экспрессию в эпителии толстой кишки генов Alox15 и Pla2g2f, ответственных за метаболизм арахидоновой кислоты, и сниженную экспрессию Cyp1a1 и Hsd17b7, регулирующих синтез стероидных гормонов. Вследствие такой регуляции происходит увеличение соотношения дигидротестостерона и эстрадиола в сыворотке, а активность ХП снижается. Кроме того, сообщается о росте количества Ruminococcus, ассоциированных с продукцией КЦЖК [50].
Особый интерес представляют результаты исследования эффективности различных пробиотиков в терапии ХП. Определено, что применение Lactobacillus paracasei CNCM I-1572 (по 2 капсулы в день в течение 3 месяцев) способствует статистически значимому снижению частоты обострений ХП и применения антимикробных препаратов. Установлено, что данный пробиотик модулирует КМ у лиц, страдающих воспалительными заболеваниями кишечника, а также влияет на иммунный ответ [51]. Сообщается о снижении концентрации провоспалительных цитокинов ИЛ-1α, -6, -8 и-15 и увеличении уровня КЦЖК и ИЛ-10 при приеме Lactobacillus paracasei CNCM I-1572 [52].
Заключение
Результаты современных исследований демонстрируют, что нарушения в составе и функционировании кишечной микробиоты могут быть связаны с хроническим простатитом. Дисбаланс между комменсальными и патогенными микроорганизмами в кишечной микробиоте может способствовать развитию воспалительного процесса в предстательной железе. Кишечная микробиота также может оказывать влияние на иммунную систему организма. Таким образом, определение взаимосвязи между состоянием кишечной микробиоты и развитием хронического простатита является актуальным направлением исследований. Наблюдаемые изменения кишечной микробиоты могут оказаться перспективными неинвазивными маркерами для диагностики хронического простатита, а также представлять собой потенциальные терапевтические цели.
Изучение роли кишечной микробиоты при хроническом простатите поможет расширить диагностические возможности в дополнение к используемым на сегодняшний день клиническим и лабораторным методам, способствовать повышению эффективности терапии данной категории пациентов.
Дополнительная информация
Публикация статьи осуществляется в рамках диссертационной работы: «Нарушение микробиоты кишечника и ее коррекция у пациентов с хроническим простатитом»



