Внедрение в клиническую практику, оценка эффективности и безопасности применения новых пероральных антикоагулянтов (НПАК) относятся к числу важнейших задач современной кардиологии. До недавнего времени в большинстве случаев пероральная антикоагулянтная терапия (АКТ) проводилась с помощью антагониста витамина К варфарина. Однако в клинической практике АКТ варфарином имеет ряд ограничений в связи с особенностями фармакодинамики, фармакокинетики, фармакогенетики препарата и необходимостью регулярного контроля международного нормализованного отношения (МНО). Эффективная и безопасная терапия варфарином возможна только при индивидуальном подборе дозы и постоянном контроле МНО, так как за пределами целевого диапазона (МНО от 2,0 до 3,0) снижается антитромботический эффект варфарина или увеличивается риск развития геморрагических осложнений.
Ограничения и трудности применения варфарина для длительной АКТ явились предпосылками к созданию НПАК, которые бы имели предсказуемые фармакологические характеристики, низкое пищевое и лекарственное взаимодействие, применялись в фиксированных дозировках, не требовали регулярного лабораторного контроля показателей свертывания крови и обладали благоприятным соотношением риска и ожидаемой пользы [1, 2]. Отличие НПАК заключается в механизме их действия: новые препараты селективно блокируют активные формы отдельных факторов коагуляционного каскада [1—4].
Среди препаратов этой группы выделяют прямые ингибиторы тромбина (дабигатран) и ингибиторы Ха фактора (ривароксабан, апиксабан, эдоксабан), фармакологические характеристики которых играют значительную роль в обеспечении эффективности и безопасности применения НПАК. К настоящему времени во многих клинических исследованиях получены доказательства эффективной АКТ при использовании препаратов нового поколения [1—3, 5—7].
Одним из НПАК является ривароксабан — первый селективный прямой ингибитор Ха фактора свертывания крови. Этот фактор играет ключевую роль в коагуляционном каскаде, образуя протромбиназный комплекс с Vа фактором, ионами кальция и тромбоцитарными фосфолипидами, который преобразует протромбин в тромбин. Особенностью действия ривароксабана является то, что препарат регулирует образование тромбина за счет блокирования активности Ха фактора, не оказывая на тромбин прямого действия. Такой механизм действия обеспечивает более эффективное предотвращение фибринообразования, чем инактивация тромбина, поскольку одна молекула Ха фактора приводит к образованию около 1000 молекул тромбина [2, 5—9].
Препарат обладает высокой биодоступностью при приеме (натощак 66%, с пищей 80—100%). Максимальная концентрация препарата в плазме крови и пик антикоагулянтного действия достигаются в течение 2—4 ч после приема внутрь. Период полувыведения составляет 5—13 ч. Примерно 2/3 препарата подвергается метаболизму и в дальнейшем выводится равными частями с мочой и калом. Оставшаяся часть выводится через почки в неизмененном виде [5, 8]. Возраст, пол, масса тела не оказывают существенного влияния на фармакокинетику ривароксабана.
 Внедренные в практику НПАК характеризуются благоприятным соотношением риска и пользы, но, как у всех лекарственных средств, у них есть риск развития побочных эффектов, среди которых самым опасным является внутреннее кровотечение. Результаты исследований II фазы по определению оптимальной дозировки ривароксабана свидетельствуют о том, что препарат имеет широкое терапевтическое окно с большим интервалом доз между возникновением антикоагулянтного эффекта и развитием кровотечения. На фоне терапии ривароксабаном не требуется мониторинга показателей свертывания крови и числа тромбоцитов [4, 8].
Внедренные в практику НПАК характеризуются благоприятным соотношением риска и пользы, но, как у всех лекарственных средств, у них есть риск развития побочных эффектов, среди которых самым опасным является внутреннее кровотечение. Результаты исследований II фазы по определению оптимальной дозировки ривароксабана свидетельствуют о том, что препарат имеет широкое терапевтическое окно с большим интервалом доз между возникновением антикоагулянтного эффекта и развитием кровотечения. На фоне терапии ривароксабаном не требуется мониторинга показателей свертывания крови и числа тромбоцитов [4, 8].
Соблюдение режима дозирования и частоты приема назначенного препарата играет важную роль в безопасности терапии антикоагулянтами [10—13]. Ингибирование активности Ха фактора при применении ривароксабана в дозе 20 мг продолжается в течение 24 ч, что обеспечивает необходимую для профилактики тромбозов и эмболий антикоагуляцию при приеме 1 раз в сутки. У пациентов с нарушением функции почек и расчетным клиренсом креатинина (КК) 30—49 мл/мин рекомендована доза 15 мг/сут, которая была изучена у больных хронической болезнью почек в проспективном исследовании ROCKET AF [5, 8, 14—16]. Регулярное применение препарата в фиксированной дозировке позволяет добиться стабильной гипокоагуляции, не требующей постоянной коррекции и регулярного лабораторного контроля [5, 11]. Однократное применение обеспечивает лучшую приверженность пациентов лечению [8, 12, 13]. F. Laliberte и соавт. был выполнен анализ 29 клинических исследований, в которых оценивалось влияние кратности приема препаратов в течение суток на приверженность пациентов к лечению [10]. Согласно полученным результатам, при назначении препарата 1 раз в сутки пациенты чаще выполняют рекомендации врача. К числу других важных характеристик ривароксабана относят низкий риск взаимодействия с пищевыми продуктами и другими лекарственными средствами.
Ривароксабан имеет наибольшее среди всех НПАК число зарегистрированных в Российской Федерации и странах Европейского союза показаний. Применение ривароксабана одобрено в мире по 7 показаниям: профилактика венозной тромбоэмболии у пациентов, подвергающихся большим ортопедическим хирургическим вмешательствам на нижних конечностях; профилактика инсульта и системной тромбоэмболии у пациентов с фибрилляцией предсердий (ФП) неклапанного происхождения; лечение тромбоза глубоких вен (ТГВ); профилактика рецидивов ТГВ; лечение тромбоэмболии легочной артерии (ТЭЛА); профилактика рецидивов ТЭЛА; профилактика смерти вследствие сердечно-сосудистых причин и инфаркта миокарда (ИМ) после острого коронарного синдрома, протекавшего с повышением кардиоспецифических биомаркеров, в комбинированной терапии с ацетилсалициловой кислотой или с ацетилсалициловой кислотой и тиенопиридинами (клопидогрелом или тиклопидином). В России зарегистрированы все 7 перечисленных показаний для препарата ксарелто.
В 2012 г. было зарегистрировано показание к назначению ривароксабана — профилактика инсульта и системной тромбоэмболии у пациентов с ФП неклапанного происхождения. ФП является одним из наиболее распространенных в общей популяции нарушений ритма сердца, которое ассоциируется с повышением риска развития тромбоэмболических осложнений (ТЭО), сердечной недостаточности (СН), ухудшением качества жизни и риска смерти. Частота развития ФП в общей популяции составляет 1—2%. В связи со старением популяции ожидается увеличение числа пациентов, страдающих ФП, с 2,3 млн в 2000 г. до 5,6 млн к 2050 г. [14, 15].
Согласно результатам крупных эпидемиологических исследований, ФП в 5 раз увеличивает риск развития инсульта и в 2 раза — сердечно-сосудистой смерти [14—16]. Несмотря на достижения современной медицины число инсультов постоянно растет и прогноз по-прежнему остается неблагоприятным. С 1990 по 2010 г. количество смертей от инсульта увеличилось на 26%, а инвалидизация вследствие перенесенного инсульта — на 19% [14, 15].
Неклапанная ФП является наиболее частой причиной кардиогенной эмболии мозга. У больных неклапанной ФП риск развития церебральных осложнений в 5—6 раз выше, чем у пациентов с синусовым ритмом. К неклапанной форме относят ФП при отсутствии ревматического митрального стеноза, механических или биопротезированных клапанов сердца, реконструктивных вмешательств на митральном клапане. Причиной ТЭО в большинстве случаев служит тромбоз ушка левого предсердия [16—21].
Ведение больных ФП остается сложной терапевтической задачей, требующей соответствия доказательно обоснованным принципам лечения и индивидуального подхода к определению лечебной тактики, основанного на использовании шкал оценки риска развития ТЭО — CHADS2 и CHA2DS2-VASc [16, 18, 22]. Решение вопроса о проведении АКТ и выбор препарата относят к числу первоочередных задач при выработке тактики ведения больного ФП. Лидирующие позиции в профилактике ТЭО при неклапанной ФП занимают НПАК [19]. По данным мета-анализа R.G. Hart и соавт. (2007), АКТ способствует снижению риска развития инсульта и смерти на 64 и 25% соответственно [23].
С внедрением НПАК изменились подходы к профилактике инсульта при неклапанной ФП, а также возросло значение дальнейших исследований для расширения возможностей использования НПАК в клинической практике [24—28]. Основными критериями назначения препарата должны быть высокая эффективность в предупреждении тромбоэмболических событий и безопасность проводимой терапии.
В крупных многоцентровых исследованиях НПАК дабигатран (RE-LY) [29], ривароксабан (ROCKET AF) [30] и апиксабан (ARISTOTLE) [31] продемонстрировали ряд преимуществ у больных неклапанной ФП по сравнению с варфарином.
Доказательства эффективности и безопасности ривароксабана. Результаты исследования ROCKET AF. В международном проспективном рандомизированном двойном слепом плацебо-контролируемом исследовании III фазы ROCKET AF (Rivaroxaban Once daily oral direct factor Xa inhibition Compared with vitamin K antagonism for prevention of stroke and Embolizm Trial in Atrial Fibrillation) сравнивалась эффективность ривароксабана и варфарина для профилактики ишемического инсульта и тромбоэмболии сосудов большого круга кровообращения у пациентов с неклапанной ФП.
В исследование были включены 14 264 пациента старше 18 лет (60,3% мужчин) с персистирующей или пароксизмальной ФП, наличием в анамнезе инсульта, транзиторной ишемической атаки (ТИА) или системной эмболии (СЭ), или двух факторов риска и более (возраст >75 лет, систолическое артериальное давление — АД>180 мм рт.ст. или диастолическое АД>100 мм рт.ст., клинические признаки СН и/или фракция выброса левого желудочка <35%, сахарный диабет). Инсульт, ТИА или СЭ до включения в исследование перенесли 54,8% пациентов. В отличие от других исследований с НПАК пациенты в исследовании ROCKET AF имели более высокий риск развития инсульта по шкале CHADS2 (>2 баллов), при этом 87% включенных пациентов имели оценку риска >3 баллов. Среднее число баллов по шкале CHADS2 составило 3,5 [30]. Таким образом, в исследование ROCKET AF было включено большое число пациентов с сочетанной патологией, что приближает популяцию этого исследования к клинической практике.
 Критериями исключения являлись патология клапанов, ФП, вызванная потенциально обратимыми причинами, планируемая кардиоверсия, высокий риск кровотечения, тяжелая почечная и печеночная недостаточность.
Критериями исключения являлись патология клапанов, ФП, вызванная потенциально обратимыми причинами, планируемая кардиоверсия, высокий риск кровотечения, тяжелая почечная и печеночная недостаточность.
Средний возраст включенных в исследование пациентов составлял 73 года.Пациенты были рандомизированы в 2 группы, получавшие ривароксабанв дозе 20 мг 1 раз в сутки или варфарин в дозе, необходимой для достижения целевого МНО (2,0—3,0). Пациенты с умеренной почечной недостаточностью (КК 30—49 мл/мин) получали ривароксабан в дозе 15 мг 1 раз в сутки. Медиана продолжительности исследования составила 590 дней.
Первичная конечная точка оценки эффективности включала инсульт и системные тромбоэмболии. Первичная конечная точка оценки безопасности была комбинированной и включала суммарную частоту больших и клинически значимых небольших кровотечений. К большим относились кровотечения с летальным исходом, кровотечения из жизненно важного органа (интракраниальные, интраспинальные, перикардиальные и пр.), а также кровотечения, сопровождавшиеся снижением уровня гемоглобина на >2 г/дл или потребовавшие переливания >2 доз цельной крови или эритроцитарной массы [30].
В исследовании была продемонстрирована эффективность ривароксабана в профилактике инсульта и СЭ при неклапанной ФП. При анализе популяции в соответствии с полученным лечением ривароксабан в дозе 20 мг/сут (15 мг/сут у пациентов с КК 30—49 мл/мин) по эффективности превосходил варфарин и показал снижение относительного риска (ОР) развития инсульта и СЭ на 21% [30, 32]. Частота развития инсульта и СЭ в группах ривароксабана и варфарина составила 1,7 и 2,2 на 100 пациенто-лет соответственно (ОР 0,79 при 95% доверительном интервале — ДИ от 0,65 до 0,95; p=0,01). При анализе общей смертности в группах ривароксабана и варфарина различия не обнаружены (1,9 и 2,2% соответственно; ОР 0,85 при 95% ДИ от 0,70 до 1,02; p=0,07).
Согласно результатам исследования, ривароксабан не отличался от варфарина по показателям безопасности. Суммарная частота побочных эффектов в обеих группах была одинаковой. По совокупности больших и клинически значимых небольших кровотечений различия в группах ривароксабана и варфарина не выявлены — 14,91 и 14,52% соответственно (ОР 1,03 при 95% ДИ от 0,96 до 1,11; p=0,442). Частота больших кровотечений у пациентов, принимавших ривароксабан и варфарин, также оказалась сопоставимой — 3,6 и 3,4% на 100 пациенто-лет соответственно (p=0,58) [30].
Анализ структуры кровотечений показал преимущество ривароксабана по сравнению с варфарином в отношении кровотечений, влияющих на прогноз. В группе ривароксабана было отмечено меньшее число фатальных кровотечений (0,24 и 0,48% соответственно; p=0,003) и кровотечений из жизненно важных органов (0,82 и 1,18% соответственно; p=0,007). Внутричерепные кровотечения также существенно реже отмечались в группе пациентов, принимавших ривароксабан, по сравнению с группой варфарина — 0,5 и 0,7% соответственно (ОР 0,67 при 95% ДИ от 0,47 до 0,93; p=0,019). В то же время в группе ривароксабана частота кровотечений из желудочно-кишечного тракта была выше, чем в группе варфарина (3,2 и 2,2% соответственно; p<0,001) [30].
Впервые в клиническом исследовании III фазы ROCKET AF было показано, что НПАК ривароксабан по сравнению с варфарином имеет более благоприятный профиль безопасности. При одинаковом общем количестве кровотечений в группе ривароксабана было значительно меньше жизнеугрожающих кровотечений, таких как внутричерепные, и кровотечений с летальным исходом.
Следующим важным этапом изучения препарата является подтверждение данных, полученных в рандомизированных клинических исследованиях, в наблюдательных исследованиях клинической практики. Необходимость в проведении подобных исследований обусловлена тем, что наблюдение в специально организованном исследовании может способствовать повышению эффективности и безопасности лечения за счет жестких критериев отбора пациентов, регулярных визитов, обеспечивающих более высокую приверженность к лечению, постоянного мониторирования безопасности.
 В настоящее время продолжается масштабная программа изучения эффективности и безопасности ривароксабана в клинической практике. Так, недавно завершившееся исследование XANTUS дополняет и подтверждает данные, полученные в исследовании ROCKET AF.
В настоящее время продолжается масштабная программа изучения эффективности и безопасности ривароксабана в клинической практике. Так, недавно завершившееся исследование XANTUS дополняет и подтверждает данные, полученные в исследовании ROCKET AF.
Результаты исследования XANTUS. На Европейском конгрессе кардиологов 2015 г. (Лондон) компания Bayer HealthCare и ее партнер по разработкам компания Janssen Pharmaceuticals Inc. объявили результаты исследования XANTUS. В исследовании было показано, что частота больших кровотечений у пациентов с ФП, принимающих пероральный ингибитор Ха фактора ривароксабан для профилактики инсульта в повседневной клинической практике, была низкой и соответствовала результатам клинического исследования III фазы ROCKET AF.
Исследование XANTUS представляло собой международное проспективное неконтролируемое наблюдательное исследование, целью которого являлась оценка безопасности и эффективности ривароксабана в клинической практике у 6784 пациентов с неклапанной ФП из 311 центров Европы, Канады и Израиля [33, 34].
В исследование включали пациентов с неклапанной ФП в возрасте >18 лет. Решение о лечении и дозировке ривароксабана принималось лечащим врачом после получения подписанного информированного согласия пациента на участие в исследовании. Подбор дозы препарата проводили с учетом функционального состояния почек. Пациентам с нормальной или незначительно сниженной функцией почек (КК>50 мл/мин) ривароксабан назначали в дозе 20 мг 1 раз в сутки. Пациенты с умеренной или выраженной почечной недостаточностью (КК 15—49 мл/мин) получали ривароксабан в дозе 15 мг 1 раз в сутки. Большинство включенных пациентов (78,7%) принимали ривароксабан в дозе 20 мг/сут, что соответствует данным, полученным в исследовании ROCKET AF [30].
До включения в исследование антитромботическая терапия пациентов включала варфарин (40,8%), дабигатран (3,1%), ацетилсалициловую кислоту (18%), двухкомпонентную антитромбоцитарную терапию (1%), гепарин (32%). Клиническая характеристика пациентов, включенных в исследование, представлена в табл. 1.
Наблюдение за пациентами продолжалось в течение одного года или 30 дней в случае досрочного прекращения лечения. Период наблюдения составил в среднем 329 дней. После завершения исследования 75,1% пациентов сообщили своему врачу, что они были «очень удовлетворены» или «удовлетворены» лечением [34].
ТО и кровотечения централизованно оценивались независимым комитетом экспертов. К концу периода наблюдения у 96,1% пациентов на фоне лечения не было зарегистрировано случаев инсульта/СЭ, больших кровотечений, смерти от всех причин.
Частота ТЭО, таких как инсульт/СЭ, ТИА, ИМ, составила 0,8, 0,5 и 0,4 на 100 пациенто-лет соответственно. Частота инсульта составила 0,7 событий на 100 пациенто-лет. Геморрагический инсульт был выявлен у 11 (0,2%) пациентов, ишемический — у 32 (0,5%). Тромбоз левого предсердия был выявлен у 6 пациентов (0,1 на 100 пациенто-лет). Важно отметить, что высокоэффективная профилактика инсульта была продемонстрирована в группах пациентов как высокого, так и умеренного (CHA2DS2-VASc=1 балл) риска.
Частота больших кровотечений, связанных с применением ривароксабана, была низкой и составила 2,1 на 100 пациенто-лет. При дальнейшем анализе результатов исследования была показана зависимость частоты больших кровотечений от возраста пациентов. Так, у пациентов моложе 65 лет частота больших кровотечений составляла 0,9 на 100 пациенто-лет, в возрасте от 65 до 75 лет — 1,7 на 100 пациенто-лет, у пациентов старше 75 лет — 3,2 на 100 пациенто-лет.
Кроме того, частота больших кровотечений анализировалась в зависимости от функционального состояния почек. КК был определен у 4452 (65,6%) пациентов, из них у 14,4% выявлено снижение функции почек (КК<50 мл/мин). Частота больших кровотечений была выше (3,4%) у пациентов с КК<50 мл/мин [34]. Для лечения большинства кровотечений использовали стандартные клинические алгоритмы [35].
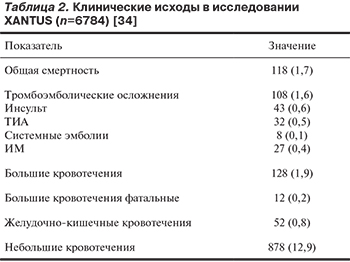
Частота кровотечений с летальным исходом в период наблюдения составила 0,2 на 100 пациенто-лет, кровотечений из жизненно важных органов — 0,7 на 100 пациенто-лет, внутричерепных кровотечений — 0,4 на 100 пациенто-лет. Клинические исходы у пациентов с неклапанной ФП представлены в табл. 2.
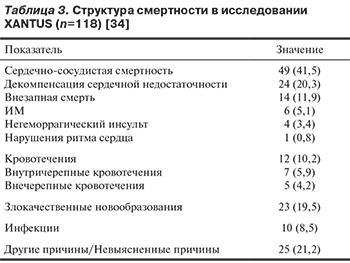
Частота летальных исходов от всех причин во время лечения составила 1,9 на 100 человеко-лет. Анализ структуры сердечно-сосудистой смертности показал наибольший вклад декомпенсации СН (20,3%) как причины смерти (табл. 3). Кроме того, обращает на себя внимание сопоставимое с СН число случаев смерти в связи со злокачественными новообразованиями (19,5%).
Анализ результатов исследования проводился в зависимости от дозы ривароксабана. Частота развития ТЭО, больших кровотечений и всех случаев смерти ожидаемо была выше при применении дозы ривароксабана 15 мг, назначенной пациентам с нарушенной функцией почек и более высоким риском по сравнению с дозой 20 мг/сут. Частота развития ТЭО (инсульт/СЭ, ТИА, ИМ) при применении ривароксабана в дозах 15 и 20 мг составила 2,3 и 1,6 на 100 пациенто-лет соответственно, частота больших кровотечений —3,1 и 1,8 случаев на 100 пациенто-лет соответственно, общая смертность — 3,7 и 1,4 на 100 пациенто-лет соответственно [34].
Сравнивая результаты исследований XANTUS и ROCKET AF, следует отметить, что средняя оценка риска развития ТЭО по шкале CHADS2 в исследовании XANTUS составляла 2,0 балла, инсульт/ТИА в анамнезе имелся у 19% пациентов. В исследовании ROCKET AF у пациентов имелся более высокий риск развития ТЭО, средняя оценка по шкале CHADS2 составила 3,5 балла, инсульт/ТИА до включения в исследование перенесли 55% пациентов [30]. Частота развития инсульта была ниже в исследовании XANTUS (0,7 на 100 пациенто-лет) по сравнению с результатами исследования ROCKET AF (1,7 на 100 пациенто-лет).
Различия выявляются и при анализе частоты больших кровотечений в сравниваемых исследованиях. При применении ривароксабана в исследовании XANTUS частота больших кровотечений была ниже и составила 2,1 на 100 пациенто-лет, в то время как в исследовании ROCKET AF частота больших кровотечений у пациентов, принимавших ривароксабан, составляла 3,6 на 100 пациенто-лет. Частота фатальных, критических и внутричерепных кровотечений в исследованиях XANTUS и ROCKET AF оказалась сопоставимой: фатальных (0,2 и 0,2 на 100 пациенто-лет соответственно), кровотечений из жизненно важных органов (0,7 и 0,8 на 100 пациенто-лет соответственно), внутричерепных (0,4 и 0,5 на 100 пациенто-лет соответственно). Частота больших желудочно-кишечных кровотечений в исследовании XANTUS была меньше (0,9 на 100 пациенто-лет соответственно), чем в исследовании ROCKET AF (2,0 на 100 пациенто-лет соответственно) [30, 34].
Сравнительная оценка результатов исследования ROCKET AF и наблюдательного исследования в условиях клинической практики XANTUS показала, что в различных исследуемых популяциях пациентов оказалась сопоставимой частота фатальных, критических и внутричерепных кровотечений. Особого внимания заслуживает то, что в повседневной клинической практике применение ривароксабана сопровождалось более низкой частотой больших и желудочно-кишечных кровотечений.
Таким образом, недавно завершившееся первое международное проспективное исследование по оценке безопасности и эффективности ривароксабана в клинической практике XANTUS дополняет данные, полученные в исследовании ROCKET AF, подтверждает положительный баланс риск/польза при применении препарата у пациентов с неклапанной ФП.
Постмаркетинговое исследование безопасности ривароксабана.На Европейском конгрессе кардиологов 2015 г. (Лондон) компания Bayer HealthCare и ее партнер по разработкам компания Janssen Pharmaceuticals Inc. объявили промежуточные результаты постмаркетингового исследования безопасности (ПМИБ) ривароксабана (ксарелто).
ПМИБ представляет собой продолжающееся 5-летнее ретроспективное наблюдательное исследование в США, разработанное с целью анализа случаев больших кровотечений, факторов риска и связанных с кровотечением клинических исходов у пациентов с неклапанной ФП, принимающих ривароксабан. Исследователи проанализировали данные, полученные с 1 января 2013 г. по 31 декабря 2014 г. с использованием комплексной системы электронных медицинских записей Министерства обороны США. Случаи больших кровотечений были установлены с использованием валидизированного алгоритма Каннингема (2011), который в целом соответствовал, но не был идентичен определению больших кровотечений в клинических исследованиях, поскольку опирался на ретроспективные электронные медицинские данные [36].
Продолжающееся в настоящее время исследование включает 39 052 пациентов с неклапанной ФП. Анализ результатов первых 2 лет наблюдения в ПМИБ свидетельствует, что при применении ривароксабана для профилактики инсульта в повседневной клинической практике частота больших кровотечений соответствует результатам исследований ROCKET AF и XANTUS. Согласно данным промежуточного анализа, частота больших кровотечений составила 2,9 на 100 пациентолет [36]. Таким образом, результаты ПМИБ дополнительно подтверждают благоприятный профиль безопасности ривароксабана.
Результаты двух исследований, которые в совокупности включают более 45 000 пациентов из Европы, России, Канады и США, подтверждают низкую частоту кровотечений при применении ривароксабана.
Исследования XANTUS и ПМИБ являются частью обширной продолжающейся программы оценки эффективности и безопасности ривароксабана, которая в общей сложности будет включать более 275 000 пациентов как в рандомизированных клинических исследованиях, так и в исследованиях клинической практики.
Заключение
В современной клинической практике возрастает частота использования новых пероральных антикоагулянтов для профилактики инсульта и системных эмболий у больных неклапанной фибрилляцией предсердий. В крупных рандомизированных клинических исследованиях получены доказательства эффективности и безопасности ривароксабана и показаны преимущества его применения. Новые данные реальной клинической практики подтверждают низкую частоту больших кровотечений при применении препарата ривароксабана (ксарелто, «Bayer») у пациентов с неклапанной фибрилляцией предсердий.



