Введение
Рак эндометрия (РЭ) является наиболее распространенной гинекологической злокачественной опухолью в странах с высоким и средним уровнями дохода. Так, по данным GLOBOCAN, в 2020 г. в мире зарегистрировано 417 367 случаев заболеваемости РЭ, из которых 358 908 (86%) – в странах с высоким и выше среднего доходами на душу населения [1]. В странах Африки, Азии и Латинской Америки с относительно низким уровнем доходов населения заболеваемость РЭ уступает раку шейки матки и яичников. Такая статистика обусловлена патогенезом РЭ, в котором ведущая роль принадлежит метаболическому синдрому, прежде всего ожирению.
Отличительной чертой РЭ является появление симптомов на ранних стадиях заболевания в виде маточных кровотечений. Этим объясняется раннее обращение пациенток к врачу и высокий процент (более 70%) выявления ранних стадий заболевания, благодаря чему прогноз при РЭ относительно благоприятный. Пятилетняя относительная выживаемость женщин в Европе, которым был диагностирован РЭ в 2000–2007 гг., составила 76% [2]. Пятилетняя выживаемость женщин СЗФО РФ, которым в 2010–2014 гг. был диагностирован РЭ, составила 71,4% [3]. Пятилетняя выживаемость больных РЭ значительно ниже при местнораспространенном и диссеминированном процессах. Так, по данным популяционного ракового регистра Санкт-Петербурга, наблюдаемая 5-летняя выживаемость больных раком тела матки при III и IV стадиях составляет 40 и 12% соответственно [3]. Несмотря на относительно благоприятный общий прогноз, РЭ имеет тенденцию к рецидивированию. Не менее 30% больных РЭ умирают в течение 5-летнего периода наблюдения от рецидивов и метастазов.
Большой вклад в понимание патогенеза РЭ внес выдающийся отечественный онкогинеколог профессор Я.В. Бохман, который в 1972 (1983) г. предложил дуалистическую модель канцерогенеза РЭ, основанную на клинических наблюдениях и клинико-патологических корреляциях [4, 5]. Основываясь на клинико-патологических наблюдениях за 366 случаями РЭ, Я.В. Бохман предположил, что существует два основных типа карциномы эндометрия. Большинство случаев РЭ (приблизительно 70–80%), обозначаемых как карциномы I типа, связано с гормональным дисбалансом и развиваются по эстроген-зависимому пути. Гистологически большинство опухолей I типа возникают на фоне гиперпластического эндометрия, демонстрируют эндометриоидную дифференцировку и имеют низкую степень злокачественности. Клинически они в целом характеризуются благоприятным клиническим течением и прогнозом. Еще 10–20% случаев РЭ, обозначаемых как карциномы II типа, не связаны с гормональными нарушениями и возникают на фоне атрофического эндометрия, чаще в постменопаузальном возрасте, примерно на 5–10 лет позже, чем опухоли I типа. Обычно это карциномы высокой степени злокачественности неэндометриоидной дифференцировки, чаще серозные, реже светлоклеточные. Карциномы типа II характеризуются агрессивным клиническим течением и плохим прогнозом. Эта дуалистическая модель впоследствии была подтверждена молекулярными исследованиями примерно десять лет спустя [6].
Новая молекулярная классификация рака эндометрия
Исследовательская сеть Атласа генома рака (TCGA) в 2013 г. опубликовала результаты углубленного полногеномного анализа карцином эндометрия у более чем 350 пациенток [7]. Основываясь на ряде геномных особенностей, авторы предлагают реклассификацию опухолей эндометрия на четыре различных типа. Эти интегрированные геномный и протеомный анализы 373 видов рака эндометрия дают представление о биологии заболеваний и диагностической классификации РЭ. Анализ, проведенный TCGA, выявил четыре молекулярных подтипа карцином эндометрия: подгруппа с ультрамутированным POLE (POLE mut), характеризуется патогенными вариантами экзонуклеазного домена ДНК-полимеразы-эпсилон (POLE); подгруппа с гипермутированной микросателлитной нестабильностью (MSI); подгруппа с низким числом копий и низкой мутационной нагрузкой; подгруппа с высоким числом копий и частыми мутациями TP53. Было показано, что эти молекулярные подгруппы четко коррелируют с беспрогрессивной и общей 5-летней выживаемостью больных (см. рисунок) [14].
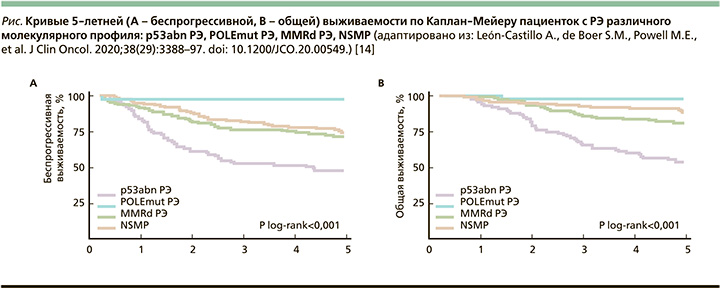
Комплексный геномный анализ карцином эндометрия, проведенный сетью TCGA, показал, что в ряде случаев молекулярный анализ может переклассифицировать гистологический тип опухоли и потенциально влиять на планирование лечения [8], что привело к созданию в 2020 г. новой гистологической классификации ВОЗ по РЭ [9].
Определение групп прогностического риска с использованием молекулярных маркеров
Несмотря на первоначальный успех подтипов TCGA в идентификации различных молекулярных подгрупп РЭ, оказалось, что их использование в клинической практике затруднено. Поэтому для определения прогноза пациентки разработана упрощенная система классификации (Проактивный классификатор молекулярного риска при РЭ – ProMisE). [10]. В классификации ProMisE используются три иммуногистохимических маркера: p53 дикого типа (p53 wt), аномалия p53 (p53 abn), белки репарации ошибочного спаривания (MMR), включая MSH6 и PMS2), и один молекулярный маркер: мутация экзонуклеазного домена POLE (POLE EDM или POLEmut), чтобы разделить больных РЭ на четыре подгруппы. Эти подгруппы включают: 1) подтип с дефицитом MMR (MMRd), аналогичный подтипу TCGA «MSI»; 2) подтип с мутациями в POLE, аналогичный «ультрамутированному» подтипу TCGA; 3) подтип с плохим прогнозом, характеризующийся аномалиями р53, аналогичный подтипу TCGA с «высоким числом копий», и 4) p53 дикого типа и без специфического мутационного профиля (NSMP) аналогично подтипу TCGA с «низким числом копий» [11].
Прогностическая ценность молекулярной классификации подтверждена массой публикаций, в которых последовательно сообщалось о ее прогностической значимости, особенно при опухолях высокой степени злокачественности и высоком риске, в нескольких независимых когортах и проспективных клинических исследованиях [12–14].
Классификацию молекулярного риска при РЭ поддержали Международное общество гинекологических патологов и Манчестерская международная консенсусная группа [15]. C 2021 г. молекулярное тестирование всем пациенткам с РЭ рекомендовали различные международные организации, в т.ч. NCCN [16], Европейское общество гинекологической онкологии [17] и Китайский экспертный консенсус по молекулярному обнаружению РЭ [18].
В обновленных рекомендациях ESGO/ESTRO/ ESP [17] предлагается определять группы прогностического риска в обоих случаях: когда молекулярная классификация известна или не известна (табл. 1).
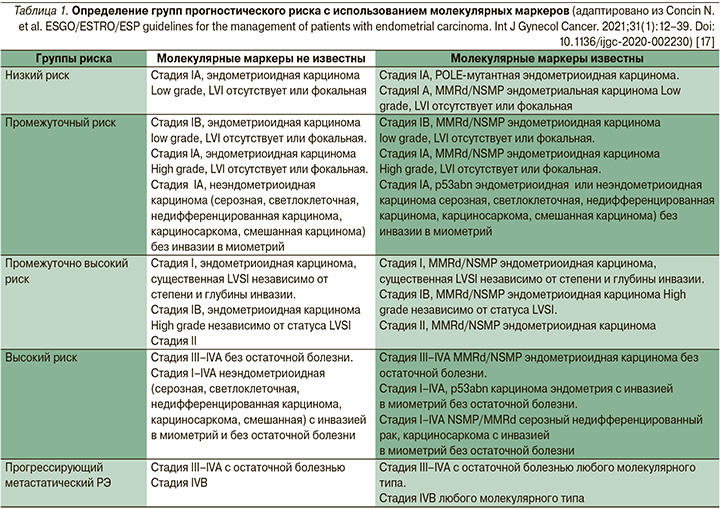
Тем не менее молекулярную классификацию рекомендуется применять при всех карциномах эндометрия, особенно при опухолях высокой степени злокачественности. Анализ мутаций POLE может не проводиться при РЭ низкого и промежуточного рисков в случае эндометриоидной карциномы низкой степени злокачественности [17]. У всех пациенток с РЭ следует регистрировать гистопатологический тип опухоли, степень дифференцировки, инвазию в миометрий и лимфо-васкулярную инвазию (LVSI). Последняя может быть очаговой, значительной или отсутствовать. Международная федерация гинекологии и акушерства (FIGO) для обозначения степени дифференцировки опухоли рекомендует использовать бинарную классификацию, которая рассматривает карциномы 1-й и 2-й степеней как низкой степени риска (low grade) карциномы, а низкодифференцированные карциномы 3-й степени – как карциномы высокой степени риска (high-grade) (табл. 2) [18].
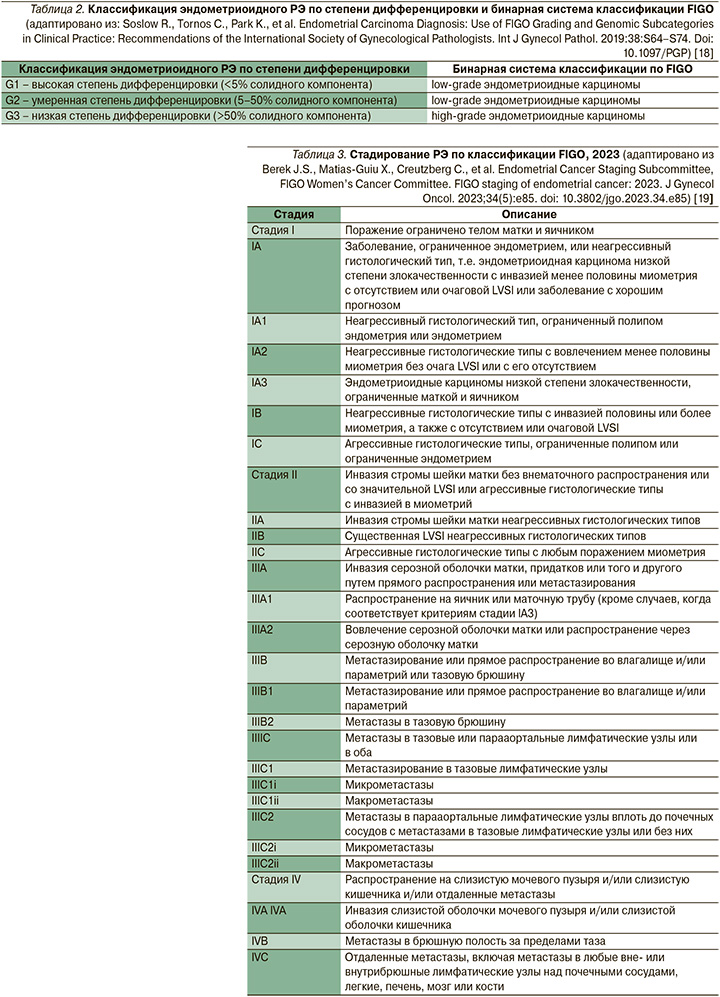
Стадирование РЭ по Классификации Международной федерации гинекологии и акушерства (FIGO) 2023 г.
Создание новой молекулярной классификации и определение новых прогностических маркеров повлияли и на изменение системы стадирования РЭ, предыдущий вариант которой был принят FIGO в 2009 г. В 2023 г. опубликована пересмотренная система стадирования по FIGO [19].
Классификация FIGO 2023 г. включает серьезные изменения для стадии I, где появилась подстадия IA3, при которой заболевание, ограниченное эндометриоидными карциномами низкой степени злокачественности, поражает эндометрий и яичники (табл. 3).
Ранее они были описаны как синхронные независимые опухоли, но молекулярный анализ установил их общее клональное происхождение [20]. FIGO одобрила критерии ВОЗ и рекомендации ESGO-ESTRO-ESP для идентификации этой группы опухолей, которые классифицируются как IA3-стадия [9, 17].
Считается, что одновременное поражение как эндометрия, так и яичников имеет хороший прогноз [21, 22] и адъювантное лечение не рекомендуется, если соблюдены все ниже перечисленные критерии: 1) присутствие не более чем поверхностной инвазии миометрия (<50%); 2) отсутствие обширной/существенной LVSI; 3) отсутствие дополнительных метастазов и 4) опухоль яичника односторонняя, ограничена яичником, без инвазии/разрыва капсулы (эквивалентно pT1a).
Комитет FIGO рекомендовал, когда это возможно, добавление молекулярного подтипа к критериям стадирования, что позволяет лучше предсказывать прогноз при стадировании (табл. 3). Выполнение полной молекулярной классификации (POLEmut, MMRd, NSMP, p53abn) рекомендуется во всех случаях РЭ для прогностической стратификации групп риска и в качестве потенциальных влияющих факторов при принятии решений об адъювантном или системном лечении. Определение молекулярного подтипа может быть выполнено при биопсии, и в этом случае его не нужно повторять при гистерэктомии, но при выполнении они должны регистрироваться на всех этапах [19].
Комитет FIGO рекомендует стадировать РЭ на основе хирургических/анатомических и гистологических результатов. В случае, если молекулярная классификация выявит ПОЛЕмут или статус p53abn, стадия FIGO изменяется на ранней стадии заболевания. Это обозначено в стадии FIGO добавлением буквы «m» для молекулярной классификации, и добавлен нижний индекс для обозначения POLEmut или статуса p53abn.
Статус MMRd или NSMP не влияет на ранние стадии РЭ, но, если же молекулярная классификация выявляет MMRd или NSMP, это должно быть записано как стадия ImMMRd или стадия ImNSMP и стадия IImMMRd или стадия IImNSMP [19].
При III и IV стадиях, если молекулярная классификация известна, ее следует записать как стадию IIIm или стадию IVm с соответствующим индексом для целей сбора данных. Например, когда молекулярная классификация выявляет p53abn, его следует записать как стадию IIImp53abn или стадию IVmp53abn [19].
Согласно рекомендациям комитета FIGO 2023 г., при раннем РЭ стандартной операцией является тотальная гистерэктомия с двусторонней сальпингоофорэктомией с использованием минимально инвазивного лапароскопического доступа. Процедуры стадирования включают оментэктомию на уровне поперечно-ободочной кишки при определенных гистологических подтипах, таких как серозная и недифференцированная карцинома эндометрия, а также карциносаркома, из-за высокого риска микроскопических метастазов в сальнике. Стадирование рака лимфатических узлов следует проводить пациенткам среднего и высокого риска. Биопсия SLN является адекватной альтернативой систематической лимфаденэктомии для определения предполагаемой стадии. Биопсия SLN также может быть рассмотрена у пациенток с низким / промежуточным риском, чтобы исключить скрытые метастазы в лимфатические узлы и выявить заболевание, действительно локализованное в матке. Таким образом, рекомендации ESGO-ESTRO-ESP допускают применение SLN у всех пациенток с карциномой эндометрия, что одобрено FIGO. При предполагаемом раннем раке эндометрия биопсия SLN является адекватной альтернативой систематической лимфаденэктомии в случаях высокого промежуточного и высокого риска с целью определения стадии рака лимфатических узлов, а также может быть рассмотрена при заболеваниях низкого/промежуточного риска для исключения скрытых метастазов в лимфатические узлы. Биопсию SLN следует проводить в сочетании с тщательным (ультрастадирующим) стадированием, поскольку это повысит выявляемость малообъемного заболевания в лимфатических узлах.
Как влияет установление стадии с учетом молекулярных данных на выбор метода лечения первичных больных РЭ
Большое влияние новые классификации РЭ оказали на выбор адъювантной терапии. Рекомендации по адъювантному лечению РЭ зависят от группы прогностического риска (табл. 1). Пациенткам с карциномой эндометрия низкого риска не рекомендуется адъювантное лечение на основании данных многочисленных рандомизированных исследований [23, 24].
Для пациенток с карциномами эндометрия I–II стадий с мутацией POLE отсутствие адъювантного лечения представляется оправданным на основании данных исследований, показывающих очень небольшое количество рецидивов в случаях наблюдения [25, 26]. От пациенток с карциномой эндометрия III–IVA-стадий и патогенной мутацией POLE в настоящее время не получено данных об исходах в отсутствие адъювантного лечении и рекомендованы дальнейшие проспективные исследования [17].
При карциномах p53abn, ограниченных полипом или без инвазии в миометрий, пациенткам промежуточного риска адъювантная терапия обычно не рекомендуется [17].
У пациенток высокого промежуточного риска при pN0 после стадирования лимфатических узлов молекулярный анализ тканей в исследовании PORTEC-3 не выявил преимуществ химиотерапии при карциномах MMRd [14, 27]. Отказ от адъювантного лечения является одним из вариантов, и его следует рассматривать, только когда гарантировано тщательное наблюдение для обеспечения выявления и оперативного лечения рецидива на ранней стадии. При значительной LVSI и при II стадии может быть рекомендована дистанционная лучевая терапия, а при high grade-карциномах и значительной LVSI может быть назначена химиотерапия [17].
Пациенткам высокого промежуточного риска при N0/pNx, когда стадирование лимфатических узлов не проводилось, рекомендуется адъювантная дистанционная лучевая терапия, особенно при значительной LVSI и/или при II стадии. Также может быть рассмотрена адъювантная химиотерапия, особенно при high grade-карциномах и/или значительной LVSI. Адъювантная брахитерапия может быть рассмотрена при high grade-карциномах и отрицательных результатах LVSI у пациенток с I стадией [17].
Карциномы высокого риска в новой классификации представляют собой либо стадию III–IVA без остаточного заболевания, либо стадию I–IVA p53abn, либо неэндометриоидные карциномы без остаточного заболевания с инвазией миометрия (табл. 3). Карциномы MMRd и NSMP включены в категорию высокого риска, если стадия III–IVA и отсутствует остаточное заболевание. Карциномы p53abn могут быть эндометриоидного, серозного, недифференцированного и светлоклеточного гистологического типов, но все они неизменно демонстрируют неблагоприятный исход и поэтому должны рассматриваться как карциномы высокого риска. На основе текущих данных сложнее делать выводы относительно карциносарком и недифференцированных карцином, которые являются карциномами эндометрия NSMP, из-за отсутствия больших рандомизированных исследований.
Что касается светлоклеточных карцином, имеющиеся данные позволяют предположить, что некоторая прогностическая информация может заключаться в молекулярной классификации. Около 40–50% светлоклеточных карцином представляют собой p53abn. В то время как серозные карциномы в исследовании PORTEC-3 имели неблагоприятный исход и значительную пользу от дополнительной адъювантной химиотерапии, у пациентов со светлоклеточными карциномами, по-видимому, исход был сходен с карциномами высокой степени злокачественности в целом и был более благоприятным, если не было p53abn [14, 27]. В молекулярном анализе исследования PORTEC-3 было показано статистически значимое преимущество в выживаемости пациентов с эндометриоидными карциномами p53abn при комбинированной терапии I–III-стадий. В этом исследовании показано значительное улучшение показателей беcпрогрессивной и незначительное улучшение общей выживаемости женщин, получавших четыре цикла химио-терапии на основе платины, проводимых последовательно до или после лучевой терапии таза, по сравнению с женщинами, получавшими только лучевую терапию [27]. Напротив, при карциномах с мутацией POLE рецидивов в обеих группах с химиотерапией и без нее практически не было. Явной пользы от дополнительной химиотерапии при MMRd также не было, в то время как карциномы NSMP имели некоторую пользу от дополнительной химиотерапии, особенно при III стадии [14].
Согласно рекомендациям ESGO/ESTRO/ESP, при РЭ высокого риска рекомендуется адъювантная дистанционная лучевая терапия с одновременной адъювантной химиотерапией или альтернативно последовательная химиотерапия и лучевая терапия. Альтернативным вариантом является только химиотерапия. Карциносаркомы следует лечить как карциномы высокого риска, но не как саркомы [17].
При карциноме эндометрия III и IV стадий (включая карциносаркому) максимальную циторедукцию, по рекомендациям ESGO/ESTRO/ESP, а также на основе данных последнего метаанализа, следует рассматривать только в том случае, если возможна макроскопическая полная резекция с приемлемой морбидностью [17, 28]. Полная системная тазовая и парааортальная лимфаденэктомия подозрительных лимфатических узлов не приводят к повышению выживаемости и поэтому не рекомендуются. Резекции должны подвергаться только увеличенные лимфатические узлы [29, 30]. При нерезектабельном РЭ возможно проведение первичной системной лекарственной терапии. В случае значимого ответа на химиотерапию может быть рассмотрена отсроченная операция [31].
При неоперабельном местнораспространенном РЭ и отсутствии признаков множественных отдаленных метастазов вариантом лечения может быть окончательная лучевая терапия или неоадъювантная химиотерапия в зависимости от ответа. Адъювантная химиотерапия также должна быть рассмотрена после первичного местного лечения (хирургического или лучевого), чтобы снизить риск отдаленных метастазов [17].
Заключение
Различные типы РЭ имеют специ-фические гистологические и молекулярные особенности, разный патогенез, различаются клиническим течением и прогнозом. Появление новой молекулярной классификации РЭ стало большим достижением с точки зрения характеристики по сравнению с клинико-морфологическим разделением РЭ на два типа. Разделение РЭ по молекулярным признакам на четыре группы в настоящее время помогает лучше определять прогноз заболевания. Новые классификации ВОЗ 2020 г. и FIGO 2023 г. позволили перейти от гистологического к молекулярно-гистологическому диагнозу, стадированию РЭ и определению риска рецидива. В частности, обнаружение POLE-мутации и р53 дикого типа определяет низкий риск рецидива и скорее всего на ранних стадиях позволит отказаться от адъювантного лечения. С другой стороны, опухоли с аномальным р53 имеют высокий риск рецидива и снижения выживаемости, что приводит к переводу в группу более высокого риска и небходимости химиотерапии. Проводящиеся в настоящее время многоцентровые клинические исследования, такие как PORTEC-4a, RAINBO, CANSTAMP и TAPER, позволят получить новые данные по персонализированному подходу к лечению РЭ на основе сопоставления молекулярных и клинико-морфологических критериев [32, 33].



