В настоящее время тактика ведения инфертильных пациенток с эндометриоидными кистами яичников (ЭКЯ) различных стадий носит дискуссионный характер [1]. Неоднозначность подходов акушеров-гинекологов, хирургов, репродуктологов к выбору метода лечения связана с многофакторностью проблемы «эндометриоз и бесплодие»: среди факторов, влияющих на реализацию фертильной функции, наиболее значимые ранговые места принадлежат степени сохранности овариального резерва (ОВР) и качеству ооцитов, состоянию рецептивности эутопического эндометрия (РЭЭ) и его способности к полноценному формированию функциональной системы «мать-плацента-плод» [2]. Общепризнанным подходом к преодолению бесплодия при ЭКЯ тяжелых стадий, выраженном болевом синдроме является лечебно-диагностическая лапароскопия, которая в идеале должна проводиться у инфертильных пациенток только один раз, с последующим ожиданием спонтанной беременности, а при отсутствии ее наступления – введение в программы вспомогательных репродуктивных технологий (ВРТ) [3]. Однако вопрос о степени негативного влияния хирургического вмешательства на половые клетки и чувствительность яичников к стимуляции суперовуляции остается спорным [4]. По результатам многочисленных исследований, операционная травма при хирургическом лечении ЭКЯ способствует снижению ОВР, что связано с усилением местного воспаления, нарушением метаболизма железа и активности ферментов в фолликулах, развитием митохондриальной дисфункции и внутриклеточного оксидативного стресса [5, 6]. Также отмечается связь между ухудшением качества яйцеклеток и размерами удаляемых кист, что следует учитывать при подготовке к операции на гонадах [7]. Метаанализ последних лет показал, что оперативное лечение ЭКЯ способствует нарушению реактивности яичников на контролируемую гиперстимуляцию в циклах ВРТ при значительном снижении ОВР [8]. Согласно большинству наблюдений, оценка исходов по состоянию ооцитов после удаления ЭКЯ крупных размеров остается трудно прогнозируемой [9, 10]. При удалении двусторонних ЭКЯ тяжелых стадий следует учитывать высокую вероятность развития синдрома преждевременного истощения яичников [11]. Несмотря на отсутствие полного понимания механизмов инфертильности при ЭКЯ, доказано, что максимально бережное удаление ЭКЯ повышает эффективность ВРТ [12]. Дисрегуляция рецепторов прогестерона (РП) и резистентность к прогестерону, несомненно, играют существенную роль в реализации ранних репродуктивных потерь. При ЭКЯ как эктопический, так и эутопический эндометрий имеют нарушенную чувствительность к прогестерону, что вызывает гиперстимуляцию эстрогенами и отрицательно сказывается на готовности эндометрия к полноценной децидуализации и имплантации [13]. В ряде исследований показано положительное влияние на качество ооцитов и РЭЭ адъювантной гормональной терапии после хирургического лечения, которая способствует торможению прогрессирования эндометриоидного процесса и превенции рецидивов. Однако назначение гормонотерапии после операции уже не может повлиять на негативные последствия хирургической травмы, связанные с сохранностью яйцеклеток [14, 15]. Следовательно, дополнительный путь практической реализации овариопротекции возможен на дооперационном этапе путем создания оптимальных условий для оперативного вмешательства с минимизацией потерь ОВР, улучшением РЭЭ и коррекцией провоспалительного состояния. Несмотря на пониженную способность к зачатию при наличии ЭКЯ больших размеров, достаточный ОВР обеспечивает вероятность наступления беременности и возможность живорождения [16]. Хорошо известно, что функциональные кисты яичников, представляя собой соединительнотканную капсулу с жидкостным содержимым, могут менять свои размеры вплоть до полного исчезновения, в зависимости от эффективности противовоспалительного/гормонального лечения, циклических процессов репродуктивной оси, устранения этиологического фактора [17]. ЭКЯ являются гормонально-чувствительными; при этом известно естественное угнетающее прогестероновое влияние на них во время беременности, вызывающее ремиссию заболевания, выраженную регрессию с уменьшением размеров и функциональной активности ЭКЯ [18, 19]. В отдельных работах показано, что длительная терапия агонистами гонадотропин-рилизинг-гормона (аГнРГ), диеногестом улучшает показатели фертильности при ЭКЯ с прогрессирующим течением. Повышение эффективности предоперационного применения аГнРГ, прогестагенов заключалось в снижении тяжести заболевания, повышении результативности восстановления фертильности за счет увеличения частоты имплантации и снижения ранних репродуктивных потерь [20–22].
Анализ информационных баз PubMed, Scopus, eLibrary.Ru, MedLine, Cochrane, Hinari показал отсутствие конкретных рекомендаций по врачебной тактике при инфертильности вследствие ЭКЯ тяжелых стадий для повышения эффективности реализации репродуктивной функции, доступных для практического применения методов сохранения ОВР и РЭЭ с широкой доказательной базой на этапах подготовки к беременности.
Цель исследования: оптимизация дооперационного этапа лечения пациенток с ЭКЯ тяжелых стадий и бесплодием для обеспечения овариопротекции, улучшения рецептивности эндометрия, нормализации провоспалительного статуса.
Материалы и методы
Проведены обследование и лечение 114 инфертильных пациенток с ЭКЯ III–IV стадий, которые составили две группы сравнения. Ведение пациенток I группы, в которую вошли 65 женщин, включало 4 этапа: дооперационный, операция, послеоперационный этап ожидания спонтанной беременности в течение 6 месяцев, этап ВРТ. В качестве предоперационной подготовки с целью снижения выраженности болевого синдрома, уменьшения размера ЭКЯ, сохранения ОВР, нормализации РЭЭ, коррекции воспалительного статуса проводилось дооперационное гормональное лечение: назначались аГнРГ в течение 3 месяцев (бусерелин, начиная в первые 5 дней цикла по 3,75 мг, внутримышечно, однократно, каждые 4 недели) или синтетический прогестаген (диеногест не менее 4–5 месяцев по 2 мг, ежедневно, перорально). Терапия аГнРГ проведена у 46,2% (30/65) женщин с выраженным болевым синдромом, диеногест получили 53,8% (35/65) пациенток с умеренно и слабо выраженным болевым синдромом. Оценку болевого синдрома проводили по визуальной аналоговой шкале (ВАШ), где 0 баллов соответствовало отсутствию боли, 1–2 балла соотносились со слабым болевым синдромом, 3–5 баллов соответствовало умеренному болевому синдрому, при 6 баллах и более синдром расценивался как выраженный [23]. Во время операции лапароскопическим доступом проводилось вылущивание ЭКЯ, иссечение очагов эндометриоза, хирургическое рассечение спаек. После хирургического лечения из I группы пациенток были выделены 3,1% (2/65) женщин с критически сниженным ОВР (уровень антимюллерова гормона (АМГ) составлял менее 0,5 нг/мл, фолликулостимулирующего гормона (ФСГ) – более 10 МЕ/мл). Обе женщины были направлены на лечение бесплодия с применением ВРТ с донацией ооцитов. Оставшимся 63 пациенткам в послеоперационном периоде с целью поддержки II фазы цикла был назначен дидрогестерон в циклическом режиме – по 30 мг/сутки, с 16-го по 25-й день цикла. Если спонтанная беременность не наступала в течение полугода, женщина направлялась на лечение ВРТ. II группу сравнения составили 49 женщин, которым для преодоления инфертильности проводилось оперативное лечение аналогично пациенткам I группы, дооперационное гормональное лечение не применялось. После хирургического лечения из пациенток II группы также были выделены 16,3% (8/49) женщин с критическим ОВР (уровень АМГ – менее 0,5 нг/мл), которые направлялись на лечение методами ВРТ с донацией ооцитов. В отношении оставшейся 41 женщины, согласно клиническим рекомендациям, в течение 6 месяцев применялась выжидательная тактика: при отсутствии спонтанной беременности пациентки направлялись на лечение бесплодия методами ВРТ [3, 24]. Контрольную III группу составили 35 условно здоровых женщин с интактными яичниками и инфертильностью вследствие мужского фактора, которым лечение бесплодия проводилось методами ВРТ. В программах ВРТ стимуляция овуляции осуществлялась по стандартной методике, применялся длинный протокол стимуляции аГнРГ. Для диагностики ЭКЯ по стадиям применялась классификация действующих клинических рекомендаций [3]. Критерии включения в I и II группы: наличие гистологического подтверждения диагноза впервые выявленных ЭКЯ, тяжелые стадии ЭКЯ (III, IV), репродуктивный возраст менее 35 лет, впервые выполненная операция по поводу ЭКЯ. Критерии невключения: гормональная терапия в течение 6 месяцев до включения в исследование, тяжелая соматическая, аутоиммунная патология, эндомиометрит, мужской фактор бесплодия (азооспермия). Критерии исключения: невыполнение индивидуального протокола обследования и лечения.
Динамика обследования женщин включала: этап постановки диагноза с уточнением причины инфертильности до начала дооперационного гормонального лечения с целью овариопротекции (I группа) или перед операцией (II группа), 3-и сутки после операции и через 6 месяцев после операции – перед циклами экстракорпорального оплодотворения (ЭКО). Обследование пациенток включало сбор жалоб и характеристику менструальной функции, оценку анамнеза, физикальное и бимануальное влагалищное исследование; интенсивность болевого синдрома оценивали по ВАШ [23]. По интраоперационным данным проводился расчет индекса фертильности [3, 25]. В ходе обследования всем женщинам выполнялись ультразвуковое исследование, допплерография (Voluson E6 GE Healthcare, GE США); при подсчете количества антральных фолликулов (КАФ) учитывались рекомендации С.Г. Хачкузова [26]. У пациенток групп сравнения методами иммуноферментного анализа, хемилюминесцентного иммуноанализа (Architect (Abbot, Англия)) до 7-го дня цикла определялись: АМГ, эстрадиол (Е2), лютеинизирующий гормон (ЛГ), ФСГ, пролактин (ПРЛ), тиреотропный гормон (ТТГ), для исключения онкопатологии учитывались маркеры неопластических процессов (СА125, НЕ4, индекс ROMA) [27]; во 2-ю фазу цикла (19–23-й дни) определяли прогестерон, провоспалительные цитокины интерлейкины (IL)-1β, IL-6; для оценки белок-синтетической функции эутопического эндометрия менструальной крови определяли концентрацию гликоделина, для иммуногистохимического (ИГХ) анализа и морфологической характеристики эндометрия использовалась пайпель-биопсия. Капсула ЭКЯ направлялась для морфологического подтверждения диагноза, фрагменты капсулы ЭКЯ подготавливались для исследования с помощью ИГХ-анализа и определения экспрессии молекулярных маркеров (тест-система Biocare, Германия). Для оценки выраженности экспрессии рецепторов половых стероидов (рецепторов эстрогенов (РЭ) и РП), маркеров клеточной пролиферации Ki-67 и апоптоза p53 применялись моноклональные антитела (клон SP1, IgG изотип; клон PGR 16, IgG1 изотип; клон MM1, IgG1 изотип; клон 100/D5, IgG1 изотип соответственно) [28].
Статистический анализ
Для статистической обработки использовали статистический пакет IBM SPSS Statistics 25 PS. Все полученные количественные параметры проверены на соответствие нормальному распределению с помощью критерия Шапиро–Уилка. Числовые параметры, имеющие нормальное распределение, представлены в формате М (SD), где М – среднее значение, SD – стандартное отклонение; для сравнения данных применяли критерии ANOVA. Для оценки равенства дисперсий в группах сравнения учитывался критерий Ливеня. Апостериорные сравнения проводили с применением критерия Тьюки. Показатели с отличным от нормального распределением представлены в формате Me [Q1 – 25%; Q3 – 75%]; сравнение данных проводилось с помощью непараметрического метода Краскела–Уоллиса, для межгрупповых сравнений учитывался U-критерий Манна–Уитни с поправкой Бонферрони (р<0,017). Внутригрупповая динамика показателей на фоне лечения оценивалась парным показателем Вилкоксона. Для категориальных показателей рассчитывали частоты, для определения статистических различий применялся критерий χ² Пирсона с поправкой Йейтса. Степень взаимосвязей рассчитывалась с использованием корреляционного анализа Спирмена. Критический уровень значимости (p) при проверке статистических гипотез принимался равным 0,05 [29, 30].
Результаты и обсуждение
Для объективизации результатов влияния дооперационного гормонального лечения у женщин с ЭКЯ тяжелых стадий на ОВР, РЭЭ, провоспалительное состояние, выраженность болевого синдрома и реализацию репродуктивной функции проведен сравнительный анализ исходных клинико-демографических характеристик пациенток групп сравнения, представленных в таблице 1.
По возрасту, социальному статусу, индексу массы тела, длительности бесплодия и паритету, уровню ПРЛ и функции щитовидной железы группы сравнения были сопоставимыми. Первоначально внимание у женщин с опухолевидными образованиями яичников обращалось на исключение злокачественного процесса путем инструментально-лабораторного обследования на онкомаркеры (данные УЗИ, допплерографии, магнитно-резонансной томографии, цисто- и колоноскопия по показаниям, СА125, HE-4, индекс ROMA); согласно результатам гистологического исследования интраоперационного материала истинный неопластический процесс отсутствовал у всех включенных в исследование пациенток. К особенностям клинических проявлений ЭКЯ тяжелых стадий следует отнести болевой синдром различной степени выраженности, дизурию, дисхезию, хронические аномальные маточные кровотечения, по частоте проявлений которых женщины I и II групп статистически не различались. Согласно данным первичного обследования, у пациенток с эндометриозом яичников групп сравнения отсутствовали значимые различия по размерам ЭКЯ, толщине и белок-синтетической функции эутопического эндометрия (α-2-микроглобулин фертильности), параметрам ОВР (КАФ, АМГ, Е2, ФСГ), концентрации прогестерона и провоспалительных IL; при этом показатели отличались от результатов обследования женщин III группы (контроль) – pI-III<0,001, pII-III<0,001. ИГХ-анализ экспрессии РЭ и РП в биоптатах эутопического эндометрия пациенток с ЭКЯ тяжелых стадий и бесплодием групп сравнения не показал статистически значимых различий; при этом различия выявлены при сопоставлении с данными III группы – отмечено повышение представительства РЭ и РП как в строме, так и железах (p<0,001). Полученные исходные данные позволили считать I и II группы сопоставимыми по медико-демографическим, клиническим показателям, исходным характеристикам ОВР, структурно-функциональному состоянию эндометрия, провоспалительному статусу.
Оценка болевого синдрома по ВАШ у женщин I группы после проведенного дооперационного гормонального лечения показала значительное снижение его выраженности по сравнению с исходными данными: у 89,2% (58/65) пациенток отмечалась слабая боль или ее отсутствие (χ²=93,63, p<0,001); 10,8% (7/65) указывали на умеренный болевой синдром (χ²=36,44, p<0,001); выраженный болевой синдром отсутствовал (χ²=22,57, p<0,001), что подтвердило антиноцицептивное действие дооперационного гормонального лечения.
Результаты, полученные в ходе лечебно-диагностической лапароскопии, подтвердили в I группе статистически значимое уменьшение среднего размера ЭКЯ до 4,2 (0,8) см по сравнению с результатами первичного УЗИ до дооперационного гормонального лечения – 7,3 (1,2) см (p<0,001); при этом интраоперационные размеры ЭКЯ у женщин I группы статистически различались с интраоперационными размерами кист во II группе – 4,2 (0,8) против 7,3 (1,3) см, p<0,001. Оценка степени тяжести ЭКЯ, их локализации не опровергла исходного межгруппового сходства по указанным параметрам (p>0,05) (табл. 1).
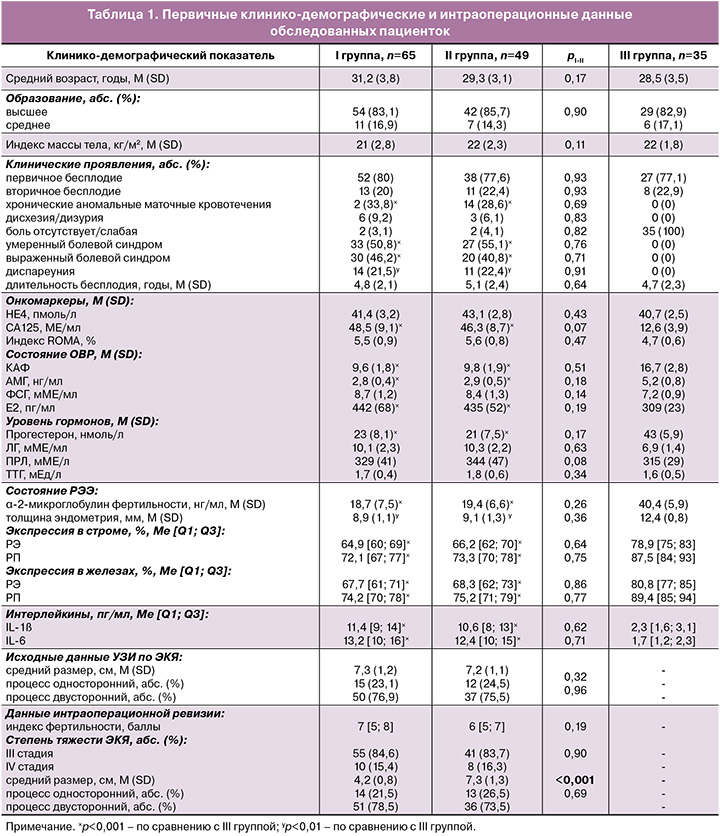
Проведенный корреляционный анализ результатов УЗИ пациенток I и II групп с интраоперационными данными показал наличие сильной ассоциативной связи между размерами ЭКЯ (k 0,81–0,89, p<0,05), латерализацией расположения кист (k 0,83–0,94, p<0,05). Кроме того, отмечены различия в наличии видимых очагов эндометриоза на брюшине. При проведении дооперационного гормонального лечения аГнРГ/прогестагеном единичные очаги выявлены у 5 (7,7%, 5/65) пациенток, при отсутствии дооперационной подготовки – у 20 (40,8%, 2/49) женщин – χ²I-II=16,02, pI-II<0,001. Расчет индекса фертильности, учитывающего данные анамнеза и интраоперационной ревизии, показал отсутствие статистической разницы между I и II группами (7 и 6 баллов соответственно, p=0,19) и свидетельствовал о возможности наступления беременности с вероятностью 40% [25].
Динамика показателей ОВР, РЭЭ, ИГХ-анализа капсул ЭКЯ, IL в зависимости от факта проведения/отсутствия дооперационного гормонального лечения представлена после оперативного лечения в таблице 2 и перед проведением ЭКО – в таблице 3.
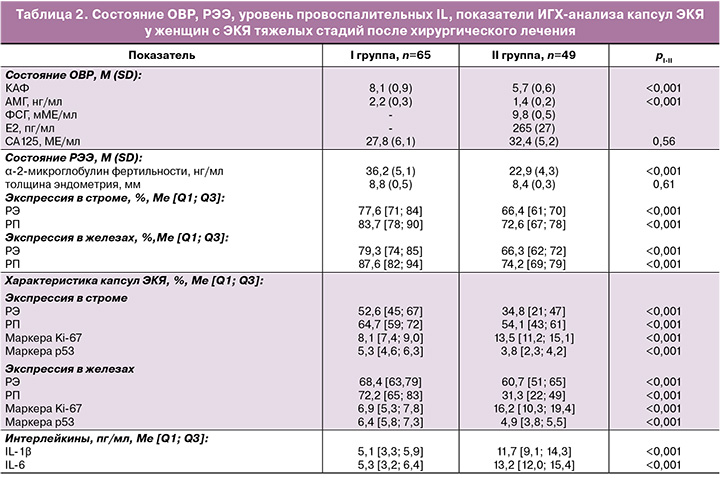
Обследование после операции по поводу ЭКЯ III–IV стадий показало значимое повышение ФСГ (p<0,01) параллельно со снижением концентрации Е2 на 39% (p<0,001) у пациенток II группы по сравнению с дооперационными показателями, что объяснимо только агрессивным влиянием операционной травмы на яичники и ОВР. Данное заключение подтверждает анализ показателя КАФ в динамике лечения: отмечено снижение КАФ с 9,8 (1,9) в дооперационном периоде до 5,7 (0,6) в послеоперационном периоде (p<0,001), а также содержания АМГ с 2,9 (0,5) до 1,4 (0,2) нг/мл (p<0,001) соответственно. Кроме того, после оперативного лечения во II группе выделены 8 пациенток (16,6%, 8/49) с резко сниженным до критических значений ОВР, которым были показаны ургентные ВРТ с донацией ооцитов; при этом в I группе с дооперационным гормональным лечением таких женщин выделены 2 (3,1%, 2/65) – χ²=4,59, p=0,03. Межгрупповые сравнения и внутригрупповая динамика КАФ и АМГ представлены на рисунках 1 и 2.
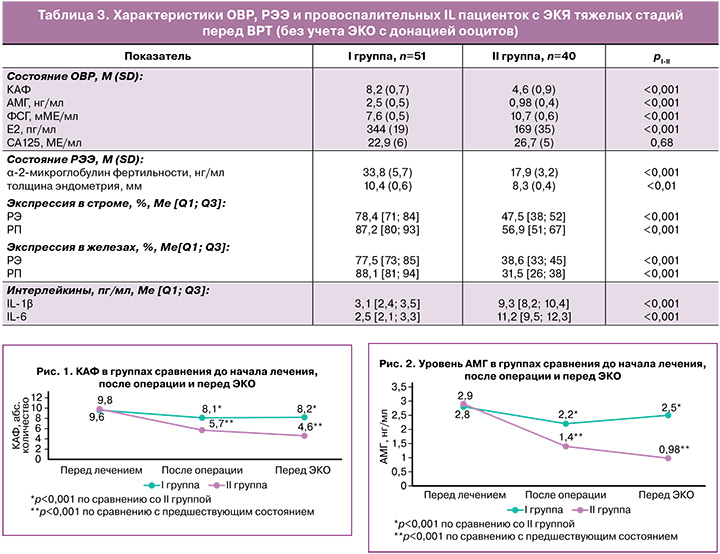
Следовательно, после операции на яичниках при отсутствии дооперационного гормонального лечения отмечено статистически значимое снижение всех показателей ОВР (КАФ, АМГ, ФСГ, Е2); при этом в I группе с дооперационной овариопротекцией в послеоперационном периоде отмечалось незначимое снижение ОВР (КАФ, АМГ). Данная закономерность была прослежена через 6 месяцев после оперативного лечения при обследовании 51 пациентки I группы (у 12 женщин наступила спонтанная беременность, у 2 – ургентное ЭКО с донацией ооцитов) и 40 пациенток II группы (у 1 – спонтанная беременность, у 8 – ВРТ с донацией ооцитов). Показатели ОВР в I группе были мало изменены – без статистических различий с исходными данными (КАФ 8,2 (0,7) против 9,6 (1,8); АМГ 2,5 (0,5) против 2,8 (0,4) нг/мл; Е2 344 (19) против 442 (68) нг/мл; ФСГ 7,6 (0,5) против 8,7 (1,2) мМЕ/мл), что объясняется овариопротективным действием назначенного дооперационного гормонального лечения аГнРГ/диеногестом. Также следует обратить внимание на стабильное сохранение уровня КАФ (8,2 (0,7) против 8,1 (0,9) при статистически значимом увеличении в протоколах ЭКО количества полученных ооцитов и М2-ооцитов – 6,5 (0,6) против 3,3 (0,4) во II группе, p<0,001, и 6,3 (0,4) против 2,7 (0,3) во II группе, p<0,001 соответственно показателям (табл. 4). Отмечено даже некоторое повышение содержания АМГ перед ЭКО (2,5 (0,5) против 2,2 (0,3) нг/мл), что, несомненно, связано с количественной и качественной сохранностью ОВР, повышением чувствительности к прогестерону, местным и системным противовоспалительным и антиноцицептивным действием, нормализацией проводимости нервных импульсов, микроциркуляции и лимфодренажа, торможением прогрессирования заболевания вследствие применения аГнРГ/диеногеста на дооперационном этапе, дидрогестерона после операции. Характеризуя ОВР во II группе, следует отметить его прогрессирующее ухудшение не только в послеоперационном периоде, но и в течение 6 месяцев после операции. Так, имела место негативная динамика КАФ (от 5,7 (0,6) до 4,6 (0,9)), АМГ (от 1,4 (0,2) до 0,98 (0,4) нг/мл)), ФСГ (от 9,8 (0,5) до 10,7 (0,6) мМЕ/мл), Е2 (от 265 (27) до 169 (35) нг/мл), что подтверждает альтерацию ооцитов вследствие операционной травмы с последующим прогрессированием процесса. Несомненно, важным свидетельством влияния дооперационного гормонального лечения на состояние ЭКЯ является характеристика ИГХ-профиля капсулы кисты с оценкой представительства молекулярных маркеров клеточной пролиферации, запрограммированной клеточной гибели, рецепторов половых стероидов. Получены разнородные данные по ИГХ-профилю капсул ЭКЯ в I и II группах сравнения (табл. 2).
В ткани капсул ЭКЯ женщин II группы представительство РП и РЭ статистически значимо снижено как по сравнению с данными по эутопическому эндометрию, так и с результатами ИГХ-анализа капсул ЭКЯ в I группе (p<0,001). Нарушенная экспрессия РЭ связана с изменением синтеза обеих форм РП [31]. Повышение рецептивности гетеротопического эндометрия к прогестерону повышает эффективность блокирования активности и прогрессирования процесса, местного противовоспалительного действия [2]. Повышение РП в I группе отмечалось как в стромальном, так и в железистом компонентах с разбросом показателя от 59 до 83%, приближаясь к данным по РЭЭ группы контроля, где разброс РП составил от 84 до 93%; при вариабельности показателя РП в капсулах ЭКЯ II группы от 43 до 61%.
В структурно-функциональном состоянии ЭКЯ ключевую роль играют процессы клеточной трансформации [32]. Нарушение синтеза белков-регуляторов запрограммированной клеточной гибели и пролиферации способствует как формированию патологических процессов, так и их прогрессированию, рецидивированию, отсутствию ожидаемого эффекта от лечения [33]. Экспрессия ядерного маркера клеточной пролиферации и рибосомальной транскрипции РНК – Ki-67, по результатам исследования ИГХ-профиля капсул ЭКЯ, значимо различалась в I группе, находясь в промежуточном положении между экспрессией маркера в контрольных образцах эутопического эндометрия и в капсулах ЭКЯ II группы (в строме: 8,1% [7,4; 9,0] против 6,6% [3,1; 7,5] в контроле и 13,5% [11,2; 15,1] в капсулах ЭКЯ II группы, pI-III<0,001 и pI-II<0,001; в железах: 6,9% [5,3; 7,8] против 4,0% [3,0; 4,8] в контроле и 16,2% [10,3; 19,4] в капсулах ЭКЯ II группы, pI-III<0,001 и pI-II<0,001). Следует отметить наличие клинико-лабораторных параллелей, заключающихся в том, что сильно выраженный постоянный болевой синдром был характерен для женщин с наибольшим увеличением экспрессии Ki-67; данное обстоятельство также объяснимо диссеминацией процесса – наличием у данных женщин инфильтрации брюшины очагами эндометриоза. Обратная закономерность выявлена в отношении маркера апоптоза p53, вариативность изменения которого зависела от наличия/отсутствия дооперационного гормонального лечения. Отмечено достоверное увеличение показателя в I группе – в 1,4 раза и в 1,3 раза соответственно в строме и железах капсул ЭКЯ по сравнению со II группой (pI-II<0,001); при статистически незначимом снижении показателя p53 в 1,2 раза относительно стромы эндометрия контрольной группы (6,2% [4,8; 6,5], p=0,08) и увеличении в 2,9 раза относительно железистого компонента контрольных образцов эндометрия (2,2% [1,5; 3,5], pI-III<0,001). В целом изменением соотношения маркеров клеточной трансформации в пользу апоптоза на фоне нормализации представительства рецепторов к половым стероидам вследствие дооперационного этапа гормональной подготовки можно убедительно объяснить статистически значимое снижение размеров ЭКЯ на 42,5% (pI-II<0,001). Среди механизмов, способствующих снижению размеров ЭКЯ, следует выделить уменьшение местного воспаления и отека тканей яичника и ЭКЯ, изменение регуляции процессов клеточной трансформации в очаге гетеротопии, снижение влияния гиперэстрогенемии и повышение чувствительности к прогестерону, уменьшение местных иммунопатологических процессов на фоне нормализации связи гормонального и иммунологического контуров регуляции состояния репродуктивной системы, преобладание резорбтивных процессов над секреторными [9, 33]. В результате уменьшения объема ЭКЯ, более четкого разграничения здоровых и патологических тканей в яичнике создаются оптимальные условия для более бережного вылущивания кисты, сохранения ОВР, снижения местного и системного воспаления, инициирующего возможное прогрессирование альтерации ооцитов, нарушения РЭЭ в отдаленном периоде.
Характеристики маркеров РЭЭ, его толщины и белок-синтетической функции в послеоперационном периоде и через 6 месяцев после операции у женщин I группы с до- и послеоперационной гормональной терапией свидетельствуют о статистически значимом повышении представительства РП и РЭ (p<0,001), концентрации гликоделина в менструальной крови (p<0,001), некотором увеличении толщины эндометрия (10,4 (0,6) против 9,6 (1,8) мм), что в совокупности свидетельствует о нормализации РЭЭ и его способности к полноценным децидуализации, имплантации, участии в процессах инвазии и формировании ранней плаценты; при этом исходно нарушенная РЭЭ у женщин II группы с тяжелыми формами ЭКЯ сохранялась в послеоперационном периоде с нарастанием изменений в течение 6 месяцев ожидания спонтанной беременности.
В настоящее время доказано негативное влияние провоспалительных цитокинов через эпигенетические механизмы на репродуктивную ось, синтез обеих форм РП и чувствительность к прогестерону, эффективность лечебных мероприятий как в отношении прогрессии эндометриоза, так и преодоления бесплодия [34]. Системные уровни IL-1β и IL-6 представлены в таблицах 1, 2, 3 и свидетельствуют о нормализации воспалительного статуса у женщин I группы и сохранении воспалительного состояния у пациенток II группы, лечение которых было ограничено только оперативным вмешательством на яичниках.
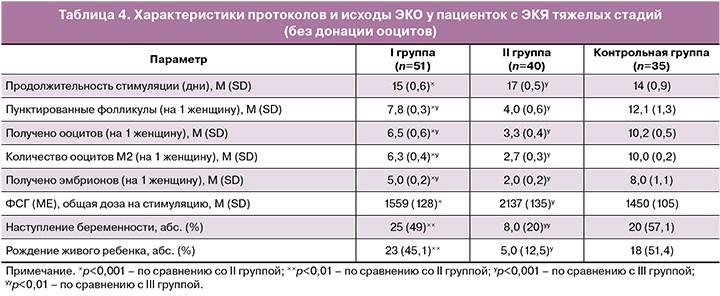
Параметры протоколов и исходы ЭКО в I, II и III группах сравнения представлены в таблице 4.
Целевыми показателями эффективности тактики ведения инфертильных женщин с ЭКЯ III–IV стадий являются наступление беременности и роды с благоприятным перинатальным исходом живым плодом. Так, во II группе после хирургического этапа лечения ЭКЯ III–IV стадий частота спонтанной беременности в течение 6 месяцев составила 2% (1/49), а по результатам послеоперационной оценки ОВР у 8 пациенток выявлено его критическое снижение, потребовавшее ЭКО с донацией ооцитов – все наблюдения закончились родами живым плодом. Через 6 месяцев ожидания спонтанной беременности ВРТ были применены у 40 пациенток, из них в 17,5% (7/40) наблюдений наступила беременность, завершившаяся в 43% (3/7) самопроизвольным абортом и в 57% (4/7) – рождением живого ребенка. В общей сложности во II группе беременность наступила в 32,7% (16/49) наблюдений, за исключением ВРТ с донацией ооцитов – в 16,3% (8/49), роды живым плодом имели место у 26,5% (13/49) пациенток, без ВРТ с донацией ооцитов – в 10,2% (5/49) наблюдений.
В I группе с дооперационным этапом гормональной овариопротекции, назначением в послеоперационном периоде дидрогестерона в циклическом периоде в течение 6 месяцев спонтанная беременность наступила в 18,5% (12/65) наблюдений; при этом в послеоперационном периоде критический ОВР выявлен лишь у 2 пациенток, которые результативно вступили в программу ЭКО с донацией ооцитов с благоприятным перинатальным исходом. Всем 51 пациенткам без спонтанной беременности применены ВРТ: беременность наступила в 25,5% (13/51), из них в 2 наблюдениях завершилась самопроизвольным выкидышем и в 21,6% (11/51) – родами живым плодом. В целом в I группе частота наступления беременности составила 41,5% (27/65), без ЭКО с донацией ооцитов – 38,5% (25/65),частота родов живым плодом составила 38,5% (25/65), без ВРТ с донацией ооцитов – 35,4% (23/65).
В III контрольной группе всем 35 пациенткам в связи с мужским фактором бесплодия назначались ВРТ; при этом беременность имела место в 57,1% (20/35), рождение живого ребенка – в 51,4% (18/35) наблюдений.
Различием в тактике ведения женщин с ЭКЯ тяжелых стадий I и II групп сравнения являлось проведение дооперационной гормональной овариопротекции аГнРГ/диеногестом, а также циклическое назначение дидрогестерона во II фазу цикла. Статистически значимое снижение частоты беременности и родов живым плодом во II группе по сравнению с I группой, при исключении применения ВРТ с донорскими ооцитами – χ²I-II=5,6, pI-II=0,02 (ОШ 3,2 [1,29; 7,94]) и χ²I-II=8,3, pI-II<0,01 (ОШ 4,8 [1,68; 13,85]) соответственно, можно объяснить лишь агрессивным влиянием операционной травмы на ОВР, нарушенной РЭЭ и провоспалительным состоянием, которые успешно скорректировались путем применения гормональной овариопротекции в I группе и позволили, благодаря более бережному оперативному вмешательству, сохраненному ОВР и нормализации РЭЭ и воспалительного статуса, оптимизировать преодоление инфертильности на последующих этапах. Данный факт подтверждает и увеличение частоты наступления спонтанной беременности в I группе в 9,3 раза (18,5% против 2%) – χ²I-II=5,92, pI-II=0,02 (ОШ 10,9 [1,36; 86,74]), что, несомненно, связано с благоприятным влиянием дооперационного гормонального лечения. Следовательно, дооперационный этап дифференцированной гормональной терапии аГнРГ/прогестагеном показал свою эффективность в отношении преодоления бесплодия у женщин с ЭКЯ III–IV стадий, что реализовалось в увеличении частоты наступления беременности (без применения донорских ооцитов) в 2,4 раза, родов живым плодом (без применения донорских ооцитов) в 3,5 раза.
Заключение
ЭКЯ тяжелых стадий – сложная междисциплинарная проблема, связанная как с патогенетической многогранностью заболевания, индивидуальными факторами риска, так и с оптимальностью применения хирургических и репродуктивных подходов. В подавляющем большинстве наблюдений результативность лечения инфертильности при тяжелых стадиях ЭКЯ ассоциирована со снижением агрессивности оперативного вмешательства на яичниках, сохранностью ОВР и РЭЭ. В связи с этим предложенный метод предоперационной овариопротекции решает важную задачу по реализации репродуктивного потенциала при сложной гинекологической патологии. Проведенное исследование с применением комплексного обследования доказывает преимущество дооперационного дифференцированного гормонального лечения пациенток с ЭКЯ III–IV стадий как в плане структурно-функционального состояния самих ЭКЯ и сохранения ОВР, нормализации РЭЭ и коррекции провоспалительного состояния, так и повышения эффективности достижения беременности с благоприятным перинатальным исходом. Полученные результаты объективизируют рациональность метода предоперационной подготовки женщин с тяжелыми формами эндометриоза яичников и бесплодием, который является патогенетически обоснованным, широко доступным для практического применения, экономически приемлемым, безопасным.



