Единого определения нарушений овуляции, называемых овуляторной дисфункцией (ОД), не существует. Одним из проявлений ОД является ановуляция; но существует целый ряд хронических или эпизодических состояний, которые даже при наличии овуляции нарушают менструальный цикл (МЦ). С другой стороны, многие женщины с нарушениями овуляции могут иметь МЦ нормальной продолжительности. Термин «нарушение овуляции» не является синонимом термина «ановуляция», поскольку расстройства овуляции существуют в диапазоне от эпизодических до хронических; при этом при возникновении единичного эпизода ановуляторный цикл проявляется отсроченным началом очередной менструации [1].
Большинство ОД клинически проявляются симптомами аномальных маточных кровотечений (АМК), варьирующих от полного отсутствия (аменорея) до редкого или нерегулярного МЦ, а также характеризуются различным объемом и продолжительностью менструальной кровопотери. В системе классификации причин АМК, разработанной FIGO (классификация PALM-COEIN; 2011), ОД отнесены к категории АМК (АМК-О), не связанных со структурными аномалиями [2].
В 2022 г. создана новая классификационная система HyPO-P конкретно для ОД, согласно которой выделяют 4 типа (уровня поражения): I – гипоталамус, II – гипофиз, III – яичник, отдельно выделен IV тип – синдром поликистозных яичников (СПКЯ). Признано, что точность определения анатомической локализации и механизма патогенеза ОД иногда затруднительна и зависит как от заболевания, так и от ресурсов, доступных клиницисту, для диагностики [1].
Определение типа ОД является принципиальным в выборе лечения, поскольку зависит от локализации поражения. Поэтому в данную классификацию включены еще два уровня, кроме уже описанного первичного (анатомического), – вторичный (генетические, аутоиммунные, ятрогенные, функциональные, инфекционные и воспалительные, травмы и сосудистые заболевания) и третичный (тип ановуляции).
Классификация причин АМК у женщин репродуктивного возраста, дополненная в 2018 г., описывает ряд симптомов, таких как межменструальное кровотечение и обильное менструальное кровотечение (ОМК) [3]. ОМК, характеризующееся кровопотерей, воспринимаемой женщинами как чрезмерная, влияет на здоровье женщин, ухудшая их физическое, эмоциональное, социальное и материальное качество жизни. Хотя АМК могут быть связаны с основной патологией, в данном контексте ОМК определяется как чрезмерное менструальное кровотечение при отсутствии другого системного или гинекологического заболевания [2].
АМК-О является наиболее частой находкой у женщин с хроническим АМК, составляя 57,7% [4]. ОМК – очень распространенное заболевание у женщин репродуктивного возраста, от которого страдают от 2 до 5 из каждых 10 женщин [2]. Ановуляция выявляется у 3,4–18,6% менструирующих женщин с регулярным МЦ [5].
ОД сопровождаются высоким риском железодефицитной анемии, гиперплазии и злокачественных новообразований эндометрия, что диктует необходимость скрининга, ранней диагностики и лечения.
Для лечения ОД и снижения ОМК используется широкий спектр лекарств. Нерегулярные и обильные менструации можно улучшить с помощью комбинированной гормональной контрацепции, эффективность которой была продемонстрирована в метаанализе с показателями ОШ 22,1 и 5,2 соответственно [6]. Пероральные прогестагены также являются наиболее часто назначаемыми препаратами; однако систематический обзор 15 рандомизированных контролируемых исследований показал, что терапия прогестагенами уступала другим средствам медикаментозной терапии, включая транексамовую кислоту, даназол, ормелоксифен и внутриматочную систему с левоноргестрелом [7]. При оценке динамики экспрессии стероидных рецепторов к эстрогену и прогестерону в стромальном и железистом компонентах эндометрия после АМК-ОД установлено, что коротких курсов гормонотерапии может быть недостаточно; для профилактики развития пролиферативных процессов и рецидива АМК-ОД прогестагены рекомендуется назначать длительностью не менее 6 месяцев [8].
Обзор 9 Кокрейновских обзоров и сетевой метаанализ, выполненный в 2020 г., показал, что первой линией терапии ОМК являются медикаментозные средства, которые были ранжированы по эффективности и представлены внутриматочной системой с левоноргестрелом, антифибринолитиками, прогестагенами (в 5–25-й дни цикла) и нестероидными противовоспалительными средствами (перечислены в порядке убывания по критерию эффективности). Вмешательствами второй линии являются хирургические [4].
Для женщин с ОД, желающих забеременеть, существует самостоятельная стратегия – индукция овуляции с помощью таких лекарств, как летрозол или кломифена цитрат, характеризующиеся показателями живорождения 27,5 и 19,1% соответственно [9].
В последние годы активно изучаются средства на основе инозитола и его изомеров – миоинозитола и D-хироинозитола. Большинство работ посвящено лечению СПКЯ, благодаря которым была показана высокая эффективность в отношении восстановления овуляции, нормализации МЦ, коррекции углеводного и липидного обмена, снижения массы тела, что подтверждено метаанализами [10–14]. В отношении восстановления регулярного МЦ у пациенток с СПКЯ средства, содержащие инозитол, были в 2 раза эффективнее плацебо [13], и показано, что миоинозитол в сочетании с D-хироинозитолом особенно эффективен для этой цели (ОШ=14,7; 95% ДИ 2,31–93,58) [15]. Определена эффективность миоинозитола для восстановления овуляции у 65% пациенток с СПКЯ [16]; аналогичный показатель достиг 70% при использовании миоинозитола с фолиевой кислотой [17].
В исследовании Обоскаловой Т.А. и соавт. длительность МЦ у пациенток с СПКЯ под влиянием средства, состоящего из мио- и D-хироинозитола в соотношении 5:1 с фолиевой кислотой и марганцем, уменьшилась с 52,7 до 33,4 дня (р=0,0001) [18]. Доброхотова Ю.Э. и соавт. показали положительное влияние того же средства на метаболические параметры, что способствовало уменьшению индекса массы тела на 9,1% через 90 дней от начала лечения [19]. В отдельных исследованиях было показано нормализующее действие мио- и D-хироинозитола на гонадотропную функцию – были достигнуты снижение уровня лютеинизирующего гормона (ЛГ) с 12,5±8 до 8,5±4,0 мМЕ/мл (р<0,05) в течение 6 месяцев лечения и нормализация показателя ЛГ/фолликулостимулирующий гормон (ФСГ) [20], что подтверждается метаанализом [11].
Учитывая столь впечатляющие результаты применения средств, содержащих мио- и D-хироинозитол, у пациенток с СПКЯ, можно предположить, что терапия ОД других типов также должна быть эффективной. Однако таких исследований в доступных публикациях нами не обнаружено. Вместе с тем ответ на этот вопрос актуален в силу ограничений по использованию гормональных средств в терапии АМК-О и представляет как научный, так и практический интерес.
Цель исследования: оценить эффективность комплексного лечения, включающего комбинацию гестагена, железосодержащего препарата и комплекса, содержащего мио-, D-хироинозитол (5:1), фолиевую кислоту и марганец, у пациенток репродуктивного возраста с АМК, связанными с ОД I–III типов.
Материалы и методы
Дизайн – многоцентровое исследование в условиях реальной клинической практики.
Организация исследования. Набор материала и наблюдение проводились с сентября 2021 г. по июнь 2023 г. в медицинских организациях Екатеринбурга, Казани, Краснодара, Москвы, Первоуральска, Саратова, Ставрополя, Ульяновска, Челябинска.
Этические аспекты. При создании протокола исследования учитывались требования Хельсинкской декларации Всемирной Медицинской Ассоциации (пересмотр 64-й Генеральной ассамблеи Всемирной медицинской ассоциации, Форталеза, Бразилия, 2013 г.), положения «Международных этических рекомендаций по проведению биомедицинских исследований с участием людей» Совета международной организации медицинских наук (ред. 2002 г.), Национального стандарта РФ ГОСТ Р52379-2005 «Надлежащая клиническая практика» (2005 г.), других законодательных и нормативных документов РФ.
Разрешение локального Этического комитета не требовалось (средства применялись в соответствии с инструкциями производителей). Все пациентки дали письменное информированное добровольное согласие на участие в исследовании.
Контингент. В исследование включены 2042 пациентки, обратившиеся за медицинской помощью в медицинские организации за указанный период с диагнозом: Обильные и частые менструации при нерегулярном цикле (N92.1), Скудные или редкие менструации у женщин с ранее нормальными менструациями (N92.3), Овуляторные кровотечения (N92.3), соответствовавшие классификации FIGO – АМК-О.
Критерии включения: возраст 18–45 лет; отрицательный тест на беременность; изокоагуляция крови; отсутствие противопоказаний к применяемому комплексу и лекарственным средствам (ЛС); наличие подписанного информированного добровольного согласия.
Критерии исключения: АМК, связанные со структурными изменениями органов репродуктивной системы (полип полости или шейки матки, миома матки, эндометриоз, гиперплазия эндометрия, интраэпителиальные поражения шейки матки); СПКЯ; кистомы яичников; кровотечения неясной этиологии; воспалительные заболевания органов малого таза (острые или хронические, в т. ч. хронический эндометрит); нарушения коагуляции крови; гипотиреоз (в том числе в анамнезе); другие заболевания органов эндокринной системы; пороки развития половых органов; тяжелые соматические заболевания.
Методы лечения. Дидрогестерон («Дюфастон», Abbott Biologicals B.V., Нидерланды) 10 мг по 1 таблетке 2 раза в день внутрь или микронизированный прогестерон («Утрожестан», Besins Healthcare, Бельгия) 100 мг по 1 таблетке 1 раз в день внутрь (по выбору врача) с 14-го по 25-й дни МЦ; при нерегулярном цикле – со дня включения в исследование или при сохраненном цикле – с 14-го дня, в течение трех последовательных циклов. Комплекс, содержащий миоинозитола 1000 мг, D-хироинозитола 200 мг, фолиевой кислоты 200 мкг, марганца 5 мг («Дикироген», Pizeta Pharma S.p.A, Италия) по 1 саше 2 раза в день, предварительно растворив в ½ стакана воды, ежедневно со дня включения в исследование в течение 6 последовательных циклов с целью восстановления овуляции, нормализации массы тела. Железа сульфат в количестве, эквивалентном 100 мг Fe2+, и аскорбиновая кислота 60 мг («Сорбифер Дурулес», ЗАО «Фармацевтический завод ЭГИС», Венгрия) по 1 таблетке 1 раз в день в течение 1 недели, далее – по 1 таблетке 2 раза в день в течение 3–4 месяцев при наличии показаний – железодефицитная анемия (D50) (уровень гемоглобина менее 120 г/л и сывороточного ферритина менее 30 мкг/л) или латентный дефицит железа (E61.1) (уровень гемоглобина 120 г/л и более и сывороточного ферритина менее 15 мкг/л).
Все ЛС использовали в соответствии с действующими инструкциями по медицинскому применению, опубликованными в Реестре лекарственных средств.
Комплаенс. Прием ЛС пациентками контролировался врачом-исследователем с помощью «подсчета саше/таблеток», которые участники отмечали в дневнике наблюдений. Комплаентность (соблюдение схемы вмешательства) считали адекватной, если пациенткой было принято более 80% исследуемых ЛС с даты начала до конца курса лечения.
Методы обследования пациенток включали комплекс клинических, принятых в акушерстве и гинекологии, и лабораторных исследований на этапе отбора пациенток в исследование – жалобы, анамнез, общий и гинекологический осмотр, ультразвуковое исследование (УЗИ) органов малого таза, тест на овуляцию, анализ крови на содержание пролактина, ЛГ, ФСГ, свободного тестостерона (на момент включения в исследование). В динамике оценивали уровни гемоглобина, сывороточного ферритина (на момент включения в исследование, через 90±7 и 180±7 дней). В течение всего периода наблюдения оценивали регулярность менструаций, продолжительность и объем менструальной кровопотери путем подсчета количества использованных прокладок («Normal» или с маркировкой 3–4 капли на упаковке) за период менструации на основании менструального дневника, который пациентки вели самостоятельно. Безопасность лечения (наличие/отсутствие нежелательных явлений) оценивали на основании дневников наблюдения, которые пациентки заполняли самостоятельно и предъявляли врачу-исследователю на каждом визите.
Наблюдение включало 3 визита: 1-й – через 90±7 дней, 2-й – через 180±7 дней и 3-й – через 360±14 дней от начала лечения.
Оценка результатов. Первичные исходы: нормализация ритма МЦ, продолжительности и объема менструации после отмены прогестинов (1-й визит) и после приема комплекса Дикироген (2-й визит), уровни гемоглобина и сывороточного ферритина (на визитах 1 и 2).
Вторичные исходы: сохранение нормального ритма МЦ, продолжительности и объема менструации после отмены лечения к 12 месяцам (3-й визит), динамика массы тела, нежелательные явления.
Критерии нормального МЦ: продолжительность МЦ – 24–38 дней, продолжительность менструации – 3–8 дней, объем менструальной кровопотери – до 80 мл.
Статистический анализ
Статистическую обработку данных выполняли, используя программу Statistica for Windows 10.0 (StatSoft Inc., США). Непрерывные переменные выражали в виде медианы (Ме) и межквартильного диапазона (Q1; Q3). Качественные признаки указывали абсолютными числами (n), а их доли – относительными величинами (%). Анализ выполняли соответственно назначенному вмешательству («до-после», before-after study). Оценка эффективности вмешательства проводилась описательным методом ввиду неприменимости методов аналитической статистки.
Результаты
Общие сведения о пациентках. Возраст пациенток варьировал от 18 до 45 лет, в среднем составил 30 (25; 35) лет. По возрастным группам пациентки распределились следующим образом: 18–24 года – 23,5% (479/2042), 25–34 года – 48,2% (984/2042), 35 лет и старше – 28,3% (579/2042). Клинико-анамнестические характеристики пациенток представлены в таблице 1.
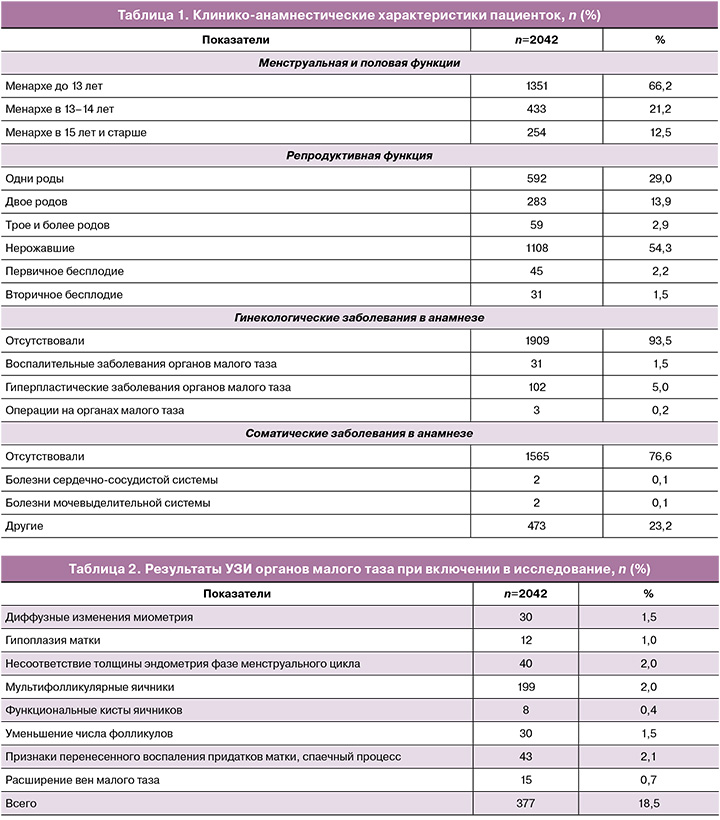
В структуре АМК у пациенток преобладали: обильные и частые менструации при нерегулярном цикле (N92.1) – 46,7% (953/2042), затем – вторичная олигоменорея, скудные или редкие менструации у женщин с ранее нормальными менструациями (N91.4) – 30,9% (630/2042) и овуляторные кровотечения (N92.3) – 22,5% (459/2042).
Средний рост пациенток составил 166 (163; 170) см, вес – 65 (58; 75,3) кг и индекс массы тела – 26,7 (21,3; 27,3) кг/м2 (избыточный вес), окружность талии – 76 (68; 84) см. Гормональный статус соответствовал уровням пролактина 329 (210,8; 430) МЕд/л, ЛГ – 7 (4,9; 10) МЕд/л, ФСГ – 6,7 (5,0; 9,0) МЕд/л, свободного тестостерона – 1,5 (1,0; 2,4) пг/мл. Ановуляция наблюдалась у 60,1% (1228/2042), циклы были овуляторными у 39,9% (814/2042) пациенток.
Показатели красной крови были представлены концентрацией гемоглобина в среднем 122 (112; 130) г/л. Пациенток с анемией было 39,9% (814/2042), средний показатель гемоглобина у них составил 110 (103,8; 115) г/л и сывороточного ферритина – 20 (12; 36) мкг/л.
По данным УЗИ органов малого таза патологических изменений не выявлено у 81,5% (1665/2042) пациенток, результаты остальных представлены в таблице 2.
Таким образом, на момент включения в исследование большинство пациенток были в среднем репродуктивном возрасте, без гинекологических и соматических заболеваний в анамнезе и патологических изменений матки и эндометрия по данным УЗИ, имели избыточную массу тела, и у 39,9% пациенток была анемия.
Оценка эффективности лечения
Результаты лечения представлены в таблице 3.
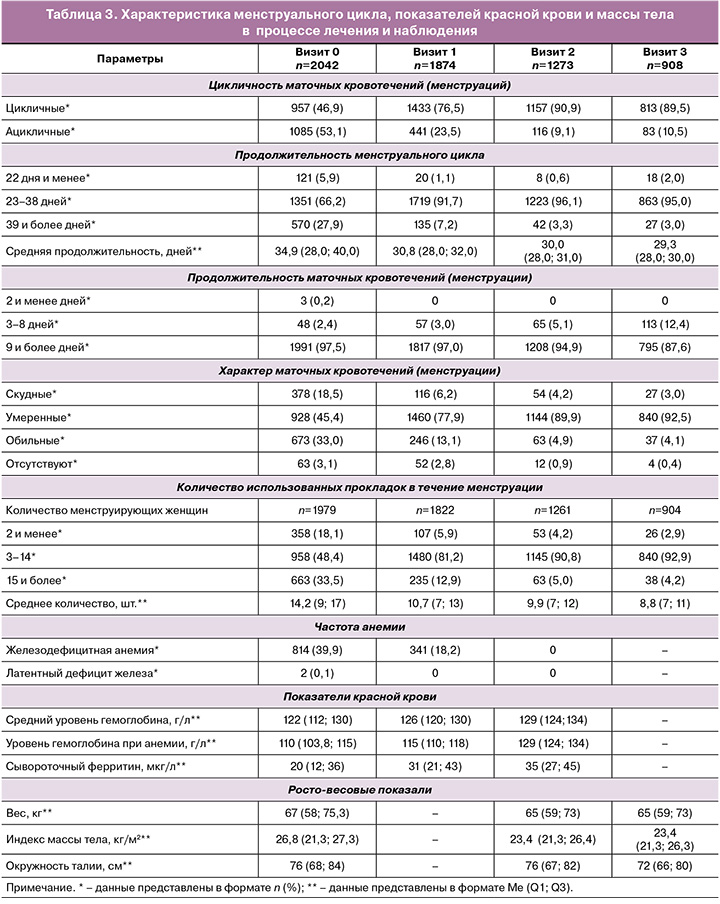
Первичные исходы. Нормальный ритм МЦ после окончания приема прогестина наблюдался у 76,5% пациенток против 46,9% до лечения, после завершения приема Дикирогена (через 6 месяцев от начала лечения) – у 90,9% и был выше в 2 раза по сравнению с исходным уровнем и на 44% выше – по сравнению с 1-м контрольным визитом (рис. 1).
Нормальная продолжительность МЦ (23–38 дней) наблюдалась через 90 дней у 91,7% пациенток против 66,2% до лечения, через 180 дней – у 96,1%, и между 0-м и 2-м визитами количество пациенток с нормальной продолжительностью МЦ увеличилось на 30%.
Продолжительность МЦ 39 дней и более была у 7,2 и 3,3% пациенток на 1-м и 2-м визитах соответственно против 27,9% до лечения и уменьшилась в 4 и 10 раз соответственно, а между 2-м и 1-м визитами сократилась в 2 раза.
Количество пациенток с продолжительностью маточных кровотечений (менструаций) 9 дней и более к 1-му визиту уменьшилось и составило 97,0% против 97,5%, ко 2-му визиту – 94,9%, разницы между 2-м и 1-м визитами практически не было. Однако количество пациенток с нормальной продолжительностью менструального кровотечения (3–8 дней) увеличилось в 2,2 раза ко 2-му визиту.
Несмотря на сохранение продолжительности менструальной кровопотери более 9 дней у большинства пациенток, они отметили уменьшение ее объема, и количество пациенток с умеренным объемом менструации увеличилось до 77,9 и 89,9% против 45,4% соответственно; количество пациенток с нормальным объемом кровопотери увеличилось в 1,7 и 2 раза соответственно, а между 1-м и 2-м визитами их стало больше на 13%. При этом количество пациенток с нормальным объемом менструальной кровопотери, использовавших от 3 до 14 прокладок, увеличилось до 81,2 и 90,8% соответственно против 48,4% до лечения, то есть почти в 2 раза. Уменьшилось и среднее количество использованных прокладок – до 10,7 (7; 13) и 9,9 (7; 12) против 14,2 (9; 17) шт. соответственно.
Частота железодефицитной анемии через 3 месяца от начала лечения составила 18,2% против 39,9% до него, а к 6 месяцам таких пациенток не было. Уровень гемоглобина у пациенток с исходной анемией повысился с 110 (103,8; 115) г/л до лечения до 115 (110; 118) и 129 (124; 134) г/л к 1-му и 2-му визитам соответственно, а сывороточный ферритин – с 20 (12; 36) до 31 (21; 43) и 35 (27; 45) г/л соответственно.
Таким образом, применение прогестина в комплексе с Дикирогеном способствовало нормализации МЦ, продолжительности и объема менструальной кровопотери у большинства пациенток, и эта тенденция сохранялась после отмены прогестинов при продолжении приема Дикирогена по сравнению с показателями до лечения. Дополнение лечения железосодержащим препаратом у пациенток с исходной железодефицитной анемией привело к нормализации уровня ферритина к 1-му визиту и гемоглобина – ко 2-му.
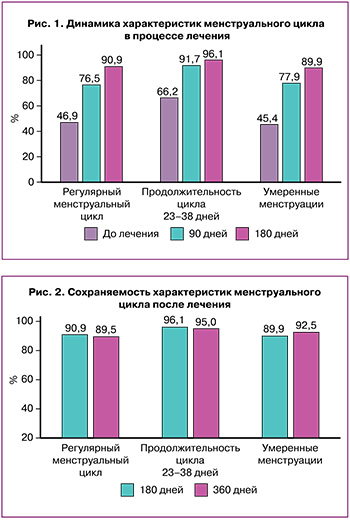
Вторичные исходы. Оценено сохранение нормального ритма МЦ, продолжительности и объема менструации после отмены комплекса «Дикироген» (визит 3 против визита 2) (рис. 2).
Цикличность МЦ была одинаковой, количество пациенток с умеренным объемом кровопотери во время менструации еще статистически значимо повысилось к визиту 3 до 92,5% против 89,9% на визите 2; равно как и количество женщин, использовавших 3–14 прокладок, немного увеличилось – с 90,8 до 92,9%, в среднем количество прокладок составило 9,9 и 8,8 шт. соответственно. Количество пациенток с продолжительностью менструаций 9 дней и более уменьшилось с 94,9 до 87,6%, а с нормальной продолжительностью, наоборот, увеличилось.
Индекс массы тела в процессе лечения снизился с 26,8 до 23,4 кг/м2 (нормальный вес) к 6 месяцам лечения и стабилизировался на этом уровне до 12 месяцев наблюдения. Между 6 и 12 месяцами окружность талии уменьшилась на 4 см (с 76 до 72 см).
Таким образом, после прекращения приема Дикирогена цикличность менструаций сохранялась на достигнутом уровне, а объем кровопотери еще статистически значимо уменьшился (на 39%), несмотря на сохранение продолжительности менструаций более 9 дней у большинства пациенток. Индекс массы тела и окружность талии уменьшились, анемия была излечена.
Нежелательные явления имели место у крайне незначительного количества пациенток (6 человек), отмечены между 1-м и 2-м визитами (в период приема прогестинов) и характеризовались появлением таких симптомов, как высыпания на коже, изжога, слабость, нерегулярный стул, запор, изжога (по одному случаю каждый).
Частота прекращения лечения. Между 1-м и 2-м визитами (в период приема гестагенов) из исследования выбыли 7 пациенток: по причине наступления беременности (3 женщины), самостоятельное решение (нормализация МЦ, выздоровление – 3), отказ от приема назначенных препаратов (1).
Обсуждение
Лечение дидрогестероном для регуляции МЦ в рутинной клинической практике в многоцентровом обсервационном исследовании Podzolkova N. et al. показало его эффективность на уровне 99,1% (по критерию ≥1 регулярного МЦ) и 79,1% (≥6 регулярных МЦ) в течение 6 месяцев [21].
В другом проспективном обсервационном исследовании достигнут регулярный МЦ в конце 3 цикла у 95,4% с продолжительностью МЦ в среднем 29,1 дня. При этом уровни половых гормонов, включая ФСГ, ЛГ, пролактин и эстрадиол, не показали статистически значимых различий до и после лечения дидрогестероном [22].
Ряд предыдущих исследований, где использовался дидрогестерон для регуляции МЦ, показали положительный результат у 96,7% пациентов в течение 3 месяцев и 94,8% – через 6 месяцев со средней продолжительностью МЦ после лечения 27,7–29,8 дня [23], приемлемая частота кровотечений была достигнута у 90,0% пациенток в период от 2 до 6 месяцев [24].
Сравнивая эти показатели с результатами настоящего исследования, можно констатировать, что комбинированное лечение дидрогестерон/Дикироген/железосодержащее ЛС, по сравнению с применением только дидрогестерона, не имело преимуществ. Однако через 6 месяцев разница имеет место, поскольку Дикироген показал эффект у 96,1% пациенток, что было выше по сравнению с приведенными результатами других авторов (90,0–94,8%) [8, 21–24].
При пероральном приеме микронизированного прогестерона МЦ стал регулярным у 81,3% женщин с АМК после 3 месяцев лечения [25]. В другом аналогичном исследовании эффектом были удовлетворены 88,6% женщин [26].
Оценивалось действие средства Дикироген в отношении регулярности МЦ. У 64,9% пациенток с СПКЯ через 3 месяца негормональной коррекции МЦ средством «Дикироген» достигнуто восстановление ритма менструаций в пределах 24–38 дней с вариабельностью не более 7 дней [27].
У пациенток с АМК-О и избытком массы тела/ожирением прием средства «Дикироген» на фоне модификации образа жизни способствовал сокращению длительности МЦ (31±12,04 дня на 2-м визите против 44±19,51 дня на 1-м; р=0,001), МЦ стал регулярным у 83% пациенток [28].
При назначении Дикирогена в качестве прегравидарной подготовки женщин с избыточной массой тела и ожирением через 80–90 дней у 87,81% установлен регулярный МЦ [29]. Эти результаты также ниже по сравнению с комплексом микронизированный прогестерон/Дикироген.
Существенным ограничением опубликованных исследований является отсутствие сведений о сохранении эффекта после завершения терапии на протяжении последующего периода. В настоящей работе такое исследование было выполнено, и оно показало отличный результат – регулярность МЦ и нормальная продолжительность менструального кровотечения сохранялись на достигнутом уровне еще в течение 6 месяцев наблюдения после окончания лечения, что говорит о стойком эффекте; а количество пациенток с умеренным объемом менструальной кровопотери даже увеличилась, что, вероятно, было получено за счет нормализации обменных процессов под действием мио-/D-хироинозитола в сочетании с витаминно-минеральным премиксом.
Средство «Дикироген», содержащее две активные формы инозитола в соотношении 5:1 (миоинозитола 1000 мг и D-хироинозитола 200 мг), марганец и фолиевую кислоту, изученное ранее у пациенток с СПКЯ, улучшало эндокринно-метаболические показатели, способствовало восстановлению овуляции и регулярности МЦ в течение 6 месяцев приема, а также способствовало снижению индекса массы тела и объема талии, в то время как прием комбинированных оральных контрацептивов приводил к увеличению массы тела и объема талии, а также к ухудшению показателей липидного спектра крови [15]. В некоторых работах показано нормализующее действие мио-/D-хироинозитола на гонадотропную функцию гипофиза (нормализация ЛГ/ФСГ) и углеводный обмен (снижение инсулинорезистентности) [11]. Было продемонстрировано, что применение фолиевой кислоты связано с нормализацией продолжительности МЦ (ОШ=0,80, 95% ДИ 0,68–0,94) [30], а более высокое содержание фолата – со снижением риска ановуляции на 10% [31]. Марганец, являясь компонентом различных ферментов (в т. ч. ферментов, модулирующих синтез холестерина и стероидных гормонов), влияет на множество метаболических процессов, а также на репродуктивную функцию за счет воздействия на гипоталамус [32]. Указанные механизмы, очевидно, действуют аналогично у пациенток с ОД, что и оказывает нормализующее действие на МЦ и объем менструальной кровопотери со стойким эффектом.
Среди пациентов, принимавших дидрогестерон в упомянутом выше многоцентровом исследовании, 1,6% сообщили о нежелательных явлениях [21]; в другом исследовании частота их составила 2,6%, которые считались не связанными с исследуемым препаратом [22], что не противоречит результатам, полученным в настоящем исследовании. Согласно литературным данным, при применении средства «Дикироген» нежелательные явления включали тошноту с частотой 0,37%, диарею с частотой 0,74–6,67% [27, 33].
Заключение
Терапия ОД прогестином/Дикирогеном/железосодержащим ЛС в первые 3 месяца с последующим приемом только Дикирогена в течение 3 месяцев является эффективной стратегией в достижении регуляции МЦ и объема менструальной кровопотери как во время лечения, так и в течение 6 месяцев после него, а также способствует устранению анемии и нормализации массы тела.
Положительные стороны и ограничения исследования
Настоящее исследование является работой высокой мощности, выполненной в условиях реальной клинической практики, и демонстрирует возможность использования средства «Дикироген» в комплексной терапии пациенток с ОД/ОМК с сокращением продолжительности приема гестагенов.
Ограничениями исследования являются отсутствие плацебо-контроля, потеря связи с 44% пациенток к визиту 3; не проводилось изучение гормонального и метаболического статуса пациенток в процессе лечения и после него, что не дает возможности установить механизм действия Дикирогена при данной нозологии и требует дополнительных исследований.



