Обоснование
Остеопороз (ОП) и саркопения (СП) – часто встречающиеся состояния при ревматоидном артрите (РА) [1–3]. Как ОП, так и СП могут быть осложнениями РА или первичными заболеваниями, формирующими коморбидный фон. Оба заболевания повышают риск падений, переломов и снижают качество жизни [4, 5]. Сосуществование у одного человека сниженной минеральной плотности кости (МПК) и низкой мышечной массы получило название «остеосаркопения» (ОСП), которая значительно утяжеляет все риски, связанные с изолированными ОП и СП [6, 7]. Нарушения состава тела и состояния костной ткани при РА могут развиваться под влиянием единых патогенетических механизмов, таких как влияние провоспалительных цитокинов, уменьшение физической активности вследствие ограничения подвижности суставов, а также сохраняющаяся необходимость использования пероральных глюкокортикостероидов (ГКС) в комплексной терапии РА [8, 9]. Кроме того, ГК и ряд других лекарственных препаратов, применяемых при лечении пациентов с РА, нередко вызывают ятрогенные поражения органов желудочно-кишечного тракта (ЖКТ), что в свою очередь может приводить к мальабсорбции и нарушениям белково-энергетического обмена, на фоне чего усугубляется дисбаланс состава тела [10, 11]. В настоящее время проблемы нутритивного статуса, объединяющего вопросы белково-энергетического обмена, макро- и микронутриентной недостаточности, связи с сопутствующими заболеваниями органов ЖКТ, привлекают все большее внимание интернистов. Разработаны различные методы изучения нутритивного статуса, включающие антропометрические измерения и индексы, инструментальную оценку состава тела, некоторые биохимические показатели, а также использование различных опросников, получивших широкое распространение в современной медицинской науке для решения самых разнообразных задач. С их помощью может быть оценена и физическая активность, недостаток которой у пациентов с РА также служит причиной усугубления ОП и СП. Физическая активность является совокупностью повседневной деятельности для обеспечения жизненных потребностей человека. Основная составляющая физической активности – движения, обеспечиваемые сокращением поперечнополосатой мускулатуры [12]. Международный опросник физической активности (International Physical Activity Questionnaire – IPAQ) используется в различных исследованиях, в т.ч. пациентов с РА [13]. В российской популяции данных по физической активности при РА с использованием IPAQ нет.
Цель исследования: установить ассоциации между ОП, СП и ОСП с нутритивным статусом и физическим состоянием женщин с РА.
Методы
В одноцентровое одномоментное исследование включены 157 женщин с РА, диагностированным на основании критериев ACR/EULAR, 2010 [14], проходивших стационарное или амбулаторное обследование и лечение в ФГБНУ НИИР им. В.А. Насоновой в 2022–2023 гг.
Всем пациенткам проведен опрос по анкете, специально созданной в соответствии с целями данной работы, с последующим внесением демографических и анамнестических данных в индивидуальную карту, также содержавшую результаты обследования.
Помимо стандартного осмотра и оценки показателей активности РА (СОЭ, С-реактивный белок, DAS28-СОЭ) для определения состояния костной и мышечной ткани проводилась двуэнергетрическая рентгеновская абсорбциометрия (Dual X-ray Absorptiometry – DXA, Lunar, GE, USA), по результатам которой диагностировали ОП и СП. Критерием ОП стало снижение МПК в поясничном отделе позвоночника (L1-L4) и/или проксимальном отделе бедра, где оценивались шейка бедра (ШБ) и общий показатель бедра (ОПБ). ОП диагностировали при значениях Т-критерия ≤-2,5 стандартных отклонений (СО) у женщин в постменопаузе или Z-критерия ≤-2,0 СО у женщин с сохраненной менструальной функцией. Также всем женщинам выполнялось DXA-сканирование по программе «Все тело» для определения массы мышц конечностей – аппендикулярной мышечной массы (АММ) и расчета аппендикулярного мышечного индекса (АМИ), представляющего собой отношение АММ (кг) к росту человека (м2). АММ <15 кг и/или АМИ <5,5 кг/м2 расценивали как СП. Об ОСП в рамках данной работы говорили при сочетании ОП и СП.
Для совокупной оценки нутритивного статуса использовали антропометрию, опросник MNA, определение потребления кальция с продуктами питания и содержание в сыворотке крови общего белка, альбумина, креатинина и 25(ОН)D. Оценка сывороточного уровня 25(ОН)D проведена с использованием иммунохемилюминисцентного анализатора Cobas E411 и набора реагентов Elecsys Vitamin D total, Roche.
Антропометрия включала определение роста и массы тела, расчет индекса массы тела (ИМТ), измерение окружности талии, левого плеча и голени; при известной леворукости в анализ включали показатели правых конечностей.
Согласно опроснику MNA [15], нутритивный статус оценивался в баллах, сумма меньше 24 баллов соответствовала его снижению. Также по MNA анализировали режим потребления пищи, богатой белком.
Суточное поступление кальция с пищей рассчитывали на основании заполнения анкеты потребления молочных продуктов по формуле: суточное потребление кальция = кальций молочных продуктов + 250 мг.
Физическое состояние определялось при помощи опросника IPAQ [16], тестов оценки силы и функционального состояния мышц (физической работоспособности).
С помощью автоматизированной русскоязычной версии опросника IPAQ определяли энергетические затраты для разных видов деятельности, общий недельный расход энергии, уровень физической активности (высокий, средний или низкий) (URL: https://drive.google.com/file/d/1gNYaRNYGXq_1QHk1RsWglWkVCthOh94I/view). С использованием анкеты IPAQ рассчитывали частоту и время занятий с интенсивной, умеренной физической нагрузкой и пеших прогулок.
По кистевой динамометрии и тесту «Встать со стула 5 раз» оценивали мышечную силу верхних и нижних конечностей соответственно; по тесту «Встаньи иди» и скорости ходьбы на 4 м – функциональное состояние скелетной мускулатуры (физическую работоспособность). Использовали критерии низкой мышечной силы (сила сжатия кисти <16 кг; время выполнения теста «Встать со стула» >15 с) и сниженной физической работоспособности (скорость ходьбы ≤0,8 м/с; время выполнения теста «Встань и иди» ≥20 с), представленные в пересмотренном европейском консенсусе по определению и диагностике саркопении [4].
Исследование осуществлено в рамках фундаментальной научной темы (№ 1021051403074-2).
Критерии соответствия
Критерии включения: подписанное информированное согласие, возраст – 40–75 лет, отсутствие в анамнезе оперативного лечения с имплантацией эндопротезов крупных суставов конечностей, металлоконструкций для остеосинтеза и вертебропластики.
Критерии невключения: 4-й функциональный класс РА, наличие асептических некрозов костей и заболеваний с известным катаболическим влиянием на костную и мышечную ткань, воспалительные и нейрогенные миопатии, когнитивные нарушения. Когнитивные нарушения оценивались по способности пациента ответить на вопросы анкет, предназначенных для самостоятельного заполнения, а также выполнения тестов оценки мышечной силы и физической работоспособности.
Этическая экспертиза
Исследование одобрено локальным комитетом по этике ФГБНУ НИИР им. В.А. Насоновой (протокол № 02 от 27.01.2022).
Статистический анализ
Размер выборки предварительно не рассчитывался. Статистическая обработка данных проводилась с использованием пакета статистических программ STATISTICA (data analysis software system, version 12, StatSoft, Inc., США). Количественные непрерывные данные представлены в виде М±СО (среднее арифметическое±стандартное отклонение) или Ме [Q25; Q75] (медиана [межквартильный размах]) в зависимости от их соответствия закону нормального распределения. Дискрет-ные величины представлены в виде абсолютных и относительных частот, n (%).
Для сравнения результатов использовали метод χ2, точный критерий Фишера, Т-критерий Стьюдента и U-тест Манна–Уитни (для двух групп), критерий Краскелла–Уоллиса (множественное сравнение) для дискретных и непрерывных величин соответственно. Для установления ассоциаций между параметрами использован однофакторный логистический регрессионный анализ с участием пациентки без патологических изменений МПК, с нормальной мышечной массой и ОП или СП или ОСП. Результаты логистической регрессии представлены как отношение шансов (ОШ) и 95%-ного доверительного интервала (95% ДИ). Статистическая значимость полагалась при р<0,05.
Результаты
Объекты (участники) исследования
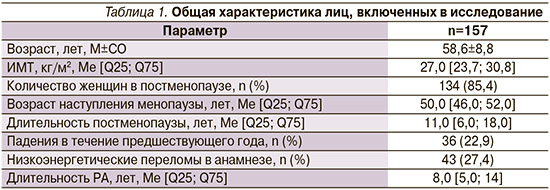
Обследованы 157 женщин с РА, общая характеристика которых представлена в табл. 1. Большинство (85,4%) пациенток находились в постменопаузальном периоде. Только у 33,1% женщин ИМТ находился в пределах нормальных значений. У 36,9 и 28,7% пациенток он соответствовал избыточной массе тела и ожирению соответственно. Низкий ИМТ отмечен у 1,3% обследованных женщин. Более половины (57,3%) участниц исследования принимали препараты кальция и витамина D.
Основные результаты исследования
У 59 (37,6%) обследованных лиц по результатам DXA выявлены ОП, СП и ОСП: у 27 (17,2%), 16 (10,2%) и 16 (10,2%) пациенток соответственно. Женщины с СП были значимо моложе и имели меньший индекс коморбидности по сравнению с таковыми двух других групп, а пациентки с ОП имели значимо более высокий ИМТ. Группы не различались по длительности РА и постменопаузы в зависимости от наличия ОП, СП или ОСП (табл. 2).
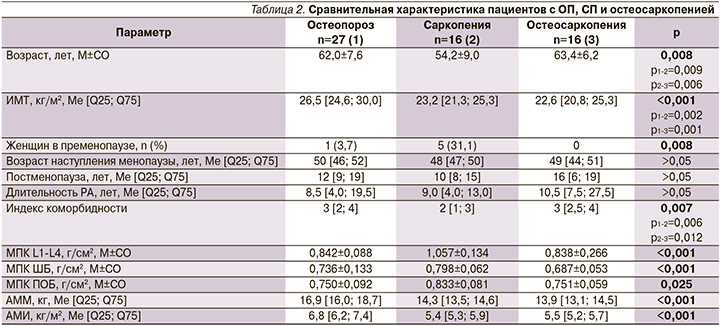
Группы не различались по показателям активности заболевания (СОЭ, СРБ, DAS28-СОЭ). Также не было значимых различий по частоте использования и кумулятивной дозе ГКС и по частоте биологической терапии. Препараты кальция и витамина D принимали 20 (74,1%) пациенток с ОП и по 12 (75%) с СП и ОСП (р>0,05).
При изучении нутритивного статуса выявлены значимые различия между группами по показателю опросника MNA, причем худший результат оказался у пациенток с ОСП, а различий между женщинами с ОП и СП по этому параметру не было (р>0,05). Суточное потребление кальция с пищей оказалось значимо более высоким у пациенток с ОП.
Антропометрические показатели, такие как окружность плеча, голени и талии, значимо различались в зависимости от наличия ОП, СП и ОСП, в то же время не получено разницы между группами по показателям общей жировой массы. Не обнаружено различий по лабораторным показателям, кроме уровня креатинина, который оказался значимо более высоким у пациенток с ОП (табл. 3).
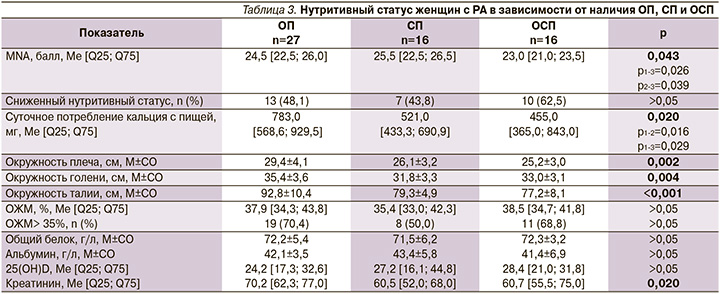
Не было различий между группами по частоте потребления белковой пищи, а также по частоте сопутствующих заболеваний органов ЖКТ в зависимости от наличия ОП, СП и ОСП.
Физическое состояние пациенток с ОП, СП и ОСП практически не различалось ни по данным тестов оценки силы и функционального состояния мышц, ни по опроснику IPAQ. Выявлены только различия по скорости ходьбы между пациентками с ОП и женщинами с СП (0,75 [0,66; 0,90] м/с и 0,92 [0,81; 1,13] м/с соответственно, р=0,036) и по еженедельным энергетическим затратам на занятия с интенсивной физической нагрузкой – между лицами с ОП и ОСП (526,4 [0; 1780,0] и 0 [0; 226,8] ккал/нед. соответственно, р=0,031).
В логистическом регрессионном анализе установлены ассоциации между наличием ОСП с частотой занятий с интенсивной физической нагрузкой <2 дней в неделю (ОШ=3,38 (95% ДИ: 1,04; 10,87), р=0,042), с оценкой нутритивного статуса по опроснику MNA (ОШ=1,39 (95% ДИ: 1,03; 1,85), р=0,029), потреблением кальция с пищей менее 500 мг/сут (ОШ=4,02 (95% ДИ: 1,28; 12,61), р=0,018).
Обсуждение
Резюме основного результата исследования
Основной целью представленного исследования был поиск ассоциаций между наличием ОП, СП и ОСП у женщин с РА и параметрами нутритивного статуса и физического состояния, в т.ч. оцененными с помощью опросников MNA и IPAQ. Установлено, что потребление кальция с пищей менее 500 мг/сут. повышало риск ОСП в 4 раза, также она ассоциирована с общей оценкой нутритивного статуса по опроснику MNA (ОШ=1,39). Кроме того, риск наличия ОСП повышался более чем в 3 раза при низкой частоте занятий с интенсивной физической нагрузкой. Не найдено ассоциаций между наличием изолированного ОП и СП с параметрами нутритивного статуса и физического состояния у женщин с РА.
Обсуждение основного результата исследования
Результаты оценки нутритивного статуса женщин с РА с помощью опросника MNA показали, что частота низкого результата была практически одинаковой у женщин с ОП и СП (48,1 и 43,8% соответственно) и несколько большей у лиц с ОСП (62,5%), также для этой группы была установлена ассоциация с результатом по опроснику MNA в регрессионном анализе. В работах других европейских исследователей, также применявших этот опросник, частота сниженного нутритивного статуса была сопоставимой с нашими результатами и составляла 33,8 и 42,8% [17, 18]. Некоторые авторы показали более яркую связь между нутритивным статусом по опроснику MNA и наличием ОП [19, 20], однако в нашем исследовании сравнение проводилось не с пациентами с нормальной МПК и составом тела, а с лицами, имевшими СП или еще более тяжелое состояние – ОСП.
Несмотря на отсутствие различий в частоте потребления молочных продуктов по данным опросника MNА, по количеству кальция, поступающего с пищей, мы получили значимые различия в сравнительном анализе, а регрессионный анализ показал значительное увеличение риска наличия ОСП при низком потреблении кальция. Сходные результаты были представлены в работах F. Petermann-Rocha et al. и M.H. Seo et al. [21, 22]. Потребление кальция с пищей пациентами в этих исследованиях было низким и сопоставимым с таковым в нашем исследовании пациентов с СП и ОСП. А в работах других авторов, в которых потребление кальция было значительно более высоким, взаимо-связи между суточным поступлением кальция с пищей и СП не было найдено [23, 24].
При сравнительном анализе мы не обнаружили существенных различий в физическом состоянии пациенток как по опроснику IPAQ, так и с помощью тестов оценки силы и функционального состояния мышц. В то же время регрессионный анализ показал, что отсутствие интенсивных физических нагрузок ассоциировано с наличием ОСП. А в работе G. Dallanezi et al. также на основании данных опросника IPAQ показано, что наличие ОП связано с более малоподвижным образом жизни по сравнению с лицами с нормальной МПК и остеопенией [25]. Необходимость объективизации результатов, полученных с помощью опросника IPAQ, неоднократно обсуждалась [26, 27], но в настоящем исследовании результаты объективных тестов практически не различались между группами в силу поставленных задач – исследование групп пациенток с РА с сопутствующими ОП, СП и ОСП.
Ограничения исследования
К ограничениям исследования относятся использование общих тестов оценки мышечной силы и работоспособности, пациенты с РА могут их не выполнять в силу выраженных суставных изменений, а не истинно мышечной слабости; среди обследованных лиц превалировали пациенты с умеренной и высокой активностью заболевания. Доля лиц с низкой активностью или ремиссией составила 3,8%.
Заключение
Таким образом, суммарная доля лиц с ОП, СП и ОСП составила 37,6%. ОСП ассоциировалась с нутритивным статусом, оцененным по опроснику MNA, низким потреблением кальция с продуктами питания и небольшой частотой занятий с интенсивной физической нагрузкой. Полученные нами сведения о наличии ассоциации между ОСП и недостаточным потреблением кальция и литературные данные об аналогичных ассоциациях позволяют сделать предположение, что именно у лиц с низким потреблением кальция с пищей назначение его в виде лекарственных добавок может оказаться полезным для предупреждения снижения мышечной массы, однако для подтвержения этого предположения необходимо проведение проспективного исследования с включением большего числа пациентов.



