Как известно, фибрилляция предсердий (ФП) является серьезным фактором риска развития сердечно-сосудистых осложнений и смертность при ФП в 2 раза выше, чем при синусовом ритме [1—3]. Наличие ФП также ухудшает ближайший и отдаленный прогноз после кардиохирургических вмешательств, значительно повышая риск развития тромбоэмболических осложнений, острой сердечной недостаточности (ОСН) и смерти [1, 4, 5]. ФП представляет и большую финансовую проблему для системы здравоохранения: часто служит основанием для госпитализации больных, при этом стоимость лечения таких больных на 35—40% выше, чем больных той же возрастной группы без ФП. Ожидается двукратное увеличение числа пациентов с ФП в течение последующих 20 лет [1, 2].
В настоящее время разработаны интервенционные и хирургические методы лечения ФП, которые показали высокую эффективность по сравнению с медикаментозной антиаритмической терапией, а также обладают фармакоэкономической выгодой, значительно улучшают качество жизни и повышают выживаемость больных ФП [6, 7]. Необходимо отметить, что обоснование проведения радиочастотной абляции (РЧА) и ее высокая антиаритмическая эффективность связаны с установлением эктопических фокусов в области ганглионарных сплетений левого предсердия (ЛП), что доказало принципиальную роль ЛП и легочных вен в запуске и поддержании ФП, по крайней мере, у 80—90% больных [8—10].
Однако эффективность РЧА при ФП колеблется от 60 до 95% и зависит от влияния множества факторов: формы ФП (пароксизмальная, персистирующая или хроническая), длительности аритмического анамнеза, выраженности структурно-функционального ремоделирования сердца, наличия сочетанной патологии, способов РЧА и т.д. [3, 9, 11]. Поэтому представляется важным дооперационное прогнозирование рецидивов ФП, так как у больных с сохраняющимся синусовым ритмом отдаленная смертность, обусловливаемая преимущественно инсультом и прогрессирующей хронической сердечной недостаточностью (ХСН), значительно ниже, чем при наличии рецидивов ФП [4, 12, 13].
В последние годы у больных ФП наряду с катетерной РЧА широко применяются интраоперационные (хирургические) методы РЧА, сочетающейся с аортокоронарным шунтированием (АКШ) и/или коррекцией клапанных пороков сердца [5, 13—15]. При этом не только устраняются зоны аритмии, но и значительно снижается аритмогенный потенциал благодаря реваскуляризации миокарда и регрессу структурно-функционального ремоделирования сердца [4, 12, 14, 16]. Важным условием широкого применения в клинической практике метода РЧА, обеспечивающим ее высокую эффективность по сравнению с медикаментозной терапией, является прогнозирование рецидивов ФП в отдаленном периоде, что позволяет уточнить показания к процедуре РЧА и разработать превентивные меры, улучшающие результаты самой процедуры [11, 13, 17, 18].

Целью настоящего исследования явилось уточнение факторов риска возникновения ФП и прогнозирование ее рецидивов после процедуры РЧА в сочетании с АКШ у больных пароксизмальной формой ФП.
Материал и методы
Обследованы 254 больных (147 мужчин и 107 женщин) ишемической болезнью сердца, сочетающейся с пароксизмальной формой ФП. Больным одномоментно проводилось АКШ и/или маммарокоронарное шунтирование и РЧА вокруг устьев всех 4 легочных вен в Федеральном центре сердечно-сосудистой хирургии (Пенза). В исследование включили больных, которым РЧА выполнялась первично и однократно. Возраст больных составил от 48 до 68 лет (в среднем 59,1±6,1 года).
Критериями исключения из исследования являлись: синоатриальная и атриовентрикулярная блокады, включая их латентные формы; клапанные пороки сердца; дополнительные предсердно-желудочковые проводящие пути; патология щитовидной железы с нарушением гормональной активности; инфаркт миокарда и мозговой инсульт, перенесенные в последние 6 мес до включения в исследование.
В течение 30 сут после операции у 95 (37,4%) больных возникли ранние рецидивы ФП и/или трепетание предсердий, а у остальных 159 (62,6%) был синусовый ритм (табл. 1). Больным после купирования тахиаритмии назначали антиаритмические препараты (ААП). При этом у 40 больных через 3 мес после отмены ААП в дальнейшем наблюдался стабильный синусовый ритм. В то же время из 33 больных, которые не имели пароксизмов ФП в ранний послеоперационный период, спустя 9–12 мес после операции у 23 больных впервые регистрировались поздние рецидивы ФП, требующие приема ААП.
Таким образом, у 124 больных пароксизмов ФП после операции не выявлено (1-я группа), у 40 больных с ранним рецидивом ФП аритмия сохранялась и в дальнейшем (2-я группа) и у 33 возникли поздние рецидивы ФП (3-я группа). В результате через 12 мес после операции у 166 (69,5%) больных наблюдался стабильный синусовый ритм, а у 73 (30,5%) имелись рецидивы ФП, при которых требовались ААП. В зависимости от развития рецидивов ФП ретроспективно анализировали структурно-функциональные и электрофизиологические показатели сердца.
Сравнение демографических и исходных клинико-инструментальных данных позволило выявить достоверное различие возраста, давности ФП, частоты застойной ХСН и дисфункции почек (скорость клубочковой фильтрации — СКФ<60 мл/мин/1,73 м2) у больных без рецидива ФП по сравнению с группами больных, имеющих ранний и поздний рецидивы ФП (табл. 2). Однако между 2-й и 3-й группами, за исключением давности ФП, различие было недостоверным.

Структурно-функциональное состояние сердца изучали с помощью допплер-эхокардиографии на аппарате Acuson X300 («Siemens-Acuson», Германия) при синусовом ритме. Вычис-ляли конечный систолический и диастолический размеры левого желудочка (ЛЖ), переднезадний размер (диаметр) ЛП, фракцию выброса (ФВ) ЛЖ, сердечный индекс и индекс массы миокарда ЛЖ. Диастолическую функцию ЛЖ оценивали путем спектрального анализа трансмитрального диастолического потока при синусовом ритме и определяли максимальную скорость быстрого и медленного наполнения ЛЖ и их соотношение (Ve, Va, Ve/Va), время изоволюмического расслабления, время замедления потока в фазу быстрого наполнения ЛЖ, а также систолическое давление в легочной артерии. На обзорных рентгенограммах органов грудной клетки определяли кардиоторакальное отношение (КТО). СКФ рассчитывали по формуле MDRD (Modification of diet in renal disease study).
Электрофизиологическое исследование сердца проводили с помощью чреспищеводной электростимуляции (ЧПЭС) ЛП на аппарате Astrocard (ЗАО «Медитек», Россия). Вычисляли продолжительность кардиоцикла (интервал R-R), дисперсию зубца Р (dP), время восстановления функции синусного узла (ВВФСУ), корригированное ВВФСУ (КВВФСУ), эффективный рефрактерный период ЛП (ЭРПЛП), показатель «точки Венкебаха», частотные пороги индуцирования аритмии (ЧПИА) и ишемии миокарда (ЧПИИ). ЧПЭС в режимах программируемой, частой и сверхчастой электростимуляции ЛП проводили для оценки «аритмогенной готовности» предсердий и эффективности РЧА [19]. Процедуру РЧА считали эффективной, если при ЧПЭС не удавалось индуцировать ФП или индуцировался короткий (менее 30 с) пароксизм ФП; частично эффективная РЧА означала возможность индуцировать пароксизм ФП более «агрессивным» режимом ЧПЭС и/или двукратное увеличение исходной величины ЧПИА.
Холтеровское мониторирование (ХМ) электрокардиограммы (ЭКГ) выполняли с помощью системы Astrocard (ЗАО «Медитек», Россия) для выявления нарушений ритма сердца, в том числе коротких и бессимптомных пароксизмов ФП. ХМ ЭКГ проводили от 7 до 24 ч неоднократно и суммарно — от 34 до 70 ч (53,9±14,4 ч).
Инструментальные исследования выполняли за несколько дней до операции, в ранний послеоперационный период и через 12 мес после операции.
Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации Всемирной медицинской ассоциации. Протокол исследования был одобрен локальным этическим комитетом института.
Статистическую обработку данных проводили с использованием пакета прикладных программ Statistica 6.0.
При нормальном распределении признаков достоверность различий в группах определяли с помощью t-критерия Стьюдента. Взаимосвязи качественных переменных определяли с помощью коэффициента ранговой корреляции Спирмена (R). Для сравнения дискретных переменных использовали критерий χ2. Данные представлены в виде среднего значения и стандартного отклонения (M±SD). Различия считали достоверными при р<0,05.
Результаты
Необходимо отметить, что у больных с ранним рецидивом ФП периоперационный инфаркт миокарда, ишемический инсульт и острое повреждение почек выявлялись достоверно чаще, а также длительность операции, искусственного кровообращения (ИК), искусственной вентиляции легких (ИВЛ) и медикаментозной инотропной поддержки была выше, чем у больных без раннего рецидива ФП (табл. 3). Однако частота развития ОСН III—IV класса по Killip достоверно не различалась (p>0,05), хотя была выше у больных с ранним рецидивом ФП, летальность у которых составила 8,4%, а у больных без рецидива ФП — 1,9% (p=0,03).
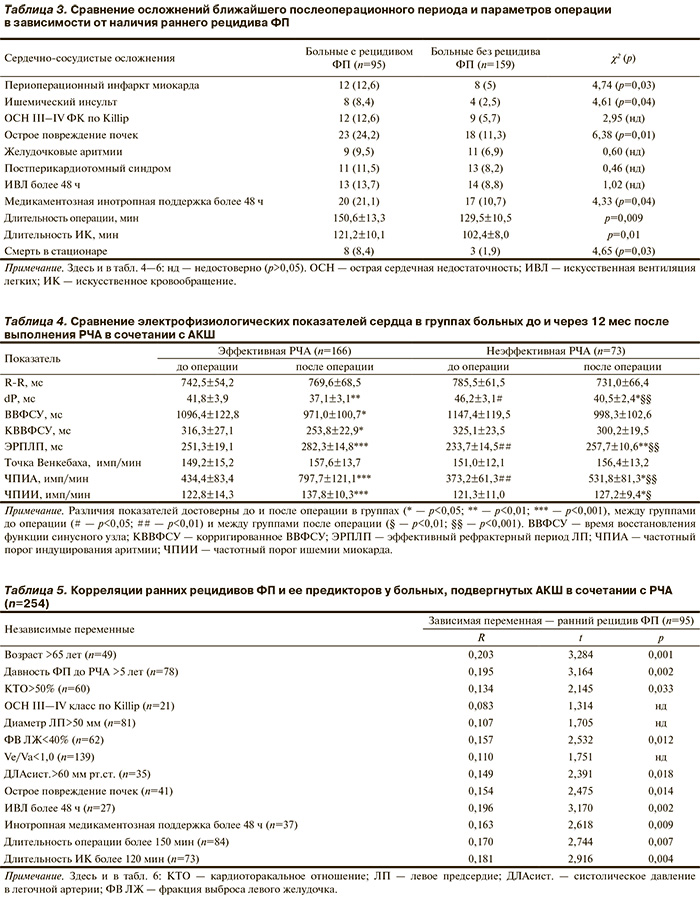
Сравнение электрофизиологических показателей сердца до операции выявило их практическую идентичность в группах (табл. 4), а также свидетельствовало о повышенной аритмогенной «готовности» предсердий, в частности увеличении дисперсии зубца Р (dP), уменьшении показателей ЭРПЛП и ЧПИА. При повторном электрофизиологическом исследовании, проведенном через 12 мес после операции, выявлены достоверные изменения изучаемых показателей, которые оказались выраженными в группе больных с успешной РЧА, и отражали повышение электрической стабильности предсердий.
Кроме того, послеоперационные показатели ЭРПЛП и ЧПИА у больных 1-й группы оказались лучше, чем во 2-й группе. Это объясняется обратной динамикой структурно-функционального ремоделирования сердца благодаря улучшению коронарного кровоснабжения и отсутствию ФП после операции. Несмотря на то что в обеих группах достоверно увеличились показатели ЧПИИ, которые свидетельствуют о повышении ишемического порога миокарда, в 1-й группе ЧПИИ был выше, чем во 2-й группе (в среднем на 7,7%; p=0,017).
Анализ причин раннего рецидива ФП показал, что основными факторами риска возникновения ФП наряду с гемодинамическими и электрофизиологическими показателями являются ближайшие послеоперационные осложнения, а также продолжительность операции более 150 мин и ИК более 120 мин (табл. 5).
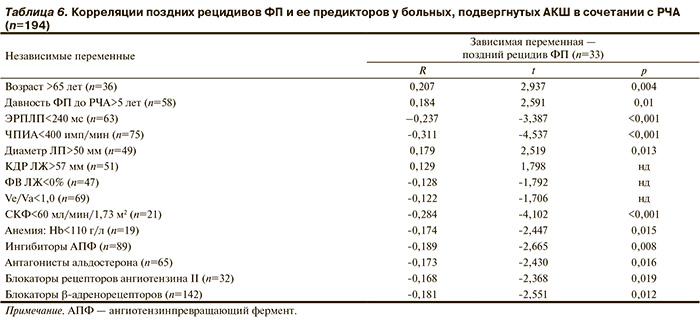
Анализ причин поздних рецидивов ФП спустя 12 мес после операции выявил корреляции с известными предикторами ФП (табл. 6). В частности, поздний рецидив ФП тесно ассоциировался с возрастом старше 65 лет, давностью ФП более 5 лет, ЭРПЛП<240 мс, ЧПИА<400 имп/мин, СКФ<60 мл/мин/1,73 м2.
Кроме того, показано, что в послеоперационном периоде лечение ингибиторами ангиотензинпревращающего фермента (АПФ), антагонистами альдостерона, блокаторами рецепторов ангиотензина II и β-адреноблокаторами уменьшает риск позднего рецидива ФП у больных, подвергнутых РЧА в сочетании с АКШ.
Обсуждение
По данным литературы, эффективность однократно выполненной катетерной РЧА без приема ААП составляет 57%, а повторных процедур — 71% [6, 7]. Проведенное нами исследование подтвердило тесную связь поздних рецидивов ФП с дооперационным диаметром ЛП. Однако в этом вопросе дискуссионной является величина размера/объема ЛП как предиктора рецидивов ФП после процедуры РЧА [11, 13, 15, 16].
Так, N. Sunderland и соавт. [11] провели мета-анализ 12 исследований, отвечающих требованиям доказательной медицины, в которых изучалось влияние дооперационного размера ЛП на вероятность рецидива ФП после процедуры «лабиринт». Выявлено, что у больных с рецидивом ФП исходный размер ЛП был достоверно больше, чем у больных со стабильным синусовым ритмом. С точки зрения ценности для прогнозирования неэффективности процедуры «лабиринт» размера ЛП показано, что объем ЛП более 135 мл имеет специфичность 100%, диаметр ЛП более 60 мм — чувствительность 100%. В одном исследовании показано, что диаметр ЛП менее 48 мм имеет чувствительность 100% в отношении сохранении синусового ритма после процедуры «лабиринт». Кроме того, не выявлено убедительных доказательств того, что диаметр ЛП менее 43 мм ассоциируется с полным успехом процедуры «лабиринт».
Необходимо отметить, что размеры ЛП более 60 мм при ФП наиболее характерны для больных митральными и/или аортальными пороками [4, 5], а у больных ФП неклапанного генеза диаметр ЛП крайне редко достигает этих размеров. В нашем исследовании достоверной оказалась корреляция поздних рецидивов ФП после 12 мес РЧА с дооперационным диаметром ЛП более 50 мм (R=0,179; p=0,013). Подтверждением этому является то, что больных с длительным анамнезом ФП и размером ЛП более 50 мм не рекомендуют включать в клинические исследования, так как ставится под сомнение эффективность процедуры РЧА [10, 12, 18, 20].
Среди потенциальных предикторов рецидива ФП после РЧА в сочетании с операцией АКШ необходимо отметить электрофизиологические маркеры «аритмической уязвимости» предсердий. Так, W.P. Beukema и соавт. [13] у пожилых больных ФП, подвергнутых кардиохирургическому вмешательству и процедуре «лабиринт», предиктором рецидива ФП кроме длительности аритмии и дооперационного диаметра ЛП определяли амплитуду волн f менее 0,1 мВ, снятой на ЭКГ до операции. При этом ФВ и размеры полости ЛЖ, инвазивные показатели гемодинамики не прогнозировали рецидива ФП после процедуры «лабиринт». Кроме того, стабильный синусовый ритм ассоциировался с уменьшением размеров ЛП и приемом ингибиторов АПФ после операции. По данным электрофизиологических исследований сердца у больных пароксизмальной формой ФП, нами установлено, что как исходные показатели ЭРПЛП и ЧПИА, так и их послеоперационные значения в группе больных со стабильным синусовым ритмом были достоверно выше, чем в группе больных с поздним рецидивом ФП. Выявлена также тенденция при сравнении исходных значений дисперсии зубца P в группах больных с рецидивом ФП и с сохраняющимся синусовым ритмом.
Нами также установлено, что одним из важных предикторов рецидивов ФП является дисфункция почек. Так, у больных с ранними рецидивами ФП острое повреждение почек диагностировалось в 24,2% случаев, а в отсутствие рецидивов ФП — в 11,3% (χ2=6,38; p=0,01). Кроме того, в группе больных с ранними и поздними рецидивами ФП хроническая болезнь почек со СКФ<60 мл/мин/1,73 м2 выявлялась в 30 и 27,3% случаев соответственно, а в группе больных со стабильным синусовым ритмом после операции — в 12,1% (p<0,05) Показано, что отдаленные результаты процедуры РЧА также зависят от послеоперационной динамики структурно-функциональных показателей сердца. Так, существенное улучшение систолической и диастолической функций сердца после операции АКШ способствует повышению аритмического порога миокарда и поддержанию синусового ритма и тем самым повышается эффективность РЧА. В свою очередь устранение ФП улучшает ближайший послеоперационный прогноз, значительно снижая риск развития тромбоэмболических осложнений и ОСН, а также летальность. Кроме того, процедура РЧА существенно не влияет на продолжительность операции АКШ и не увеличивает суммарного операционного риска сердечно-сосудистых осложнений [4, 5, 14, 15].
Нами выявлено, что предикторами рецидивов ФП в ранний послеоперационный период наряду с возрастом, длительностью ФП и легочной гипертензией, являются длительность ИК, проведение ИВЛ и инотропной медикаментозной поддержки более 48 ч после завершения операции.
Заключение
Выявлено, что основными предикторами поздних рецидивов фибрилляции предсердий являются пожилой возраст и дооперационный размер левого предсердия более 50 мм.
Риск рецидивов фибрилляции предсердий также коррелирует с послеоперационной динамикой структурно-функциональных и электрофизиологических показателей сердца, функциональным состоянием почек. Улучшение диастолической функции левого желудочка, вызванное восстановлением коронарной перфузии и локальной сократимости миокарда, способствует стабилизации синусового ритма после аортокоронарного шунтирования и радиочастотной абляции. Эффективный рефрактерный период ЛП менее 240 мс и частотный порог индуцирования аритмии ниже 400 имп/мин ассоциируются с высокой вероятностью рецидивов фибрилляции предсердий. Установлено, что спустя 12 мес после выполнения радиочастотной абляции в ходе аортокоронарного шунтирования у больных с пароксизмальной формой фибрилляции предсердий стабильный синусовый ритм без применения антиаритмических препаратов сохраняется в 69,5% случаев, а поздние рецидивы фибрилляции предсердий отмечаются в 13,8%. Это свидетельствует о высокой эффективности и целесообразности выполнения одномоментных кардиохирургических вмешательств в сочетании с радиочастотной абляцией у больных с пароксизмальной формой фибрилляции предсердий.



