Способность кардиомиоцитов изменять электрофизиологические свойства в ответ на действие патогенных факторов определяется как электрическая нестабильность миокарда (ЭНМ). В зависимости от силы раздражителя подобная ответная реакция клинически может проявляться фатальными нарушениями ритма сердца и проводимости [1]. Своевременное выявление и коррекция ЭНМ позволят предотвратить неблагоприятные исходы [2]. Среди предикторов активно исследуются неинвазивные электрокардиографические параметры, в частности, длительность интервалов QT и J—T, их корригированные значения (QTc и J—Tc соответственно), а также дисперсии (QTd и J—Td). Установлено, что удлинение интервала QTc (450 мс и более) и увеличение QTd (60 мс и более) служат маркерами неблагоприятных сердечно-сосудистых исходов [3, 4]. Мужской пол считается самостоятельным фактором риска развития сердечно-сосудистых заболеваний (ССЗ) и внезапной сердечной смерти (ВСС) [2, 5]. Так, у мужчин отмечаются более раннее начало и быстрое прогрессирование CCЗ, чаще диагностируются артериальная гипертензия (АГ) и синдром обструктивного апноэ/гипопноэ во сне (СОАГС) [5, 6]. Однако крайне мало работ по изучению особенностей циркадных изменений интервалов QT и J—T во взаимосвязи с динамикой частоты сердечных сокращений (ЧСС), артериального давления (АД) и дыхания.
Цель настоящего исследования — оценить частоту выявления удлиненного интервала QTс и увеличенной QTd при СОАГС различной степени тяжести у мужчин с АГ, установить предикторы увеличения длительности интервалов QTc и J—Tc.
Материал и методы
На базе поликлиники и госпиталя ФКУЗ «Медико-санитарная часть МВД России по Воронежской области» проводилось одномоментное (поперечное) исследование. Критерии включения в исследование: мужской пол, возраст от 20 до 60 лет, впервые диагностированная АГ при очередной ежегодной диспансеризации, жалобы на храп и/или повышенную дневную сонливость, добровольное согласие пациента на участие в исследовании. Критерии исключения из исследования: ассоциированные с АГ ССЗ, постоянная форма фибрилляции предсердий, полные блокады ножек пучка Гиса, сахарный диабет и другие эндокринные заболевания, прием антиаритмических препаратов и антибиотиков. Согласно указанным критериям в исследование включены 138 мужчин в возрасте от 22 до 59 лет (средний возраст 40,5±6,9 года). Средний индекс массы тела (ИМТ) достигал 34,5±4,7 кг/м2. Длительность наблюдения от момента выявления АГ до госпитализации в стационар составила от 3 до 6 нед. Обследование некоторых пациентов проводили на фоне антигипертензивной терапии, включавшей прием препаратов из следующих групп: ингибиторы ангиотензинпревращающего фермента (эналаприл или периндоприл), диуретики (индапамид) и β-адреноблокаторы (метопролол). Монотерапия использовалась у 15 (10,9%), комбинированная терапия из двух препаратов — у 29 (21,0%), из трех препаратов — у 8 (5,8%).
 Диагностику АГ проводили в соответствии с клиническими рекомендациями [5]. С целью выявления поражения органов-мишеней рассчитывали скорость клубочковой фильтрации (СКФ) по формуле CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration) и индекс массы миокарда левого желудочка (ИММЛЖ), используя универсальный медицинский калькулятор [7]. Всех пациентов тестировали по Эпвортской шкале дневной сонливости (Epworth Sleepiness Scale, ESS). Колебание суммарной оценки по ней может достигать от 0 до 24 баллов. Суммарная оценка 0—10 баллов характеризует отсутствие дневной сонливости, 11—15 баллов — избыточную и 16—24 балла — выраженную дневную сонливость [8]. Диагностику СОАГС осуществляли при 24-часовом полифункциональном исследовании с кардиореспираторным мониторированием во время сна с 1-го по 3-й день после госпитализации в терапевтический стационар. На протяжении суток одно-временно регистрировали: электрокардиограмму (ЭКГ) в 12 отведениях, АД (по тонам Короткова и осциллометрическим методом), интегральную реопневмограмму и актограмму, во время сна — насыщение кислородом гемоглобина в периферической крови (SpO2) и ороназальный поток воздуха. Датчик регистрации ороназального потока и портативный пульсоксиметр пациенты самостоятельно накладывали перед сном после предварительного инструктажа. Суточное мониторирование АД (СМАД) проводили в автоматическом режиме с интервалами 15 мин (с 7.00 до 23.00) и 30 мин (с 23.00 до 7.00). Нормальным считали АД менее 135/85 мм рт.ст. в дневное время, менее 120/70 мм рт. ст. — в ночные часы. Обработку результатов выполняли с помощью программного обеспечения «KT Result 3», версия 3.4.206.
Диагностику АГ проводили в соответствии с клиническими рекомендациями [5]. С целью выявления поражения органов-мишеней рассчитывали скорость клубочковой фильтрации (СКФ) по формуле CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration) и индекс массы миокарда левого желудочка (ИММЛЖ), используя универсальный медицинский калькулятор [7]. Всех пациентов тестировали по Эпвортской шкале дневной сонливости (Epworth Sleepiness Scale, ESS). Колебание суммарной оценки по ней может достигать от 0 до 24 баллов. Суммарная оценка 0—10 баллов характеризует отсутствие дневной сонливости, 11—15 баллов — избыточную и 16—24 балла — выраженную дневную сонливость [8]. Диагностику СОАГС осуществляли при 24-часовом полифункциональном исследовании с кардиореспираторным мониторированием во время сна с 1-го по 3-й день после госпитализации в терапевтический стационар. На протяжении суток одно-временно регистрировали: электрокардиограмму (ЭКГ) в 12 отведениях, АД (по тонам Короткова и осциллометрическим методом), интегральную реопневмограмму и актограмму, во время сна — насыщение кислородом гемоглобина в периферической крови (SpO2) и ороназальный поток воздуха. Датчик регистрации ороназального потока и портативный пульсоксиметр пациенты самостоятельно накладывали перед сном после предварительного инструктажа. Суточное мониторирование АД (СМАД) проводили в автоматическом режиме с интервалами 15 мин (с 7.00 до 23.00) и 30 мин (с 23.00 до 7.00). Нормальным считали АД менее 135/85 мм рт.ст. в дневное время, менее 120/70 мм рт. ст. — в ночные часы. Обработку результатов выполняли с помощью программного обеспечения «KT Result 3», версия 3.4.206.
При анализе полифункциональной мониторограммы выделяли периоды сна и бодрствования с учетом характера ЧСС, паттерна дыхания и двигательной активности, синхронно записанных с датчиков [9]. Цикл сон—бодрствование в каждом случае был индивидуальным. По данным суточной ЭКГ анализировали ритм сердца, среднюю ЧСС за 1 мин во время сна и бодрствования, наджелудочковую эктопическую активность (НЭА), характерную (одиночные, парные и групповые наджелудочковые экстрасистолы) и не характерную (пароксизмы наджелудочковой тахикардии и ускоренные наджелудочковые ритмы) для здоровых лиц [10], градацию желудочковых нарушений ритма (ЖНР) [11], нарушения проводимости сердца, среднесуточные, среднедневные и средненочные значения интервалов QT, J—T и их дисперсии. Длительность интервалов QT, J—T и их производных оценивали в автоматическом режиме по 8 отведениям ЭКГ (II, III, V1—V6). Интервалы QTс и соответственно J—Tс рассчитывали как значения интервалов QT и J—T, отнесенные к корню квадратному из среднего интервала R—R. Дисперсии QT и J—T определяли как разницу между максимальным и минимальным значениями. Удлинение интервала QTс констатировали при достижении его значений ≥450 мс в течение 1 мин и более. Рассчитывали процент времени удлинения этого показателя. Увеличение QTd расценивали как 60 мс и более [3].
 При анализе результатов кардиореспираторного мониторирования во время сна оценивали общую длительность сна, продолжительность, число и тип эпизодов апноэ и гипо-пноэ, индекс апноэ/гипопноэ (ИАГ), минимальное и среднее (от англ. minimum и mean соответственно) значение SpO2 (minSpO2 и mSpO2), индекс гипоксемии (ИГ). Апноэ и гипо-пноэ определяли как снижение амплитуды сигнала в течение 10 с и более на 90% и более и 50% и более соответственно. ИГ рассчитывали в автоматическом режиме как среднее число эпизодов снижения насыщения кислородом гемоглобина периферической крови (десатурации) на 3,5% и более в час за время сна, пригодное для анализа насыщения кислородом гемоглобина в периферической крови. Легкую степень СОАГС определяли при ИАГ от 5 до 14/ч, среднюю степень — при ИАГ от 15 до 29/ч и тяжелую степень — при ИАГ 30/ч и более. Всех пациентов разделили на 4 группы согласно значениям ИАГ: в 1-ю вошли 34 пациента без СОАГС (группа сравнения), во 2-ю — 36 с легкой степенью, в 3-ю — 32 со средней степенью и в 4-ю — 36 с тяжелой степенью СОАГС.
При анализе результатов кардиореспираторного мониторирования во время сна оценивали общую длительность сна, продолжительность, число и тип эпизодов апноэ и гипо-пноэ, индекс апноэ/гипопноэ (ИАГ), минимальное и среднее (от англ. minimum и mean соответственно) значение SpO2 (minSpO2 и mSpO2), индекс гипоксемии (ИГ). Апноэ и гипо-пноэ определяли как снижение амплитуды сигнала в течение 10 с и более на 90% и более и 50% и более соответственно. ИГ рассчитывали в автоматическом режиме как среднее число эпизодов снижения насыщения кислородом гемоглобина периферической крови (десатурации) на 3,5% и более в час за время сна, пригодное для анализа насыщения кислородом гемоглобина в периферической крови. Легкую степень СОАГС определяли при ИАГ от 5 до 14/ч, среднюю степень — при ИАГ от 15 до 29/ч и тяжелую степень — при ИАГ 30/ч и более. Всех пациентов разделили на 4 группы согласно значениям ИАГ: в 1-ю вошли 34 пациента без СОАГС (группа сравнения), во 2-ю — 36 с легкой степенью, в 3-ю — 32 со средней степенью и в 4-ю — 36 с тяжелой степенью СОАГС.
Статистический анализ полученных данных провели с помощью пакета прикладных программ Statistica 10.0. Для обработки данных использовали методы параметрической и непараметрической статистики. В первом случае данные представлены в виде средней и стандартного отклонения (M±SD), во втором случае — в виде медианы и межквартильного интервала — Me (25-й процентиль; 75-й процентиль). Межгрупповые различия определяли с помощью метода ANOVA по Крускалу—Уоллису с последующим апостериорным сравнением групп. По частоте изучаемого признака различия между группами оценивали с помощью критерия χ2 Пирсона. Различия при р<0,05 считали статистически значимыми. Для выявления предикторов, ассоциированных с увеличением длительности интервалов QTc и J—Tc, применили многофакторный регрессионный анализ (множественная линейная регрессия). Данные представили в виде регрессионного коэффициента (β) и точного значения уровня достоверности (р).
Результаты
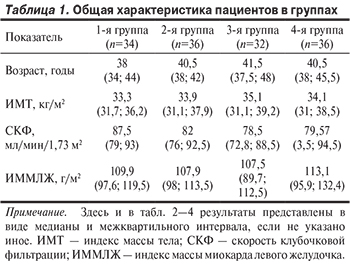
Все пациенты имели 3 фактора риска развития АГ и более. Так, дислипидемия выявлялась у 129 (93,5%), абдоминальное ожирение — у 127 (92%), семейный анамнез ранних ССЗ — у 106 (76,8%), курение — у 48 (34,8%), гипергликемия натощак — у 7 (5,1%) и нарушение толерантности к глюкозе — у 3 (2,2%), возраст старше 55 лет — у 4 (2,9%) пациентов. Субклиническое поражение органов-мишеней диагностировали у 47 (34%), из них гипертрофию миокарда левого желудочка — у 41 (87,2%), нарушение функции почек — у 6 (12,8%) пациентов. По уровню офисного АД АГ 1-й степени выявлялась у 103 (74,6%), 2-й степени — у 26 (18,9%) и 3-й степени — у 9 (6,5%) пациентов. Гипертоническую болезнь (ГБ) I стадии диагностировали у 91 (66%), ГБ II стадии — у 47 (34%) пациентов. В табл. 1 представлена общая характеристика обследованных пациентов.
 Согласно представленным в табл. 1 данным, группы сопоставимы по возрасту, ИМТ, СКФ и ИММЛЖ. Однако прослеживалась тенденция к более высоким значениям ИМТ и более низким значениям СКФ у пациентов с СОАГС средней степени, а также более высоким значениям ИММЛЖ у пациентов с СОАГС тяжелой степени.
Согласно представленным в табл. 1 данным, группы сопоставимы по возрасту, ИМТ, СКФ и ИММЛЖ. Однако прослеживалась тенденция к более высоким значениям ИМТ и более низким значениям СКФ у пациентов с СОАГС средней степени, а также более высоким значениям ИММЛЖ у пациентов с СОАГС тяжелой степени.
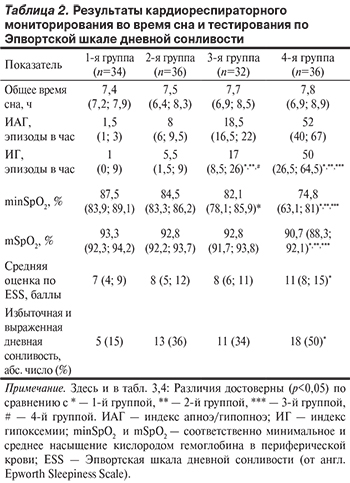
Все пациенты в анализируемых группах предъявляли жалобы на храп. Результаты тестирования по ESS показали наличие избыточной и выраженной дневной сонливости у 1/3 пациентов в группах с СОАГС легкой и средней степени, у 1/2 — в группе с СОАГС тяжелой степени. Однако средняя оценка по ESS в группе больных СОАГС тяжелой степени была достоверно выше, чем в группе контроля (табл. 2).
Согласно общепринятой классификации, minSpO2 менее 75% свидетельствовало о выраженной ночной гипоксемии у пациентов с СОАГС тяжелой степени по сравнению с остальными группами. В группе с СОАГС средней степени, в отличие от группы контроля, наблюдалась умеренная гипоксемия, поскольку minSpO2 находилось в интервале от 89 до 75%. У больных с СОАГС тяжелой степени регистрировалось достоверно меньшее mSpO2 как при сравнении с группой контроля, так и с остальными группами. Пациенты с СОАГС средней и тяжелой степени, в отличие от остальных групп, имели достоверно бóльший ИГ, который отражает число эпизодов десатурации во время сна. Общая продолжительность времени сна в группах не различалась (см. табл. 2).
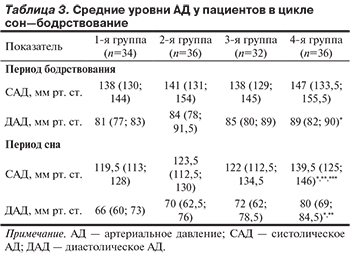
При оценке результатов СМАД выявлено, что больные с СОАГС тяжелой степени имели более высокие систолическое (САД) и диастолическое (ДАД) АД. При этом по уровню САД в период сна различия были достоверными по сравнению с группой контроля и группами пациентов с СОАГС легкой и средней степени. По уровню САД в период бодрствования межгрупповые различия отсутствовали. По уровню ДАД в период бодрствования больные с СОАГС тяжелой степени достоверно отличались только от группы контроля, тогда как в период сна — от группы контроля и группы с СОАГС легкой степени (табл. 3).
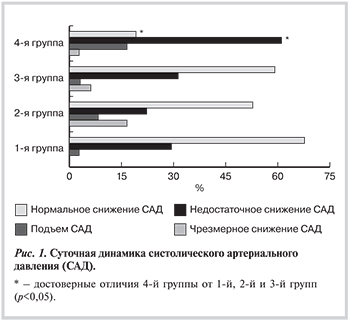
Как известно, нарушения суточной динамики АД, оцениваемые по суточному индексу (СИ), ассоциируются с неблагоприятным прогнозом. В нашей выборке более выраженные нарушения суточного ритма АД наблюдались у пациентов с СОАГС тяжелой степени. Так, в этой группе по сравнению с остальными чаще выявлялись подъем (отрицательные значения СИ) и недостаточное снижение САД в ночные часы (СИ от 0 до 10%). Чрезмерное снижение САД в ночные часы (СИ более 20%) чаще диагностировалось в группе с СОАГС легкой степени. Нормальное снижение САД в ночные часы (СИ от 10 до 20%) наблюдалось более чем у 50% пациентов как в группе контроля, так и в группах с СОАГС легкой и средней степени. Однако в группе с СОАГС тяжелой степени только 19,4% пациентов имели нормальный суточный профиль САД (рис. 1).
 Согласно данным 24-часового мониторирования ЭКГ, у всех пациентов регистрировался синусовый ритм со средней ЧСС от 60 до 100 уд/мин. Выявлено, что у пациентов с СОАГС тяжелой степени ЧСС за изучаемые периоды была выше, чем в группе контроля и группе СОАГС средней степени. Полученные результаты свидетельствуют о симпатической активации у пациентов с ИАГ 30/ч и более. Симпатическая активация, в частности увеличение ЧСС, считаются независимыми предикторами смерти от ССЗ (табл. 4).
Согласно данным 24-часового мониторирования ЭКГ, у всех пациентов регистрировался синусовый ритм со средней ЧСС от 60 до 100 уд/мин. Выявлено, что у пациентов с СОАГС тяжелой степени ЧСС за изучаемые периоды была выше, чем в группе контроля и группе СОАГС средней степени. Полученные результаты свидетельствуют о симпатической активации у пациентов с ИАГ 30/ч и более. Симпатическая активация, в частности увеличение ЧСС, считаются независимыми предикторами смерти от ССЗ (табл. 4).
При сравнительном анализе длительности интервалов QTc и J—Tc установлено, что у больных с СОАГС тяжелой степени средние значения этих показателей достоверно выше, чем в группе контроля и группе СОАГС средней степени. Однако межгрупповые различия по средним значениям QTd и J—Td за изучаемые периоды отсутствовали. Таким образом, у пациентов с ИАГ 30/ч и более наблюдалось замедление процессов реполяризации миокарда (табл. 4).
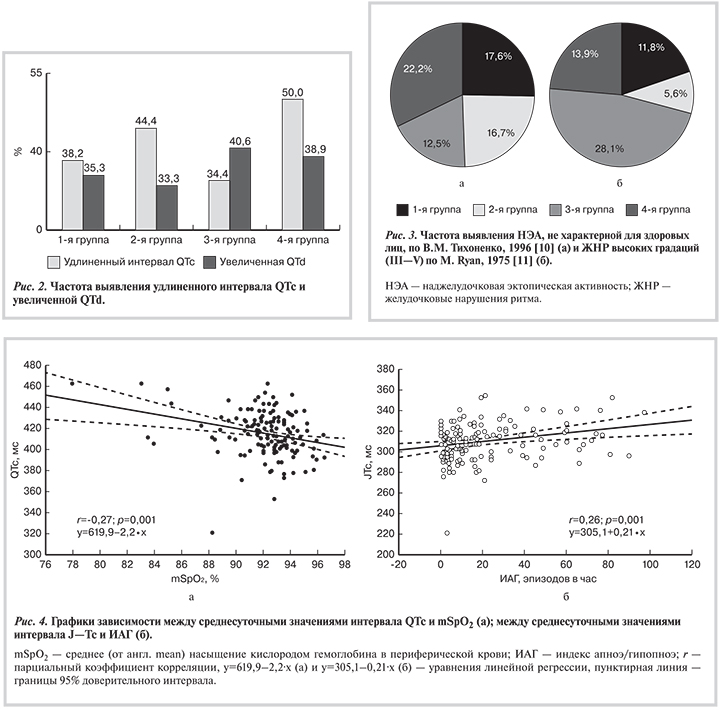
На рис. 2 отражена частота выявления удлиненного интервала QTc и увеличенной QTd.
Как видно, в группе с СОАГС тяжелой степени по сравнению с контрольной и остальными группами прослеживалась тенденция к более высокой частоте выявления удлиненного интервала QTc (см. рис. 2). При этом частота выявления увеличенной QTd во всех группах оказалась примерно одинаковой. Однако у пациентов с СОАГС средней и тяжелой степени прослеживалась тенденция к наибольшим значениям этого показателя. Среди пациентов с удлиненным интервалом QTc наблюдалась следующая частота выявления увеличенной QTd: в 1-й группе у 6 (46,2%), во 2-й — у 8 (50%), в 3-й — у 7 (63,6%) и в 4-й — у 10 (55,6%). Иными словами, во всех группах около 50% пациентов с удлиненным интервалом QTc имели увеличенную QTd.
Удлиненный интервал QTc и увеличенная QTd отражают замедление и негомогенность электрофизиологических процессов в миокарде. Это способствует развитию опасных для жизни аритмий. В нашей выборке обнаружена тенденция к более высокой частоте выявления НЭА, не характерной для здоровых лиц в группе с СОАГС тяжелой степени (рис. 3, а), и ЖНР высоких градаций (III—V) в группе с СОАГС средней степени (рис. 3, б).
Нарушения проводимости сердца регистрировались в единичных случаях. Так, синоатриальная блокада в 1-й группе выявлена у 1 (2,8%) пациента, во 2-й — у 4 (11,1%), атриовентрикулярная блокада II степени Мобитц-1 во 2-й группе — у 2 (5,9%), в 3-й — у 1 (3,1%) и в 4-й — у 3 (8,3%).
 Согласно данным многофакторного регрессионного анализа (рис. 4), удлинение среднесуточного интервала QTc ассоциировалось со снижением уровня mSpO2 во время сна (β=–0,27; p=0,001), тогда как удлинение среднесуточного интервала J—Tc — с увеличением ИАГ (β=0,26; p=0,001).
Согласно данным многофакторного регрессионного анализа (рис. 4), удлинение среднесуточного интервала QTc ассоциировалось со снижением уровня mSpO2 во время сна (β=–0,27; p=0,001), тогда как удлинение среднесуточного интервала J—Tc — с увеличением ИАГ (β=0,26; p=0,001).
Таким образом, при сравнении групп пациентов, сопоставимых по возрасту, ИМТ, СКФ и ИММЛЖ, выявлены некоторые особенности динамики изучаемых показателей у больных с ИАГ 30/ч и более. Во-первых, наблюдались более частые эпизоды десатурации и, как следствие, более низкие показатели гипоксемии во время сна. Во-вторых, чаще отмечались пароксизмы наджелудочковой тахикардии и ускоренные наджелудочковые ритмы, а также нарушения суточного профиля АД. В-третьих, регистрировалась более высокая ЧСС наряду с более продолжительными интервалами QTc и J—Tc за сутки, периоды сна и бодрствования. В-четвертых, прослеживалась тенденция к более высокой частоте выявления удлиненного интервала QTc и увеличенной QTd.
Обсуждение
Настоящее исследование представляет результаты обследования 138 мужчин (средний возраст 40,5±6,9 года) с впервые диагностированной АГ в сочетании с СОАГС различной степени тяжести (n=104; 75,4%), а также без СОАГС (n=34; 24,6%). Высокий общий риск развития ССЗ отмечался у 134 (97,1%) пациентов, очень высокий риск — у 4 (2,9%).
В данном исследовании установлено, что частота выявления удлиненного интервала QTc и увеличенной QTd у больных АГ с СОАГС и без СОАГС не различалась. Вместе с тем прослеживалась тенденция к более высокой частоте выявления удлиненного интервала QTc (50%) в группе с СОАГС тяжелой степени (n=36). Выявлено, что независимо от наличия или отсутствия СОАГС, а также значений ИАГ, около 50% пациентов с удлиненным интервалом QTc имели увеличенную QTd. В литературе имеются сведения о том, что замедление процессов реполяризации в миокарде сравнительно часто наблюдается при различных ССЗ. В частности, у пациентов с впервые диагностированной АГ (n=140) удлиненный интервал QTс встречался в 52,1% случаев, увеличенная QTd — в 36,4% [12]. В наблюдении популяционного уровня (n=1357) у больных сахарным диабетом 2-го типа удлинение интервала QTc диагностировалось в 25,8% случаев, увеличенная QTd — в 33,1% [13]. В настоящее время отсутствуют общепринятые значения удлиненного интервала QTc и увеличенной QTd, при которых можно выявлять пациентов с высоким риском ВСС. В указанных выше работах авторы считали интервал QTc удлиненным при его значениях 440 мс и более, увеличение QTd считали при значениях 80 мс и более. Высокая частота выявления перечисленных показателей, вероятно, связана с тем, что на процессы реполяризации в миокарде влияет ряд эндогенных и экзогенных факторов [14].
Результаты 15-летнего наблюдения многочисленной когорты пациентов с СОАГС (n=10 701) показали, что mSpO2 ≤93% и ИАГ ≥20/ч служат независимыми предикторами ВСС [15]. В ходе настоящего исследования выявлено, что уровень mSpO2 и ИАГ являются предикторами увеличения среднесуточных значений интервалов QTc и JTc соответственно. Ранее сообщалось о взаимосвязи длительности интервала QTc с ИАГ и уровнем гипоксемии у пациентов с АГ и СОАГС [16, 17], с уровнем АД и гипертрофией миокарда у пациентов с АГ [18]. Однако в настоящем исследовании не подтвердилась зависимость длительности интервала QTc от уровня АД и ИММЛЖ.
Крайне мало работ по изучению длительности интервала JTс у пациентов при различных заболеваниях. Известно об увеличении этого показателя при чреспищеводной стимуляции левого предсердия у пациентов с АГ и гипертрофической кардиомиопатией [19]. Согласно собственным наблюдениям, длительность интервала JTc ассоциировалась с ИАГ и ИГ у мужчин с АГ и СОАГС [16].
Взаимосвязь длительности интервалов QTс и JTc с уровнем mSpO2 и ИАГ у пациентов с СОАГС можно объяснить некоторыми звеньями патогенеза. Так, интермиттирующая гипоксия, микропробуждения и перепады внутригрудного давления во время обструктивных апноэ вызывают структурное и электрическое ремоделирование миокарда. Подобные изменения приводят к замедлению процессов реполяризации и возникновению опасных для жизни аритмий [14].
Следует отметить, что данное исследование имеет некоторые ограничения. Во-первых, выборка представлена лицами мужского пола. Во-вторых, небольшое число пациентов в группах. В-третьих, ИММЛЖ и СКФ рассчитывались с помощью универсального медицинского калькулятора. В-четвертых, не проводилась оценка показателей электролитного и гормонального обмена.
Замедление процессов реполяризации — одно из проявлений электрической нестабильности миокарда. Последняя рассматривается в качестве морфофункционального субстрата для возникновения опасных для жизни аритмий и ВСС. Выявлено, что с увеличением числа эпизодов обструктивных апноэ/гипопноэ и нарастанием гипоксемии во время сна происходит удлинение интервалов QTс и JTс. В этой связи планируется в будущем исследовать динамику продолжительности интервалов QTс и JTс на фоне неинвазивной респираторной поддержки во время сна у пациентов с АГ и СОАГС.
Выводы
- У мужчин с впервые диагностированными артериальной гипертонией и синдромом обструктивного апноэ/гипопноэ во сне различной степени тяжести частота выявления удлиненного интервала QTc (450 мс и более) и увеличенной QTd (60 мс и более) не различалась. Обнаружена тенденция к более частому выявлению удлиненного интервала QTc (50%) среди пациентов с индексом апноэ/гипопноэ 30/ч и более. Около 50% пациентов с удлиненным интервалом QTc имели увеличенную QTd независимо от наличия синдрома обструктивного апноэ/гипопноэ во сне и его степени тяжести.
- Установлены предикторы увеличения продолжительности интервалов QTc и JTc. Так, удлинение среднесуточного интервала QTc ассоциировалось со снижением уровня среднего насыщения гемоглобина кислородом в периферической крови во время сна, тогда как удлинение среднесуточного интервала JTc — с увеличением индекса апноэ/гипопноэ.



