Благодаря расширению сети оказания кардиохирургической помощи населению и совершенствованию хирургической тактики аортокоронарного шунтирования (АКШ), увеличилась численность больных с периоперационной дисфункцией почек [1—3]. Установлено, что наличие хронической болезни почек (ХБП), а также развитие периоперационного острого повреждения почек (ОПП) ухудшают ближайший и отдаленный прогноз у больных, подвергшихся операции АКШ [1, 4—7]. Известно, что у больных, перенесших операции на сердце с использованием искусственного кровообращения (ИК), независимо от наличия исходной дисфункции почек частота развития периоперационного ОПП колеблется от 5 до 60%, а летальность — от 6 до 32,5% [8—12].
Однако послеоперационный прогноз у больных данной категории значительно отличается, что, возможно, обусловлено различной степенью дисфункции почек как до операции, так и после нее [5, 6, 9, 13]. Наряду с неблагоприятным влиянием дисфункции почек на кардиоваскулярный прогноз [4, 7, 13] также необходимо учитывать влияние гемодинамической эффективности реваскуляризации миокарда, особенно у больных с застойной хронической сердечной недостаточностью (ХСН), на прогноз поражений почек [2, 14, 15]. Поэтому общность патогенетических механизмов поражений сердца и почек, а также их взаимоотягощающее влияние на прогноз должны учитываться при разработке профилактических мер и тактики медикаментозной терапии у кардиохирургических больных [11, 13, 16, 17].
Кроме того, в литературе дискутируется вопрос о прогностическом эффекте ОПП у больных ХБП, подвергшихся АКШ, а также о влиянии операции реваскуляризации миокарда на послеоперационную динамику ХБП, в том числе после перенесенного ОПП [3, 8, 9, 12]. В связи с этим представляет интерес изучение риска развития периоперационного ОПП и отдаленного прогноза в зависимости от исходного функционального состояния почек у больных, подвергшихся АКШ [5, 7, 10, 15].
Цель исследования — оценить прогностическое значение ХБП и периоперационного ОПП в ближайшем и отдаленном периоде после АКШ.
Материал и методы
В открытое исследование были включены 657 больных (419 мужчин и 238 женщин) в возрасте от 54 до 68 лет (средний возраст 60,6±5,3 года), которым в плановом порядке выполнялось АКШ с применением ИК в Пензенском федеральном центре сердечно-сосудистой хирургии. Через 5—7 дней после операции больных для дальнейшего наблюдения переводили в кардиологическое отделение ГКБ СМП им. Г.А. Захарьина. В зависимости от исходной скорости клубочковой фильтрации (СКФ) больных распределили на 2 группы: в 1-ю группу вошли 411 больных с СКФ выше 90 мл/мин/1,73 м2, определяемой по формуле MDRD (Modification of diet in renal disease study), во 2-ю группу — 246 больных с СКФ от 89 до 45 мл/мин/1,73 м2. Критериями исключения являлись перенесенный за 6 мес до операции инсульт; первичные заболевания почек; программный гемодиализ; ранние осложнения, требующие повторной операции.

Сроки наблюдения больных составили 12 мес после операции, ближайший период – первые 30 суток после операции и отдаленный – через 12 мес после операции.
Периоперационное ОПП диагностировали и классифицировали по уровню креатинина в сыворотке крови (sCr), используя критерии AKIN [18]. Содержание sCr и СКФ определяли за 2—3 дня до операции, после операции ежедневно в стационаре, через 6 и 12 мес после операции. Операционный риск развития ССО определяли по индексу EuroSCORE (European system for cardiac operative risk evaluation).
Исходы ОПП определяли с учетом динамики максимальных уровней sCr при развитии ОПП по сравнению с уровнями sCr до операции и спустя 3 мес от начала ОПП. Транзиторное ОПП означало восстановление дооперационных уровней sCr в течение 4 нед, в том числе у больных с ХБП. У больных с исходно сохранной функцией почек, перенесших периоперационное ОПП, манифестация ХБП предполагала снижение СКФ ниже 60 мл/мин/1,73 м2 в течение 3 мес и более, что в свою очередь свидетельствует о персистирующем течении ОПП. Стойкое увеличение исходной СКФ у больных с предшествующей ХБП в течение 1 года после операции рассматривали как регресс дисфункции почек. Прогрессирование предшествующей ХБП независимо от развития ОПП характеризовалось снижением СКФ на 5 мл/мин/1,73 м2 и более за 1 год.
Допплер-эхокардиографию проводили с помощью аппарата Acuson X300 («Siemens-Acuson», Германия), вычисляли конечный систолический размер (КСР) и конечный диастолический размер (КДР) левого желудочка (ЛЖ), фракцию выброса (ФВ) ЛЖ, сердечный индекс (СИ), индекс массы миокарда ЛЖ (ИММЛЖ) и удельное периферическое сосудистое сопротивление (УПСС). Диастолическую функцию ЛЖ оценивали по данным трансмитрального потока при синусовом ритме. Определяли максимальную скорость быстрого наполнения (Ve) и максимальную скорость медленного наполнения (Va) ЛЖ, их соотношение (Ve/Va), время изоволюмического расслабления (ВИР). По данным рентгенографии органов грудной клетки вычисляли кардиоторакальное отношение (КТО).
Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации Всемирной медицинской ассоциации. Протокол исследования был одобрен Этическим комитетом института. До включения в исследование больные подписывали письменное информированное согласие.
Количественную обработку результатов исследования проводили с помощью пакета программ Statistica 6.0. Нормальность распределения переменных определяли по тесту Колмогорова—Смирнова. Средние величины двух выборок при нормальном распределении признака сравнивали с помощью критерия t Стьюдента. Для сравнения качественных (дискретных) переменных использовали непараметрический критерий χ2 с поправкой Йетса. Данные были представлены в виде M±SD. Различия считали статистически значимыми при р<0,05.
Результаты
В ранний послеоперационный период ОПП диагностировали в 1-й группе у 97 (23,6%) больных, во 2-й группе — у 102 (41,5%; χ2=22,4; p<0,001). В результате в каждой группе выделили 2 подгруппы больных — с ОПП и без него.
Изучение причинно-следственных связей между вероятностью развития ОПП и клинико-анамнестическими данными показало, что в группе больных с исходно сохранной функцией почек (1-я группа) наличие перенесенного инфаркта миокарда (ИМ) и мозгового инсульта, различных форм фибрилляции предсердий (ФП), хронической железодефицитной анемии и ХСН часто ассоциируются с развитием периоперационного ОПП (табл. 1). Необходимо отметить, что во 2-й группе эти связи были менее выражены. Суммарный операционный риск развития ССО при вмешательстве на сердце — индекс EuroSCORE — в обеих группах был достоверно выше при развитии ОПП, а также во 2-й группе по сравнению с 1-й группой независимо от развития ОПП. В обеих группах возраст больных с ОПП превышал таковой у больных без ОПП (p<0,05).
Частота перенесенного ИМ (p=0,039), мозгового инсульта (p=0,032), ФП (p=0,032), анемии (p=0,021) и сахарного диабета (СД) 2-го типа (p=0,007) у больных без ОПП во 2-й группе была выше, чем в 1-й группе. Среди больных, перенесших ОПП, во 2-й группе по сравнению с 1-й группой чаще выявлялись артериальная гипертензия (p=0,014), застойная ХСН (p=0,038), ожирение (p=0,02) и СД 2-го типа (p=0,026).
Исходные уровни sCr и СКФ в 1-й группе в зависимости от наличия или отсутствия ОПП различались недостоверно. Однако во 2-й группе исходный уровень sCr у больных, перенесших ОПП, был достоверно выше, чем у больных без ОПП (p=0,023).
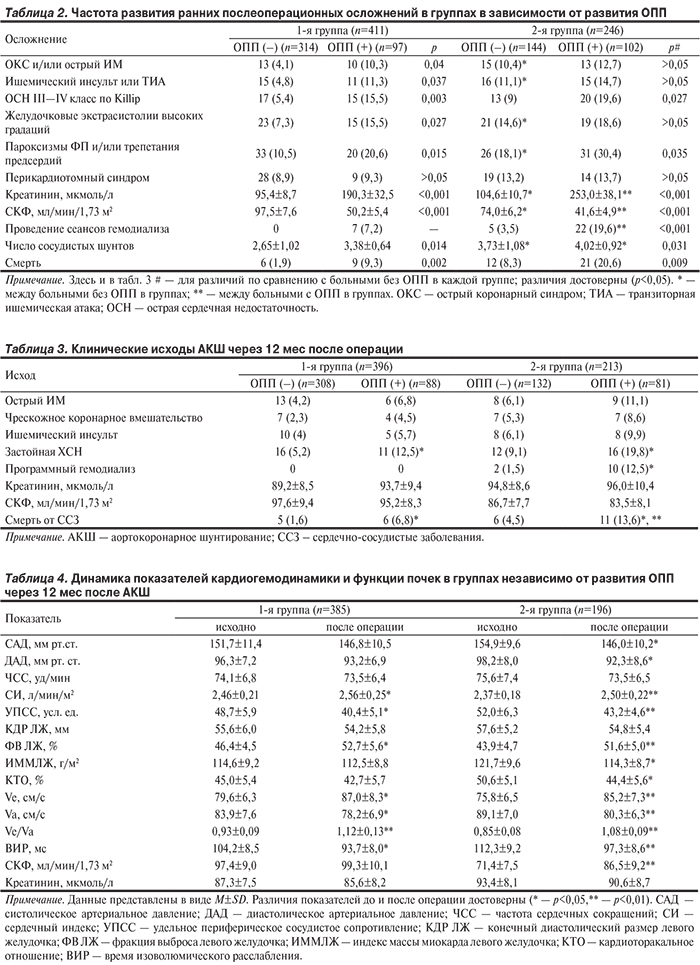
Необходимо отметить, что ранние послеоперационные осложнения достоверно чаще выявлялись у больных с периоперационным ОПП, особенно в 1-й группе (табл. 2). Кроме того, у больных без ОПП частота острого коронарного синдрома и/или ИМ (p=0,017) и мозгового инсульта (p=0,021), а также выявляемость желудочковых экстрасистолий высоких градаций (p=0,023) и пароксизмальных наджелудочковых тахиаритмий (p=0,037) во 2-й группе была достоверно выше, чем в 1-й группе. Однако у больных с ОПП различия по частоте развития ССО в сравниваемых группах недостоверно (p>0,05).
Кроме того, СКФ и уровень sCr в зависимости от развития ОПП и исходного функционального состояния почек различались достоверно. В связи с развитием острой почечной недостаточности (III стадия ОПП) сеансы гемодиализа проводились в 1-й группе у 7,2% больных, во 2-й группе — у 19,6% (p=0,008), а также у 3,5% больных 2-й группы без ОПП. Выявлено, что число сосудистых шунтов, выполненных в ходе АКШ, характеризующее тяжесть поражения коронарного русла, у больных с периоперационным ОПП и исходной дисфункцией почек было достоверно больше, чем у больных без ОПП и с исходно сохранной функцией почек. Летальность составила от 1,9 до 20,6% и в обеих группах у больных с ОПП была достоверно выше, чем у больных без ОПП. Во 2-й группе летальность по сравнению с 1-й группой была выше как у больных без ОПП (p=0,003), так и у больных с ОПП (p=0,042).
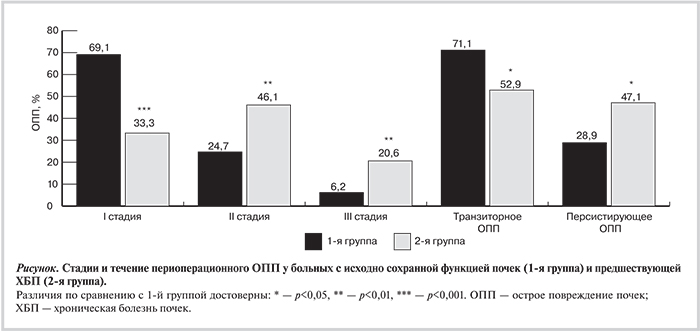
При верификации тяжести периоперационного ОПП по критериям AKIN выявлено различие в сравниваемых группах как по стадиям ОПП, так и по исходам (течению) ОПП (см. рисунок). Следует отметить, что I стадия и транзиторное ОПП достоверно чаще выявлялись в 1-й группе, а III стадия и персистирующее ОПП — во 2-й группе.
Сравнение отдаленных результатов в группах через 12 мес после операции АКШ показало, что в зависимости от перенесенного ОПП частота развития ИМ и инсульта, а также количество выполненных чрескожных коронарных вмешательств различается недостоверно (табл. 3). Однако застойная ХСН в обеих группах у больных, перенесших ОПП, выявлялась в 2—2,5 раза чаще (p<0,05), чем у больных, не перенесших ОПП. Кроме того, 12 больных 2-й группы, в том числе 10 больных, перенесших ОПП (p=0,003), находились на программном гемодиализе. Во 2-й группе СКФ была ниже в сравнении с 1-й группой и после операции, независимо от перенесенного ОПП.
Показано также, что за 12 мес наблюдения в 1-й группе у 6 (6,8%) больных, перенесших ОПП, развилась (манифестировала) ХБП. Во 2-й группе стойкое улучшение функции почек (регресс ХБП) отмечено у 46 (45,1%) больных, перенесших ОПП, и у 81 (61,4%) без ОПП (p>0,05), в то время как прогрессирование ХБП диагностировалось у 15 (14,7%) и 7 (5,4%) больных соответственно (χ2 =8,09; p=0,004).
Сравнение динамики функции почек через 12 мес после АКШ показало, что независимо от развития ОПП в 1-й группе изменения гемодинамики менее выражены, чем во 2-й группе (табл. 4). В целом во 2-й группе в отличие от 1-й достоверно уменьшились уровни систолического и диастолического артериального давления, ИММЛЖ и КТО по сравнению с исходными значениями. Увеличение СИ и ФВ во 2-й группе было достоверно выше, чем в 1-й группе, в среднем на 17,0 и 22,2% (p<0,01) соответственно. В обеих группах значительно улучшились показатели диастолической функции ЛЖ. В результате, во 2-й группе достоверно увеличилась исходная СКФ (p<0,01), а уровни sCr в сравниваемых группах отличались недостоверно.
Обсуждение
Неблагоприятное влияние ХБП и периоперационного ОПП на ближайший и отдаленный прогноз после операции АКШ изучалось достаточно [1, 3, 6, 10]. Однако результаты клинических исследований, посвященных оценке кумулятивного влияния хронической и острой дисфункции почек на кардиоренальный прогноз у больных, подвергшихся АКШ, противоречивы [4, 5, 7, 13]. Как известно, на прогноз наряду с наличием и выраженностью дисфункции почек влияют характер патологии сердца, наличие сочетанных состояний и тактика операции (применение ИК, симультанные вмешательства и т.д.), которые определяют уровень суммарного риска развития ССО и почечных осложнений [2, 11, 14].
В настоящем исследовании показано, что основным фактором риска развития ОПП у больных, подвергшихся АКШ, является наличие в анамнезе ХБП. Кроме того, у больных с ХБП провоцирующими факторами развития ОПП могут быть факторы, связанные с операцией — ее длительность, ранние осложнения, обусловливающие необходимость повторной операции, применение ИК и т.д. [3]. Установлено, что операция АКШ без применения ИК сопровождается относительно низким риском развития ОПП и более благоприятными исходами, чем АКШ с использованием ИК [2].
Нами показано, что в группе больных с исходно сохранной функцией почек риск развития периоперационного ОПП часто ассоциируется с наличием в анамнезе ИМ, инсульта, СД 2-го типа, ФП, анемии и застойной ХСН, а также возрастом больных.
Необходимо отметить, что на ближайший и отдаленный прогноз выраженное влияние оказывает проведение программного гемодиализа у больных с клиническими проявлениями острой почечной недостаточности (III стадия ОПП) и/или в связи с прогрессированием ХБП. Показано, что применение программного гемодиализа до и после кардиохирургического вмешательства дает более благоприятные результаты, чем его применение после операции [6, 14, 19].
Нами также выявлено, что отдаленный кардиоренальный прогноз зависит и от тяжести ОПП и послеоперационной динамики ХБП. Так, вероятность прогрессирования ХБП у больных, перенесших ОПП, достоверно выше, чем у больных, не перенесших ОПП (в 14,7 и 5,4% случаев соответственно; p=0,004). Кроме того, у больных с прогрессированием ХБП после перенесенного периоперационного ОПП потребность в проведении программного гемодиализа, частота развития ССО и смертность были достоверно выше, чем у больных с дооперационной ХБП и не перенесших ОПП.
Однако регресс предшествующей ХБП в зависимости от развития ОПП отличался недостоверно (в 45,1 и 61,4% случаев), что свидетельствует о возможности улучшения функции почек даже после перенесенного периоперационного ОПП. Это, вероятно, объясняется положительным гемодинамическим эффектом операции реваскуляризации миокарда на дальнейшее течение ХБП, что согласуется с данными исследования, проведенного N. Khosla и соавт. [15].
Таким образом, прогноз у больных, подвергшихся операции АКШ с применением ИК, зависит от многообразий кардиоренальных взаимоотношений и их послеоперационной динамики. Поэтому для оптимизации ближайших и отдаленных результатов операции АКШ у больных с сочетанной дисфункцией почек требуется проведение комплекса лечебно-профилактических мероприятий, включая широкое внедрение тактики операции на «работающем сердце», заместительной почечной терапии (гемодиализа) в пред- и послеоперационном периоде и адекватной кардио- и нефропротективной терапии. Все это подчеркивает важность дальнейших крупных клинических исследований.
Выводы
- Наличие исходной дисфункции почек является фактором риска развития периоперационного острого повреждения почек, неблагоприятного ближайшего и отдаленного прогноза у больных, подвергшихся операции аортокоронарного шунтирования в условиях искусственного кровообращения.
- У больных с исходно сохранной клубочковой фильтрацией почек, перенесших периоперационное острое повреждение почек, через 12 мес после аортокоронарного шунтирования манифестация хронической болезни почек отмечалась в 6,8% случаев. Прогрессирование хронической болезни почек у больных, перенесших острое повреждение почек, отмечено в 14,7% случаев, а у больных без острого повреждения почек — в 5,4% (p=0,004), регресс течения хронической болезни почек — в 45,1 и 61,4% случаев соответственно (p>0,05).
- В случае развития острого повреждения почек после аортокоронарного шунтирования у больных с предшествующей хронической болезнью почек потребность в проведении программного гемодиализа составила 12,5%, а у больных без острого повреждения почек — 1,5% (p=0,003). Смертность за 12 мес наблюдения после выписки была достоверно выше у больных, перенесших острое повреждение почек, по сравнению с больными без острого повреждения почек независимо от исходной функции почек, а также у больных с острым повреждением почек при наличии предшествующей хронической болезни почек по сравнению с отсутствием таковой.



