Сердечно-сосудистые заболевания (ССЗ) справедливо называют эпидемией ХХ и ХХI веков. В течение нескольких десятилетий они являются главной причиной смерти населения в индустриально развитых странах, в том числе в России, где от ССЗ ежегодно умирают почти 1,2 млн человек, что составляет 55,5% от общей смертности [1].
По влиянию на состояние здоровья пациента, риску фатальных состояний, трудностям диагностики, профилактики и лечения, социальному значению острый коронарный синдром (ОКС) первенствует среди кардиальной патологии [2].
Известно, что атеросклероз — это системное, мультифокальное заболевание [3, 4]. По данным исследований, распространенность периферического атеросклероза среди взрослого населения составляет от 13,5 [5] до 95% [3, 6].
Периферический атеросклероз, как и хроническая болезнь почек (ХБП), является наиболее распространенным заболеванием среди лиц старше 65 лет и одним из факторов, влияющих на развитие неблагоприятных сердечно-сосудистых исходов [7]. Результаты крупных эпидемиологических исследований (NHANES III, Okinawa Studу и др.), выполненных в последние десятилетия, показали высокую распространенность дисфункции почек (ДП) в общей популяции (10—20%) [8], что сопоставимо с распространенностью заболеваний, традиционно рассматриваемых как социально значимые — бронхиальной астмы, ишемической болезни сердца (ИБС) и др. При этом лишь около 1/4 лиц со сниженными скоростью клубочковой фильтрации (СКФ) и клиренсом креатинина (ККр) информированы о наличии у них ХБП [9].
 В ранее проведенных исследованиях показано, что у больных инфарктом миокарда (ИМ) ДП регистрируется значительно чаще, чем в общей популяции за счет ишемической нефропатии на фоне комплексного воздействия таких факторов, как снижение насосной функции миокарда, артериальная гипертензия (АГ), мультифокальный атеросклероз (МФА) и сахарный диабет (СД) 2 типа [10]. По данным регистра ADHERE, у 30% всех госпитализированных больных с острой сердечной недостаточностью (СН) имелась ХБП или концентрация креатинина в плазме крови более 2 мг/дл в анамнезе [11].
В ранее проведенных исследованиях показано, что у больных инфарктом миокарда (ИМ) ДП регистрируется значительно чаще, чем в общей популяции за счет ишемической нефропатии на фоне комплексного воздействия таких факторов, как снижение насосной функции миокарда, артериальная гипертензия (АГ), мультифокальный атеросклероз (МФА) и сахарный диабет (СД) 2 типа [10]. По данным регистра ADHERE, у 30% всех госпитализированных больных с острой сердечной недостаточностью (СН) имелась ХБП или концентрация креатинина в плазме крови более 2 мг/дл в анамнезе [11].
Как известно, стойкое снижение СКФ и наличие МФА являются независимыми предикторами повышенного риска смерти от ССЗ [3, 12]. Можно предполагать, что пациенты с ИМ с подъемом сегмента ST (ИМпST), имеющие сочетанную патологию (МФА и ХБП), составляют группу повышенного риска развития сердечно-сосудистых осложнений (ССО) по сравнению с пациентами, имеющими только одно из этих заболеваний.
Цель настоящего исследования состояла в оценке частоты выявления и выраженности ДП, а также ее прогностического значения у больных ИМпST и МФА.
Материал и методы
Исследование основано на регистре ОКС с подъемом сегмента ST, проводимого в Кемеровском кардиологическом диспансере в период с 2008 по 2009 г. В исследование были включены 529 пациентов. Критерием включения был установленный, согласно рекомендациям Всероссийского научного общества кардиологов, диагноз ИМпST давностью до 24 ч от начала заболевания [13]. Исследование было одобрено локальным этическим комитетом, все больные после ознакомления подписали форму информированного согласия. Схема обследования включала сбор жалоб, анамнеза, клинический осмотр кардиологом, запись электрокардиограммы, оценку уровня кардиоспецифических ферментов, контроль показателей системной гемодинамики, проведение эхокардиографии. Всем больным рассчитаны ККр по формуле Кокрофта—Гаулта и СКФ по формуле MDRD [12]. Помимо общепринятых общеклинических исследований 423 больным на 5—10-е сут госпитального периода проведено цветовое дуплексное сканирование (ЦДС) артерий нижних конечностей (АНК) и экстракраниальных артерий (ЭКА) при помощи линейных датчиков с частотой 5—7 МГц (для ЭКА), конвексного датчика с частотой 2,5—3 МГц и линейного — 5 МГц (для АНК). Оценку толщины интима—медиа (ТИМ) осуществляли в дистальной, средней и проксимальной точках общей сонной артерии с вычислением среднего значения, при этом нормальным считали значение менее 1 мм. Признаки МФА констатированы у 95% больных (стенозы любой степени или увеличение ТИМ). На основании данных ЦДС больные были распределены в 4 группы. В 1-ю группу вошли 22 (5,2%) пациента без МФА, во 2-ю — 201 (47,5%) с ТИМ ≥1 мм или стенозами менее 30%, в 3-ю — 75 (17,7%) больных со стенозами от 30 до 50%, в 4-ю — 125 (29,6%) больных со стенозами 50% и более. Разделение на группы осуществляли согласно модифицированной классификации атеросклеротического поражения некоронарных артерий, предложенной в работе З.А. Суслиной (2006) [14].
 Всем пациентам в кратчайшие сроки определяли предпочтительный метод реперфузии миокарда — чрескожное коронарное вмешательство (ЧКВ) или проведение системной тромболитической терапии (ТЛТ). Реваскуляризацию миокарда не проводили в случае наличия технических ограничений, сложной коронарной анатомии, противопоказаний к ТЛТ или ЧКВ. Клиническая характеристика больных представлена в таблице. Следует отметить, что включенные в исследование пациенты характеризовались наличием большого числа традиционных факторов риска развития ССО, что соответствует результатам ранее опубликованных работ [3, 4].
Всем пациентам в кратчайшие сроки определяли предпочтительный метод реперфузии миокарда — чрескожное коронарное вмешательство (ЧКВ) или проведение системной тромболитической терапии (ТЛТ). Реваскуляризацию миокарда не проводили в случае наличия технических ограничений, сложной коронарной анатомии, противопоказаний к ТЛТ или ЧКВ. Клиническая характеристика больных представлена в таблице. Следует отметить, что включенные в исследование пациенты характеризовались наличием большого числа традиционных факторов риска развития ССО, что соответствует результатам ранее опубликованных работ [3, 4].
В стационаре всем пациентам назначали стандартную терапию, включающую нефракционированный гепарин, ацетилсалициловую кислоту, клопидогрел, ингибиторы ангиотензинпревращающего фермента (АПФ), β-адреноблокаторы, статины. В 157 (37,1%) случаев реперфузию не проводили, 53 (12,5%) больным проведена ТЛТ, 213 (50,4%) — ЧКВ. При выписке назначали статины, клопидогрел, ацетилсалициловую кислоту, ингибиторы АПФ, β-адреноблокаторы. При необходимости дополнительно пациенты принимали нитраты, антагонисты медленных кальциевых каналов, диуретики.
Госпитальная летальность вследствие осложненного течения ИМ (кардиогенный шок, разрывы миокарда, угрожающие жизни нарушения ритма) составила 10,9%. Из числа больных, которым проводилась визуализация периферических артерий (ПА), умерли 7 (1,6%): 3 — от нарушений ритма, остальные — от рефрактерного кардиогенного шока.
Через год у 397 пациентов оценили выживаемость путем телефонного опроса. Учитывали только сердечно-сосудистую смертность. Смертельные исходы зарегистрированы у 39 (9,8%) больных. Смертность через год среди 148 пациентов, не подвергшихся реперфузии на госпитальном этапе, составила 18,9%, среди 48 пациентов, которым проводилась только ТЛТ — 10,4%, среди 201 пациента, которым проводилось экстренное ЧКВ — 3%.
 Статистическую обработку полученных данных осуществляли с помощью программы SPSS версии 16.0 (США). Для исследования зависимостей между переменными использовали коэффициент ранговой корреляции Спирмена, для анализа различий частот — критерий χ2 Пирсона.
Статистическую обработку полученных данных осуществляли с помощью программы SPSS версии 16.0 (США). Для исследования зависимостей между переменными использовали коэффициент ранговой корреляции Спирмена, для анализа различий частот — критерий χ2 Пирсона.
Две независимые группы по количественному признаку сравнивали с помощью U-критерия Манна—Уитни. Для определения прогностической ценности нового метода применяли построение ROC-кривой с последующим расчетом площади под ней (С-статистика). Различия считали статистически значимыми при уровне р<0,05.
Результаты
При расчете СКФ по формуле MDRD выявлено, что у 188 (35,5%) больных этот показатель составил от 30 до 60 мл/мин/1,73 м2, а у 26 (4,9%) — менее 30 мл/мин/1,73 м2. В то же время по формуле Кокрофта—Гаулта ККр от 30 до 60 мл/мин регистрировался у 156 (29,5%) больных, менее 30 мл/мин — у 16 (3,0%).
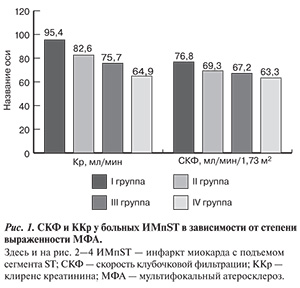
При анализе связи между степенью выраженности МФА и функцией почек выявлено, что уже при начальных проявлениях МФА (стенозы до 30%) достоверно снижены средние ККр (р=0,048) и СКФ (р=0,045): с 95,4 (81,8; 109,0) до 82,6 (78,2; 87,0) мл/мин и с 76,8 (68,7; 84,8) до 69,3 (66,5; 72,2) мл/мин/1,73 м2 соответственно. Максимальные снижения показателей фильтрационной способности почек регистрировались при стенозах некоронарных артерий 50% и более — 64,9 (61,1; 68,7) мл/мин и 63,3 (59,4; 67,3) мл/мин/1,73 м2 для ККр и СКФ соответственно (рис. 1). Коэффициент корреляции между степенью МФА и значением ККр составил – 0,29 (р<0,0001), между степенью МФА и СКФ — -0,17 (р<0,0001).
Ввиду того что степень выраженности стенозов некоронарных артерий положительно коррелирует с возрастом, проведено уравнивание групп по возрасту: из анализа исключены больные старше 70 лет и моложе 50 лет.
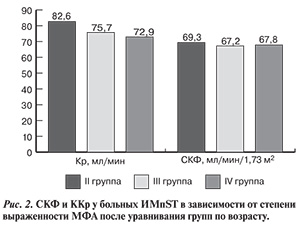
Во вновь сформированных группах СКФ не различалась, тогда как ККр у больных со стенозами некоронарных артерий более 50% был статистически значимо ниже (р=0,03), чем во 2-й группе (рис. 2). Таким образом, связь между МФА и ДП, оцененной по формуле Кокрофта—Гаулта, оказалась более выраженной.
Госпитальная летальность регистрировалась только в 4-й группе больных: умер 1 (0,4%) пациент без ДП (n=265), 4 (2,8%) из 144 — с умеренным нарушением функции почек (СКФ от 60 до 30 мл/мин/1,73 м2) и 2 (14,3%) из 14 — с выраженным нарушением (СКФ менее 30 мл/мин/1,73 м2) (р=0,0002). Подобная закономерность выявлена и при расчете данных показателей на основании определения ККр — 0,3, 4,4 и 11,1% соответственно (р=0,001).
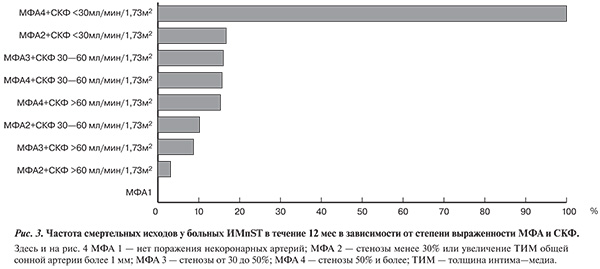
Смертность в течение года у больных, разделенных только по группам МФА, составила соответственно 0, 5, 7, 11 и 17,7% (p=0,01). При разделении групп по степени выраженности МФА и ДП, рассчитанной по формуле MDRD, выявлено, что наибольшее число смертельных исходов констатировано в группе пациентов с СКФ менее 30 мл/мин/1,73 м2 и стенозами некоронарных артерий 50% и более — 100% (4 больных). Следует отметить, что у всех пациентов с СКФ менее 30 мл/мин/1,73 м2 имелись стенозы некоронарных артерий более 50%. Промежуточные точки по смертности регистрировались в группах МФА со стенозами менее 50% и любым уровнем СКФ, еще ниже — у больных без ДП и стенозами некоронарных артерий до 50% (рис. 3). В группе из 18 больных без МФА летальные исходы отсутствовали, при этом следует учитывать, что среди них только у 1 пациента СКФ была менее 60 мл/мин/1,73 м2. Таким образом, получены статистически значимые различия (р=0,002) при оценке смертности между группой пациентов со стенозами ПА менее 50% без ДП (4,8%) и группой, в которую вошли пациенты с любыми стенозами ПА в сочетании со снижением СКФ или стенозами 50% и более без снижения СКФ (16,3%).
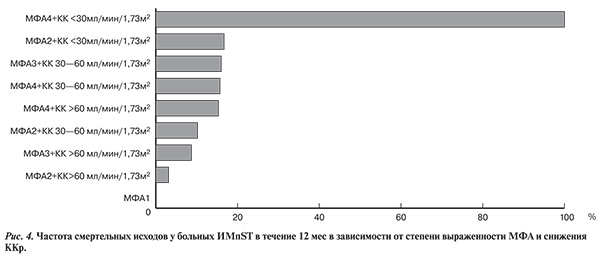
Несколько другие данные получены при анализе смертности в течение года при распределении больных на группы по степени ДП, рассчитанной по формуле Кокрофта—Гаулта, и выраженности МФА (рис. 4). Так, выявлена дополнительная группа очень высокого риска, в которой смертность составила 31,9% (умерли 15 пациентов из 62) — пациенты с ККр от 30 до 60 мл/мин и стенозами ПА 30% и более или ККр менее 30 мл/мин и стенозами ПА более 50%. В то же время смертность в группах умеренного риска (стенозы ПА более 50% без ДП или стенозы ПА менее 30% с ККр от 30 до 60 мл/мин) и низкого риска (стенозы ПА менее 50% без снижения ККр) составила 13,7 и 3,2% соответственно. Выявлены статистически значимые различия между группами больных очень высокого риска и умеренного риска (р=0,03), умеренного и низкого риска (р=0,001), очень высокого риска и низкого риска (р=0,0001). В группе из 18 пациентов без МФА не было ни одного случая смерти и снижения ККр, а среди 4 больных со стенозами ПА более 50% в сочетании с ККр менее 30 мл/мин не было выживших.
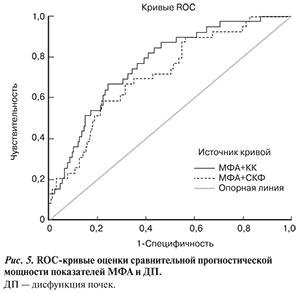
Таким образом, определение тяжести МФА в сочетании с оценкой степени снижения ККр в отличие от оценки СКФ представляет большую ценность в отношении стратификации риска смерти в течение года после ИМпST, что подтверждает анализ ROC-кривых: 0,77 (0,70; 0,85) против 0,70 (0,62; 0,78) (рис. 5).
Обсуждение
В многочисленных исследованиях выявлена тесная ассоциация между тяжестью ДП и риском смерти от всех причин, а также возникновением различных ССО, включая ИМ [15]. Изучение патофизиологических основ этой ассоциации привело к формированию концепции кардиоренального синдрома (КРС), основанной на существовании взаимно влияющих патогенетических факторов, оказывающих отрицательное действие как в отношении контрактильной способности миокарда, так и определяющих проградиентное снижение функциональной способности и выживаемости почки [8]. При этом в качестве основных механизмов, способствующих формированию КРС, рассматривают повышение центрального венозного давления, снижение перфузии почки, внутрипочечную гипертензию, недостаточность эндогенных механизмов, обеспечивающих эффективный салурез и натрийурез (система натрийуретических пептидов), дисфункцию эндотелия, системную провоспалительную и нейрогуморальную активацию, прооксидантный стресс и некоторые другие факторы [8].
Считается, что ДП обусловлена, главным образом, падением сердечного выброса или общего периферического сосудистого сопротивления и нейрогуморальной активацией, в результате чего ухудшается почечный кровоток, снижается давление на стенки приносящих артериол и доставка натрия к восходящей части петли Генли [8].
Неблагоприятному влиянию продуктов нейрогуморальной активации на ранних стадиях СН препятствуют система натрийуретических пептидов (предсердный, мозговой натрийуретический пептид — НУП, уродилатин), простагландины Е2 и I2, оксид азота, оказывающие нефропротективное и вазодилатирующее действия, повышающие почечный кровоток и натрийурез [8]. Однако в долгосрочном отношении эффективность компенсаторных нейрогуморальных механизмов оказывается недостаточной. Прогрессирующие нарушения функции миокарда усугубляют ДП и приводят к структурным изменениям почек, чем замыкается порочный круг КРС [16].
Результаты многочисленных исследований показали, что клиническое определение НУП в плазме позволяет оценить тяжесть и прогнозировать дальнейшее течение таких патологических состояний, как хроническая СН [17],
ОКС [18]. У пациентов с нефротическим синдромом, острой и хронической почечной недостаточностью уровень НУП в крови также может быть увеличен, что в значительной мере связано не только с поражением сердца, но и с изменениями объема циркулирующей крови [19].
 Таким образом, ИМ ассоциируется со снижением функции почек, а многочисленные эпидемиологические исследования выявляют высокую частоту ДП у пациентов, госпитализированных с ОКС [20].
Таким образом, ИМ ассоциируется со снижением функции почек, а многочисленные эпидемиологические исследования выявляют высокую частоту ДП у пациентов, госпитализированных с ОКС [20].
В то же время тяжесть течения ИМ может быть обусловлена действием факторов, приводящих к формированию ДП в доинфарктный период. Так, анализ данных крупных исследований TIMI и InTIME-II выявил повышение 30-дневной летальности у пациентов с ИМпST при легкой, умеренной и тяжелой ХБП в 1,4, 2,1 и 3,8 раза соответственно по сравнению с таковой у пациентов без ДП [21].
Увеличение концентрации креатинина в сыворотке крови более чем на 0,5 мг/дл в течение суток в период пребывания больного в стационаре в связи с ОКС существенно увеличивает риск смерти в течение последующих 12 мес.
В недавно проведенных исследованиях выявлена тесная связь между патологическими изменениями в сердце, сосудах и почках, а также подтвердилось, что эти изменения обусловлены одинаковыми факторами риска: АГ, гипергликемией, дислипидемией и ожирением [22, 23].
Механические и химические повреждения, обусловленные перечисленными факторами риска, ускоряют прогрессирование сосудистых изменений, начальными проявлениями которых служат дисфункция эндотелия и атеросклероз [24]. Многие признают, что одним из важнейших маркеров дисфункции эндотелия, играющей ключевую роль в атерогенезе, является показатель ТИМ стенки сосуда [25].
Увеличение ТИМ — важный прогностический маркер, о чем свидетельствуют данные Cardiovascular Health Study — у лиц с утолщением стенки сонных артерий наблюдался более высокий риск развития ИБС и ИМ. Роттердамское исследование продемонстрировало значение увеличения ТИМ сонных артерий как индикатора поражений других сосудов и независимого фактора риска развития ССО [7]. Тесная взаимосвязь утолщения стенки сонной артерии и риска развития кардиальных и цереброваскулярных осложнений ассоциируется с высокой распространенностью повышенных значений ТИМ в отсутствие симптомов у пациентов с высоким риском развития ССО [26].
Атеросклероз почечных артерий служит одной из причин, приводящих к развитию ХПН. По аналогии с ИБС симптомокомплекс, связанный с формированием атеросклеротических бляшек в сосудах почек, предлагается обозначать как ишемическая болезнь почек (ИБП) или ишемическая нефропатия. ИБП, как правило, сочетается с атеросклеротическим поражением других артерий [27] и наиболее распространена у пациентов из группы высокого риска, колеблясь от 30% у пациентов с ИБС до 50% у пациентов с диффузным атеросклеротическим поражением сосудов [28].
J.M. Alcasar и соавт. (2001) провели многоцентровое обсервационное исследование, посвященное течению и исходам ИБП у 156 больных. У большинства из них наблюдали распространенный атеросклероз (82%), самой частой локализацией которого были периферические (67,9%) и коронарные (45%) артерии [29]. Частота сопутствующих ССЗ при ИБП объясняется не только тем, что ИБП редко становится первым проявлением системного атеросклероза, но и тем, что ХПН как типичный симптом ИБП сама становится проатерогенным состоянием [30, 31]. В одном из исследований A.M. О’Хара и соавт. отметили, что у пациентов с умеренной и тяжелой ХБП значительно увеличивается риск смерти при наличии распространенного периферического атеросклероза, что и подтвердили результаты нашего исследования [32].
По данным другого исследования, проведенного J.P. Liew и соавт., оценивших 6-летнюю летальность пациентов (n=284) с ХБП и/или клиническими проявления МФА, летальность составила 28%. При этом у пациентов с МФА и ХБП регистрировалась наиболее высокая 6-летняя смертность — 45%. У пациентов только с ХБП смертность в 6-летнем периоде составила 28%, при наличии только МФА — 26%. У пациентов без МФА и ХБП смертность составила 18% [33].
Однако в настоящее время нет исследований, посвященных взаимному влиянию ДП и бессимптомного МФА на прогноз у пациентов, перенесших ИМпST. По результатам настоящего исследования показано, что у больных ИМпST и МФА в сочетании с ДП прогноз через 12 мес значительно хуже, чем у больных ИМпST без признаков МФА и/или ХБП. При этом дополнительно показано преимущество в стратификации риска при определении ККр.
Заключение
Наличие стенозов периферических артерий у больных инфарктом миокарда с подъемом сегмента ST ассоциируется с ухудшением фильтрационной функции почек. У больных, перенесших инфаркт миокарда, любое проявление периферического атеросклероза и нарушение функции почек следует рассматривать как предикторы смерти в течение года.



