Известно, что легочная гипертензия (ЛГ) ухудшает прогноз различных сердечно-сосудистых заболеваний. Наиболее неблагоприятной в этом ряду является идиопатическая легочная гипертензия (ИЛГ). Диагностика ИЛГ основана, главным образом, на результатах катетеризации правых отделов сердца и легочной артерии. Однако инвазивность данного метода обусловливает необходимость поиска альтернативных путей для ранней диагностики ЛГ. Эхокардиография (ЭхоКГ), являясь доступным неинвазивным методом, позволяет не только определить уровень ЛГ, но и ответить на ряд дифференциально-диагностических вопросов. Комплексная ЭхоКГ дает возможность получить подробную информацию о структурно-функциональном состоянии сердца у больных с ЛГ различной этиологии. С помощью современных эхокардиографических технологий становится возможным по-новому исследовать правый желудочек (ПЖ), что ранее представляло трудности.
 Всплеск интереса к изучению ПЖ возник после публикации ряда исследований, доказывающих влияние функции ПЖ на прогноз у пациентов с различными сердечно-сосудистыми заболеваниями. Показано, что правожелудочковая дисфункция неблагоприятно влияет на исходы заболеваний у пациентов с ЛГ различной этиологии, в том числе с ИЛГ [1], инфарктом миокарда ПЖ [2], хронической сердечной недостаточностью (ХСН) [3, 4], тромбоэмболией легочной артерии и ее ветвей [5, 6]. Доказано значение объема, систолической и диастолической дисфункций и массы миокарда ПЖ в определении прогноза у пациентов с ЛГ [1, 4].
Всплеск интереса к изучению ПЖ возник после публикации ряда исследований, доказывающих влияние функции ПЖ на прогноз у пациентов с различными сердечно-сосудистыми заболеваниями. Показано, что правожелудочковая дисфункция неблагоприятно влияет на исходы заболеваний у пациентов с ЛГ различной этиологии, в том числе с ИЛГ [1], инфарктом миокарда ПЖ [2], хронической сердечной недостаточностью (ХСН) [3, 4], тромбоэмболией легочной артерии и ее ветвей [5, 6]. Доказано значение объема, систолической и диастолической дисфункций и массы миокарда ПЖ в определении прогноза у пациентов с ЛГ [1, 4].
В настоящее время не вызывает сомнения важность комплексной оценки состояния правых и левых отделов сердца при различных заболеваниях сердечно-сосудистой системы, однако оценка структуры и функции ПЖ до настоящего времени остается сложной задачей. Трудности анализа связаны прежде всего с особенностями геометрической формы и строения ПЖ — более выраженной трабекуляцией и меньшей толщиной стенок по сравнению с левым желудочком.
В рекомендациях Американского (ASE) и Европейского (EAE) обществ по ЭхоКГ, опубликованных в 2005 г. [7], основные измерения относились к исследованию левых отделов сердца, и лишь небольшой их раздел касался ПЖ и правого предсердия. В 2010 г. по результатам многоцентровых исследований с участием большого числа больных и в связи с получением новых данных о роли ПЖ в центральной гемодинамике были разработаны и созданы отдельные рекомендации по эхокардиографической оценке правых камер сердца [8]. Они более подробно освещают вопросы измерения ряда необходимых параметров, оценки систолической и диастолической функций ПЖ, в том числе с помощью современных эхокардиографических технологий, таких как тканевая допплеро-графия миокарда (ТДМ) и трехмерная эхокардиография (3D-ЭхоКГ). В новых рекомендациях с учетом данных последних исследований скорректированы некоторые количественные критерии, а также уделено особое внимание необходимости комплексного подхода не только к определению размеров, объемов, но и к исследованию параметров систолической и диастолической функций ПЖ. Однако стандартизация протокола по оценке правых отделов сердца до сих пор не завершена. Отчасти это связано с небольшим количеством крупных исследований с использованием современных эхокардиографических технологий, а также с появлением новых эхокардиографических методов (технология speckle tracking, 3D Strain), применение которых требует дальнейшего изучения.
В статье приводится обзор диагностических возможностей различных эхокардиографических технологий в оценке состояния ПЖ, а также предложен алгоритм обследования больных с легочной гипертензией различной этиологии.
Стандартная одно- и двумерная ЭхоКГ. Попытки измерения ПЖ с использованием ЭхоКГ предпринимались с момента открытия возможностей ультразвука в кардиологии. Еще в 1980 г. G. Louridas и соавт. [9] показали, что при измерении в одномерном режиме размеры ПЖ у здоровых людей и пациентов с хроническим легочным сердцем существенно различались. Однако измерения в М-режиме не всегда точны, так как зависят от угла сечения ПЖ ультразвуковым лучом, поэтому использование двумерной ЭхоКГ стало новой важной ступенью в изучении правых камер сердца. В настоящее время для полного и всестороннего изучения структуры ПЖ рекомендовано использовать все режимы ЭхоКГ и все ультразвуковые доступы, позволяющие визуализировать правые отделы сердца: левый парастернальный (длинная и короткая ось), апикальный четырехкамерный и субкостальный.
 Из линейных размеров прежде всего доказана необходимость оценки диаметров выносящего тракта правого желудочка (ВТПЖ) — дистального и проксимального [10, 11]. Особенно важны измерения ВТПЖ у пациентов с ЛГ, приводящей к перегрузке объемом правых отделов сердца. Нужно помнить, что у пациентов с выраженной деформацией грудной клетки размеры ВТПЖ могут быть искажены.
Из линейных размеров прежде всего доказана необходимость оценки диаметров выносящего тракта правого желудочка (ВТПЖ) — дистального и проксимального [10, 11]. Особенно важны измерения ВТПЖ у пациентов с ЛГ, приводящей к перегрузке объемом правых отделов сердца. Нужно помнить, что у пациентов с выраженной деформацией грудной клетки размеры ВТПЖ могут быть искажены.
Толщину свободной стенки ПЖ рекомендовано измерять из субкостального доступа, желательно при увеличении изображения (Zoom). Несмотря на отсутствие достаточной информации о прогностической роли толщины свободной стенки ПЖ, увеличение ее более 0,5 см либо ассоциируется с длительной перегрузкой давлением правых отделов сердца, либо является следствием стеноза легочной артерии, признаком гипертрофической кардио-миопатии, болезнью накопления с вовлечением миокарда ПЖ [12, 13]. Истончение же миокарда ПЖ наблюдается при аритмогенной дисплазии, инфаркте миокарда ПЖ и аномалии Уля [8] — редкой врожденной патологии, характеризующейся выраженной гипоплазией или почти полным отсутствием миокарда одного из желудочков, чаще — правого.
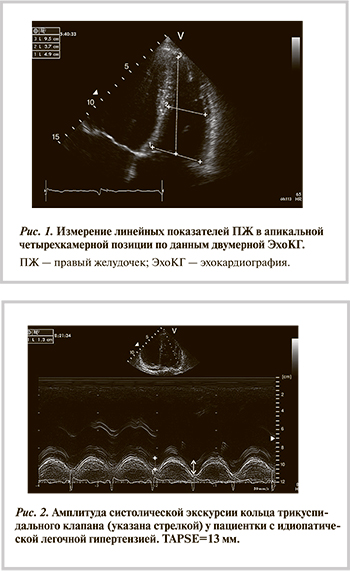
Для всесторонней оценки ПЖ измерения проводятся также из апикальной четырехкамерной позиции. В норме в этой позиции ПЖ меньше левого желудочка и составляет не более 2/3 его размера, верхушка сердца сформирована левым желудочком. У пациентов с визуальными признаками увеличения ПЖ рекомендовано определение базального (в базальной трети ПЖ), среднего (на уровне папиллярных мышц) диаметров и длинника ПЖ (рис. 1). Увеличение базального размера ПЖ более 4,2 см указывает на дилатацию, которая, как правило, ассоциирована с перегрузкой правых отделов объемом или давлением, и с правожелудочковой недостаточностью [8].
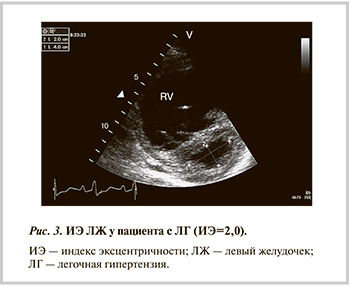
Важным параметром оценки сократительной функции ПЖ является систолическая экскурсия кольца трикуспидального клапана (TAPSE) (рис. 2). В последнее время все большее число работ демонстрирует диагностическую значимость этого критерия. В исследовании B.A. Samad и соавт. [14] показатель TAPSE был достоверно меньше у 194 пациентов с острым инфарктом миокарда с вовлечением ПЖ по сравнению с таковым у здоровых добровольцев. TAPSE <15 мм по сравнению с TAPSE >20 мм ассоциировалась с повышением смертности. Согласно результатам последних исследований, TAPSE <16 мм отражает снижение систолической функции ПЖ [8], но необходимо помнить, что при локальном нарушении сократимости базального сегмента ПЖ TAPSE является показателем региональной, а не глобальной его сократительной функции.
 Косвенной характеристикой функции ПЖ служит размер правого предсердия (ПП). В ряде исследований показано, что площадь ПП в группе пациентов с ЛГ была предиктором неблагоприятных исходов (смерти и трансплантации сердца) [8]. Площадь ПП является более чувствительным индикатором диастолической дисфункции ПЖ, нежели его линейные размеры.
Косвенной характеристикой функции ПЖ служит размер правого предсердия (ПП). В ряде исследований показано, что площадь ПП в группе пациентов с ЛГ была предиктором неблагоприятных исходов (смерти и трансплантации сердца) [8]. Площадь ПП является более чувствительным индикатором диастолической дисфункции ПЖ, нежели его линейные размеры.
В связи с невозможностью визуализировать ПП в 2 взаимно перпендикулярных проекциях, а также недостатками стандартизации, в настоящее время не рекомендовано измерять объем ПП методом двумерной ЭхоКГ. Это положение касается определения объемов и фракции выброса (ФВ) ПЖ.
Попытки определения объемов и сократимости ПЖ с помощью двумерной ЭхоКГ предпринимались давно. Так, R. Levine и T. Gibson и соавт. [15, 16] для расчета объема ПЖ предлагали метод площадь—длина, в которой используются 2 эхокардиографические позиции: изображение ПЖ из апикального четырехкамерного доступа и ВТПЖ из субкостального доступа. Более доступным и простым методом определения ФВ ПЖ казался метод, предложенный S. Kaul и соавт. [17]. Согласно ему, для расчета ФВ ПЖ достаточно определить лишь точку соединения плоскости кольца трикуспидального клапана со свободной стенкой ПЖ и вычислить показатель сократимости по формуле, составленной по уравнению линейной регрессии между ФВ ПЖ и расстоянием, которое проходит плоскость кольца трикуспидального клапана за сердечный цикл. Однако данные методики определения ФВ ПЖ не прижились в клинической практике, поскольку, во-первых, обладают низкой воспроизводимостью, большим разбросом нормативных значений, а во-вторых, на ФВ ПЖ, измеренную таким образом, влияют не только сократимость ПЖ, но также и пред- и посленагрузка, внутригрудное, трансторакальное давление, следовательно, снижение ФВ ПЖ может и не свидетельствовать о нарушенной сократимости ПЖ.
В то же время площадь ПЖ, измеренная планиметрически, а также фракция укорочения ПЖ (FAC), определенная по формуле: (конечная диастолическая площадь – конечная систолическая площадь) / (конечная диастолическая площадь) × 100%, достаточно точно отражают систолическую функцию ПЖ и высоко коррелируют с ФВ ПЖ, определенной методом магнитно-резонансной томографии [18, 19]. Снижение FAC является независимым предиктором развития сердечной недостаточности и внезапной сердечной смерти в исследованиях у пациентов, перенесших тромбоэмболию легочной артерии [20] и инфаркт миокарда [21, 22].
 В новых рекомендациях приведены нормативные значения размеров ПП и ПЖ (табл. 1).
В новых рекомендациях приведены нормативные значения размеров ПП и ПЖ (табл. 1).
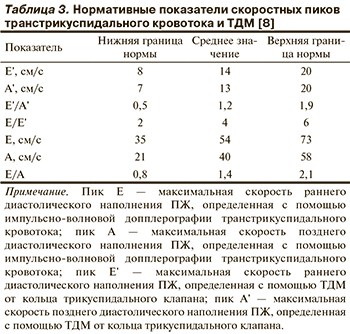
Прогрессирующее течение ЛГ приводит к компрессии левых отделов сердца с отсутствием нормального наполнения левого желудочка (ЛЖ) и снижением сердечного выброса. Это является плохим прогностическим признаком, свидетельствующим о перегрузке ПЖ [23]. ЭхоКГ позволяет оценить степень дисфункции ЛЖ. Количественная оценка компрессии ЛЖ может быть проведена с помощью расчета индекса эксцентричности (ИЭ): соотношения продольного и поперечного диаметров ЛЖ по короткой оси в систолу и диастолу [24] (рис. 3).
ИЭ может также быть использован для дифференциальной диагностики между перегрузкой ПЖ объемом и перегрузкой давлением. В норме ИЭ ЛЖ близок к 1,0 как в систолу, так и в диастолу. Его значение более 1,0 в конце диастолы предполагает перегрузку ПЖ объемом, тогда как увеличение ИЭ и в систолу, и в диастолу указывает на перегрузку давлением [25].
Дилатация ПЖ, вызывая компрессию левых камер сердца, приводит к ухудшению наполнения ЛЖ, что может быть оценено по соотношению пиков Е и А трансмитрального кровотока. Отношение Е/А <1 (нарушение диастолической функции ЛЖ по типу замедленной релаксации) часто наблюдается при тяжелой ЛГ.
 Еще один важный параметр, который должен быть оценен у пациентов с выраженной ЛГ, — сердечный выброс ЛЖ, рассчитанный как отношение диаметра выносящего тракта ЛЖ к интегралу линейной скорости трансаортального кровотока. Данный показатель является прогностическим, несколько вариабелен, однако подходит для оценки клинического состояния конкретного пациента в динамике.
Еще один важный параметр, который должен быть оценен у пациентов с выраженной ЛГ, — сердечный выброс ЛЖ, рассчитанный как отношение диаметра выносящего тракта ЛЖ к интегралу линейной скорости трансаортального кровотока. Данный показатель является прогностическим, несколько вариабелен, однако подходит для оценки клинического состояния конкретного пациента в динамике.
Допплер-эхокардиография (допплер-ЭхоКГ). До эры допплер-ЭхоКГ методы, позволяющие определять степень повышения давления в правых отделах сердца, были косвенными и представляли собой лишь способы выявления последствий перегрузки давлением ПЖ. Так, у пациентов с ЛГ была обнаружена корреляция индексированной площади ПЖ с давлением в легочной артерии, но это был ненадежный показатель для использования при оценке степени ЛГ у конкретных пациентов [26, 27]. С внедрением допплер-ЭхоКГ в широкую практику значительно расширились возможности неинвазивной оценки гемодинамических показателей.
Определение давления в легочной артерии (ДЛА) важно не только в плане постановки верного диагноза, но и в определении прогноза у пациентов, оценки динамики их состояния на фоне терапии.
Определение систолического давления в легочной артерии (СДЛА) рекомендовано у всех пациентов при выполнении ЭхоКГ. При выявлении повышения СДЛА необходимо также измерять диастолическое (ДДЛА) и среднее (срДЛА) давление.
При сравнении значений ДЛА, измеренного при ЭхоКГ, с данными катетеризации правых отделов сердца показано, что значения коррелируют между собой. Проведен ряд исследований, основной задачей которых было выявление взаимосвязей СДЛА, определенного с помощью различных диагностических методов. В работе C. Falletta и соавт. [28] пациентам с ЛГ различной этиологии были проведены ЭхоКГ и катетеризация правых отделов сердца с определением давления в ПП, СДЛА, ДДЛА и срДЛА. При сопоставлении данных, полученных инвазивным и неинвазивным методом, было выявлено, что из всех параметров наиболее тесно коррелируют между собой СДЛА и ДДЛА.
В исследовании G. Ensing и соавт. [29] ДДЛА и конечный диастолический градиент давления на легочном клапане также оказались сопоставимы, однако при более детальном анализе оказалось, что с показателями, полученными при катетеризации правых отделов сердца, теснее коррелирует СДЛА, а не ДДЛА.
Таким образом, сочетанная оценка потоков трикуспидальной и легочной регургитаций позволяет более точно определять ДЛА неинвазивным методом, тем более что в ряде случаев оценка одним из способов бывает затруднена.
При скрининговом обследовании с целью выявления больных с ЛГ достаточно измерять только пиковую скорость трикуспидальной регургитации или максимальный систолический градиент давления на трикуспидальном клапане (мГДсТК). В крупном исследовании B. McQuillan [30], включающем 3212 пациентов с хорошим «ультразвуковым окном» и без подозрения на повышение ДЛА, пиковая скорость трикуспидальной регургитации в среднем составила 2,6 м/с, а мГДсТК — 18 мм рт.ст. Было также показано, что возраст, индекс массы тела (ИМТ), пол, ФВ ЛЖ оказывают существенное влияние на пиковую скорость.
У пациентов старше 60 лет, с ИМТ >30 кг/м2 мГДсТК составил в среднем чуть более 30 мм рт.ст., что соответствовало срДЛА 24 мм рт.ст. Основываясь на полученных данных, авторы сформировали критерии, на основании которых можно предполагать наличие у пациента ЛГ (табл. 2) [31].
3D-ЭхоКГ. Появление новой эхокардиографической технологии — 3D-ЭхоКГ – открывает возможность более точно оценить объемы и систолическую функцию ПЖ. Доказано, что данные, полученные при 3D-ЭхоКГ у экспериментальных животных, с высокой точностью совпадают с результатами, полученными при измерении объемов ПЖ изолированного сердца [32—34]. А. Grison и соавт. [35], сравнивая ультразвуковые и интраоперационные данные, также показали, что у детей с дефектом межпредсердной перегородки, сопровождающимся перегрузкой объемом правых отделов сердца, 3D-ЭхоКГ является точным неинвазивным методом оценки объемов ПП и ПЖ.
Эта методика позволяет получить наибольшую информацию о морфологии и функции ПЖ. Последующая обработка трехмерных изображений (нарезка в разных плоскостях и сечениях) используется для получения необходимых данных об интересующем исследователя объекте. Появляется возможность оценить ПЖ во взаимно перпендикулярных плоскостях и более точно определить его ФВ, чего нельзя сделать с помощью двумерной ЭхоКГ.
Опубликованные исследования сообщают о высокой корреляции между данными, полученными при 3D-ЭхоКГ и магнитно-резонансной томографии (МРТ), как у взрослых, так и у детей [36, 37]. Так, A. Gopal и соавт. [38] сравнивали конечный систолический, конечный диастолический, ударный объемы и ФВ ПЖ, полученные с помощью 2D-, 3D-ЭхоКГ и МРТ в группе из 71 здорового добровольца. Результаты 3D-ЭхоКГ показали наиболее тесную корреляцию с данными МРТ, в отличие от показателей, полученных при 2D-ЭхоКГ.
Объединенные данные нескольких небольших и одного крупного исследования свидетельствуют, что в среднем верхняя граница нормы для индексированного конечного диастолического объема ПЖ составляет 89 мл/м2, индексированного конечного систолического объема — 45 мл/м2 (у женщин — на 10—15% меньше, чем у мужчин). ФВ ПЖ в норме не должна быть менее 44% [39]. Но до тех пор, пока не проведено большее количество крупных исследований, эти данные не могут являться абсолютным эталоном. Кроме того, до сих пор не существует точных формул расчета ФВ, учитывающих особенности строения ПЖ, в связи с чем для этих целей также используется метод суммации дисков. Продолжаются многочисленные исследования, целью которых является адаптация возможностей 3D-ЭхоКГ для максимально точного исследования структуры и функции ПЖ.
ТДМ. Такой сравнительно новый метод, как ТДМ, также дает возможность получить большое количество информации, позволяющей оценить как глобальную и региональную систолическую, так и диастолическую функцию ПЖ. В основе метода лежит эффект Допплера, однако при этом предметом изучения являются не внутрисердечные потоки, а собственно миокард. ТДМ позволяет количественно определить пиковые скорости, амплитуду систолического смещения, продолжительность фаз сердечного цикла, а также скорость и амплитуду деформации миокарда [40]. Как правило, определяют скорости только от кольца трикуспидального клапана (при обычной ЭхоКГ не оцениваются скорости от средних и верхушечных сегментов свободной стенки ПЖ), для этого контрольный объем устанавливают на фиброзное кольцо трикуспидального клапана в области свободной стенки ПЖ.
Кривая ТДМ представлена тремя пиками — систолическим (S′) и двумя диастолическими (E′, A′), соответствующими фазам раннего диастолического наполнения ПЖ и систолы ПП (рис. 4, см. цветную вклейку).
Для оценки систолической функции ПЖ производится измерение систолического пика (S′). При анализе данных 43 различных исследований, включающих в общей сложности более 2000 человек, установлено, что систолическую дисфункцию ПЖ можно констатировать при снижении S′< 10 см/с [8]. Диастолическая функция ПЖ, по данным ТДМ, определяется на основании измерения пиков Е′ и А′, а также их соотношения с пиками транстрикуспидального кровотока. В табл. 3 представлены данные, полученные в ходе последних исследований, касающихся диастолической функции миокарда ПЖ.
Диастолическая дисфункция ПЖ, так же, как и ЛЖ, подразделяется на несколько типов:
- замедленная релаксация (Е/А<0,8);
- псевдонормализация (Е/А от 0,8 до 2,1; Е/Е′ >6);
- рестрикция (Е/А >2,1; DT <120 мс).
Значения пиков транстрикуспидального кровотока и ТДМ показали высокую сопоставимость с показателями гемодинамики. Так, повышение Е/Е′ >8 ассоциируется с увеличением давления в ПП более 10 мм рт.ст. [41].
При исследовании кривой ТДМ может быть получен еще один немаловажный показатель глобальной систолической и диастолической функции ПЖ — индекс функции миокарда (MPI), или Тей-индекс (Tei-index). Он представляет собой отношение суммы периодов изоволюмического сокращения и расслабления ко времени изгнания. В настоящее время активно изучается прогностическая роль индекса функции миокарда ПЖ и в ряде работ уже показано, что этот индекс является диагностически значимым критерием у пациентов с ПЛГ [42], инфарктом миокарда ПЖ [43], врожденными пороками сердца [44]. В 23 исследованиях, включающих более 1000 человек, определено, что Тей-индекс, измеренный методом ТДМ, не должен превышать 0,55 [8]. Однако данный показатель рекомендовано использовать лишь в комплексе с другими методами, оценивающими систолодиастолическую функцию ПЖ.
Кроме скоростных и временны'х показателей, ТДМ позволяет определять деформацию миокардиальных волокон (strain) и скорость их деформации (strain rate). Параметр деформации оценивает изменение длины кардиомиоцитов и измеряется в процентах от исходной длины миокардиального волокна. Скорость изменения длины называют скоростью деформации. При оценке региональной деформации ПЖ обращает внимание неоднородность strain и strain rate: средние значения этих показателей у здоровых добровольцев являются наименьшими в базальном сегменте и увеличиваются к верхушке, в противоположность региональным пиковым скоростям ТДМ. Показатели деформации ПЖ в настоящее время активно изучаются при аритмогенной дисплазии ПЖ, тромбоэмболии легочной артерии, ИЛГ, амилоидозе [45—48], но несмотря на это, получено недостаточно нормативных данных, в связи с чем оценка strain и strain rate используется в основном в исследовательских работах и очень редко — в клинической практике.
Метод ТДМ технически прост в использовании, однако имеет ряд недостатков, связанных с зависимостью от угла сканирования, — угол между ультразвуковым лучом и направлением движения исследуемой структуры не должен превышать 15—20°, иначе значительно возрастает ошибка измерений и резко снижается воспроизводимость метода.
Технология двумерного стрейна (2D-strain или Speckle Tracking Imaging). В настоящее время бурное развитие ультразвуковых технологий привело к появлению принципиально новых подходов к оценке функционального состояния миокарда как ЛЖ, так и ПЖ. С помощью этих методов уже на ранних стадиях развития сердечно-сосудистых заболеваний можно выявлять минимальные изменения физиологических параметров сердца. Одна из таких методик — технология Speckle Tracking Imaging — основана на определении движения миокарда при помощи отслеживания перемещения естественных акустических маркеров — зернистых структур миокарда на стандартном серошкальном изображении в В-режиме. Суть метода заключается в том, что акустические маркеры случайным образом распределяются по миокарду, а затем положение каждого пятна определяется и отслеживается на серии последовательных кадров, что позволяет определить расстояние, на которое смещается пятно от кадра к кадру. Таким образом, по движению этих структур можно получить данные о скорости движения и деформации участков миокарда [49]. Технология двумерного стрейна имеет ряд преимуществ перед ТДМ, поскольку измерения менее зависят от угла сечения ПЖ ультразвуковым лучом, что позволяет определять функцию верхушечных сегментов, а также оценивать скорость и деформацию волокон одновременно в двух направлениях в продольном и радиальном, отсюда и название — двумерный стрейн (2D-strain) (рис. 5, см. цветную вклейку).
Начиная с 2010 г., в литературе появляется все больше данных, касающихся исследования ПЖ при различных патологических состояниях, с помощью технологии двумерного стрейна. Например, I. Garcia Lunar и соавт., исследуя деформацию и скорость деформации методом двумерного стрейна в группе пациентов с ЛГ различной этиологии, выявили достоверное снижение глобального и регионального продольного стрейна по сравнению с таковым у здоровых лиц. Кроме того, авторы выявили высокую корреляцию показателей деформации со значениями TAPSE и FAC [50]. Деформация методами двумерного стрейна и ТДМ изучалась и у пациентов с аритмогенной дисплазией ПЖ. У этих пациентов, как и в предыдущем исследовании, выявлено достоверное снижение пиков деформации по сравнению с группой контроля, а чувствительность и специфичность двумерного стрейна оказались выше, чем у ТДМ [51].
Все это убеждает в необходимости продолжения изучения новой технологии двумерного стрейна применительно к оценке функции ПЖ при различных заболеваниях. Однако недостаточное количество исследований и нормативных данных на настоящий момент ограничивает применение этого метода в клинической практике.
Заключение
За последние годы возможности эхокардиографии в изучении структурно-функционального состояния правого желудочка при легочной гипертензии различной этиологии значительно возросли. Появились первые работы с использованием трехмерного стрейна (3D-strain) в оценке дисфункции правого желудочка, продолжается изучение роли двумерного стрейна, тканевого миокардиального допплера, трехмерной эхокардиографии в исследовании правого желудочка. Если раньше из-за сложности морфологии правого желудочка эхокардиографическая оценка носила в основном качественный характер, то теперь появляется все больше количественных критериев, которые делают исследование правого желудочка более точным и объективным. Все это позволяет надеяться, что в скором времени стандартизация протокола исследования правых отделов сердца будет доработана и завершена с учетом новых данных.
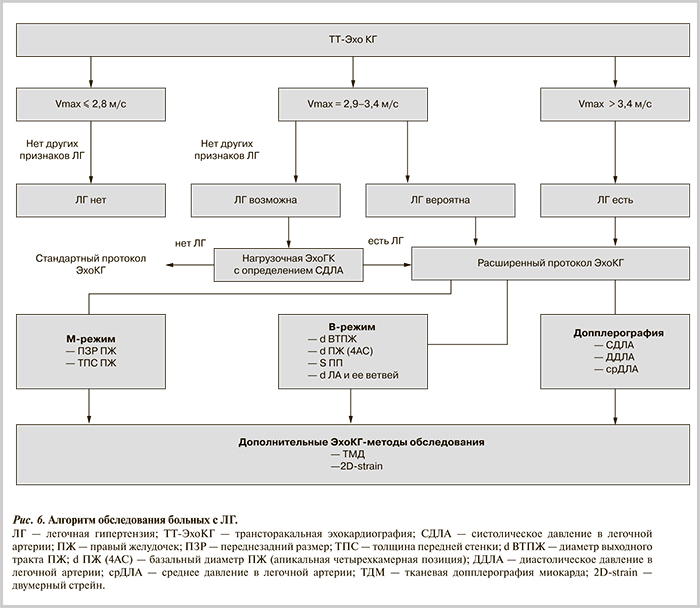
Сегодня же мы предлагаем алгоритм эхокардиографического обследования больных в зависимости от степени выраженности легочной гипертензии (рис. 6). Небольшое повышение скорости или систолического градиента давления на трикуспидальном клапане еще не означает однозначно наличие у больного повышения давления в легочной артерии. В отсутствие других признаков легочной гипертензии рекомендовано проведение нагрузочной эхокардиографии с определением систолического давления в легочной артерии при нагрузке. Подтверждение высокого систолического давления в легочной артерии, а также наличие у больного в покое выраженной легочной гипертензии обусловливает необходимость применения расширенного эхокардиографического протокола для уточнения стадии заболевания и в дальнейшем оценки эффективности проводимого лечения. Исследование правого и левого желудочков сердца с использованием дополнительных эхокардиографических технологий может помочь в определении параметров компенсации патологического процесса.



