Коронарное шунтирование (КШ) — основной метод инвазивного лечения больных ишемической болезнью сердца (ИБС). Хирургическая реваскуляризация миокарда позволяет в значительной степени уменьшить либо вовсе ликвидировать ангинозный болевой синдром и увеличить продолжительность жизни пациентов с тяжелым многососудистым поражением коронарного русла. Между тем у больных ИБС с выполненной операцией КШ сохраняется риск развития рецидива симптоматики ИБС вследствие прогрессирования атеросклеротического поражения нативных нешунтированных коронарных артерий и закрытия сформированных аортокоронарных и маммарокоронарных анастомозов.
Наиболее уязвимым материалом с позиций стенозирующих процессов являются венозные трансплантаты. Приблизительно у 10% больных, перенесших операцию КШ, происходит окклюзия венозных аортокоронарных шунтов в течение 2 мес и еще у 10% — в течение 1 года после операции [1, 2]. Через 10 лет после операции только около 45% аутовенозных шунтов остаются проходимыми [3]. Причины рецидива стенокардии после КШ можно разделить на две большие группы: хирург-ассоциированные и пациент-ассоциированные. Первую группу подразделяют на две категории: технические ошибки (некорректное выделение шунта-графта, формирование анастомоза с возникновением гемодинамически значимого стеноза, избыточная или недостаточная длина шунта, перегиб шунта) и тактические ошибки — неполная или неадекватная реваскуляризация. Вторая группа причин включает прогрессирование атеросклероза в графтах шунтированных и интактных коронарных артерий, а также тромбоз, гиперплазию интимы и мышечной оболочки венозного шунта [4].
Если тромбоз и гиперплазия венозного шунта ответственны за ранние механизмы клинического рецидива ИБС, то спустя 1 год после операции реваскуляризации миокарда доминирующим процессом, лежащим в основе дисфункции шунтов и возвращения клинических симптомов ИБС, помимо гиперплазии становится атеросклероз [5]. Наиболее эффективными средствами, снижающими риск развития атеросклеротических сердечно-сосудистых заболеваний и их осложнений, являются ингибиторы ГМГ-КоА-редуктазы (статины).
К современным высокоактивным статинам уже в начальной суточной дозе (5—10 мг/сут) относится розувастатин, гиполипидемическая активность которого возрастает с повышением дозы до максимальной (40 мг/сут). Клиническая эффективность розувастатина доказана в большой программе GALAXY, в рамках которой проведено 18 многоцентровых исследований препарата, разделенных на 3 большие категории: 1) изучение влияния розувастатина на липиды и маркеры воспаления: COMETS, DISCOVERY, ECLIPSE, EXPLORER, LUNAR, MERCURY I, MERCURY II, ORBITAL, POLARIS, PULSAR, STELLAR; 2) изучение влияния розувастатина на атеросклеротическое поражение коронарных и сонных артерий: ASTEROID, METEOR, ORION; 3) изучение влияния розувастатина на риск развития сердечно-сосудистых осложнений, сердечно-сосудистую и общую смертность: AURORA, CORONA, JUPITER [6]. В этих исследованиях установлено положительное влияние розувастатина на всех этапах развития атеросклеротического процесса.
 В настоящее время необходимость назначения статинов перед КШ пациентам разделяется не всеми исследователями. Противники такого подхода считают нецелесообразным назначение статинов в периоперационном периоде с позиции безопасности. Вместе с тем в серии ранее проведенных исследований не выявлено увеличения частоты гепатотоксических и миопатических побочных эффектов статинов в периоперационном периоде [7, 8]. Более того, показано благоприятное влияние коротких предоперационных курсов статинов в отношении ограничения интра- и послеоперационных осложнений при КШ [9, 10].
В настоящее время необходимость назначения статинов перед КШ пациентам разделяется не всеми исследователями. Противники такого подхода считают нецелесообразным назначение статинов в периоперационном периоде с позиции безопасности. Вместе с тем в серии ранее проведенных исследований не выявлено увеличения частоты гепатотоксических и миопатических побочных эффектов статинов в периоперационном периоде [7, 8]. Более того, показано благоприятное влияние коротких предоперационных курсов статинов в отношении ограничения интра- и послеоперационных осложнений при КШ [9, 10].
Цель настоящего исследования — оценка гиполипидемической эффективности розувастатина и его влияния на пролиферативные процессы в большой подкожной вене (БПВ) у пациентов с ИБС при КШ.
Материал и методы
В исследование включали пациентов со стабильной стенокардией напряжения II—IV функционального класса (ФК), направленных на хирургическую реваскуляризацию миокарда. В конечном результате были отобраны 62 больных. Специальным критерием отбора являлся прием симвастатина исходно при направлении на КШ в дозе 20 мг/сут. Средний возраст отобранных пациентов на момент исследования составил 51,4±7,9 года, всего включены 54 (87%) мужчин и 8 (13%) женщин. Продолжительность анамнеза ИБС в виде стенокардии напряжения различных ФК до включения в исследование составила в среднем 3,8±3,4 года. Стенокардия напряжения II ФК определена у 10 (16%) больных, III ФК у 39 (63%), у 13 (21%) больных имелась клиническая картина стенокардии IV ФК. Средняя выраженность стенокардии соответствовала 2,96±0,2. Не включали в исследование больных, перенесших Q-инфаркт миокарда, нарушение мозгового кровообращения, с клинически значимой артериальной гипертензией, сахарным диабетом, системными заболеваниями, нарушениями функции почек и печени, застойной сердечной недостаточностью и выраженной дисфункцией левого желудочка (фракция выброса – ФВ <40%).
Все больные, которым планировалась ориентировочно через 4 нед хирургическая реваскуляризация миокарда, после компьютерной рандомизации были разделены на 2 равные группы: группа А — 31 больной группы контроля продолжал прием симвастатина в дозе 20 мг/сут; группа В — 31 больной основной группы, которым вместо симвастатина был назначен розувастатин (мертенил, «Gedeon Richter», Венгрия) в максимально разрешенной дозе 40 мг/сут. Кроме того, пациенты до КШ получали стандартную терапию, включающую прием дезагрегантов (отменялись перед КШ), ингибиторов ангиотензин-превращающего фермента (или сартанов), β-адреноблокаторов и/или антагонистов кальция, при необходимости нитратов. Продолжительность наблюдения за результатами лечения высокодозной терапией розувастатином составила в большинстве случаев 4 нед, в течение которых были определены 3 визита. Во время первого визита рандомизации проводили обследование, общеклиническое и биохимическое исследование крови с определением общего холестерина (ОХС), холестерина (ХС) липопротеинов низкой плотности (ЛНП), триглицеридов (ТГ) и холестерина липопротеинов высокой плотности (ЛВП). Через 2 нед осуществляли контроль уровня печеночных ферментов и креатинфосфокиназы. Заключительный, 3-й визит проводили непосредственно накануне КШ с контрольным полным лабораторным исследованием, повторным определением уровня липидов в крови. Последний прием розувастатина осуществляли утром в день операции, возобновляли в 1-е сутки послеоперационного периода в той же дозе и продолжали в течение всего госпитального периода с рекомендациями его дальнейшего приема на амбулаторном этапе.
Морфологические особенности БПВ изучали в образцах, полученных во время операции КШ. Для гистологического и иммуногистохимического исследования полученный интраоперационный материал фиксировали в 10% формалине, обезвоживали в спиртах восходящей плотности и заливали в парафин. Гистологическое исследование проводили на парафиновых срезах, окрашенных гематоксилином и эозином, по ван Гизону. Морфометрический анализ осуществлялся с помощью анализатора изображения Leica Scope.
Схема приготовления иммуногистохимических препаратов сводилась к следующим этапам: после депарафинизации парафиновых срезов проводили блокирование активности эндогенной пероксидазы в 3% растворе перекиси водорода с последующим промыванием в дистиллированной воде. Восстановление активности антигенов достигали путем кипячения в ЭДТА-буфере (pH 9,0) в водяной бане в течение 30 мин с последующим промыванием в Трис-буфере с Tween 20. Затем следовала инкубация с первичными антителами (18 ч, при температуре 6°С), после этого — инкубация с вторичными антителами Real Rabbit/Mouse (Dako), реакция с DAB, промывание в дистиллированной воде, затем — докрашивание ядер гематоксилином, обезвоживание и заключение в среду Bio Mount. Использовали антитела к Ki-67 — наиболее изученному биомаркеру пролиферативной активности клеток. Во всех препаратах подсчитывали процент клеток с экспрессией антигена при исследовании не менее 1000 клеток, за исключением эндотелия, число клеток которого не всегда достигало заданного.
Полученные первичные данные подвергали математической обработке с использованием прикладных программ Statistica version 6,0. Данные представлены в виде средних арифметических значений и ошибки среднего (M±m). Критический уровень достоверности нулевой статистической гипотезы (об отсутствии различий) был принят равным 0,05. Достоверность различий оценивали по критерию t Стьюдента для независимых выборок и для парных измерений.
Результаты и обсуждение
Суммарно в основной исследуемой группе больных через 4 нед наблюдения переход с симвастатина 20 мг/сут на розувастатин 40 мг/сут сопровождался дополнительным снижением уровня ОХС на 20% (5,5±0,6 и 4,4±0,3 ммоль/л соответственно), а ХС ЛНП на 29% (3,81 и 2,71 ммоль/л соответственно; табл. 1). У 6 (20%) больных терапия привела к снижению уровня ХС ЛНП менее 1,8 ммоль /л, т.е. был достигнут целевой уровень согласно последним международным рекомендациям, у 15 (50%) концентрация ХС ЛНП снизилась до менее 2,5 ммоль/л. В целом высокодозная терапия розувастатином хорошо переносилась, не зафиксировано ни одного случая миопатии. У 1 пациента гиполипидемическая терапия с учетом подготовки к операции КШ была отменена на 2-м визите в связи с двукратным повышением уровня печеночных ферментов. В дальнейшем у данного больного отмечалась быстрая положительная динамика лабораторных показателей, и ему было выполнено КШ в запланированные сроки. Как и ожидалось, в контрольной группе пациентов, продолжающих прием симвастатина 20 мг/сут, динамика липидных показателей отсутствовала.
Высокая гиполипидемическая активность розувастатина вполне объяснима фармакодинамическими особенностями препарата. Розувастатин — синтетический статин четвертого поколения. Это свойство препарата связано с присоединением метансульфониламидной группы к молекуле, что обусловливает улучшение взаимодействия с ГМГ-КоА-редуктазой и более мощное дополнительное ингибирующее воздействие на фермент по сравнению с другими статинами [11]. Необходимый эффект от терапии розувастином проявляется на 1-й неделе, а через 2 нед достигает 90%. К 4-й неделе наблюдается максимальное действие розувастина и удерживается в дальнейшем при условии постоянного применения препарата. По итогам сравнительного исследования STELLAR [12] розувастатин 40 мг/сут понижает концентрацию ЛНП на 55% и повышает концентрацию ЛВП на 10%, что является лучшим показателем среди статинов. Данные исследования LUNAR [13] отражают более высокую эффективность розувастатина 40 мг/сут по сравнению с аторвастатином 80 мг/сут (снижение на 46,8 и 42,7% соответственно). Уменьшение уровня ЛНП после приема розувастатина в дозе 20 мг было аналогичным при использовании аторвастатина в дозе 80 мг. Увеличение концентрации ЛВП также было в пользу розувастатина: прием 40 мг обеспечил рост показателя на 11,9%, тогда как 80 мг аторвастатина увеличивали уровень ЛВП на 5,6%. Следует подчеркнуть, что в нашем исследовании наблюдался не только очевидный гиполипидемический эффект препарата, но и клинически значимое дополнительное снижение уровня ОХС и ХС ЛПНП у больных, которые ранее получали симвастатин в дозе 20 мг.
Важной характеристикой гиполипидемических препаратов являются их нелипидные, так называемые плейотропные свойства, которые, вероятно, имеют существенное значение в конечной клинической эффективности терапии, в том числе у больных после КШ. Применительно к основным патогенетическим процессам дисфункции венозных шунтов интересной представляется оценка частоты развития тромботических осложнений при использовании розувастатина в исследовании JUPITER. В данном исследовании все тромботические осложнения делили на неспровоцированные (т.е. диагностированный тромбоз глубоких вен и тромбоэмболия легочной артерии, которые не связаны с травмой, госпитализацией, хирургической операцией или онкологическим заболеванием) и на спровоцированные (если в момент развития тромботического эпизода у больного имелись указанные состояния) [14]. Всего в исследовании зафиксировано 94 случая клинически проявляющихся тромбозов глубоких вен и эпизодов тромбоэмболии. При этом в группе пациентов, леченных розувастатином, таких эпизодов оказалось 34, тогда как в группе плацебо – 60. Степень снижения риска развития тромбоэмболических осложнений составила 43% (р=0,007). При этом если различия в неспровоцированных эпизодах не достигли статистической значимости, то частота спровоцированных тромбоэмболических осложнений оказалась достоверно более низкой в группе больных, леченных розувастатином.
 Кроме известных закономерностей атеросклеротического и тромботического процессов в шунтирующем материале большое патогенетическое значение в развитии дисфункции венозных шунтов имеет гиперплазия интимы—медии ввиду появления изменений на ранних сроках (от 1 мес до 1 года) после КШ. Пролиферация и миграция клеток интимы и гладких мышечных клеток (ГМК) являются ключевыми механизмами в атерогенезе, патогенезе окклюзии венозных шунтов после операции КШ. Исследования in vitro показали, что большинство статинов уменьшают пролиферацию ГМК и их миграцию [15]. Считается, что этот механизм включает регулирование процессов пролиферации, дифференцировки, миграции и апоптоза клеток, экспрессии эндотелиальной NO-оксидазы. Таким образом, опосредованные через блокаду 3-гидрокси-3-метилглютарил-коэнзима-А-редуктазы печени пролиферативные процессы в сосудах и шунтах определяют потенциальную эффективность статинов в отношении ближайших и отдаленных исходов КШ за счет профилактики окклюзии преимущественно венозных шунтов.
Кроме известных закономерностей атеросклеротического и тромботического процессов в шунтирующем материале большое патогенетическое значение в развитии дисфункции венозных шунтов имеет гиперплазия интимы—медии ввиду появления изменений на ранних сроках (от 1 мес до 1 года) после КШ. Пролиферация и миграция клеток интимы и гладких мышечных клеток (ГМК) являются ключевыми механизмами в атерогенезе, патогенезе окклюзии венозных шунтов после операции КШ. Исследования in vitro показали, что большинство статинов уменьшают пролиферацию ГМК и их миграцию [15]. Считается, что этот механизм включает регулирование процессов пролиферации, дифференцировки, миграции и апоптоза клеток, экспрессии эндотелиальной NO-оксидазы. Таким образом, опосредованные через блокаду 3-гидрокси-3-метилглютарил-коэнзима-А-редуктазы печени пролиферативные процессы в сосудах и шунтах определяют потенциальную эффективность статинов в отношении ближайших и отдаленных исходов КШ за счет профилактики окклюзии преимущественно венозных шунтов.
В нашем исследовании венозные кондуиты использовались в качестве материала для шунтирования различных коронарных бассейнов у всех исследованных больных. Наиболее часто венозные шунты применялись при реваскуляризации огибающей артерии и правой коронарной артерии, в то время как для лечения поражений передней межжелудочковой артерии (ПМЖА) в основном использовалась внутренняя грудная артерия. Кроме поражений собственно ПМЖА, венозные трансплантаты часто использовались для шунтирования ее крупных диагональных ветвей вместе с аутоартериальными шунтами. Всего использовно 123 венозных аортокоронарных шунта: один венозный шунт у 18 (30%) больных, два венозных шунта у 25 (40%) и три венозных шунта у 18 (30%). В 95% случаев была выполнена полная реваскуляризация, в 5% – неполная. Полной считали случаи, когда шунтировали все артерии диаметром более 1 мм и стенозом более 60%.
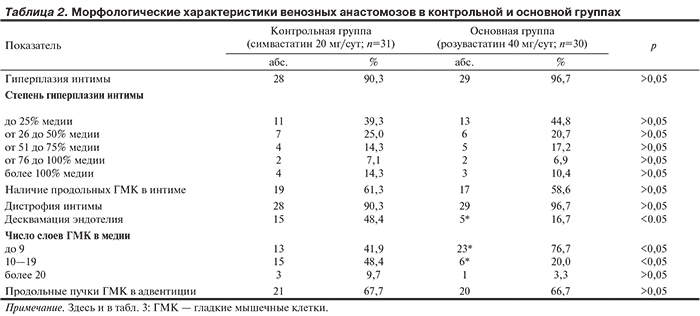
Результаты морфологического исследования образцов вен пациентов основной и контрольной группы представлены в табл. 2.
Признаков атеросклеротического поражения вен не было выявлено ни в одном случае. Воспалительная инфильтрация медии диагностирована в 24,5% случаев, лимфоцитарно-макрофагальная инфильтрация адвентиции — в 27,9%. Хронический флебит выявлен у 23% пациентов, флебосклероз — у 39,3%. Морфометрическое исследование показало, что средняя толщина интимы вен составила 0,12±0,18 мм, медии вен — 0,21±0,09 мм.
Гиперплазия интимы образцов вен в контрольной группе наблюдения пациентов, получающих симвастатин 20 мг/сут, наблюдалась в 90,3% случаев, среди них циркулярная гиперплазия интимы в 46,4% случаев, очаговая гиперплазия в 53,6% случаев. При анализе выраженности гиперплазии интимы получены следующие данные: гиперплазия интимы до 25% толщины медии составила 39,3%, до 50% толщины медии — 25%, до 75% толщины медии — 14,3%, 75% и более — 21,4%. В 90,3% случаев выявлены дистрофия и десквамация эндотелия, в 80% случаев — пролиферация эндотелия vasa vasorum. Морфометрические показатели венозных анастомозов в группе пациентов, получающих розувастатин 40 мг/cут, не отличались от показателей больных, получающих симвастатин в контрольной группе (см. табл. 2). Вместе с тем установлены достоверные различия между группами по показателю десквамации эндотелия (48,4% случаев в контрольной группе и 16,7% в основной; р<0,05).
В контрольной группе у 61,3% пациентов мышечный каркас вен был усилен наличием продольных слоев ГМК в интиме, а у 67,7% — в адвентиции. Аналогичные показатели оказались в основной группе пациентов. Вместе с тем нами установлены достоверные отличия по слоистости ГМК медии у пациентов, получающих высокодозную терапию розувастатином. У большинства больных контрольной группы количество слоев ГМК венозного кондуита составило 10—19 (в среднем 12,23±2,76), в то время как в основной группе — до 9 (в среднем 7,15±2,04; см. табл. 2).
В настоящее время известно несколько ядерных и мембранных антигенов, изменение экспрессии которых связано с пролиферативной активностью клеток. Одним из наиболее изученных молекулярных биомаркеров является показатель пролиферативной активности Ki-67, антитела к антигену которого реагируют с пролиферирующими клетками, находящимися в G1, S, M, G2 стадиях клеточного цикла. Если клетка не пролиферирует, такого взаимодействия не происходит. При иммуногистохимическом анализе по показателю Ki-67 нами обнаружена относительно более низкая пролиферативная активность как клеток эндотелия (4,8±0,04 и 3,4±0,03 соответственно), так и ГМК (7,48±0,06 и 3,98±0,02 соответственно) в группе пациентов, получавших розувастатин (табл. 3).
Таким образом, результаты иммуногистохимического анализа подтверждают данные, полученные при гистологическом исследовании отрезков вен, взятых для КШ. Розувастатин в дозе 40 мг/сут в течение 4 нед приводит к снижению индекса пролиферации в эндотелиоцитах и ГМК анализируемого материала, что сопровождается уменьшением десквамации эндотелия интимы вен и слоистости ГМК медии. Именно пролиферативные процессы в интиме и медии венозного шунта во многом определяют его «артериализацию», развитие «болезни венозного шунта» с последующим формированием стенозов и окклюзий после КШ. Основной механизм развития негативных процессов связан с тем, что аутовенозный графт функционирует в не свойственных ему гемодинамических условиях (высокое внутрисосудистое давление). Исходно большинство вен подвержено фиброзным изменениям. В свою очередь, интима почти всех имплантированных в артериальную систему вен подвергается утолщению в течение 4—6 нед. Клетки эндотелия играют ключевую роль в регуляции клеточного роста. Потеря целостности эндотелия истощает функцию роста нормальной клетки, являясь причиной тромбоза, а также приводит к цитогенезу, в результате которого освобождаются макрофаги из активированных клеток эндотелия, что способствует миграции ГМК в интиму. В дальнейшем синтез и перемещение внутриклеточного матрикса приводят к прогрессированию роста ГМК и активизации фиброза интимы [16—18]. ГМК медии, подвергаясь гиперплазии, ответственны за изменения в просвете сосуда. В венозных шунтах действуют и другие механизмы развития гиперплазии интимы и ГМК, одним из них является транзиторная ишемия венозного шунта, подвергающегося реперфузии после КШ. Это приводит к выделению NO и аденозина, а также супероксидного радикала, действующего непосредственно на внутренние слои сосудистой стенки венозного шунта [19]. Потеря vasa vasorum также может быть продолжением цикла ишемии и фиброза. Другим фактором, приводящим к гиперплазии интимы и ГМК, является повышение нагрузки на венозную стенку за счет высокого артериального давления после пуска кровотока по венозным шунтам, что также может вызывать повреждение интимы и медии [16, 18].
Анализ данных литературы и результаты проведенного исследования свидетельствуют о новых возможностях гиполипидемической терапии у больных ИБС после КШ. Принятые в 2013 г. клинические рекомендации ACC/AHA по дислипидемии относят пациентов после реваскуляризации миокарда к группе высокого риска, при этом показано высокодозное применение в качестве монотерапии двух статинов — помимо традиционно применяемого аторвастатина в дозе 80 (40) мг/сут, также розувастатина в дозе 40 (20) мг/сут [20]. Выраженные гиполипидемические эффекты розувастатина 40 мг/сут в нашем исследовании, установленный антипролиферативный эффект в отношении интимы и ГМК, безопасность применения в периоперационном периоде у больных ИБС позволяют предполагать положительное влияние препарата на отдаленный прогноз у пациентов после КШ.
В 2004 г. были проанализированы фармакоэкономические аспекты применения розувастатина [21]. При моделировании результатов исследований STELLAR, MERCURY I, HeFT установлено, что розувастатин имеет более высокую клиническую эффективность в расчете на 1 мг, и его применение оптимально с точки зрения эффективности затрат по сравнению с другими оригинальными статинами. Такая тенденция отмечена у всех подгрупп пациентов, но наиболее выражена у больных с высоким риском. Важной составляющей решения задачи по снижению затрат любой лекарственной терапии является возможность применения качественных генерических препаратов с фармацевтической, биологической и терапевтической эквивалентностью с оригиналом. С этих позиций привлекательной особенностью мертенила является значительное количество отечественных исследований, свидетельствующих о высокой терапевтической эффективности препарата в различных клинических ситуациях [22—24]. Эти исследования и результаты проведенной нами работы позволяют использовать экономические преимущества препарата при уверенности в качестве проводимой гиполипидемической терапии. В любом случае в настоящее время назрела необходимость более активного внедрения в клиническую практику стратегии применения у больных высокого риска, включая пациентов при КШ, современных гиполипидемических средств в максимально рекомендованных и переносимых дозах.
Заключение
Розувастатин (мертенил 40 мг/сут) у больных ишемической болезнью сердца перед коронарным шунтированием, принимающих ранее симвастатин 20 мг/сут, хорошо переносится и приводит к дополнительному снижению концентрации общего холестерина на 20% и холестерина липопротеинов низкой плотноcти на 29%.
Высокодозная терапия розувастатином (мертенилом 40 мг/сут) в течение 4 нед приводит к уменьшению десквамации эндотелия интимы, числа слоев гладких мышечных клеток медии в участках большой подкожной вены, используемых для аортокоронарного анастомоза. Применение розувастатина приводит к снижению индекса пролиферации по экспрессии Кi-67 в эндотелиальных и гладких мышечных клетках большой подкожной вены.
Работа выполнена в рамках Государственного задания Министерства здравоохранения Российской Федерации «Разработка методов этапной реабилитации и критериев эффективности снижения риска повторных коронарных событий у пациентов, перенесших реваскуляризацию миокарда».



