Введение. В последней Международной гистологической классификации опухолей почки (ВОЗ, 2022) ангиомиоаденоматозная опухоль (АМАО) не выделена в самостоятельную категорию и по сей день рассматривается в статусе неопределенной нозологической формы. В настоящее время в мировой литературе насчитывается около 50 случаев АМАО. Большинство экспертов уверены, что АМАО является редким подвидом светлоклеточной папиллярной почечно-клеточной опухоли (ПКО), а по мнению некоторых авторов, опухоль следует расценивать в рамках группы почечно-клеточных карцином (ПКК) с лейомиоматозной стромой [1–4].
Цель настоящего исследования: сравнительный анализ гистологических, иммунофенотипических, ультраструктурных, молекулярных параметров АМАО и светлоклеточной папиллярной ПКО.
Материалы и методы. Объектом исследования послужил архивный биологический материал от 5 больных (3 мужчины и 2 женщины) в возрасте от 53 до 69 лет, проходивших хирургическое лечение по поводу АМАО почки в Урологической клинике ФГАОУ ВО «Первый Московский государственный медицинский университет им. И. М. Сеченова» Минздрава России. В качестве группы сравнения изучили биоптаты 10 пациентов (6 мужчин и 4 женщины) в возрасте от 48 до 72 лет, проходивших хирургическое лечение по поводу светлоклеточной папиллярной ПКО в урологической клинике ФГАОУ ВО «Первый Московский государственный медицинский университет им. И. М. Сеченова» Минздрава России.
Гистологическое исследование. Биоптаты фиксировали в 10%-ном растворе нейтрального формалина. После стандартной гистологической проводки кусочки заливали в парафин. Срезы толщиной 4–5 мкм окрашивали гематоксилином и эозином. Степень ядерной градации оценивали по четырехуровневой системе согласно классификации ВОЗ/Международной ассоциации урологических патологов (ISUP) 2016 г. [5].
Иммуногистохимическое исследование (ИГХ). Серийные срезы толщиной 5 мкм депарафинировали и регидратировали по стандартной методике. Для «демаскировки» антигенов срезы подвергали высокотемпературной обработке в цитратном буфере и инкубировали 5 мин с 3%-ной Н2О2 (для каждого антитела в соответствии с рекомендуемым протоколом). Использовали мышиные моноклональные антитела к HMWCK (готовый к использованию), к AE1/AE3 (готовый к использованию), к СК7 (готовый к использованию), к E-Cadherin (готовый к использованию) производства «Novocastra» (Великобритания), к EMA (готовый к использованию), к PAX8 (готовый к использованию) производства «Cell Marque» (США) и СА9 (в разведении (1:200) производства «DAKO» (Дания). В качестве вторичных антител использовали систему EnVision («DAKO Cytomation», Дания).
Электронно-микроскопическое исследование (ЭМИ). Кусочки ткани опухолей почки фиксировали в 2,5%-ном глутаральдегиде на 0,1 М фосфатном буфере (рН 7,4), затем постфиксировали в 1%-ном растворе четырехокиси осмия (OsO4). Дегидратацию материала и заливку образцов ткани проводили в ЭПОН-812 по общепринятой методике. Полутонкие срезы толщиной 1–2 мкм готовили на ультрамикротоме LKB-3 (Швеция), окрашивали толуидиновым синим, контрастировали ацетатом уранила и цитратом свинца, а затем исследовали в электронном микроскопе Philips TECNAI 12 BioTwinD-265 (Нидерланды).
Флюоресцентная гибридизация in situ (FISH). Для проведения реакций флюоресцентной in situ гибридизации (FISH-реакции) использовались центромерные пробы СЕР1-2, CEP4, CEP9, CEP11, CЕР17, CEP18, CEP20, конъюгированные с оранжевой флюоресцентной меткой, и центромерные пробы CEP6-8, CEP10, CEP12, CEP15-16, конъюгированные с зеленой флюоресцентной меткой; локусспецифические пробы LSI 13/21 и LSI N25 /LSI ARSA; теломерная проба TelVysion к хромосоме 14q фирмы Abbott Vysis (США) и двухцветная проба VHL/СЕР3 фирмы Zytovision ( ФРГ). Для определения делеции VHL считали число сигналов на 100–150 опухолевых клеток при 1000-кратном увеличении с помощью флюоресцентного микроскопа (Zeiss Axioplan, Германия) и вычисляли соотношение числа сигналов ген/центромера (3р25/СЕР3). Критерием делеции считали коэффициент ≤0,7 по L. Wang и соавт. [6]. Для оценки сигналов остальных проб вычисляли в процентах количество сигналов каждой пробы на 100–150 клеток в нормальной почечной паренхиме и опухолевой ткани каждого образца при увеличении 1000, после чего вычисляли в процентах среднее значение и среднеквадратическое отклонение (δ) каждого типа сигнала в нормальной почечной паренхиме. Пороговое значение каждого типа сигнала соответствовало сумме среднего значения и трехкратного среднеквадратического отклонения по P. Cossu-Rocca и соавт. [7].
Результаты. На светооптическом уровне АМАО отличалась полифазной архитектоникой: эпителиальный компонент, как и в светлоклеточной папиллярной ПКО, был представлен тубулярными и железистыми структурами клеток со светлой цитоплазмой. Экстрацеллюлярный матрикс АМАО характеризовался фасцикулярной пролиферацией гладкомышечных элементов; вокруг толстостенных кровеносных сосудов с набухшими эндотелиоцитами определялась умеренно выраженная муфтообразная перицитарная реакция. Истинные папиллярные формации в АМАО отсутствовали, а ядра опухолевых клеток аналогично светлоклеточной папиллярной ПКО имели реверсивную полярность и были ориентированы к базальной мембране. В обоих гистологических вариантах во всех случаях степень ядерной градации в опухолевых клетках была низкой (рис. 1–3).
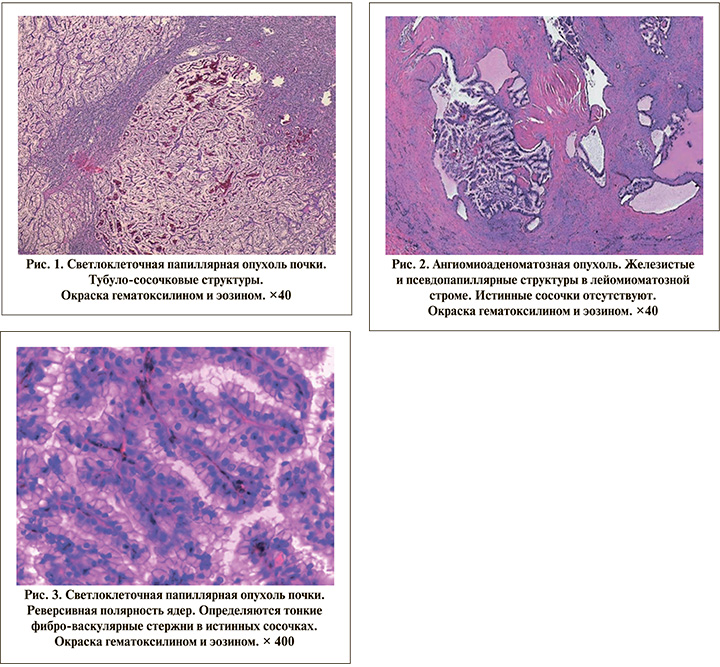
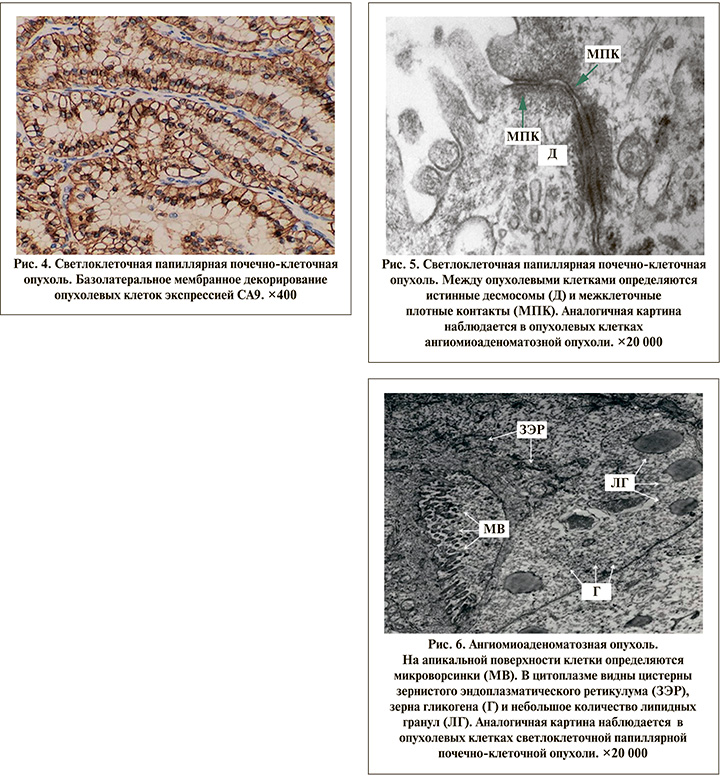
При ИГХ-исследовании АМАО и светлоклеточная папиллярная ПКО демонстрировали аналогичный иммунопрофиль. Так, во всех образцах в опухолевых клетках была выявлена положительная коэкспрессия CA9, HMWCK, AE1/AE3, CK7, ЕМА, E-Cadherin и PAX8. Однако в отличие от АМАО в светлоклеточной папиллярной ПКО при декорировании клеток экспрессией CA9 наблюдалась базолатеральная мембранозная реакция (рис. 4).
При ЭМИ в АМАО и светлоклеточной папиллярной ПКО были обнаружены ультраструктурные признаки проксимальных канальцев нефрона в виде коротких микроворсинок на апикальной и латеральной поверхностях опухолевых клеток, цитоплазматических интердигитаций и межклеточных плотных контактов. Кроме того, в обоих гистологических вариантах в цитоплазме опухолевых клеток в большом количестве обнаруживались зернистый эндоплазматический ретикулум, митохондрии, рибосомы, лизосомы, промежуточные филаменты, гликоген и немногочисленные липидные гранулы (рис. 5, 6).
При FISH-исследовании в обоих гистологических вариантах в объеме использованных проб хромосомные аберрации не идентифицированы.
Обсуждение. Полученные результаты подтверждают, что АМАО и светлоклеточная папиллярная ПКО имеют схожий ультрафенотип и соответствуют электронно-микроскопическим признакам высокодифференцированной светлоклеточной ПКК [8]. Вместе с тем, несмотря на существующие определенные ультраструктурные аналогии между АМАО и светлоклеточной папиллярной ПКО, эти новообразования, по сути, являются разными гистологическими вариантами. Так, было установлено, что обнаруженные во всех образцах светлоклеточной папиллярной ПКО истинные сосочки в АМАО отсутствуют. Более того, в отличие от светлоклеточной папиллярной ПКО эпителиальный компонент АМАО состоит из клеток относительно меньшего размера. Наряду с этим характерной для светлоклеточной папиллярной ПКО прерывистой, «чашеобразной» (базолатеральной) мембранозной экспрессии СА9 в АМАО не наблюдается. Аналогичные данные были получены в исследованиях V. Anik Sahni и соавт. [9]. В результате проведенных исследований и полученных на их основе данных есть все основания предполагать, что АМАО является отдельным представителем семейства ПКК с лейомиоматозной стромой. Наше предположение согласуется с данными R. Williamson и соавт. и E. Kuhn и соавт., которые вследствие комплексного исследования определили, что ПКК с ангиолейомиомоподобной стромой представляют собой гетерогенную группу заболеваний [10–11]. Ввиду этого дифференциальная диагностика и верификация АМАО должны осуществляться методом исключения с учетом полного спектра иммунофенотипических и молекулярно-генетических характеристик опухолей почки с лейомиоматозной стромой.
Заключение. Таким образом, необходимо учитывать, что новообразования почки с лейомиоматозной стромой – группа опухолей, имеющих особенности клинического течения и требующих индивидуального подхода к лечению. В связи с этим морфологическая верификация АМАО имеет большое диагностическое значение в онкоурологической практике, так как из-за крайне низкой частоты встречаемости и гистологической распознаваемости клиническое течение данной опухоли до сих пор остается неясным. Клиническая оценка риска прогрессирования АМАО в послеоперационном периоде расширит представления об истинном биологическом потенциале новообразования и позволит выработать наиболее эффективные методы лечения.



