Хроническая сердечная недостаточность (ХСН) является клиническим синдромом, осложняющим течение наиболее распространенных сердечно-сосудистых заболеваний, ассоциирующимся со снижением работоспособности, частыми госпитализациями и высокой смертностью [1]. Традиционно развитие ХСН связывали с нарушением систолической функции сердца, однако с помощью эхокардиографии у 50% больных и более с типичными симптомами выявляется сохраненная фракция выброса (ФВ) левого желудочка (ЛЖ). В последнем случае клинические проявления ХСН обусловлены повышенной диастолической жесткостью ЛЖ, нарушением его релаксации с тенденцией к повышению давления наполнения вследствие ряда патофизиологических реакций [2, 3]. Заболеваемость ХСН с сохраненной ФВ ЛЖ будет быстро увеличиваться в связи со старением населения, а также распространением ожирения и сахарного диабета [4, 5].
За последние годы удалось существенно снизить смертность и частоту госпитализаций больных с ХСН со сниженной ФВ ЛЖ благодаря широкому применению ингибиторов ангиотензинпревращающего фермента (АПФ), блокаторов рецепторов к ангиотензину II, β-адреноблокаторов, антагонистов минералокортикоидных рецепторов, доказавших свою эффективность в крупных рандомизированных исследованиях [6—8]. Несмотря на аналогичные симптомы и сопоставимый прогноз, у пациентов с ХСН и сохраненной ФВ ЛЖ никакой из применявшихся способов лечения до настоящего времени не обеспечивал снижения смертности [9—14]. Поэтому у таких пациентов в настоящее время рекомендуется только проводить терапию, корригирующую проявления основного и сопутствующих заболеваний [15]. Наличие ограниченной доказательной базы применительно к лечению ХСН с сохраненной ФВ ЛЖ обусловливает необходимость новых клинических исследований фармакотерапии, способной оказаться эффективной у больных данной категории.
Эксперты Европейского общества кардиологов не рекомендуют применять верапамил и дилтиазем у больных с ХСН со сниженной ФВ ЛЖ [15]. Между тем антагонисты кальция в целом не только оказывают антигипертензивный и антиангинальный эффекты, но и способны улучшать релаксацию ЛЖ, которая зависит от функции кальциевых каналов клеточной мембраны и динамики концентрации кальция в кардиомиоцитах. Примечательно, что среди участников исследования ALLHAT с артериальной гипертензией (АГ) и ХСН с ФВ ЛЖ <50% в группах лечения хлорталидоном, лизиноприлом или амлодипином смертность не различалась, но при ФВ ≥50% оказалась существенно ниже в группе амлодипина [16]. Следовательно, амлодипин, который не противопоказан и при систолической дисфункции ЛЖ [15], может иметь перспективы применения при ХСН с сохраненной ФВ ЛЖ. Это важно, так как при ХСН с сохраненной ФВ ЛЖ, с одной стороны, представляется целесообразным продление диастолы путем урежения ритма, однако указывается и на неспособность синусного узла вырабатывать более 100 импульсов в минуту даже при максимальной нагрузке («хронотропная некомпетентность») у части пациентов данной категории [3].
Таким образом, сравнительная оценка эффективности и безопасности патогенетически обоснованных комбинаций доступных антигипертензивных препаратов (АГП) для терапии пациентов с ХСН и сохраненной ФВ ЛЖ на фоне АГ представляется актуальной.
Цель исследования — сравнение эффективности лечения ХСН с сохраненной ФВ ЛЖ у пациентов с гипертонической болезнью верапамилом или амлодипином.
Материал и методы
 В исследовании участвовали 167 больных в возрасте от 48 до 70 лет с ХСН II/III функционального класса по классификации Нью-Йоркской ассоциации сердца и сохраненной ФВ ЛЖ на фоне гипертонической болезни III стадии.
В исследовании участвовали 167 больных в возрасте от 48 до 70 лет с ХСН II/III функционального класса по классификации Нью-Йоркской ассоциации сердца и сохраненной ФВ ЛЖ на фоне гипертонической болезни III стадии.
Критерии включения в исследование: АГ в анамнезе; одышка, утомляемость, сердцебиение при физической нагрузке; ФВ ЛЖ 50% и более [15]; синусовый ритм; 1-й тип диастолической дисфункции ЛЖ (с замедленной релаксацией); подписанное информированное согласие.
Наличие у пациентов диастолической дисфункции ЛЖ констатировали в соответствии с алгоритмом из консенсуса Европейского общества кардиологов [17] и с учетом рекомендаций Европейской ассоциации эхокардиографии и Американского общества эхокардиографии [18].
В исследование не включали больных с гемодинамически значимым поражением клапанов сердца; кардиомиопатиями; перенесенными острыми коронарными синдромами и/или инсультом; синдромом слабости синусного узла; фибрилляцией предсердий; атриовентрикулярной блокадой; вторичной АГ; ожирением (индекс массы тела более 30 кг/м2); заболеваниями органов дыхания с дыхательной недостаточностью; анемией (уровень гемоглобина ниже 130 г/л у мужчин и 120 г/л у женщин); нарушениями функции печени и/или почек; сахарным диабетом, требовавшим инсулинотерапии; непереносимостью применявшихся в исследовании препаратов.
Получено одобрение локального комитета по этике на проведение исследования.
Лечение больных АГ проводили, переводя их на прием периндоприла (престариум А, «Servier», Франция) и титруя дозу от 2,5 до 10 мг 1 раз в сутки, с добавлением к периндоприлу после рандомизации верапамила (изоптин SR, «Abbott», Германия) в дозе 120—240 мг 1 раз в сутки или амлодипина (норваск, «Pfizer», США) в дозе 2,5—10 мг до достижения и поддержания офисного артериального давления (АД) ниже 140 и 90 мм рт.ст. В связи с высоким риском развития сердечно-сосудистых осложнений все пациенты получали рекомендацию принимать аторвастатин (липримар, «Pfizer», США) в дозе 10 мг 1 раз в сутки.
Комплексное обследование больных проводили исходно и через 12 мес подобранной терапии. Кроме общеклинического исследования такое обследование включало электрокардиографию в 12 отведениях; тест с 6-минутной ходьбой; оценку клинического состояния при ХСН (шкала ШОКС в модификации В.Ю. Мареева), оценку качества жизни с использованием Миннесотского опросника (MLHFQ); определение концентрации N-концевого предшественника мозгового натрийуретического пептида (NT-proBNP) в крови (на анализаторе СOBAS H 232), эхокардиографию.
ЭхоКГ в М- и В-режиме, импульсноволновую, в том числе тканевую, допплерографию выполняли по стандартным рекомендациям [18, 19] с использованием ультразвуковой системы Aloka Alpha 7 и векторного датчика с частотой 2,5 МГц. Размеры и объем ЛЖ определяли по методу Simpson. Рассчитывали объем левого предсердия, ФВ ЛЖ в автоматическом режиме с помощью интегрированного программного обеспечения, массу миокарда ЛЖ по формуле R.B. Devereux.
Для оценки диастолической функции ЛЖ использовали максимальные скорости раннего диастолического наполнения (Е) и наполнения в систолу предсердий (А), их соотношение (Е/А), время изоволюмического расслабления ЛЖ (IVRT), время замедления кровотока раннего диастолического наполнения (DТ). Показатели Е, А и DT оценивали из апикального доступа в проекции четырехкамерного сечения с помощью импульсноволновой допплерографии, размещая контрольный объем между концами створок митрального клапана. Максимальную скорость диастолического подъема основания ЛЖ в раннюю диастолу (e’) определяли при помощи импульсноволновой тканевой допплерографии из апикального доступа, устанавливая контрольный объем на митральное кольцо в области межжелудочковой перегородки и боковой стенки ЛЖ. Величину е’ получали путем усреднения скоростей из области межжелудочковой перегородки и боковой стенки ЛЖ. Значения отношения E/е’ усредняли из 3 последовательных сердечных циклов.
В статистическую обработку включали результаты обследования пациентов, постоянно принимавших назначенные АГП (допускалось как применение, так и неприменение аторвастатина), используя пакет прикладных программ Statistica 6.1. Образовавшиеся группы проверяли на нормальность распределения с помощью одностороннего теста Колмогорова—Смирнова. Все данные представлены в виде средней арифметической (М), стандартного отклонения средней арифметической (SD). Достоверность различий показателей по количественным признакам определяли по критерию t Стьюдента, по качественным — с использованием критерия χ2, признавая их статистически значимыми при р<0,05.
Результаты
Характеристики пациентов, включенных в исследование и рандомизированных в группы запланированных способов терапии, представлены в табл. 1. Обследованные образовавшиеся 2 группы оказались хорошо сбалансированными по ряду показателей.
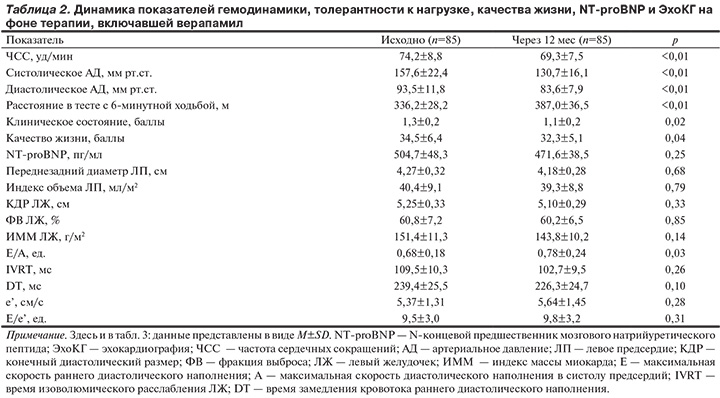
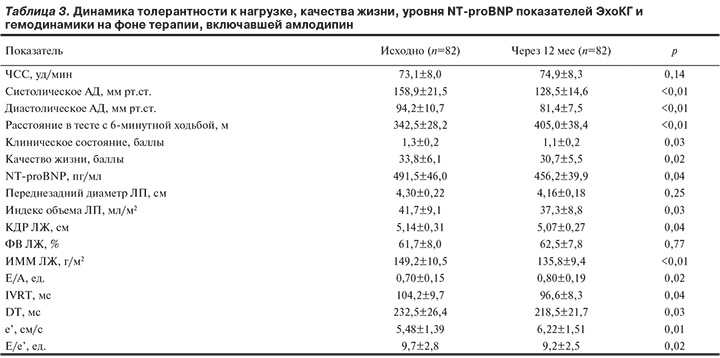
Изменения показателей гемодинамики, нагрузочных тестов, биохимического исследования крови, качества жизни и данные ЭхоКГ в процессе длительной терапии, включавшей верапамил или амлодипин, представлены в табл. 2 и 3.
Заключение о наличии у включенных в исследование диастолической дисфункции ЛЖ I типа (с замедленной релаксацией) подтверждалось величиной отношения E/A менее 0,8 (с учетом возраста), IVRT более 100 мс и DT более 200 мс. Отношение Е/е’ не превышало 15, что позволяло предполагать отсутствие значительного повышения конечного диастолического давления в ЛЖ в покое, характерного для более тяжелого II типа (псевдонормального) диастолической дисфункции ЛЖ.
В обеих группах у всех обследованных доза периндоприла составляла 10 мг/сут. Для достижения и поддержания целевого уровня АД в 76,5% случаев применяли верапамил в дозе 240 мг/сут, а амлодипин — в дозе 5 или 10 мг/сут (46,3 и 43,9% случаев соответственно). При этом отмечалась ожидаемая разнонаправленная динамика средней частоты сердечных сокращений в сопоставлявшихся группах. Среднее расстояние, пройденное в тесте с 6-минутной ходьбой, существенно увеличивалось при лечении, включавшем как верапамил (на 15,1%), так и амлодипин (на 18,2%). Оба препарата обеспечивали улучшение клинического состояния и качества жизни. Уровень NT-proBNP существенно снижался только в группе амлодипина, что соответствовало его антиремоделирующему эффекту (уменьшение индекса объема левого предсердия, конечного диастолического размера и гипертрофии ЛЖ). Отношение E/A существенно повышалось в обеих группах, но другие, более специфичные показатели диастолической функции ЛЖ (e', Е/e', DT) улучшались только при длительном лечении амлодипином.
Обсуждение
Одной из главных задач лечения больных с ХСН и сохраненной ФВ ЛЖ признается коррекция АГ, характерной для большинства таких пациентов, с регрессией гипертрофии ЛЖ для улучшения его диастолической функции [20—22], что наиболее успешно достигается с помощью блокаторов рецепторов к ангиотензину II (сартанов) [23]. Однако в двух исследованиях сартанов, в которых для сравнения влияния антигипертензивной терапии на диастолическую функцию ЛЖ применялась тканевая допплерография, получены противоречивые результаты [24, 25]. В первом из них через 48 нед лечения ирбесартан, в отличие от атенолола, улучшал ключевой показатель E/е' у больных с гипертрофией ЛЖ и без нее [24]. Напротив, во втором исследовании валсартан оказался не лучше стандартной терапии АГ во влиянии на диастолическую функцию ЛЖ через 38 нед терапии [25].
По данным мета-анализа 16 рандомизированных исследований (n=54 621), ингибиторы АПФ снижают смертность и частоту госпитализаций больных с ХСН, но этот эффект ослабевает с увеличением ФВ ЛЖ [6]. Выбор оригинального препарата периндоприла (престариум А) для нашего исследования, во-первых, был обусловлен способностью только этого ингибитора АПФ улучшать прогноз у больных АГ, в том числе снижать их смертность [26]. Во-вторых, в проекте PEP-CHF, являющемся наиболее крупным в настоящее время исследованием ингибитора АПФ при ХСН с сохраненной ФВ ЛЖ, также применялся периндоприл [10]. В этом двойном слепом многоцентровом плацебо-контролируемом рандомизированном исследовании участвовали 850 пациентов в возрасте ≥70 лет с ХСН и сохраненной ФВ ЛЖ, госпитализировавшихся в течение последних 6 мес по причине сердечно-сосудистого заболевания. В течение первого года наблюдения события, включенные в комбинированную первичную конечную точку (смерть от любой причины и госпитализация из-за сердечной недостаточности), регистрировались у 15,3% пациентов, получавших плацебо, и 10,8% пациентов, получавших периндоприл (относительный риск — ОР 0,69 при 95% доверительном интервале — ДИ от 0,47 до 1,01; р=0,055), а только госпитализация из-за сердечной недостаточности — у 12,4 и 8% пациентов соответственно (ОР 0,63 при 95% ДИ от 0,41 до 0,97; р=0,033). Однако отмечавшиеся различия утрачивались к концу исследования на фоне быстрого выбывания пациентов из наблюдения с минимизацией статистической мощности проекта. В группе периндоприла через год также значительно снижался средний функциональный класс ХСН и увеличивалось расстояние в тесте с 6-минутной ходьбой по сравнению с таковыми в группе плацебо. В отличие от PEP-CHF в небольшом исследовании другого ингибитора АПФ квинаприла у 74 пожилых пациентов с ХСН и сохраненной ФВ ЛЖ не удалось продемонстрировать повышения толерантности к физической нагрузке, качества жизни, предупреждение ухудшения течения ХСН и уменьшение числа госпитализаций [27].
В нашей работе все пациенты получали периндоприл в дозе, в 2 раза большей, чем в проекте PEP-CHF, что способствовало достижению более выраженного антигипертензивного и плейотропных эффектов препарата.
Приносит ли дополнительную пользу подобным пациентам прием антагонистов кальция? Анализ когорты пожилых больных с ХСН и сохраненной ФВ ЛЖ из проекта OPTIMIZE-HF (по 810 пар больных, исходно сбалансированных по 114 показателям) показал, что частота смертельных исходов и госпитализаций по поводу ХСН у получавших или не получавших антагонисты кальция существенно не различалась (ОР 1,03 при 95% ДИ от 0,92 до 1,14) [28]. В то же время при наблюдении за 438 больными ХСН с сохраненной ФВ ЛЖ до 12 лет выявлялось снижение смертности и риска развития тяжелых сердечно-сосудистых осложнений при лечении ингибиторами АПФ и антагонистами кальция [29]. В настоящее время проводится рандомизированное исследование нифедипина замедленного высвобождения у больных с ХСН и сохраненной ФВ ЛЖ на фоне АГ и/или ишемической болезни сердца DEMAND (NCT01157481), в котором запланирована оценка клинических исходов на протяжении 4—5 лет [30].
B.P. Dhakal и соавт. [31] установили, что в сравнении с обследованными, страдавшими ХСН со сниженной ФВ ЛЖ, при ХСН с сохраненной ФВ ЛЖ преобладающим фактором, ограничивающим толерантность к физической нагрузке, являлось снижение извлечения кислорода из крови на периферии. По мнению авторов исследования, выявленное ими нарушение может отражать внутренние изменения в скелетных мышцах или функции микрососудов, представляет собой потенциальную мишень для терапевтического вмешательства. Учитывая эти данные, можно предполагать преимущество амлодипина перед верапамилом при лечении больных с ХСН и сохраненной ФВ ЛЖ, так как первый реализует свое клиническое действие путем дилатации артерий и артериол.
В субисследовании проекта ASCOT с помощью тканевой допплерографии сопоставляли влияние антигипертензивной терапии, основанной на приеме амлодипина (n=413) или атенолола (n=411), на диастолическую функцию ЛЖ. Через 12 мес лечения в группе амлодипина регистрировались существенно лучшие эхокардиографические показатели диастолической функции ЛЖ (выше е', ниже отношение Е/е', меньше диаметр левого предсердия, короче DT), более низкий уровень мозгового натрийуретического пептида в плазме. Эти эффекты не зависели от других факторов, ассоциирующихся с диастолической функцией ЛЖ, включая влияние препарата на уровень АД и индекс массы миокарда ЛЖ [32].
Важно подчеркнуть наличие прямой связи между величиной отношения E/e', даже в пределах нормального или субнормального диапазона, и риска развития кардиальных осложнений у пациентов с АГ [33]. В нашей работе данный показатель уменьшался в группе лечения амлодипином, но не верапамилом.
Верапамил изучался у больных с ХСН и сохраненной ФВ ЛЖ в то время, когда тканевая допплерография, признаваемая необходимой для точной оценки диастолической функции ЛЖ [17, 18], еще не применялась. В исследовании у 20 мужчин 5-недельная терапия верапамилом повышала толерантность к физической нагрузке на 33% на фоне улучшения диастолического заполнения ЛЖ [34]. В другом исследовании у 15 пожилых пациентов с ХСН II/III функциональных классов верапамил в дозе 120 мг/сут существенно увеличивал время ходьбы на тредмиле на фоне укорочения IVRT, что отражало улучшение релаксации ЛЖ [35].
В новых рекомендациях Европейского общества кардиологов [15] верапамил противопоказан, а амлодипин может применяться при ХСН с систолической дисфункцией ЛЖ с учетом результатов исследования PRAISE [36]. Всегда ли практикующий врач контролирует и вовремя выявляет переход пациента с ХСН от фазы болезни с сохраненной ФВ ЛЖ к фазе со сниженной ФВ ЛЖ? Имеется ли единая точка зрения экспертов по вопросу о границе между нормальной и сниженной ФВ ЛЖ? Ответ на первый вопрос скорее отрицательный. Второй вопрос до последнего времени также не имел однозначного ответа, в научных публикациях упоминались две различные «точки отсечения» (50% и 55%), а диапазон ФВ ЛЖ 40—50% именовали «серой зоной». Эксперты Европейского общества кардиологов предложили называть величину ФВ ЛЖ 40—49% «средней», а ≥50% «сохраненной» [15].
Хронотропная некомпетентность (неспособность синусного узла вырабатывать более 100 импульсов в минуту даже при максимальной нагрузке) закономерно чаще встречается с возрастом. Такое нарушение нередко выявляется у больных с ХСН и сохраненной ФВ ЛЖ [3], продлевает диастазис (период слабого кровотока через митральное отверстие из-за выравнивания давления в ЛЖ и левом предсердии перед систолой левого предсердия) и тем самым может способствовать усилению одышки при физической нагрузке. Учитывая противоположный хроноторпный эффект верапамила и амлодипина, только последний может безопасно применяться в такой ситуации.
Необходимо отметить, что все пациенты в качестве фонового лечения принимали периндоприл (престариум А, оригинальный препарат, «Servier», Франция), поэтому полученные результаты обеспечивались комбинированной терапией. Тем не менее выявленные различия можно объяснить особенностями действия верапамила и амлодипина.
Заключение
При лечении больных с хронической сердечной недостаточностью и сохраненной фракцией выброса левого желудочка у пациентов с гипертонической болезнью амлодипин, по меньшей мере, не уступает верапамилу в способности повышать толерантность к нагрузке и превосходит его в улучшении диастолической функции левого желудочка, может оказаться перспективным при наличии «хронотропной некомпетентности».



