Сердечно-сосудистые заболевания (ССЗ) представляют собой глобальные медицинские и экономические проблемы. По данным Всемирной организации здравоохранения, ССЗ, обусловленные нарушением кровообращения тканей и органов вследствие стенозирующего поражения сосудов, такие как ишемическая болезнь сердца, ишемический инсульт и ишемические заболевания нижних конечностей, в том числе обусловленные диабетической ангиопатией, являются ведущей причиной инвалидности и смертности населения трудоспособного возраста во всем мире. Например, по данным на 2008 г., в США на ССЗ приходится 32,8% ежегодных смертей [1].
Лечение ССЗ направлено на восстановление кровотока в ишемизированной ткани, при этом выбор методов лечения обусловлен тяжестью и локализацией нарушения кровоснабжения [2, 3]. Несмотря на развитие эффективных методов сосудистой хирургии, некоторые из них применимы только у отдельных больных, а существующие консервативные методы лечения зачастую оказываются неэффективными у тяжелых больных [2, 4, 5]. Одной из альтернатив в таких случаях является терапия ангиогенными факторами роста (АФР), направленная на стимуляцию роста новых сосудов в зоне ишемии, которая позволяет (иногда в сочетании с хирургическими методами) улучшить кровоснабжение, остановить дегенеративные процессы, стимулировать регенерацию и восстановить структуру и функцию поврежденного органа или ткани [6]. Эта стратегия была названа терапевтическим ангиогенезом и является одной из технологий регенеративной медицины, активно развивающейся за рубежом и в России [5, 7, 8]. В основе терапевтического ангиогенеза лежит стимуляция роста и ремоделирования сосудов в ишемизированных тканях с помощью введения рекомбинантных АФР или генетических конструкций для их экспрессии.
Ангиогенез и связанные с ним факторы роста как терапевтические мишени. Рост и образование сосудов в постнатальном периоде осуществляется за счет трех процессов: ангиогенеза, артериогенеза и васкулогенеза. Под термином «ангиогенез» понимают процесс формирования новых кровеносных сосудов из существующих за счет пролиферации и миграции эндотелиальных клеток [9—12].
Основным стимулирующим фактором ангиогенеза является недостаток кислорода (гипоксия или ишемия) [13]. Система рецепции парциального напряжения кислорода включает факторы транскрипции из группы факторов, индуцируемых гипоксией (PHD-2, индуцируемые гипоксией факторы — HIF-1α, HIF-2α), которые стимулируют транскрипцию целого ряда АФР и других проангиогенных молекул [14].
При гипоксии наблюдается активация эндотелия, сопровождающаяся экспрессией протеаз, способных разрушать белки внеклеточного матрикса с последующей пролиферацией и миграцией клеток [15] и образованием незрелой сосудистой сети [16]. Вновь сформированные структуры удлиняются, ветвятся и формируют анастомозы, что приводит к возникновению капиллярной сети [17, 18]. В дальнейшем сформированные сосуды могут подвергаться ремоделированию, сопровождающемуся таксисом гладких мышечных клеток (ГМК) и перицитов с формированием сосудов разного калибра [19].
Помимо ангиогенеза несомненный вклад в восстановление кровоснабжения вносит артериогенез, который запускается преимущественно увеличением напряжения сдвига при острой окклюзии или критическом стенозе просвета магистрального сосуда [17, 18]. При увеличении напряжения сдвига происходит ремоделирование небольших шунтирующих артериол, которые приобретают выраженную артериальную морфологию. Причем показана важная роль пульсовидных колебаний давления для образования полноценного гладкомышечного слоя стенки сосуда [20].
В процессах ремоделирования ключевую роль играют матриксные металлопротеиназы (ММП) различных типов, а также урокиназный активатор плазминогена (uPA) [21]. Последний помимо протеолитического разрушения базальной мембраны сосудов активирует различные факторы роста (фактор роста эндотелия сосудов — VEGF, фактор роста гепатоцитов — HGF и др.), которые являются митогенами для эндотелиоцитов, ГМК и перицитов [19, 21].
За счет сопровождающей артериогенез пролиферации ГМК и гипертрофии толщина медии увеличивается иногда в несколько раз [22], а объем всей коллатерали может увеличиваться от 2 до 20 раз [23].
Рост и состояние сосудов контролируются целым спектром молекул, что необходимо учитывать при использовании факторов роста для терапевтических целей [16]. Помимо прямых инициирующих стимулов (гипоксии, роста напряжения сдвига) существуют большие группы позитивных (стимулирующих) и негативных (стабилизирующих) регуляторов ангиогенеза. В постнатальном периоде стабильное состояние сосудов поддерживается балансом между активаторами ангиогенеза (факторами роста и цитокинами) и его ингибиторами (тромбоспондином, ингибиторами ММП и активаторов плазминогена, эндостатином и др.) [16, 24]. Сдвиг этого баланса в сторону активаторов, даже кратковременный, приводит к запуску ангиогенеза. Среди белков, способных запускать и поддерживать процессы роста сосудов, особого внимания заслуживают АФР, которые были предложены в качестве терапевтических мишеней еще Дж. Фолькманом [25, 26].
Изначально их предполагалось использовать для стимуляции роста сосудов при ишемии или блокировать их эффекты для борьбы с опухолевым неоангиогенезом при лечении сóлидных опухолей. Последнее направление в настоящее время также переживает бурный рост, особенно после успеха бевацизумаба (препарата моноклональных антител к VEGF165) в целом ряде клинических исследований.
Первым выделенным и охарактеризованным АФР был VEGF — основной регулятор ангиогенеза как в эмбриональном, так и в постнатальном периодах развития. В скором времени было описано семейство его рецепторов — VEGFR, которые оказались гетерогенны по функциональным свойст-вам и экспрессии в различных типах клеток и тканей [27, 28]. VEGF стимулирует пролиферацию, миграцию эндотелиальных клеток и их предшественников, а также моноцитов, экспрессирующих VEGFR. VEGF увеличивает выживаемость эндотелия при гипоксии и сосудистую проницаемость, способствуя выпотеванию белков плазмы в окружающие ткани. Выпотевание белков плазмы считается способом формирования «временного матрикса» для миграции эндотелиальных клеток [29]. VEGF также индуцирует продукцию NO [13], что способствует вазодилатации и стимулирует экспрессию протеаз, разрушающих связи между эндотелиальными клетками и внеклеточным матриксом, облегчая процессы миграции [30, 31]. Следует отметить, что повышение проницаемости сосудов под воздействием VEGF считается причиной побочных эффектов: отеков и нарушений трофики, наблюдавшихся в ряде исследований в клинике.
В семейство VEGF входит 5 изоформ, однако для терапевтического ангиогенеза наибольшее распространение получила изоформа VEGF165, которой посвящено большинство клинических и экспериментальных исследований.
Еще одним АФР, хорошо зарекомендовавшим себя в исследованиях, стал HGF. Изначально он был обнаружен как белок, характеризующийся способностью поддерживать в жизнеспособном состоянии культуру первичных гепатоцитов крысы. Более поздние исследования показали, что HGF оказывает выраженные митогенный, антиапоптотический и антифибротический эффекты за счет связывания со своим рецептором с-met, который экспрессируется на ГМК, эндотелиальных, гемопоэтических стволовых клетках и фибробластах миокарда и печени [32]. Последнее свойство также вызвало широкий интерес к этому фактору в плане профилактики постинфарктного кардиосклероза, а также фиброза в исходе токсических и первичных поражений печени. Важным свойством HGF является его способность вызывать не только формирование новых капилляров, но и стимулировать таксис ГМК, за счет чего уменьшается выраженность отека, который зачастую сопровождает VEGF-индуцированный ангиогенез [33].
Значительное внимание как терапевтический белок привлекает также основной фактор роста фибробластов (bFGF), который обладает свойством эффективно стимулировать как ангиогенез, так и артериогенез. В основе этих свойств bFGF лежит то, что рецепторы FGF экспрессируются как на эндотелии, так и на ГМК, что потенциально должно обеспечивать формирование зрелой сети кровеносных сосудов за счет активации обоих типов клеток [10, 32].
Перечислены лишь некоторые АФР из большого спектра потенциальных агентов для терапевтического применения, так как по ним имеются репрезентативные данные клинических исследований и накоплен наибольший экспериментальный материал. К перспективным факторам терапевтического ангиогенеза относят и ряд других ключевых регуляторов ангиогенных процессов, например ангиопоэтин-1, уменьшающий проницаемость сосудистой стенки, способствующий привлечению перицитов и стабилизации сосудов. Кроме того, опубликованы работы по эффективности применения (на животных моделях и в пилотных клинических исследованиях) тромбоцитарного фактора роста ВВ (PDGF-BB_ [34], uPA [35] и др.
Терапевтический ангиогенез с помощью АФР: рекомбинантные белки и генная терапия. Введение рекомбинантных АФР. Первые попытки восстановления перфузии тканей проводились на животных моделях ишемии нижней конечности и инфаркта миокарда (ИМ) [26, 36], на начальном этапе в них использовалось прямое введение рекомбинантных белков. Несмотря на эффективность данной методики в опытах на животных, при использовании этих подходов в клинике выяснилось, что для поддержания постоянной концентрации терапевтического агента в зоне ишемии необходимы огромные количества белка, имеющего высокую стоимость и короткое время жизни в ткани [37].
Затруднения вызвали также способы доставки таких количеств белка и наблюдавшаяся при системном введении диссеминация факторов роста.
Использование биоматериалов для доставки рекомбинантных АФР. Для повышения эффективности терапии рекомбинантными белками в настоящее время предлагается использовать полимерные биоматериалы, которые функционируют как депо факторов и обеспечивают их постепенное высвобождение. В идеальных условиях такие системы должны поддерживать локальное содержание АФР в пределах физиологической нормы в течение нескольких дней или недель, что служило бы решением проблемы короткого времени жизни рекомбинантных белков и их быстрой диссеминации. Полимерные биоматериалы, используемые для терапевтического ангиогенеза, обеспечивают регулируемое высвобождение терапевтических факторов по мере деградации за счет активности ММП и других протеаз [37].
Чаще всего для терапевтического ангиогенеза используются синтетические сополимеры на основе молочной и гликолевой кислот (PLGA), полиэтиленгликоль (PEG), а также природные полимеры: альгинат или желатин. PLGA был одним из первых полимеров, который использовался для депонирования и регулируемого высвобождения VEGF [38–40].
Использование PLGA является предпочтительным из-за способности этого полимера к деградации в биологических системах и контролируемому высвобождению лекарства; однако при деградации PLGA повышается кислотность, что потенциально может вызывать воспаление. PEG — биосовместимый полимер, который является инертным по своей природе, но легко может быть подвержен биохимическим и механическим модификациям [41]. PEG активно используется для создания гидрогелей, депонирующих VEGF, высвобождение которого регулируется за счет активности окружающих клеток [42]. Альгинат и желатин представляют собой натуральные полимеры, с которыми взаимодействуют клетки в условиях in vivo, однако их сложно стандартизовать и для них характерна вариабельность состава. Кроме того, они менее доступны химической модификации по сравнению с синтетическими полимерами.
Критической характеристикой такой системы является скорость высвобождения АФР из биополимера, в котором они депонированы. Для большинства систем доставки характерно «взрывное высвобождение», когда значительное количество АФР высвобождается в первые часы. Механизмы, лежащие в основе этого феномена, не выяснены. Считается, что критическую роль в регуляции высвобождения лекарства из матрицы играют условия обработки, поверхностные характеристики и геометрия биополимеров [43]. Было разработано несколько методов для подавления «взрывного высвобождения», включающих изменения физических, биохимических взаимодействий и использование ковалентного связывания между молекулами биопрепарата и полимерным биоматериалом [37].
Известно, что соотношение размеров терапевтического белка и поры в структуре биополимера регулирует скорость высвобождение белка из матрицы-носителя. На моделях ИМ и ишемии задней конечности показано, что в опытах с использованием PLGA регулируемое таким образом высвобождение VEGF стимулирует ангиогенез достоверно лучше, чем введение свободного белка [39, 40, 44]. Эти данные свидетельствуют о преимуществах пролонгированного высвобождения АФР.
Включенные в состав полимера АФР могут образовывать водородные связи или участвовать в ионных взаимодействиях с макромолекулами, такими как гепарансульфат.
Это свойство может быть использовано для снижения скорости высвобождения белка за счет включения гепарина, гепарансульфата или гиалуроновой кислоты в состав полимерных биоматериалов [45—47]. Этот подход был использован при введении рекомбинантного bFGF в сочетании с гепарин-содержащими хитозановыми гидрогелями, что привело к значительному усилению ангиогенного ответа на моделях in vivo и in vitro [46, 48].
Наконец, некоторые биологические препараты могут быть ковалентно сшиты с полимерным остовом [42, 49]. Так, было показано, что VEGF, ковалентно связанный через деградируемый ММР линкерный участок с матрицей, стимулирует формирование более стабильной и функциональной сосудистой сети, чем свободный VEGF [50]. Тем не менее ковалентная связь приводит к химической модификации биологических молекул, что может влиять на их биологическую активность, поэтому выбор линкера требует тщательной разработки, чтобы предотвратить нежелательные иммунные реакции [41].
Поскольку ангиогенез представляет собой динамический многоступенчатый процесс, предпринимались попытки использовать сочетание факторов роста в составе биодеградирумых гелей с целью повышения эффективности.
Так, совместная доставка VEGF и PDGF с использованием PLGA или альгинат-гидрогеля приводит к формированию более крупных и зрелых сосудов и увеличивает кровоток [51, 52]. Биодеградируемые гидрогели на основе гиалуроновой кислоты также нашли применение при осуществлении доставки VEGF и фактора роста кератиноцитов [53]. Гидрогель на основе желатина был использован как депо для bFGF и гранулоцитарного колониестимулирующего фактора (Г-КСФ) при совместной доставке этих факторов [54].
В работе J. Saif и соавт было показано, что при введении трех рекомбинантных АФР (VEGF, HGF и ангиопоэтина-1) в состав биополимера на основе PLGA эффективность терапии эндотелиальными клетками-предшественниками существенно повышалась, что приводило к значительному восстановления перфузии ишемизированной скелетной мышцы [55]. Был также разработан гидрогель на основе декстрана, который использован для депонирования сразу 4 АФР (VEGF, SDF-1, IGF, Ang-1). Было обнаружено значительное увеличение числа и размеров сосудов при сочетанном введении этих четырех факторов роста на модели подкожной имплантации Матригеля in vivo у мышей по сравнению с доставкой одного или двух факторов роста [52].
Применение рекомбинантных АФР для терапевтического ангиогенеза в настоящее время распространено мало, т.к. при введении свободных или упакованных рекомбинантных белков, как уже упоминалось, довольно высока вероятность их системной диссеминации и, как следствие, нежелательной стимуляции ангиогенеза в органах, отдаленных от места введения (сетчатке глаза, латентных опухолях). В настоящий момент еще не накоплено достаточного количества исследований с проспективной частью наблюдений, которые позволили бы сделать вывод о безопасности таких способов доставки.
Генная терапия с использованием АФР для терапевтического ангиогенеза. На фоне препятствий, возникавших на пути методов, связанных с введением рекомбинантных АФР, активное развитие получила генная терапия, использующая экспрессионные векторы для продукции в ишемизированной ткани белка, стимулирующего рост сосудов. Достаточно быстро в этой области были достигнуты первые успехи, касающиеся лечения критической ишемии нижних конечностей (КИНК) [56]. За результатами, полученными на животных моделях, последовали пилотные исследования, показавшие хорошую переносимость генной терапии для лечения ишемической болезни сердца (ИБС) [57, 58]. Все это позволило в начале 2000-х гг. XXI века приступить к испытаниям II—III фазы [59] и в настоящий момент приблизиться к появлению генно-терапевтических препаратов на фармацевтическом рынке [60]. При этом следует отметить, что многие авторы сходятся во мнении, что в существующем виде использование «моногенной терапии» имеет ограниченные возможности применения при ишемических заболеваниях. Остановимся более подробно на данных клинических исследований в этой области.
Клинические исследования эффективности генной терапии VEGF. Начало практическому использованию ангиогенных свойств VEGF было положено в 1996 г., когда J.M. Isner опубликовал первую работу по успешному применению плазмиды с геном VEGF человека для лечения КИНК. В дальнейших работах было установлено, что внутримышечное введение векторов с геном VEGF эффективно и хорошо переносится больными за исключением случаев развития отеков конечности, связанных со свойством VEGF повышать проницаемость сосудистой стенки [56].
В клиническом исследовании I. Baumgartner и соавт. [61, 62] использовалось внутримышечное введение плазмиды с геном VEGF человека больным КИНК с болями в покое и незаживающими трофическими язвами, а эффективность плазмиды оценивалась по данным ангиографии. На ангиограммах, выполненных через 8 нед после введения конструкции, были зафиксированы формирование коллатералей и признаки кровотока по ним. При дополнительно проведенном гистологическом исследовании ампутационного материала от 1 больного были обнаружены фокусы пролиферации эндотелиальных клеток и увеличение плотности капилляров, что указывало на успешную стимуляцию ангиогенеза при введении плазмиды с VEGF.
Первая работа по изучению эффективности плазмиды с геном VEGF для терапевтического ангиогенеза в ишемизированном миокарде представляла собой открытое клиническое исследование, в котором плазмиду вводили субэпикардиально после выполнения микроторакотомии больным стенокардией с нестабильным течением (n=5). В этом исследовании были показаны возможность и безопасность введения плазмид прямым способом [63], однако при оценке конечных точек не было выявлено клинически значимого улучшения течения заболевания. В дальнейшем M. Laitinen и соавт. предложили менее инвазивный вариант внутрикоронарного введения плазмиды с геном VEGF в составе липосомных комплексов. Однако при оценке коронарного кровотока и перфузии миокарда ни в одной из групп не было обнаружено признаков уменьшения стеноза или улучшения кровоснабжения миокарда [64].
Следующим важным шагом стало клиническое исследование II фазы Kuopio Angiogenesis Trial. В его задачи входило сравнение внутрикоронарного введения плазмиды и аденовируса с геном VEGF (АВ-VEGF) при чрескожной ангиопластике со стентированием, а также изучение влияния такой терапии на динамику развития рестеноза и перфузию миокарда. Больные (n=103) с симптомами ИБС и наличием показаний к проведению чрескожной реваскуляризации были разделены на группы внутрикоронарного введения АВ-VEGF165, плазмиды c VEGF в составе липосом или плацебо. Внутрикоронарное введение оказалось безопасным способом доставки препарата, однако авторы не смогли обнаружить статистически значимых различий групп по предусмотренным в исследовании первичным точкам. Генная терапия VEGF не смогла замедлить рестеноз стентированных артерий, однако к концу 6-го месяца наблюдения перфузия миокарда, по данным однофотонной эмиссионной компьютерной томографии (ОФЭКТ), в группе аденовируса была выше, чем в группе пациентов, которым вводили липосомы с плазмидой [65].
В рандомизированном исследовании с двойным слепым контролем (EuroInject One) оценивали эффективность введения плазмидной ДНК с геном VEGF для лечения больных ИБС, которым невозможно провести хирургическую реваскуляризацию. Больных (n=80) разделили на 2 группы, пациентам первой в миокард вводили плазмиду с геном VEGF, второй — плацебо. При этом зона введения с помощью системы NOGA ограничивалась ишемизированной областью миокарда, которую определяли при помощи ОФЭКТ и электромеханического картирования миокарда. Через 3 мес в группе VEGF было отмечено увеличение регионарной сократимости миокарда, а также улучшение функции левого желудочка. После окончания исследования был выполнен дополнительный анализ с применением альтернативных методов оценки данных электромеханического картирования и ОФЭКТ, который показал умеренное улучшение перфузии миокарда в области введения плазмиды с VEGF [66, 67], хотя функциональный класс стенокардии у больных оставался без изменений.
Таким образом, в двух самых крупных исследованиях с использованием гена VEGF было выявлено улучшение показателей в группе терапии по сравнению с контролем.
В поисках способов повышения эффективности генной терапии R.S. Ripa и соавт. провели исследование, в котором для лечения больных ИБС использовали комбинацию генной терапии VEGF с курсом введения Г-КСФ [68], роль которого заключалась в мобилизации клеток костного мозга, обладающих регенеративным потенциалом. Всего для проведения сочетанного лечения были набраны 16 больных рефрактерной ИБС, которым невозможно было провести хирургическую реваскуляризацию миокарда ввиду тяжести поражения коронарного русла. Ретроспективный контроль составили 16 больных, которым вводили плазмиду с геном VEGF, и 16 больных, получавших инъекции контрольной плазмиды. После курса Г-КСФ число циркулирующих клеток CD34(+) статистически значимо увеличивалось в группе лечения, однако в конечной точке стрессовая перфузия миокарда не отличалась от таковой в группе, в которой после введения плазмиды с VEGF проводился курс Г-КСФ. Авторы предположили, что отсутствие эффекта связано с неадекватным хоумингом мобилизованных стволовых клеток в инфарктную зону; при этом есть данные, что хоуминг может быть усилен за счет локального введения в ткани плазмиды с геном стромального фактора-1α (SDF-1α — stromal cell-derived factor-1α) — мощного аттрактанта прогениторных клеток.
Не следует исключать и другие возможные причины неудовлетворительных результатов в исследованиях, например метод ОФЭКТ может иметь недостаточную чувствительность для регистрации изменений, возникающих при локальной генной терапии, а при проведении курса Г-КСФ через неделю после введения плазмиды пик его концентрации мог не совпасть с пиком секреции VEGF, что также сказалось на синергичности их воздействия.
В настоящее время в литературе еще недостаточно данных о долгосрочном прогнозе у больных, которые были включены в клинические исследования. Частично ответ на вопрос об отдаленных эффектах генной терапии дает работа, опубликованная в 2012 г., в которой описаны результаты 10-летней проспективной части клинического исследования. В ней проводилась оценка состояния больных, которым по поводу КИНК проводили генную терапию VEGF с использованием аденовирусов или плазмидных конструкций. В обеих группах за 10 лет наблюдения не было отмечено роста смертности, а также не было выявлено существенных различий по частоте развития опухолей, сахарного диабета и ретинопатии диабетического генеза [69]. Эти данные позволяют с оптимизмом смотреть на перспективы применения VEGF в терапевтическом ангиогенезе с позиций отсроченной безопасности, которая долгое время была под вопросом.
Клинические исследования эффективности генной терапии HGF.
Доклинические и пилотные клинические испытания плазмид с геном HGF проводились группой R. Morishita. Полученные в них данные по эффективности этого метода стали основой для исследования II фазы под названием STAT.
В данной работе больных КИНК (n=104) распределили в группe плацебо и группу введения плазмиды с HGF в низкой или высокой дозе [70, 71]. Оценка эффективности ангиогенной терапии проводилась по данным чрескожного измерения парциального напряжения кислорода (TcPO2), которая показала, что положительная динамика была достигнута в группе с высокой дозой pHGF, чего не отмечалось в контроле и в группе низкой дозы. Полученные данные внушали оптимизм, однако некоторые специалисты указывали на ряд недостатков этой работы. В частности, указывали на то, что у больных с выраженным атеросклерозом периферических артерий использование TcPO2, лодыжечно-запястного индекса, а также ультразвукового допплеровского исследования пригодно для популяционных исследований, но в оценке ответа на лечение они значительно уступают ангиографическим методам визуализации сосудистого русла.
Перед началом исследования III фазы было проведено еще одно плацебо-контролируемое двойное слепое исследование, в котором из 121 кандидата были отобраны 46 больных КИНК, не имевших по данным скрининга подозрений на онкологическую патологию, диабетическую ретинопатиюи иные тяжелые осложнения [72]. В соотношении 2:1 больные были рандомизированы в группы phHGF (n=30) и плацебо (n=16). Введение плазмиды, зарегистрированной в Японии под названием Collategene, или контрольного вещества выполнялось в нулевой точке исследования и повторялось в конце 4-й недели, причем зоны для внутримышечного введения выбирали с учетом данных ангиографии, а сами инъекции выполняли под ультразвуковым контролем. Анализ первичных точек (степень тяжести ишемии по Резерфорду, средняя площадь и заживление одного и более язвенных дефектов) показал эффективность Collategene у больных с тяжелыми формами поражения периферических артерий.
По истечении 12-й недели среди больных ишемией IV и V степени, получавших Collategene, в 70,4% случаев было отмечено улучшение, в контроле аналогичный показатель составил 30,8%. У пациентов с наиболее тяжелым течением (V степень) улучшение было достигнуто в 100% случаев против 40% в контроле. В этой же подгруппе у больных, получавших Collategen, отмечалось уменьшение на 70% средней площади язвенных дефектов, в то время как в группе плацебо положительной динамики не было ни у одного из пациентов.
К 12-й неделе среди больных ишемией V степени, получавших Collategene, полное заживление 1 язвы и более было зафиксировано в 36,4% случаев, что превышало показатели группы плацебо, в которой только у 20% больных отмечено заживление хотя бы одного язвенного дефекта. Прочие показатели — лодыжечно-плечевой индекс, частота ампутаций и выраженность болей покоя между группами не различались.
Оценка безопасности показала хорошую переносимость Collategene. Всего было зафиксировано 39 случаев нежелательных эффектов (27 в группе HGF и 12 в контроле), среди которых на долю выраженных побочных эффектов выпало 9 (6 в группе HGF и 3 в контроле). Ни у одного из больных не было отмечено антител против HGF или двухцепочечной ДНК, а также не выявлено повышения содержания самого HGF по сравнению с исходным уровнем, что свидетельствует об отсутствии выраженной диссеминации белка. Авторы отмечали, что после введения phHGF транзиторные отеки наблюдали лишь у нескольких больных, в то время как частота их возникновения в исследованиях с геном VEGF достигала 60%.
Еще одно интересное исследование было проведено с использованием плазмидной ДНК, экспрессирующей две изоформы HGF [73]. В основу клинической работы легла серия экспериментальных исследований, в которых был использован оригинальный вектор, кодирующий два сплайс-варианта гена HGF, несущих 723 или 728 аминокислотных остатков (dHGF и cHGF соответственно) [74, 75]. Использование вектора для экспрессии двух изоформ HGF является оправданным с позиции эффективности, т.к. было показано, что у крыс с ИМ показатели фракции выброса, диастолической функции и толщины левого желудочка были выше после введения плазмиды с cHGF/dHGF по сравнению с dHGF [74]. Сходные данные были получены на моделях ишемии задней конечности кролика [76] и ИМ у свиней [77].
Клиническое испытание данного препарата включало 21 больного КИНК. Пациентам внутримышечно многократно вводили суммарную дозу от 4 до 16 мг плазмиды pCK-HGF-X7, кодирующей cHGF и dHGF. По истечении 3 мес было отмечено клинически значимое улучшение состояния пациентов вне зависимости от дозировки. Оно выражалось в уменьшении интенсивности болей в покое и ходьбе и тенденции к заживлению язвенных дефектов (у 6 пациентов), а также увеличении TcPO2 на дорзальной поверхности стопы и обеих поверхностях голени.
Даже с учетом того, что в описанных исследованиях не было получено данных об эффективности препаратов с геном HGF по первичным конечным точкам, в них отмечен ряд положительных изменений по вторичным конечным точкам, касавшихся симптомов заболевания и качества жизни.
С учетом еще одного важного фактора — высоких показателей безопасности этих препаратов — можно ожидать, что в ближайшее время будут начаты их полномасштабные многоцентровые исследования.
Клинические исследования по генной терапии с использованием FGF. В настоящее время известно 22 различных фактора роста фибробластов, участвующих в регуляции ангиогенеза, эмбрионального развития и ряда других процессов [78]. Исходно название этим факторам было дано благодаря их способности активировать пролиферацию фибробластов, однако они обладают митогенными свойствами в отношении ряда других типов клеток, в т.ч. эндотелиоцитов и ГМК, а также способны регулировать выживаемость и гипертрофию кардиомиоцитов [79, 80]. Среди работ, касающихся лечения КИНК, первым стало открытое клиническое исследование, в котором была проведена оценка эффективности внутримышечного введения плазмиды с геном FGF1, получившей название NVFGF1 [81].
В 2009 г. было проведено неконтролируемое клиническое исследование с использованием плазмиды NV1FGF, в которое были включены 6 пациентов. Больным, которым планировалось проводить ампутации, вводили плазмиду и изучали распределение продуктов экспрессии введенного генетического материала. Проведенный анализ показал, что распределение и экспрессия введенных генов ограничивается местами введения, свидетельствуя об отсутствии диссеминации и безопасности мультисайтового введения для терапевтического ангиогенеза [82].
Следующим шагом стало проведение исследования II фазы под названием TALISMAN 201, в которое были включены 59 больных КИНК, получавших NVFGF1, и 66 пациентов, которым вводили плацебо. По истечении 25 нед оказалось, что доля больных с заживлением трофических язв в группе NVFGF1 составила 19,6%, при том что в контроле этот показатель равнялся 14,3%; статистической значимости данные различия между группами не достигали. При этом частота ампутаций в группе NVFGF1 была значительно ниже, чем в контроле (37,3 и 55,4% соответственно; р=0,015), а также отмечалось уменьшение общей смертности.
После исследования TALISMAN в 2011 г. была инициирована следующая фаза исследования, которая получила название TAMARIS. Оно представляло собой двойное слепое контролируемое исследование, в III фазу которого вошли 525 пациентов более чем из 30 стран с КИНК, ишемическими язвами или гангренами. В течение года 36% пациентов исследуемой группы умерли или перенесли значительные по объему ампутации по сравнению с 33% пациентами контрольной группы. Таким образом, клинически значимых положительных изменений при лечении плазмидой, содержащей FGF, выявлено не было [83, 84].
В 2012 г. было закончено исследование эффективности и безопасности использования плазмидного вектора NV1FGF для лечения КИНК. Исследование проводилось с использованием базы данных США (OPTIMIST) и Европы (EuroOPTMIST) на базе 4 клинических центров. Исследование проводилось в течение 3 лет и продемонстрировало безопасность данного метода (не было зарегистрировано увеличения смертности, риска возникновения злокачественных опухолей, ретинопатии и др.). Однако разницы в числе крупных ампутаций у пациентов, получавших лечение, и у получавших плацебо, обнаружено не было, что, впрочем, было объяснимо незначительным размером группы [85].
С учетом накопленных данных было инициировано исследование III фазы по изучению эффективности NV1FGF, результаты которого будут опубликованы в ближайшее время.
Вторым фактором из этого семейства, который был использован в клинике, является FGF-4. Целый ряд исследований под общим названием AGENT показал безопасность и первичную эффективность аденовирусного вектора с геном FGF4 (Ad5FGF4) при его введении интракоронарно. В дальнейшем оказалось, что при использовании Ad5FGF4 уменьшение зоны ишемии у женщин было более выраженным, чем у мужчин [86, 87]. Объяснение этому авторы нашли в том, что у женщин, страдающих ИБС, в значительно большей степени, чем у мужчин, выражена микроциркуляторная дисфункция, но нет таких тяжелых субэпикардиальных стенозов коронарных артерий, как у лиц мужского пола [88, 89].
Терапия FGF-4, по мнению авторов, влияет именно на микроциркуляторное звено ишемии и, соответственно, может оказаться более эффективной у женщин, особенно пожилого возраста.
Возможные причины недостаточно высокой эффективности терапевтического ангиогенеза и способы их решения. Несмотря на то что с момента начала первых работ по терапевтическому ангиогенезу прошло 15 лет, следует признать, что клинические результаты, которых с таким нетерпением ждали после выполнения первых экспериментальных работ, пока что далеки от идеала [60]. Для дальнейшего развития этого подхода необходимо проанализировать используемые методы генной терапии и способы оценки эффективности их применения, чтобы понять их недостатки и возможные источники ошибок, которых следует избегать в дальнейшем.
Ограниченные возможности животных моделей. Начальным этапом, на который обращают внимание, является доклиническое исследование новых методик на животных моделях. В таких работах обычно используются молодые, здоровые животные, которые не отражают характеристик типичного пациента — пожилого, зачастую с рядом вредных привычек и целым набором сопутствующих заболеваний и метаболических расстройств, ухудшающих течение заболевания и снижающих эффективность лечения [90]. Ряд авторов указывают на то, что у людей (как и у животных) с возрастом ухудшается способность клеток-предшественников к хоумингу в область ишемии [91], а также падает базальная экспрессия факторов роста [92] и в целом снижается ангиогенный потенциал ткани [93—95]. Таким образом, данные, полученные на молодых линейных животных, с трудом можно экстраполировать на весьма гетерогенную популяцию больных хотя бы по причине роли возрастных изменений, которая никак не учитывается в таких модельных исследованиях.
Еще одним фактором, который следует принимать во внимание, является существенное отличие экспрессии генов, доставляемых в ткани животных и человека. Известно, что чем крупнее животное, тем ниже эффективность трансфекции его тканей при введении плазмиды [6]. Для сравнения: у 2-недельных мышей линии BALB/C эффективность трансфекции скелетной мышцы составляет 50%, а у высших приматов — не более 8—10% [96, 97]. Это связывают с более толстым перимизием, который может ограничивать объем распространения введенного раствора. Кроме того, определенную роль может играть и большой объем мышц у крупных животных, который приводит к снижению относительной концентрации плазмидной ДНК вокруг мышечных волокон [98]. Аналогичные данные получены и в опытах по сравнению эффективности аденовирусных векторов у мышей и человека [99, 100].
Принимая во внимание все эти факты, следует признать, что в текущем состоянии животные модели годятся для доказательства эффективности вектора и биологической активности выбранного гена. В идеальных условиях для оценки терапевтической эффективности следует использовать более «правдоподобные» модели с применением животных зрелого возраста, линий с повышенной склонностью к атеросклерозу, артериальной гипертонии и сахарному диабету [101].
Выбор вектора для доставки терапевтических генов. Всего за период с 1989 по 2010 г. было завершено 1522 клинических исследования по генной терапии. Среди них 148 (10%) посвящены терапевтическому ангиогенезу. В большей части этих исследований использована плазмидная ДНК (74 исследования), на втором месте – аденовирусные частицы (55 исследований) [102].
Выбор вектора является еще одной важной составляющей успеха генной терапии. «Идеальный» вектор должен обладать высокой эффективностью трансфекции/трансдукции, давать хорошую экспрессию целевого белка, хорошо переноситься больными после введения и иметь низкую иммуногенность. В большинстве клинических исследований в качестве векторов использовали плазмидную ДНК или аденовирусы.
К настоящему моменту с позиций безопасности бесспорными лидерами являются плазмидные векторы, в первую очередь из-за транзиторной экспрессии белка и низкой вероятности интеграции в геном [103, 104]. При этом терапевтическая активность плазмид ограничена низкой эффективностью трансфекции и сравнительно небольшими количествами экспрессируемого белка при однократном введении. Близкая к нулю иммуногенность плазмид оставляет возможность для их повторных введений, что может оказаться путем решения этой проблемы.
Аденовирусные векторы характеризуются более высокой эффективностью трансдукции и длительным периодом экспресии, но могут вызывать иммунный ответ и становиться неэффективными у больных с циркулирующими антителами после перенесенной аденовирусной инфекции. Хотя аденовирусные векторы потенциально очень перспективны с точки зрения высокой эффективности трансдукции и экспрессии АФР, в клинических исследованиях по терапевтическому ангиогенезу они по распространенности остаются вторыми после плазмид [104]. Проблему иммунного ответа реципиентов в настоящее время предлагается решать с помощью иммунологического скрининга и создания химерных вирусов, капсидные антигены которых не будут вызывать иммунного ответа у больных, перенесших инфекцию аденовирусами «дикого типа».
Аденоассоциированные вирусы очень вариабельны и некоторые их серотипы обладают низкой иммуногенностью, а также тропностью в отношении тех или иных органов и тканей. Наиболее ценными их свойством является эписомальная локализация трансгена и очень низкая частота интеграции в геном [105]. К сожалению, пока что в большинстве работ отмечается слабая и недостаточно продолжительная экспрессия белка в ткани после введения векторов на базе аденоассоциированных вирусов, что сильно осложняет работу с ними. При этом аденоассоциированные вирусы остаются ценным инструментом для модификации в терапевтических целях мезенхимальных, стволовых и прогениторных клеток [106]. В будущем их можно будет использовать для гиперэкспрессии АФР, антиапоптотических белков или рецепторов к ним в трансплантируемых клетках, что приведет к повышению выживаемости клеток и эффективности клеточной терапии.
Применение весьма эффективных векторов на базе ретровирусов и лентивирусов ограничено тем, что они интегрируют в геном клеток хозяина, что ставит вопрос о возможности злокачественной трансформации за счет активации протоонкогенов. В настоящее время активно исследуются механизмы встраивания ретровирусов в геном с целью создания систем контролируемой интеграции. Основной областью применения таких векторов по-прежнему остаются летальные и моногенные заболевания (миодистрофия Дюшенна, синдром Вискотта—Олдрича, боковой амиотрофический склероз и т.д.).
Таким образом, можно констатировать, что в настоящий момент среди всех используемых in vivo векторов наибольший интерес для терапевтического ангиогенеза представляют плазмиды. Их безопасность, транзиторная экспрессия трансгена, удобство в использовании и большое количество исследований, показавших их эффективность и безопасность, делают их оптимальным инструментом для доставки терапевтических генов в ткани.
Дозировка и продолжительность введения. Исследования пока что не дали однозначных ответов на вопросы об оптимальной дозировке и временны'х рамках для проведения ангиогенной терапии, причем речь идет как о продолжительности, так и о начале лечения. Известно, что процесс ангиогенеза в нормальных условиях занимает недели и даже месяцы, в течение которых происходит созревание капилляров, которые в свою очередь нуждаются в стимуляции АФР [107].
При этом пока неясно, необходима ли столь долгосрочная стимуляция в тканях в условиях ишемии [108, 109]. Кроме того, при планировании исследований по генной терапии следует учитывать и продолжительность экспрессии белка после введения тех или иных векторов. Например, однократное введение плазмиды позволяет добиться медленно снижающейся экспрессии белка в течение 1—2 нед [110], а использование аденовируса расширяет этот период до 1 мес [105].
Многие исследователи пришли к выводу, что невысокая эффективность однократного введения генетической конструкции может быть связана с тем, что период, в течение которого в ткани создается достаточная концентрация терапевтического белка, оказывается слишком коротким. Показано, что у кроликов с тяжелой ишемией задней конечности только при многократных инъекциях плазмиды с геном VEGF удавалось достичь клинически значимого восстановления кровотока и улучшения состояния ишемизированной ткани [111]. Еще одним лимитирующим фактором может оказаться то, что мы не всегда можем полностью адекватно прогнозировать эффективность доставки трансгена при разных способах введения, а также что все виды ткани характеризуются различной эффективностью трансфекции/трансдукции [112]. Вероятно, по мере накопления данных о безопасности этих методов, все больше исследований будет посвящено подбору дозировки и отработке оптимального режима введения и наблюдения с целью оценки эффективности.
Использование комбинированной генной терапии для стимуляции ангиогенеза. В поисках более эффективных методов стимуляции ангиогенеза с помощью генной терапии исследователи обращались к применению комбинаций векторов, кодирующих несколько АФР. Этот подход основан на том, что ангиогенез является комплексным процессом, в котором чередуются процессы деградации и стабилизации матрикса, соблюдается баланс пролиферации и апоптоза клеток, а также важную роль играет регуляция миграции ГМК, эндотелиальных клеток и перицитов. Все эти стадии находятся под контролем различных регуляторных молекул, которые связываются со своими рецепторами, активируя сигнальные каскады и меняя активность клеточных систем.
Логичным оказалось предположение о том, что при стимуляции процессов ангиогенеза при гиперэкспрессии нескольких факторов, каждый из которых реализует свои эффекты через специфический рецептор, возможна комплексная активация реваскуляризации. Под последней следует понимать пролиферацию эндотелиальных клеток и ГМК, таксиса моноцитов и клеток-предшественников, артериогенные процессы и ремоделирование, т.е. спектр реакций, приводящих к формированию нового функционально зрелого сосуда или ремоделированию коллатералей.
Усиление ангиогенного эффекта наблюдалось при доставке с помощью аденовирусов и плазмид целого ряда комбинаций факторов роста. В большинстве исследований использовали ген VEGF165 в сочетании со вторым фактором роста, который отличается от VEGF характером воздействия на эндотелий или может уменьшать негативные эффекты VEGF — отечность и воспалительные реакции. При этом предпочтение отдавалось белкам, которые сами обладают доказанными ангиогенными свойствами.
Ангиогенная активность комбинации VEGF и HGF была проверена на модели ишемии задней конечности кролика, однако в этом исследовании АФР вводились в форме рекомбинантных белков [113]. В другой работе активацию аниогенеза наблюдали при сочетании VEGF и HGF в случае введения в роговицу глаза крысы [114]. Эффективность восстановления кровотока в ткани и увеличение плотности сосудов были продемонстрированы в ряде исследований при использовании следующих комбинаций генов: VEGF и bFGF [115, 116], VEGF и PDGF-BВ [117], VEGF и ангиопоэтина-1 [118—120], VEGF и SDF-1a [121].
Наша группа также проводила исследования и поиск новых ангиогенных генов и их комбинаций, которые обладают высоким терапевтическим потенциалом. Одной из них оказалась комбинация VEGF и uPA, которая была испытана на моделях ишемии задней конечности мыши и ИМ у крысы [35].
На обоих видах животных показано, что введение плазмиды с геном uPA обладает собственным ангиогенным эффектом, выражавшимся как в увеличении плотности сосудов, так и в уменьшении площади постинфарктного фиброза в миокарде. Эти результаты стали логическим продолжением ранее полученных нами данных о том, что uPA, помимо своих тромболитических свойств, обладает способностью активировать процессы миграции и пролиферации клеток за счет связывания со своим рецептором — uPAR, а также за счет протеолитических свойств и способности высвобождать и активировать депонированные белки АФР [122—124].
В нашей работе эффект введения комбинации плазмид с генами VEGF и uPA (в соотношении 1:1) оказался сопоставимым с наблюдавшимся при введении плазмидных ДНК по отдельности, несмотря на то что в комбинации доза каждой из плазмид была в 2 раза ниже [35].
При сочетании VEGF с другим фактором роста — HGF мы обнаружили, что введение смеси плазмид приводит к более выраженному восстановлению кровотока в ишемизированной задней конечности мыши [125], чем при введении каждой плазмиды по отдельности (рис. 1, см. цветную вклейку). Перспективность использования комбинации генов VEGF и HGF подтверждается еще и тем, что эти факторы, обладая плейотропией эффектов, могут дополнять друг друга [126]. Например, HGF может уменьшать выраженность индуцированных VEGF отеков за счет влияния на таксис ГМК и проницаемость сосудов [33]. В наших опытах совместная активация тирозинкиназных рецепторов к VEGF и HGF на поверхности эндотелия приводила к увеличению фосфорилирования сигнальных киназ — ERK1/2 и p38 [125], а также уменьшала активность сигнального каскада ядерного фактора (NF-κВ) [127], который является ключевым фактором транскрипции, регулирующим продукцию провоспалительных цитокинов и молекул адгезии.
Наши предварительные данные, полученные на аналогичной животной модели, также указывают на то, что сочетание HGF и ангиопоэтина-1 может быть перспективным для терапевтического ангиогенеза. В данном случае речь может идти о взаимно дополняющей комбинации факторов, где HGF представляет собой плейотропный индуктор ангио- и артериогенеза с доказанными антиапоптотическими и антифибротическими свойствами [33], а ангиопоэтин-1 является фактором стабилизации сосудов, оказывающим противовоспалительное и антиапототическое действия [128]. Совместное их использование может обеспечивать формирование стабильных и функционально зрелых кровеносных сосудов.
С учетом имеющихся данных по безопасности «монотерапии» плазмидными конструкциями с генами VEGF, HGF, bFGF и еще целого ряда факторов в ближайшее время следует ожидать появления первых пилотных работ по комбинированному использованию этих генов в условиях клиники.
Среди упоминаемых в литературе нестандартных комбинаций следует выделить HIF-1a и VEGF[129], а также гемоксигеназу-1 и bFGF [130]. Возможным направлением также является стимуляция хоуминга стволовых и прогениторных клеток для увеличения ангиогенного ответа. В работе Y. Tan и соавт. при сочетании двух наиболее часто используемых хемоаттрактантов для клеток-предшественников (Г-КСФ и SDF-1a) отмечалось улучшение кровоснабжения ткани в ишемизированной скелетной мускулатуре [131]. Данный подход физиологически оправдан и потенциально является весьма перспективным с точки зрения увеличения эффективности терапевтического ангиогенеза.
Использование кондиционированных сред для стимуляции ангиогенеза и регенерации тканей. Еще одним подходом, основанным на комбинированной доставке АФР, может стать использование кондиционированных сред, содержащих продукты секреции стволовых/прогениторных клеток. Кондиционированные среды представляют собой своего рода коктейль, включающий комплекс белковых молекул, факторов роста, цитокинов, микровезикул и других компонентов, которые обладают ангиогенным потенциалом.
Перспективным источником клеток для получения кондиционированных сред является жировая ткань. Стромальные клетки жировой ткани (СКЖТ) могут быть легко получены в большом количестве в ходе хирургических вмешательств или при липосакции [106]. СКЖТ обладают определенным дифференцировочным потенциалом, однако основной терапевтический эффект при введении СКЖТ в ишемизированные ткани связан с паракринной активностью этих клеток [132].
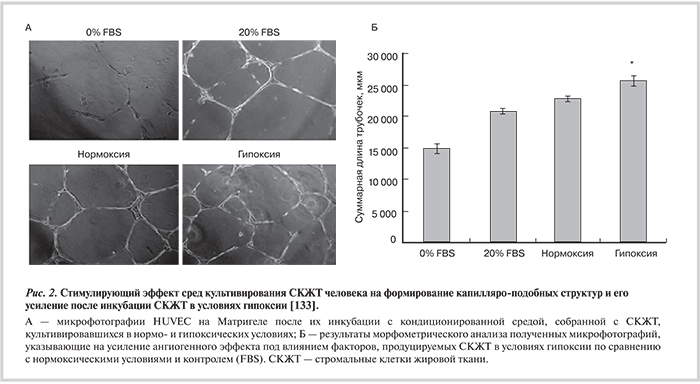
Они также характеризуются активной продукцией ряда АФР и белков, участвующих в паракринной регуляции тканевого гомеостаза и регенерации тканей [132]. Результаты наших исследований и работы других групп указывают на то, что при гипоксическом прекондиционировании СКЖТ резко увеличивается продукция ими АФР (рис. 2) и это позволяет использовать данные метод для повышения терапевтического потенциала препаратов на основе сред культивирования [95].
Таким образом, в настоящее время использование кондиционированных сред, содержащих большой спектр биологически активных молекул в оптимальном соотношении, в качестве терапевтического агента представляется перспективным и более безопасным способом стимуляции ангиогенеза, чем использование клеточной терапии.
Помимо гипоксического прекондиционирования еще одним способом повышения продукции определенных факторов роста стволовыми/прогениторными клетками является их генетическая модификация. При использовании генетически модифицированных СКЖТ человека с повышенной продукцией VEGF165 нами было показано, что по сравнению с немодифицированными такие клетки обладают более высоким терапевтическим потенциалом при введении животным с ишемией задней конечности [106]. Областью применения сред на основе генно-модифицированных клеток может быть лечение ожогов, ишемических и воспалительных заболеваний, терапия язвенных поражений кожи и слизистых оболочек. При этом тип клеток, которые могут использоваться для создания кондиционированных сред, не ограничивается СКЖТ — для этой цели могут использоваться циркулирующие эндотелиальные клетки-предшественники [134], мезенхимальные клетки костного мозга [135] и некоторые другие.
Заключение
Терапевтический ангиогенез в настоящее время переживает период критического анализа результатов первых клинических исследований, который необходим для выявления наиболее острых проблем, касающихся эффективности лечения. Отмечается рост интереса к комбинированным подходам, новым мишеням, которые можно использовать в генной терапии, и новым способам доставки векторов. Целый ряд векторов (в большинстве своем — плазмидных) с «классическими» терапевтическими генами АФР (VEGF, HGF, bFGF и др.) находятся в III фазе исследований, пройдя сложный путь от экспериментальных разработок до медицинских препаратов. Несмотря на то что с момента начала первых работ по терапевтическому ангиогенезу прошло более 15 лет, следует признать, что клинические результаты, которых с таким нетерпением ждали после выполнения первых экспериментальных работ, не всегда оправдывали надежды. Это свидетельствует о том, что для развития данного перспективного направления необходимы новые исследования с использованием современных подходов терапевтического ангиогенеза или их сочетания, а также адекватных методов оценки эффективности терапии.
Исследование выполнено за счет гранта Российского научного фонда (проект №14-24-00086.



