У женщин в период перименопаузы и при беременности происходит перестройка организма, затрагивающая не только гормональный фон, но и функционирование вегетативной нервной системы (ВНС). Так, при физиологически протекающей беременности возникает активация симпатико-адреналового звена ВНС, с одной стороны, необходимая для обеспечения в этот период потребностей растущего плода, с другой — как следствие адаптационных процессов, происходящих в организме будущей матери, которые могут компенсировать возможные осложнения беременности [1, 2]. Общепризнанной является гипотеза об активации симпатической части ВНС (С-ВНС) у женщин в перименопаузе, когда происходят изменения гормонального статуса, сопровождающиеся повышением возбудимости гипоталамо-гипофизарных структур c нарушением центральной и периферической регуляции сосудистого тонуса [3—5]. Подобные изменения, сопровождающиеся вегетососудистыми проявлениями климактерического синдрома, в значительной степени характерны для пациенток на раннем этапе инволютивного процесса. Существует мнение, что активация С-ВНС в перименопаузе возникает в результате естественного для этого периода жизни женщины дефицита эндогенных эстрогенов, которые обладают симпатолитическими свойствами, тем самым вызывая снижение выброса норадреналина из периферических нервных окончаний [6] и уменьшение концентрации норадреналина и адреналина в крови [7]. В то же время в течение всей беременности отмечается высокий уровень прогестерона, его понижение происходит лишь к концу беременности и тесно коррелирует с увеличением эндогенных эстрогенов. Однако вопрос состояния вегетативного статуса у пациенток с артериальной гипертонией (АГ) в изучаемые периоды жизни остается открытым. Так, казалось бы, изменения ВНС, происходящие у женщины во время беременности и в перименопаузе, имеют явное патогенетическое обоснование, заключающееся, в частности, в активации С-ВНС. При этом физиологическая активация симпатико-адреналового звена ВНС приводит к формированию гиперкинетического типа кровообращения, что может явиться пусковым моментом в развитии [8] или, возможно, усугубить течение имеющейся у пациентки АГ. Вместе с тем ряд авторов полагают, что вегетососудистые симптомы климактерического синдрома могут выражаться как в преобладании симпатического тонуса, так и в преобладании парасимпатической части ВНС, а также в дисфункции обоих этих отделов [9, 10]. По данным исследования, проведенного у пациенток в постменопаузе с мягкой и умеренной АГ, выявлены превалирование гипокинетического типа кровообращения, повышение общего периферического и почечного сосудистого сопротивления и снижение эффективного почечного кровотока по сравнению с таковыми у больных АГ женщинами в репродуктивном периоде и у мужчин с АГ [11].
Для исследования вегетативных функций разработано множество методов: микронейрография, оценка вариабельности ритма сердца, определение концентрации катехоламинов в плазме крови и экскреции катехоламинов с мочой, импедансная кардиография, лазерная допплерфлоуметрия, плетизмография мышцы и др. Вместе с тем, несмотря на огромное количество методик, определяющих активность симпатико-адреналовой системы (САС), мы вынуждены отметить отсутствие метода, который мог бы рассматриваться в качестве «золотого стандарта». В то же время исследования, выполненные в последние годы, убедительно доказывают прогностическую значимость формирования ночных типов суточного ритма артериального давления (АД), или феноменов нон-диппер и найт-пикер, в плане развития поражения органов-мишеней и различных типов вегетативной дисфункции [12, 13]. Кроме того, установлено, что эритроциты отражают общие закономерности изменений мембранных и клеточных структур под действием катехоламинов и могут считаться адекватной моделью системных проявлений активности САС [14—16]. С учетом того, что адреномиметики и адреноблокаторы, связываясь с β-адренорецепторами эритроцитов человека, изменяют степень гипоосмотического гемолиза [17], И.Г. Длусской и Р. И. Стрюк (1995) был разработан метод определения адренореактивности организма. Кроме того, рядом авторов доказано, что достаточно удобным и простым для расчета показателем, определяющим превалирование той или иной части ВНС является вегетативный индекс, или индекс Кердо [18].
В связи с этим интересной явилась сравнительная оценка вегетативного статуса на основании исследования суточного ритма АД, вегетативного индекса и адренореактивности организма по величине β-адренорецепции мембран эритроцитов (β-АРМ) у беременных и у женщин в перименопаузе с АГ.
Материал и методы
В исследование включены 137 пациенток, из них 72 женщины (53%) во II триместре беременности (1-я группа) и 65 (47%) пациенток в перименопаузе (2-я группа). Средний возраст в 1-й группе составил 37,6±3,7 года, во 2-й группе 49,3±3,6 года. У всех пациенток была диагностирована АГ, которая по данным анамнеза и клинико-инструментального обследования была расценена как гипертоническая болезнь (ГБ) I—II стадии 1—2-й степени [19].
Офисное измерение АД на обеих руках проводили трижды с 5-минутным интервалом сфигмоманометром в положении больной сидя в удобной позе, рука на столе по стандартной методике. За конечное (регистрируемое) значение офисного АД принимали среднее из трех измерений.
Суточное мониторирование АД (СМАД) осуществляли с помощью суточного монитора АД «BPLab». Процедуру мониторирования проводили в течение 24 ч. С 07:00 до 23:00 измерения АД проводили с 15-минутными интервалами, с 23:00 до 07:00 — с 30-минутными интервалами. При определении суточного индекса АД использовали индивидуальные временны`е рамки, выделяющие период сна и бодрствования. При расчете показателей нагрузки давлением за верхнюю границу нормы в дневное время принимали 135/85 мм рт.ст., в ночное время — 120/80 мм рт.ст.
Состояние вегетативного тонуса оценивали по индексу Кердо (V.I.), который рассчитывали по формуле:
V.I. = (1–d/p)×100, где d — ДАД,
мм рт.ст., p — пульс, уд/мин.
V.I.>0 — сдвиг вегетативного тонуса в сторону симпатического преобладания, V.I. <0 — в сторону парасимпатического, V.I.=0 — отсутствие симпатического или парасимпатического преобладания — эйтония [20].
Активность САС определяли по β-АРМ авторским методом, основанным на изменении осморезистентности эритроцитов в присутствии β-адреноблокатора с использованием набора реагентов «АРМ-АГАТ» [21].
Статистическую обработку полученных данных осуществляли с помощью пакета прикладных программ Statistica версии 6.0. При непараметрическом распределении признака рассчитывали медиану (Ме) и интерквартильный размах (25-й квартиль; 75-й квартиль). Сравнение двух независимых групп проводили с использованием непараметрического теста Манна—Уитни. Оценку межгрупповых различий по качественным порядковым и бинарным признакам выполняли с использованием критерия χ2. Для анализа корреляции двух признаков при непараметрическом распределении использовали метод Спирмена. Оценку полученных результатов производили по принятой классификации силы корреляции в зависимости от значения коэффициента корреляции (r): |r| ≤ 0,25 — слабая корреляция; 0,25<|r|<0,75 — умеренная корреляция; |r|≥0,75 — сильная корреляция. Долю вариабельности одного признака, зависящего от вариабельности второго признака (долю объясняемой дисперсии), вычисляли по формуле: r2×100 (%). Для всех видов анализа статистически достоверными считались значения при p<0,05.
Результаты
Наличие АГ в анамнезе у одного и/или двух родственников первой линии выявлено в 56% случаев у беременных с ГБ и в 93% — у женщин с ГБ в перименопаузе, в то время как перенесенные острое нарушение мозгового кровообращения и острый инфаркт миокарда у ближайших родственников обследуемых наблюдали в анамнезе примерно в одинаковых соотношениях (12 и 15% соответственно).
Все обследуемые 1-й группы знали о наличии у них ГБ и в качестве антигипертензивной терапии непостоянно, при повышении АД, которое чаще всего проявлялось головной болью, использовали ингибиторы ангиотензинпревращающего фермента — АПФ (n=29; 40%), β-адреноблокаторы (n=12; 17%) или нифедипин (n=6; 8%). С установлением беременности все женщины самостоятельно прекратили прием антигипертензивных препаратов; 25 (35%) обследованных не принимали антигипертензивные препараты и до беременности.
Женщины с ГБ в перименопаузе (2-я группа) принимали эпизодически ингибиторы АПФ (n=11; 17%), β-адреноблокаторы (n=15; 23%), блокаторы кальциевых каналов (n=5; 8%) или комбинацию препаратов — ингибиторы АПФ и β-адреноблокаторы (n=22; 34%), ингибиторы АПФ и диуретик (n=12; 18%); нередко лечение проводили курсами, с перерывами. При сборе анамнеза было установлено, что на момент обследования все пациентки этой группы не принимали антигипертензивные препараты в течение последних 2—3 нед.
Показатели СМАД соответствовали наличию АГ у пациенток обеих групп. При анализе показателей СМАД статистически значимых различий по временному гипертоническому индексу по систолического артериального давления (САД) и диастолического артериального давления (ДАД) между группами выявлено не было (табл. 1). Между тем структура составляющих временной гипертонический индекс была различной. Так, у беременных с ГБ (1-я группа) повышение временного гипертонического индекса — 49,5(36; 68)% (норма до 25%) выявлено за счет достоверного увеличения среднего дневного и ночного ДАД по сравнению с таковым во 2-й группе. В то же время у пациенток с ГБ в перименопаузе (2-я группа) увеличение временного гипертонического индекса происходило за счет достоверного по сравнению с 1-й группой увеличения максимального САД. Средняя частота сердечных сокращений (ЧСС) была значимо выше в 1-й группе — 88 (82; 93) уд/мин по сравнению со 2-й группой — 72 (67; 79) уд/мин (см. табл. 1).
Таблица 1. Показатели СМАД при ГБ у беременных и женщин в перименопаузе
Примечание. * — p<0,05 по сравнению с 1-й группой. СМАД — суточное мониторирование артериального давления; Здесь и в табл. 2 ГБ — гипертоническая болезнь; САД — систолическое артериальное давление; ДАД — диастолическое артериальное давление; СИ — суточный индекс; ЧСС — частота сердечных сокращений.
В 1-й группе пациенток β-АРМ составил 56 (43,5; 68) усл. ед. и значимо (по медиане в 2,4 раза) превышал аналогичный показатель во 2-й группе обследованных — 23 (12,5;31) усл. ед. (p<0,05).
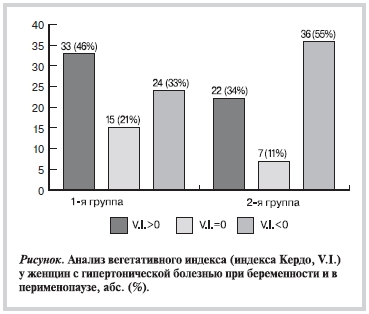
По значениям вегетативного индекса пациентки 1-й группы разделились следующим образом: эйтония (V.I.=0) — у 15 (21%), симпатикотония (V.I.>0) — у 33 (46%), парасимпатикотония (V.I.<0) — у 24 (33%). Во 2-й группе у большинства пациенток наблюдали парасимпатикотонию — 36 (55%), симпатикотония выявлена в 22 (34%) случаях, эйтония — в 7 (11%) (см. рисунок). Анализ таблиц сопряженности АГ в изучаемые периоды жизни женщин и вегетативного индекса выявил наличие связей в обследуемых группах (χ2=10,425; число степеней свободы=2; р=0,005). Так, у пациенток с ГБ достоверно чаще выявляли симпатикотонию, в то время как у женщин с ГБ в перименопаузу превалировала парасимпатикотония.
При анализе таблиц сопряженности АГ в изучаемые периоды жизни женщин и суточного индекса по САД выявлены связи в обследуемых группах (χ2=12,361; число степеней свободы=3; р=0,008). У беременных с ГБ достоверно чаще встречались тип суточного ритма диппер, у женщин с ГБ в перименопаузу — типы суточного ритма нон-диппер и найт-пикер. При этом суточный индекс по ДАД значимо не различался в группах (χ2=152; число степеней свободы =3; р>0,05) (табл.2).
Таблица 2. СИ по САД и ДАД у женщин с ГБ при беременности и в перименопаузе
Примечание. Данные представлены в виде абсолютного числа больных (%).
Следующим этапом исследования для реализации поставленной цели по всем изучаемым параметрам вегетативного статуса (суточный ритм АД, вегетативный индекс и показатель β-АРМ) проведен непараметрический анализ по Спирмену для выявления возможных корреляций.
Умеренная прямая корреляция выявлена между следующими показателями:
— индексом Кердо и β-АРМ в 1-й группе — беременных с ГБ (r=0,504918; р<05; доля объясняемой дисперсии 25%); при этом во 2-й группе — у пациенток АГ в перименопаузе — обнаружена слабая прямая корреляция (r=0,139463; р<0,05; доля объясняемой дисперсии 2%);
— временны`м гипертоническим индексом по САД и показателем β-АРМ в 1-й группе (r=0,621616; р<0,05; доля объясняемой дисперсии 38%); во 2-й группе (r=0,018103) корреляция не выявлена;
— временны`м гипертоническим индексом по ДАД и показателем β-АРМ в 1-й группе (r=0,453159; р<0,05; доля объясняемой дисперсии 20%); во 2-й группе (r=–0,004412) корреляция не выявлена.
Умеренная обратная корреляция выявлена между:
— показателем β-АРМ и СИ по САД в 1-й группе (r=–0,367734; р<0,05; доля объясняемой дисперсии 14%); при этом слабая обратная корреляция обнаружена во 2-й группе (r=–0,165498; р<0,05; доля объясняемой дисперсии 3%);
— показателем β-АРМ и СИ по ДАД в 1-й группе (r=–0,330058; р<0,05; доля объясняемой дисперсии 11%), умеренная обратная корреляция — во 2-й группе (r=–0,272330; р<0,05; доля объясняемой дисперсии 7%).
Полученные данные проанализированы с позиции развития неблагоприятного прогноза в плане осложнений беременности и поражения органов-мишений в перименопаузу у женщин с ГБ и различным вегетативным статусом.
Выявлено, что преэклампсия в сроки беременности 24—35 нед была диагностирована у 18 (25%) с ГБ женщин. При этом у беременных с преэклампсией β-АРМ был достоверно выше — 66 (58; 72) усл. ед., чем у пациенток без преэклампсии — 49 (43; 65) усл. ед. (р<0,002).
Результаты проведенного исследования также показали достоверное выявление увеличения гипертрофии левого желудочка по массе миокарда у женщин с ГБ в перименопаузе с величиной β-АРМ более 20 усл. ед. (норма до 20 усл. ед.) —190,28 (179,34; 212,65) г, по сравнению с пациентками, у которых β-АРМ был менее 20 усл. ед. — 174,20 (158,45; 189,54) г.
Приведенные корреляции свидетельствует о взаимосвязи показателя β-АРМ с СИ и индексом Кердо, и отражают неблагоприятный прогноз у пациенток с ГБ в плане развития преэклампсии при беременности и гипертрофии левого желудочка в перименопаузе при наличии соответствующих корреляций.
Обсуждение
В данном исследовании при СМАД у беременных с ГБ выявлены достоверно более высокие среднее дневное и среднее ночное ДАД, ЧСС и более низкое максимальное САД по сравнению с аналогичными показателями у пациенток с АГ в перименопаузе. С одной стороны, увеличение ДАД во время беременности может свидетельствовать об изменении функции почек и быть предиктором развития преэклампсии [22, 23]. При этом исследования, оценивающие среднее АД (15 000 беременных) и ДАД (38000 беременных), убедительно не доказали повышения риска преэкламсии, связанного с увеличением САД и/или ДАД [24]. С другой стороны, снижение ДАД у пациенток с ГБ в перименопаузе доказано и свидетельствует об увеличении жесткости сосудистой стенки с возрастом [25]. Увеличение максимального САД в перименопаузе может свидетельствовать о течении АГ с частыми подъемами АД. Таким образом, период перименопаузы в большей степени характеризуется кризовым течением АГ, что является неблагоприятным в плане развития таких фатальных и инвалидизирующих осложнений, как инфаркт миокарда, острое нарушение мозгового кровообращения.
Достоверное увеличение ЧСС у беременных по сравнению с пациентками в перименопаузе можно объяснить гемодинамическими изменениями, характерными для физиологического течения беременности. Так, известно, что ЧСС во время беременности в норме увеличивается на 15—20 уд/мин.
Анализ параметров, оценивающих активность ВНС, показал, что в 1-й группе полученное нами значимое увеличение β-АРМ может свидетельствовать о гестационной гиперсимпатикотонии, характерной для беременности, и гиперсимпатикотонии, связанной с АГ [26]. Эти данные соответствуют расчетному вегетативному индексу Кердо, который у большинства беременных с ГБ характеризует повышение вегетативного индекса в сторону превалирования симпатического звена. В то же время у пациенток с ГБ в перименопаузе по сравнению с беременными с ГБ отмечается не только достоверное снижение β-АРМ, но и достоверное преобладание парасимпатикотонии по значениям вегетативного индекса. Данное наблюдение подтверждается наличием умеренной прямой корреляции в 1-й группе и слабой прямой корреляции во 2-й группе между индексом Кердо и показателем β-АРМ. Кроме того, ряд авторов придерживаются мнения, что симпатикотония, возникающая в перименопаузе, может свидетельствовать о признаках поражения сосудов головного мозга, а наличие парасимпатикотонии по индексу Кердо — об отсутствии хронической ишемии [27]. В нашем исследовании выявлено достоверное увеличение частоты гипертрофии левого желудочка у женщин с ГБ в перименопаузе, вегетативный тонус которых характеризовался гиперсимпатикотонией по исследуемым параметрам ВНС. В пользу симпатикотонии у беременных с ГБ свидетельствуют умеренные прямые корреляции между временны`ми гипертоническими индексами по САД и ДАД и показателем β-АРМ, которых не выявлено во 2-й группе.
В нашем исследовании у женщин с ГБ в перименопаузе достоверно чаще встречались типы суточного ритма по САД нон-диппер и найт-пикер, в то время как у беременных с ГБ чаще выявлялся тип суточного ритма диппер. На данный момент проведен ряд крупных исследований, по итогам которых можно говорить о независимой прогностической значимости и степени выраженности ночных изменений АД [28]. Снижение СИ у пациентов с АГ напрямую связано с поражением органов-мишеней и более высокой частотой развития сердечно-сосудистых осложнений [29].
Несмотря на то что на основании многочисленных работ ритмической деятельности ВНС делается однозначный вывод о преобладании активности симпатического отдела днем, а парасимпатического — ночью, исследования, которые бы указывали на корреляцию вегетативной дисфункции с СИ, очень немногочисленны и свидетельствуют о повышении симпатического тонуса при снижении СИ [30]. Это не соответствует нашим данным о снижении типов суточного ритма у пациенток 2-й группы, в которой также выявлены более низкие β-АРМ и индекс Кердо. Однако нами получена умеренная обратная корреляция между величинами β-АРМ и СИ по САД и ДАД у пациенток обеих групп, что свидетельствует о связи снижения СИ с повышением показателя β-АРМ и реализуется во 2-й группе за счет пациенток, у которых показатель β-АРМ выходил за пределы референсных величин.
Выводы
1. Выявлены различия показателей суточного мониторирования артериального давления в 1-й и 2-й группах, которые характеризуются повышением диастолического артериального давления у беременных с гипертонической болезнью и снижением диастолического артериального давления, а также увеличением максимальных уровней систолического артериального давления у женщин в перименопаузе с гипертонической болезнью, что может быть обусловлено возрастными особенностями.
2. У беременных с гипертонической болезнью вегетативный тонус по величине адренорецепции мембран эритроцитов и индексу Кердо характеризуется гиперсимпатикотонией, обусловленной собственно беременностью. У пациенток с гипертонической болезнью в перименопаузе преобладает парасимпатикотония, по-видимому, связанная с дисгормональными нарушениями.
3. Снижение суточного индекса у пациенток с гипертонической болезнью в перименопаузе встречается достоверно чаще, чем у беременных с гипертонической болезнью, что может являться прогностически неблагоприятным фактором риска поражения органов-мишеней.
4. Снижение суточного индекса умеренно коррелирует с повышением показателя адренорецепции мембран эритроцитов в обеих группах, что прогностически неблагоприятно в плане развития гестоза при беременности и поражения органов-мишеней в перименопаузе у женщин с гипертонической болезнью.



