Успешно выполненное чрескожное коронарное вмешательство (ЧКВ) со стентированием приводит к восстановлению кровотока в ишемизированных участках миокарда, увеличению зоны жизнеспособного миокарда, препятствует развитию дилатации и дисфункции левого желудочка (ЛЖ) [1—3]. Поэтому при лечении пациентов с хронической сердечной недостаточностью (ХСН) ишемической этиологии помимо медикаментозного воздействия на процессы ремоделирования сердца, улучшения сократительной способности, важным является эффективное восстановление коронарного кровотока. В связи с этим большие надежды в коррекции нарушений при ХСН ишемической этиологии связывают с применением немедикаментозных методов лечения, таких как эндоваскулярная и хирургическая реваскуляризация миокарда.
Цель работы — изучить влияние ЧКВ со стентированием на клиническое течение заболевания, перфузию и сократительную способность миокарда у пациентов с ХСН ишемической этиологии.
Материал и методы
В исследование был включен 71 пациент с ХСН II—III функционального класса (ФК) по классификации NYHA ишемической этиологии. Среди обследованных было 64 мужчины и 7 женщин, средний возраст которых составил 58,6±8,8 года, продолжительность заболевания ХСН — 1,5±1,8 года и ишемической болезнью сердца (ИБС) — 7,6±6,6 года.
В исследование включали больных моложе 80 лет с клиническими проявлениями стенокардии напряжения II—III ФК и наличием ХСН II—III ФК по классификации NYHA со сниженной (<40%) и сохраненной (>45%) фракцией выброса (ФВ) ЛЖ по данным двухмерной эхокардиографии; с различной степенью и распространенностью атеросклеротического поражения коронарных артерий по данным коронарографии (КГ), с успешно выполненной ангиопластикой.

Критериями исключения были инфаркт миокарда (ИМ) менее чем за 6 мес до процедуры ЧКВ; нестабильная стенокардия; постоянная форма мерцательной аритмии; тяжелая неконтролируемая артериальная гипертония (артериальное давление более 180/100 мм рт.ст.); ХСН неишемической этиологии; наличие сопутствующих заболеваний, которые могли бы повлиять на течение основного заболевания и результаты исследования.
Пациенты были разделены на 2 группы: 1-я — больные со сниженной ФВ ЛЖ <40%, 2-я — с сохраненной ФВ ЛЖ >45% (табл. 1).
Всем больным выполнено ЧКВ со стентированием коронарных артерий. Стандартная лекарственная терапия проводилась согласно российским и международным рекомендациям по лечению ИБС и ХСН [4, 5] и не менялась в течение всего периода наблюдения (12 мес).
Клинико-функциональный статус оценивали при помощи следующих методик: шкала оценки клинического состояния (ШОКС) в модификации В.Ю. Мареева, Миннесотский опросник качества жизни при сердечной недостаточности (MLHFQ), динамика ФК ХСН и ИБС, тест с 6-минутной ходьбой.
Для оценки влияния ангиографически успешного ЧКВ на перфузию и сократительную способность сердца был выбран метод синхронизированной однофотонной эмиссионной компьютерной томографии (С-ОЭКТ) миокарда, поскольку он позволяет при однократном введении радиофармпрепарата (РФП) одновременно оценивать перфузию и сократительную функцию ЛЖ, выявлять нарушения кровоснабжения миокарда на уровне микроциркуляции, диагностировать преходящую ишемию миокарда [6], обусловленную коронарным атеросклерозом, дифференцировать участки жизнеспособного и необратимо поврежденного миокарда и объективно оценивать влияние эндоваскулярной реваскуляризации на перфузию и функцию сердца [7].
Исследование проводили по стандартной методике на двухдетекторной гамма-камере SkyLight по протоколу, согласно которому в первый день проводили исследование в покое через 60—90 мин после внутривенного введения 370—555 МБк 99mТс-МИБИ, во второй — с нагрузочной пробой через 45—60 мин после введения РФП такой же активности. При нагрузочной С-ОЭКТ миокарда РФП вводили при достижении критериев прекращения нагрузки во время велоэргометрической пробы и через 5 мин после сублингвального применения нитроглицерина. Обработку изображений осуществляли по 17-сегментарной модели ЛЖ с применением программ «AutoSPECT+» и «AutoQUANT», QPS и 5-балльной шкалы, с помощью которых определяли локализацию, количественно оценивали распространенность и объем дефекта перфузии по стенкам, сегментам ЛЖ и бассейнам коронарных артерий: передней нисходящей, огибающей, правой коронарной артерии. Дополнительно с помощью программы QGS и 6-балльной шкалы определяли ФВ ЛЖ, оценивали региональное движение ЛЖ по стенкам, сегментам миокарда ЛЖ и бассейнам основных коронарных артерий.
Статистический анализ данных проводили с помощью пакета прикладных программ Excel 7.0 и Statistica 6.0 (StatSoft). Выборочные параметры представлены в таблицах в виде M±σ или Me (lq; uq), где М — среднее, σ — стандартное отклонение, Me — медиана, lq; uq — нижний и верхний квартили. Критическое значение уровня значимости принимали равным 0,05.
Результаты и обсуждение
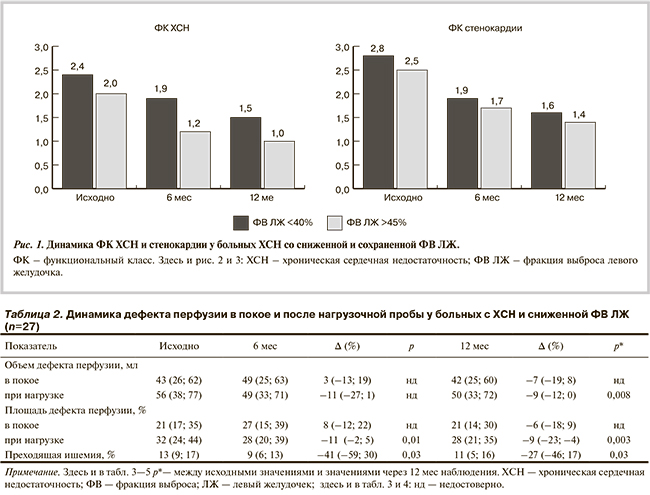
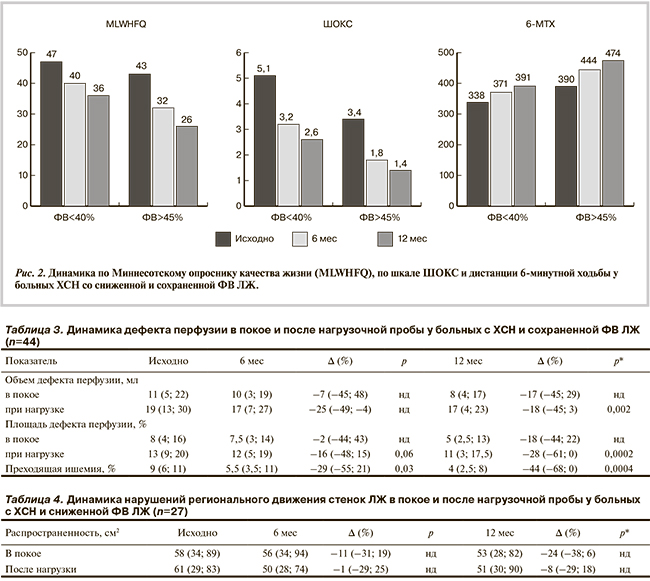
Оценка влияния ЧКВ со стентированием на клинико-функциональный статус пациентов с ХСН со сниженной и сохраненной ФВ ЛЖ. Результаты настоящего исследования показали, что улучшение клинико-функционального состояния наблюдалось у большинства больных наряду с повышением ФВ ЛЖ, нормализацией или улучшением показателей систолической и диастолической функций сердца. В группах со сниженной и сохраненной ФВ ЛЖ отмечалось достоверное улучшение ФК стенокардии и ХСН (рис. 1), что подтверждалось достоверным уменьшением количества баллов по ШОКС и MLHFQ: в группе со сниженной ФВ на 49 и 23%, в группе с сохраненной ФВ ЛЖ на 59 и 40% соответственно. Было получено достоверное увеличение дистанции 6-минутной ходьбы в этих группах на 16 и 18% (p<0,05) к концу периода наблюдения соответственно (рис. 2).
Полученные результаты подтверждаются данными многих авторов [8, 9]. M.C. Morice и соавт. [10] сообщают об отсутствии симптомов стенокардии через 6 мес после эндоваскулярной реваскуляризации в 68,2—90,3% случаев. Среди обследованных в данном исследовании больных отсутствие симптомов стенокардии через 12 мес отмечено у 78% пациентов в группе со сниженной ФВ ЛЖ и у 81% — в группе с сохраненной ФВ ЛЖ.
Тем не менее, несмотря на положительные результаты в целом по группам, у 8 (30%) больных со сниженной ФВ ЛЖ и у 6 (14%) с сохраненной ФВ ЛЖ улучшения клинико функционального состояния не наблюдалось через 12 мес. У 8 пациентов 1-й группы и у 6 больных 2-й группы сохранялись клинические проявления стенокардии напряжения, у 3 больных 1-й группы и у 1 больного 2-й группы наступала декомпенсация кровообращения, потребовавшая повторной госпитализации в стационар для коррекции медикаментозного лечения и проведения 14 больным повторного ЧКВ со стентированием коронарных артерий.
Возможными причинами отсутствия улучшения в клиническом течении заболевания при ангиографически успешном ЧКВ могут быть многие факторы, прежде всего, отсутствие улучшения кровоснабжения на уровне микроциркуляции.
Оценка влияния ЧКВ со стентированием на перфузию миокарда у пациентов с ХСН. При количественной оценке томосцинтиграмм, зарегистрированных в покое, в группе со сниженной ФВ ЛЖ медиана распространенности (площадь) нарушенной перфузии составила 21 (17; 35)%, медиана объема — 43 (26; 62) мл. В ответ на нагрузочную пробу у 19 (70,4%) больных 1-й группы выявлялись достоверные признаки преходящей ишемии миокарда, что проявлялось расширением имеющейся в покое области сниженной аккумуляции РФП. У 8 (29,6%) больных достоверных ишемических изменений сцинтиграфической картины не отмечалось. Полученные данные визуального анализа подтверждались результатами количественной оценки, при которой отмечено увеличение площади с 21 (17; 35) до 32 (24; 44)% (p<0,05) и объема дефекта перфузии с 43 (26; 62) до 56 (38; 77) мл (p<0,05).
В группе с сохраненной ФВ ЛЖ медиана распространенности (площади) нарушенной перфузии составила 7 (4; 16) %, медиана объема — 11 (5; 22) мл. В ответ на нагрузочную пробу у 35 (79,5%) из 44 больных отмечалось расширение имеющейся в покое области сниженной аккумуляции РФП, что является отражением преходящей ишемии миокарда. У 9 (20,5%) больных достоверных изменений сцинтиграфической картины не получено. Данные визуального анализа подтверждались результатами количественной оценки, при которой отмечено увеличение площади с 7 (4; 16) до 13 (9; 20)% (p<0,05) и объема ДП с 11 (5; 22) до 19 (13; 30) мл (p<0,05). Динамика дефекта перфузии по площади и объему, преходящей ишемии миокарда у больных ХСН со сниженной и сохраненной ФВ ЛЖ представлена в табл. 2 и 3.
Эффект ЧКВ у больных 1-й и 2-й групп несколько различался, поскольку у больных 1-й группы с выраженными распространенными дефектами перфузии вследствие трансмуральных рубцовых повреждений миокарда динамика нарушений перфузии была менее значимой в покое. Тем не менее общая направленность результатов была схожей. Несмотря на отсутствие достоверного уменьшения дефектов перфузии в покое, в общем по группам в ответ на нагрузку отмечалось достоверное уменьшение дефектов перфузии по площади и по объему в течение всего периода наблюдения (p<0,05).
В данном исследовании проведен корреляционный анализ между появлением преходящей ишемии до реваскуляризации и наличием положительной динамики перфузии миокарда через 6 мес после ЧКВ. Оказалось, что у пациентов с достоверной индуцированной нагрузочными пробами ишемией до ЧКВ в большинстве случаев наблюдалась положительная динамика показателей перфузии через 6 мес после реваскуляризации (k=0,34; р=0,003).
Эти данные хорошо согласуются с материалами исследований других авторов [11, 12]. Согласно результатам исследования COURAGE [13], среди больных со средней ФВ ЛЖ 60,8±11,2% эффективная ангиопластика была достигнута у 93%. Через 18 мес наблюдения по данным С-ОЭКТ в группе ЧКВ объем ишемизированного миокарда уменьшился на 2,7%. При выполнении нагрузочных проб в 15,2% случаев не удавалось вызвать ишемию миокарда. При умеренно выраженной или тяжелой ишемии до вмешательства выполнение ЧКВ приводило к уменьшению площади и распространенности ишемии миокарда у 78% больных (p<0,05), нормализация перфузии получена в 31,4% случаев. Авторы данного исследования полагают, что целевым значением успешного лечения больного со стабильным течением ИБС может считаться уменьшение объема миокарда, в котором по данным нагрузочной пробы выявляются признаки ишемии, на 5% и более.
Тем не менее, несмотря на положительное влияние ЧКВ на перфузию миокарда в ответ на нагрузку, у ряда обследованных больных регистрировались признаки ишемии миокарда; в 1-й группе у 11 больных через 6 мес и у 6 больных через 12 мес, во 2-й группе — у 17 и у 9 больных соответственно. Отсутствие положительной динамики на сцинтиграммах ассоциировалось с возобновлением приступов стенокардии, что обусловило необходимость проведения повторной КГ, по данным которой выявлено возникновение рестенозов и появление новых стенозов у 8 больных со сниженной ФВ ЛЖ и у 10 больных с сохраненной ФВ ЛЖ.
Оценка влияния транслюминальной баллонной коронарной ангиопластики (ТБКА) со стентированием на сократительную функцию миокарда у больных с ХСН. По данным С-ОЭКТ миокарда, у 27 больных 1-й группы до проведения эндоваскулярной реваскуляризации ФВ ЛЖ составила 38 (29; 40)% и в течение всего периода наблюдения увеличения ФВ ЛЖ не наблюдалось (p>0,05). Во 2-й группе у 44 больных до проведения эндоваскулярной реваскуляризации медиана ФВ ЛЖ составила 52,5 (48; 56)%. Через 6 и 12 мес после проведения ТБКА со стентированием наблюдалось достоверное увеличение ФВ ЛЖ до 55 (51; 59)% и 55 (52; 62)% (p<0,05). Динамика нарушения регионального движения стенок ЛЖ в покое и в ответ на нагрузку представлена в табл. 4 и 5.
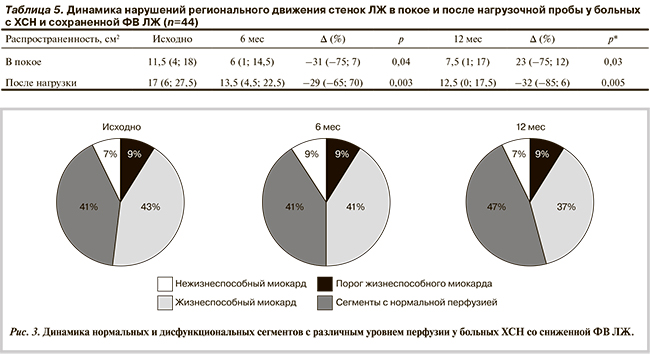
Таким образом, успешно выполненная ТБКА со стентированием у больных со сниженной ФВ ЛЖ не способствует росту ФВ ЛЖ и улучшению регионального движения стенок ЛЖ, а у больных с сохраненной ФВ способствует росту ФВ ЛЖ и улучшению регионального движения стенок в течение всего периода наблюдения (p<0,05).
Сходные данные приводят и другие авторы [14], при этом улучшение движения стенок ЛЖ большинство из них объясняют отсутствием ишемии, восстановлением контрактильности гибернированного и станнированного миокарда на фоне восстановления магистрального кровотока и перфузии миокарда и нормализации симпатической активности и уровня NT-proBNР. В группе со сниженной ФВ ЛЖ достоверного прироста ФВ ЛЖ у больных не получено. Вероятнее всего, это связано с тем, что исходные показатели у больных данной группы были изменены в большей степени, и выраженность процессов ремоделирования была более значимой. Так, исходная ФВ, конечный диастолический объем (КДО) и конечный систолический объем (КСО) ЛЖ у обследованных больных со сниженной ФВ ЛЖ составляли 38 (29; 40)%, 171 (150; 211) мл и 111 (91; 123) мл соответственно. По данным A. Schinkel и соавт., исходное увеличение КСО более 150 мл является независимым предиктором невозможности обратного ремоделирования ЛЖ после реваскуляризации; авторы сделали вывод, что дилатация полости ЛЖ препятствует улучшению общей сократительной способности даже у пациентов с жизнеспособным миокардом [15]. В настоящем исследовании выраженная дилатация полости ЛЖ (КСО >150 мл) отмечалась у 6 больных. J. Bax и соавт. [16] показали, что после реваскуляризации (аортокоронарное шунтирование 3 АКШ/ЧКВ) у пациентов с наличием более 4 жизнеспособных сегментов было увеличение ФВ ЛЖ с 27±6 до 33±7% (p<0,01), снижение ФК ХСН по классификации NYHA с 3,2±0,7 до 1,6±0,5 (p<0,01) и ФК стенокардии с 2,9±0,3 до 1,2±0,4 (p<0,01). Тем не менее у большинства больных 1-й группы также отмечено снижение ФК стенокардии и ХСН. С. Chung и соавт. [17] полагают, что для статистически значимого улучшения показателей функции ЛЖ после реканализации стенозированной коронарной артерии у больных, перенесших ИМ, большое значение имеет наличие жизнеспособного миокарда в кровоснабжаемом ею регионе. Результаты настоящего исследования подтверждают тезис о том, что у больных со сниженной ФВ ЛЖ должно быть достаточное количество жизнеспособного миокарда, чтобы после восстановления коронарного кровотока в результате реваскуляризации миокарда улучшилась сократительная функция ЛЖ.
Оценка влияния ЧКВ со стентированием на региональное движение стенок ЛЖ в жизнеспособных и нежизнеспособных сегментах и глобальную сократимость миокарда у больных ХСН со сниженной ФВ ЛЖ. Оценка жизнеспособности миокарда проведена у 27 больных со сниженной ФВ ЛЖ. Проанализированы 459 сегментов по 17-сегментарной модели ЛЖ.
Пациенты этой группы отличались значительными изменениями миокарда: в 59% случаев отмечен как минимум 1 сегмент с выраженным снижением (≥ 3 балла) перфузии и функции миокарда, отражающим глубокое рубцовое повреждение ЛЖ, у 22 была аневризма ЛЖ. У 46% больных эти изменения составили более 15% площади ЛЖ. Среди 459 проанализированных сегментов 294 были с высоким уровнем накопления РФП. Эти сегменты расценены как нормальные. В 165 сегментах уровень поглощения РФП был снижен; 24 сегмента с уровнем аккумуляции РФП <35% характеризовались как нежизнеспособные, 92 — как жизнеспособные, в 49 сегментах уровень аккумуляции РФП был пограничным (порог жизнеспособности). При сопоставлении синхронизированных и перфузионных изображений 173 сегмента расценены как нормальные, 183 — как жизнеспособные, 28 — как нежизнеспособные и 44 дисфункциональных сегмента были с пограничным уровнем перфузии. Динамика сегментов с различным уровнем перфузии представлена на рис. 3.
Таким образом, у больных со сниженной ФВ ЛЖ после выполненной ТБКА со стентированием количество дисфункциональных сегментов в участках миокарда, расцененных по уровню аккумуляции РФП как нежизнеспособные (или с порогом жизнеспособности), существенно не изменилось в течение всего периода наблюдения. К концу периода наблюдения отмечено некоторое увеличение числа сегментов с нормальной перфузией и сократимостью, преимущественно за счет уменьшения дисфункциональных сегментов в участках жизнеспособного миокарда, однако эти изменения не достигли статистической достоверности.
Анализ факторов, влияющих на восстановление перфузии и сократительной функции миокарда у больных с ХСН со сниженной и сохраненной ФВ ЛЖ при ангиографически успешном ЧКВ со стентированием. Мы проанализировали, какие факторы оказывают неблагоприятное воздействие на восстановление коронарного кровотока при успешно выполненном ЧКВ. Для этого мы разделили больных на 2 группы. В 1-ю группу вошли 29 больных, у которых констатировано ухудшение или отсутствие динамики через 6 мес, во 2-ю группу — 42 больных, у которых отмечалось улучшение перфузии через 6 мес наблюдения. Оказалось, что к факторам, оказывающим неблагоприятное воздействие на восстановление коронарного кровотока и улучшение перфузии, относятся ишемическая кардиомиопатия, отсутствие ишемии миокарда при проведении нагрузочного теста до ЧКВ и более длительный анамнез ХСН. По данным одно- и многофакторного анализа оказалось, что отношение шансов в плане восстановления перфузии лучше у тех больных, у которых исходно была выявлена преходящая ишемия миокарда при проведении нагрузочного теста до эндоваскулярного лечения. Анализ полученных данных позволил выявить, что преходящая ишемия миокарда является основным фактором, определяющим показание к проведению реваскуляризации, поскольку ассоциируется с улучшением перфузии миокарда при ангиографически успешно выполненной ТБКА.
Заключение
В данной работе показано, что улучшение перфузии миокарда после ангиопластики со стентированием наблюдалось у больных с верифицированной ишемией миокарда. При этом у больных, у которых ишемия миокарда не была выявлена, существенного улучшения клинических и гемодинамических показателей не отмечалось.
Таким образом, на основании полученных данных показаниями к проведению реваскуляризации миокарда являются гемодинамически значимое поражение коронарных артерий с индуцируемой ишемией миокарда с помощью нагрузочных проб, а также наличие жизнеспособного миокарда. Больным с сохраненной фракцией выброса проведение эндоваскулярной реваскуляризации возможно при одно- или двухсосудистом поражении коронарных артерий, а для больных со сниженной фракцией выброса, согласно Европейским рекомендациям по диагностике и лечению сердечной недостаточности (2012) [18], приоритетным методом лечения является коронарное шунтирование. Тем не менее мы считаем, что при наличии одно- или двухсосудистого поражения коронарных артерий, а также в случае отказа больного от операции коронарного шунтирования возможно рассмотрение вопроса о проведении эндоваскулярной реваскуляризации. В отсутствие признаков жизнеспособного миокарда и ишемии показано медикаментозное лечение [18].



