Одним из ключевых факторов в развитии атеросклероза является хроническое системное воспаление с локальными специфическими проявлениями в интиме сосудов. Воспаление играет важную роль в происхождении и прогрессировании атеросклеротической бляшки, эволюции ее в ранимую бляшку, ослаблении и разрыве покрышки [1].
В последнее время внимание ученых привлекла липопротеинассоциированная фосфолипаза А2 (Лп-ФЛА2), которая является маркером внутрисосудистого воспаления. В многочисленных исследованиях показана роль Лп-ФЛА2 как фактора риска развития сердечно-сосудистых заболеваний (ССЗ) и непосредственного участника развития и прогрессирования атеросклероза.
Лп-ФЛА2 относится к семейству фосфолипаз А2 и продуцируется моноцитами, тучными клетками, клетками Купфера и Т-лимфоцитами [2]. В плазме крови 80% Лп-ФЛА2 связано с липопротеинами низкой плотности (ЛНП), оставшиеся 20% связано с липопротеинами высокой плотности (ЛВП) и липопротеином (а). Лп-ФЛА2 осуществляет гидролиз окисленных липопротеидов низкой плотности, что ведет к образованию лизофосфотидилхолина, который является медиатором воспаления и проатерогенным фактором [3—6]. Повышение уровня Лп-ФЛА2 не только свидетельствует о поражении коронарных артерий [7], но может определять прогноз и риск развития сосудистых осложнений [7—17].
В последние годы появились сообщения о перспективах использования дарапладиба — селективного ингибитора фосфолипазы А2 для лечения больных ишемической болезнью сердца (ИБС). Однако необходимо подтверждение имеющихся данных результатами крупных длительных рандомизированных исследований, которые проводятся в настоящее время. Наряду с вновь появившимися препаратами оценивается влияние известных гиполипидемических препаратов на уровень Лп-ФЛА2. Показано, что статины (правастатин, аторвастатин, симвастатин и розувастатин) достоверно снижали уровень Лп-ФЛА2 [18—31].
Целью настоящей работы было изучение влияния монотерапии симвастатином и комбинированной терапии симвастатином и эзетимибом на концентрацию (массу) Лп-ФЛА2 в сыворотке крови у больных ИБС.
Материал и методы
В исследование включены 100 человек: 76 мужчин и 24 женщины в возрасте от 39 до 73 лет, медиана, верхний и нижний квартили составили 61 (54; 65) год. У всех больных диагноз ИБС был верифицирован при помощи коронарографии (КГ) на этапе включения в исследование или ранее при постановке диагноза. Все пациенты, включенные в исследование, даже с установленным ранее диагнозом ИБС, не принимали гиполипидемические препараты как минимум в течение 6 мес до включения в исследование. Больным объясняли цели и задачи данной работы, потенциальную клиническую пользу от приема лекарств и возможные побочные эффекты, связанные с применением исследуемых препаратов. Все пациенты подписывали информированное согласие перед включением в исследование.
Пациентов распределяли на 2 группы лечения методом конвертов: группа активного лечения (комбинированная терапия) — прием эзетимиба 10 мг/сут и симвастатина 20—80 мг/сут; контрольная группа (монотерапия) — симвастатин 20—80 мг/сут. Через 6 нед оценивали эффект гиполипидемической терапии и увеличивали дозу симвастатина до 40—80 мг/сут, если уровень холестерина (ХС) ЛНП превышал 2,5 ммоль/л. Продолжительность лечения составила от 6 до 9 мес в зависимости от скорости подбора индивидуальной дозы симвастатина.
В исследование не включали пациентов с острым коронарным синдромом, инфарктом миокарда давностью менее 6 мес, семейной гиперлипидемией, тяжелым поражением печени и почек, застойной сердечной недостаточностью, острыми воспалительными заболеваниями.
Отягощенный по ССЗ семейный анамнез определен у 73 человек, 61 пациент курил в прошлом и продолжает курить. Артериальная гипертония диагностирована у 92 больных, ожирение — у 26. ИМ перенесли 54 пациентов, у 19 в анамнезе была операция коронарного шунтирования (КШ), у 24 — чрескожные коронарные вмешательства (ЧКВ). После включения в исследование 2 пациента были направлены на плановую операцию КШ, которая была проведена после завершения участия в нашем исследовании, 30 пациентам проведено ЧКВ после включения в исследование. Функциональный класс (ФК) стенокардии у пациентов оценивали на этапе включения в исследование: I ФК — у 4, II ФК — у 49, III ФК — у 47. По данным КГ у 26 больных выявлен гемодинамически значимый стеноз одной магистральной коронарной артерии, у 38 больных — 2 артерий и у 36 — 3 коронарных артерий. У 7 пациентов выявлен стеноз ствола левой коронарной артерии более 50%.
Достоверных различий между группами по возрасту, полу, степени ожирения, факторам риска, сопутствующим заболеваниям, выраженности стенокардии, тяжести поражения коронарного русла и показателям липидного состава крови не выявлено. По уровню ХС ЛНП было выявлено достоверное различие: в группе комбинированной терапии данный показатель был выше, чем в группе монотерапии: 4,02 (3,4; 4,8) и 3,68 (3,0; 4,1) ммоль/л соответственно (р=0,01).
В обеих группах концентрация Лп-ФЛА2 превысила физиологический уровень (>200 нг/мл) в 98% случаев, при этом медиана концентрации составила 351,89 и 352,97 нг/мл в группе комбинированной терапии и группе монотерапии соответственно. Достоверных различий между группами по концентрации Лп-ФЛА2 не выявлено. Большинство больных при включении в исследование получали терапию бисопрололом, аспирином, эналаприлом, 30% пациентов дополнительно получали клопидогрел, 23% — амлодипин, 19% — нитраты, 14% — индапамид. Достоверных различий между двумя группами по проводимой сопутствующей терапии не выявлено.
Образцы крови брали из локтевой вены утром натощак исходно и через 6—9 мес лечения. Кровь центрифугировали в течение 20 мин при 3000 об/мин. Полученные сыворотки хранили при температуре –70 °С до проведения анализа, но не более 2 лет. Определение концентрации общего ХС (ОХС), триглицеридов (ТГ), ХС ЛВП, активности аспартатаминотрансферазы, аланинаминотрансферазы, креатинкиназы в сыворотке крови производили ферментативным колориметрическим методом на анализаторе Architect-C 8000 («Abbott», CША) с использованием реактивов этой же фирмы. Содержание ХС ЛНП вычисляли по формуле Фридвальда: ХС ЛНП = ОХС – ХС ЛВП – ТГ/2,2 (ммоль/л).
Концентрацию (массу) Лп-ФЛА2 определяли в сыворотке крови с помощью «сэндвич»-метода иммуноферментного анализа с использованием двух высокоспецифичных моноклональных антител (The PLAC Test ELISA format, «DiaDexus», США), результаты выражали в нано-граммах на миллилитр [3, 32].
Статистическую обработку полученных данных проводили в соответствии со стандартными методами вариационной статистики. В таблицах полученные значения представлены в виде Мe (LQ; UQ), где Мe — медиана, LQ; UQ — межквартильный размах. Для проверки нормальности распределения количественных признаков использовали тесты Шапиро—Уилка. Достоверность различий всех параметров количественных признаков определяли с помощью парных и непарных методов анализа для непараметрических величин по критерию U Манна—Уитни для независимых групп и по Вилкоксону для зависимых параметров. Достоверность различий параметров качественных признаков оценивали с помощью двустороннего точного критерия Фишера. Для оценки взаимосвязи количественных признаков использовали метод ранговой корреляции по Спирмену. Для всех видов анализа различия считали статистически значимыми при р<0,05.
Результаты
Исследование завершили все включенные больные, по 50 человек в каждой из групп. Целевых уровней ХС ЛНП (<2,5 ммоль/л) достигли 46 (92%) больных из группы комбинированной терапии и 46 (92%) из группы монотерапии. Уровня ХС ЛНП <1,8 ммоль/л удалось достичь 13 (26%) больным из группы комбинированной терапии и 5 (10%) из группы монотерапии. Снизить уровень ХС ЛНП более чем на 50% удалось 26 (52%) больным из группы комбинированной терапии и 10 (20%) из группы монотерапии. Таким образом, целевых уровней ХС ЛНП, установленных согласно V пересмотру Российских рекомендаций по диагностике и коррекции нарушений липидного обмена с целью профилактики и лечения атеросклероза, достигли 39 (78%) пациентов из группы комбинированной терапии и 15 (30%) из группы монотерапии.
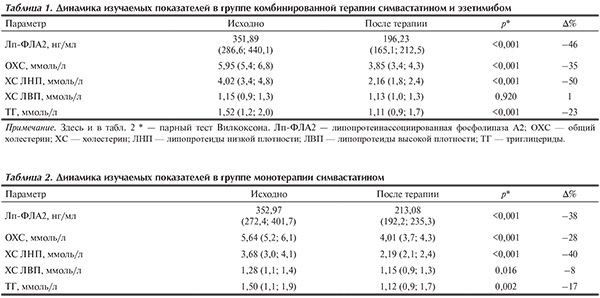
Динамика показателей липидного состава крови и Лп-ФЛА2 на фоне комбинированной терапии симвастатином и эзетимибом. В группе больных, получавших симвастатин с эзетимибом, отмечено достоверное снижение концентрации Лп-ФЛА2 с 351,89 (286,6; 440,1) до 196,23 (165,1; 212,5) нг/мл к 6-му месяцу терапии (–46%; р<0,001). По сравнению с исходными данными терапия симвастатином и эзетимибом привела к значимому снижению концентрации ОХС на 35% — c 5,95 (5,4; 6,8) до 3,85 (3,4; 4,3) ммоль/л (р<0,001), ХС ЛНП на 50% — с 4,02 (3,4; 4,8) до 2,16 (1,8; 2,4) ммоль/л (р<0,001), ТГ на 23% — с 1,52 (1,2; 2,0) ммоль/л до 1,11 (0,9; 1,7) ммоль/л к 6-му месяцу терапии (р<0,001; табл. 1).
Динамика показателей липидного состава крови и Лп-ФЛА2 на фоне монотерапии симвастатином. В группе монотерапии также отмечено статистически значимое снижение уровней Лп-ФЛА2 и показателей липидного состава крови. Концентрация Лп-ФЛА2 снизилась на 38% — с 352,97 (272,4; 401,7) до 213,08 (192,2; 235,3) нг/мл (р<0,001). Концентрация ОХС снизилась на 28% — с 5,64 (5,2; 6,1) до 4,01 (3,7; 4,3) ммоль/л (р<0,001), ХС ЛНП — на 40% — с 3,68 (3,0; 4,1) до 2,19 (2,1; 2,4) ммоль/л (р<0,001), ТГ на 17% — с 1,5 (1,1; 1,9) до 1,12 (0,9; 1,7) ммоль/л к 6 мес терапии (р=0,002; табл. 2).
При сравнении двух тактик гиполипидемической терапии выявлено, что концентрации Лп-ФЛА2, ОХС и ХС ЛНП в группе комбинированной терапии снизились в большей степени, чем в группе монотерапии. Так, снижение концентрации Лп-ФЛА2 составило 46% в группе комбинированного лечения против 38% в группе монотерапии (р=0,04). Уровень ОХС снизился на фоне комбинированной терапии на 35%, а на фоне монотерапии на 28% (р=0,003). Снижение концентрации ХС ЛНП на фоне комбинированной терапии составило 50% против 40% на фоне монотерапии симвастатином (р<0,001).
Динамика показателей липидного состава крови и Лп-ФЛА2 на фоне комбинированной терапии симвастатином и эзетимибом в зависимости от дозы симвастатина.
В группе комбинированной терапии симвастатин в дозе 20 мг/сут принимали 37 пациентов, увеличение дозы симвастатина до 40 мг/сут потребовалось 10 пациентам и до 80 мг/сут — 3 пациентам. Средняя доза симвастатина по группе составила 27,6 мг/сут, медиана и квартили 20 (20; 40) мг/сут.
В группе комбинированной терапии не выявлено статистически значимых различий по влиянию на концентрацию Лп-ФЛА2 и показатели липидного состава крови разных доз симвастатина (20 или 40 мг/сут), входящих в комбинацию (р>0,1).
Комбинированная терапия с симвастатином 20, 40 и 80 мг/сут одинаково снижала концентрацию Лп-ФЛА2 на 43—45%. При проведении комбинированной терапии с возрастанием дозы симвастатина от 20 до 40—80 мг/сут уровень ОХС снижался на 33—40%, ХС ЛНП на 49—55%. Однако полученные различия статистически незначимы. Таким образом, дозозависимого влияния комбинированной терапии симвастатином и эзетимибом на концентрацию Лп-ФЛА2 и показатели липидного состава крови (ОХС, ХС ЛНП) не выявлено.
Динамика показателей липидного состава крови и Лп-ФЛА2 на фоне монотерапии симвастатином в зависимости от подобранной дозы препарата. В группе монотерапии симвастатин в дозе 20 мг/сут принимали 2 пациента, увеличение дозы симвастатина до 40 мг/сут потребовалось 29 и до 80 мг/сут — 19 пациентам. Средняя доза симвастатина по группе составила 54,4 мг/сут, медиана и квартили — 40 (40; 80) мг/сут.
После лечения выявлено, что максимальное снижение концентрации Лп-ФЛА2 на 49% (до 207 нг/мл) зафиксировано на фоне терапии симвастатином 80 мг/сут, минимальное снижение концентрации Лп-ФЛА2 на 29% (до 220 нг/мл) — на фоне терапии симвастатином 40 мг/сут, в группе монотерапии симвастатином 20 мг/сут концентрация Лп-ФЛА2 снизилась на 35% (до 213 нг/мл).
Максимальное снижение уровней ОХС и ХС ЛНП зафиксировано в группе симвастатина 80 мг/сут и составило для ОХС 37% и для ХС ЛНП 45%. В группе терапии симвастатином 40 мг/сут снижение составило 26 и 39% соответственно, в группе симвастатина 20 мг/сут — 8 и 22% соответственно. Уровни ОХС после лечения составили 4,45, 3,99 и 4,19 ммоль/л, уровни ХС ЛНП — 2,615, 2,16 и 2,32 ммоль/л соответственно возрастанию доз симвастатина 20, 40 и 80 мг/сут.
Таким образом, на фоне монотерапии симвастатином выявлен достоверный дозозависимый эффект.
В плане снижения концентрации Лп-ФЛА2 и показателей липидного состава крови (ОХС и ХС ЛНП) монотерапия симвастатином 80 мг/сут оказалась более эффективной, чем монотерапия симвастатином 40 мг/сут.
Достоверных различий по влиянию различных доз симвастатина на уровень ХС ЛВП и ТГ не выявлено.
Сравнение двух тактик гиполипидемической терапии. При сравнении комбинированной терапии симвастатином и эзетимибом и монотерапии симвастатином получены следующие результаты. На фоне комбинированной терапии симвастатином 20 мг/сут выявлено достоверно большее, чем на фоне монотерапии симвастатином 40 мг/сут, снижение концентраций Лп-ФЛА2, ОХС и ХС ЛНП. Концентрация Лп-ФЛА2 в группе комбинированной терапии снизилась на 45% (с 387,17 до 204,5 нг/мл) против 29% (с 319,76 до 220,3 нг/мл; p=0,003) в группе монотерапии. Концентрация ОХС снизилась в группе комбинированной терапии с симвастатином 20 мг/сут на 33% (с 5,84 до 3,84 ммоль/л) против 26% (с 5,36 до 3,99 ммоль/л; р=0,001) в группе монотерапии с симвастатином 40 мг/сут. Концентрация ХС ЛНП в группе комбинированной терапии с симвастатином 20 мг/сут снизилась на 50% (с 3,86 до 2,1 ммоль/л), в группе монотерапии с симвастатином 40 мг/сут снижение ХС ЛНП составило 39% (с 3,25 ммоль/л до 2,16 ммоль/л; p<0,001).
При сравнении начальной дозы симвастатина 20 мг/сут в группе комбинированной терапии с максимальной дозой симвастатина 80 мг/сут в группе монотерапии статистически значимые различия по влиянию препаратов на концентрацию Лп-ФЛА2, ОХС и ХС ЛНП нивелировались.
При сравнении влияния комбинированной терапии с симвастатином 40 мг/сут и монотерапии с симвастатином 80 мг/сут на показатели липидного состава крови и Лп-ФЛА2 достоверных различий между этими двумя группами не выявлено. Определена достоверная корреляция между исходной концентрацией Лп-ФЛА2 и ОХС (r=0,28), ХС ЛНП (r=0,33).
Обсуждение
Ввиду того что в большинстве исследований установлена связь между повышенной концентрацией Лп-ФЛА2 и риском развития сердечно-сосудистых осложнений [33—42], в настоящее время активно изучается эффективность снижения активности данного маркера [43, 44]. Информация о том, что гиполипидемические препараты, в частности статины, снижают концентрацию Лп-ФЛА2, свидетельствует о том, что Лп-ФЛА2 можно рассматривать как мишень для действия терапии с целью подавления процессов воспаления и достижения стабилизации атеросклеротической бляшки [25].
Результаты нашего исследования показали, что терапия статинами не только дает гиполипидемический эффект, но и приводит к значительному снижению концентрации Лп-ФЛА2 у пациентов с ИБС. Оба эти эффекта в группе комбинированной терапии симвастатином и эзетимибом были выражены сильнее, чем в группе монотерапии симвастатином. Так, в группе комбинированной терапии снижение концентрации Лп-ФЛА2 составило 46% против 38% в группе монотерапии, снижение уровня ОХС — 35% против 28%, уровня ХС ЛНП — 50% против 40%.
В работах, в которых оценивалось влияние статинов на концентрацию Лп-ФЛА2, получены следующие результаты: в исследовании WOSCOPS у пациентов с ИБС правастатин 40 мг/сут по сравнению с плацебо снижал концентрацию Лп-ФЛА2 на 17%, а концентрацию ХС ЛНП на 24% [26]. В исследовании М.А. Albert и соавт. [18] правастатин 40 мг/сут снижал концентрацию Лп-ФЛА2 и ХС ЛНП на 22% у пациентов без ССЗ.
В исследовании Heart Protection Study монотерапия симвастатином 40 мг/сут снижала концентрацию Лп-ФЛА2 на 27% и ХС ЛНП на 41% [27]. По данным E. Schaefer и соавт. [19], монотерапия аторвастатином 40 мг/сут у 84 пациентов снижала концентрацию Лп-ФЛА2 на 26% и ХС ЛНП на 48%. В этой же работе монотерапия симвастатином 20—40 мг/сут у 16 пациентов снижала концентрацию Лп-ФЛА2 на 10% и ЛНП на 37%.
В исследовании MIRACLE по сравнению с плацебо монотерапия аторвастатином 80 мг/сут у 1264 пациентов приводила к снижению концентрации Лп-ФЛА2 на 35,8% [28]. На базе исследования JUPITER показано, что монотерапия розувастатином 20 мг/сут у 8901 пациента без признаков ССЗ снижает концентрацию Лп-ФЛА2 на 33,8% и ХС ЛНП на 48,7% [29]. В исследовании V. Saougos и соавт. [22] выявлено снижение концентрации Лп-ФЛА2 на 28% и ХС ЛНП на 35% на фоне терапии розувастатином 10 мг/сут у 50 пациентов с гиперлипидемией IIА. В этой же работе продемонстрировано, что монотерапия эзетимибом снижает концентрацию Лп-ФЛА2 на 18% и ХС ЛНП на 17% у других 50 пациентов с гиперлипидемией IIA.
Согласно представленной информации по влиянию статинов на концентрацию ХС ЛНП, наша работа согласуется с данными мировой литературы, а вот по влиянию на концентрацию Лп-ФЛА2 результаты расходятся: в нашей работе выявлено более значительное снижение концентрации Лп-ФЛА2 на фоне как монотерапии, так и комбинированной терапии. Мы предположили, что подобный результат связан с тем, что в нашей работе приняли участие пациенты с более высокой концентрацией Лп-ФЛА2. У пациентов из представленных выше исследований уровень Лп-ФЛА2 был заметно ниже и редко превышал 320 нг/мл. Подтверждение нашей гипотезе мы нашли в работе J. Muhlestein и соавт. [30], в которой показано, что противовоспалительные плейотропные эффекты симвастатина зависят от степени повышения маркеров воспаления до начала терапии. Так, симвастатин 20 мг/сут снижал концентрацию Лп-ФЛА2 на 34,5%, ХС ЛНП на 34% и С-реактивного белка (СРБ) на 16% в группе из 100 пациентов с сахарным диабетом 2-го типа и гиперлипидемией. В подгруппах пациентов с медианой концентрации Лп-ФЛА2 320,9 нг/мл и более или уровнем СРБ >2 мг/дл выявлено достоверно более выраженное снижение маркеров воспаления. На фоне терапии симвастатином 20 мг/сут концентрация Лп-ФЛА2 снизилась на 47,5%, а уровень СРБ на 24,8% [30]. Таким образом, комбинированная терапия является более эффективной в плане снижения концентрации Лп-ФЛА2 и показателей липидного состава крови (ОХС и ХС ЛНП).
В ходе проведения комбинированной терапии симвастатином и эзетимибом дозозависимого влияния на концентрацию Лп-ФЛА2 и показателей липидного профиля (ОХС, ХС ЛНП) не выявлено. При монотерапии симвастатином достоверный дозозависимый эффект препарата выявлен не только по показателям липидного состава крови (ОХС, ХС ЛНП), но и по влиянию на концентрацию Лп-ФЛА2. На фоне монотерапии симвастатином концентрация Лп-ФЛА2 в большей степени снижалась в группе больных, получавших 80 мг/сут препарата (на 49%), в меньшей степени в группе пациентов, получавших 40 мг/сут препарата (на 29%), а у пациентов, принимавших 20 мг/сут симвастатина, концентрация Лп-ФЛА2 снизилась на 35%. По-видимому, это связано с малым числом пациентов в данной группе (n=2), что затрудняет прямое сравнение. У пациентов, находившихся на монотерапии симвастатином в дозе 20, 40 и 80 мг/сут, уровень ОХС снизился на 8, 26 и 37%, а уровень ХС ЛНП — на 22, 39 и 45% соответственно.
При сопоставлении двух тактик гиполипидемической терапии выявлено, что комбинированная терапия с начальной дозой симвастатина 20 мг/сут по влиянию на концентрацию Лп-ФЛА2, ОХС и ХС ЛНП так же эффективна, как монотерапия симвастатином в максимальной суточной дозе 80 мг/сут. На фоне комбинированной терапии с симвастатином 20 мг/сут выявлено достоверно более выраженное, чем на фоне монотерапии симвастатином 40 мг/сут, снижение концентрации Лп-ФЛА2, ОХС и ХС ЛНП. При сравнении влияния комбинированной терапии с симвастатином 40 мг/сут и монотерапии с симвастатином 80 мг/сут на показатели липидного состава крови и Лп-ФЛА2 достоверных различий между этими двумя группами не выявлено. Показано, что удвоение дозы статина обеспечивает дополнительное снижение содержания ХС ЛНП на 6% [31, 45, 46]. Комбинация симвастатина и эзетимиба по 10 мг значительно эффективнее снижала уровень ХС ЛНП, чем монотерапия симвастатином по 10, 20 и 40 мг. Если комбинированная терапия малыми дозами этих препаратов сразу снизила уровень ХС ЛНП на 46%, то при монотерапии симвастатином и последовательном назначении по 10, 20, 40 и 80 мг/сут соответствующее снижение ХС ЛНП составило 27, 37, 38 и 45% (p<0,01) [23]. Лечение эзетимибом 10 мг и симвастатином 10 мг оказалось столь же эффективным в плане снижения уровня ХС ЛНП, как и монотерапия симвастатином в дозе 80 мг, и более эффективным, чем монотерапия этим статином в дозах 10, 20 и 40 мг/сут (p<0,01). При комбинированной терапии с дозой симвастатина 10, 20, 40 или 80 мг уровень ХС ЛНП снизился на 44, 45, 53 и 57%, тогда как при лечении только симвастатином в дозах 10, 20, 40 и 80 мг снижение уровня ХС ЛНП составило соответственно 27, 36, 36 и 44% [47].
С. Ballantyne и соавт. [48] сравнивали эффективность комбинации эзетимиба 10 мг и симвастатина 80 мг с монотерапией аторвастатином 80 мг. Комбинация оказалась эффективнее: уровень ХС ЛНП снизился соответственно на 59,4 и 52,5% (p<0,001), а содержание ХС ЛВП повысилось на 12,3 и 6,5% (p<0,001).
Данные по корреляции согласуются с данными мировой литературы. Так, в наиболее крупных исследованиях по изучению прогностического значения Лп-ФЛА2 были получены следующие результаты: максимальная корреляция Лп-ФЛА2 и ХС ЛНП (r=0,51) получена в исследовании Women’s Health Study [49]. В других известных исследованиях получены примерно одинаковые результаты, выявлена слабая корреляция концентрации Лп-ФЛА2 с показателями липидного состава крови (ХС ЛНП, ОХС), в случае с ХС ЛВП в ряде работ корреляция отсутствует, а в некоторых работах выявляется слабая отрицательная корреляция [7, 17, 24, 40, 42, 50]. Корреляцию уровня Лп-ФЛА2 и ХС ЛНП, как правило, объясняют тем фактом, что 80% циркулирующей в крови Лп-ФЛА2 связано с ХС ЛНП [3, 26].
Таким образом, нами впервые в мире в рамках рандомизированного клинического исследования у больных ИБС показано, что применение эзетимиба 10 мг/сут в комбинации со стандартной дозой симвастатина способствует значимому снижению не только показателей липидного состава крови, но и важного маркера внутрисосудистого воспаления Лп-ФЛА2. При этом показано, что максимальное снижение активности Лп-ФЛА2 достигалось уже при приеме начальной дозы комбинированной терапии и не носило дозозависимого эффекта. Начальная доза комбинированной терапии сопоставима по эффективности с максимальной дозой монотерапии симвастатином. В целом в группе комбинированной терапии получен более значимый противовоспалительный и гиполипидемический эффект с использованием в 2 раза меньшей средней дозы симвастатина, чем в группе монотерапии.
Понимание механизмов, посредством которых гиполипидемические препараты оказывают влияние на течение ИБС, важно для формирования лечебных подходов к ведению больных. Полученные нами данные по влиянию комбинированной терапии эзетимибом и симвастатином на концентрацию маркера внутрисосудистого воспаления могут быть учтены при разработке новых методов лечения больных ИБС.
Выводы
- У больных ишемической болезнью сердца комбинация эзетимиба с симвастатином приводит к достоверно более выраженному снижению уровней липопротеинассоциированной фосфолипазы А2, общего холестерина и холестерина липопротеидов низкой плотности по сравнению с монотерапией симвастатином через 6 мес терапии: снижение концентрации липопротеинассоциированной фосфолипазы А2 составило 46% против 38%, общего холестерина — 35% против 28%, холестерина липопротеидов низкой плотности — 50% против 40% соответственно.
- Комбинированная терапия эзетимибом и симвастатином 20 и 40 мг/сут оказалась одинаково эффективной по влиянию на концентрацию липопротеинассоциированной фосфолипазы А2 и общего холестерина, холестерина липопротеидов низкой плотности. При этом монотерапия симвастатином 80 мг/сут приводила к более выраженному, чем монотерапия симвастатином 40 мг/сут, снижению концентрации липопротеинассоциированной фосфолипазы А2 и общего холестерина, холестерина липопротеидов низкой плотности.
- Комбинированная терапия эзетимибом и симастатином 20 и 40 мг/сут оказалась столь же эффективной по влиянию на концентрацию липопротеинассоциированной фосфолипазы А2 и показатели липидного профиля, как монотерапия симвастатином 80 мг/сут.



