В мире насчитывают около 23 млн пациентов, страдающих хронической сердечной недостаточностью (ХСН), их число продолжает неуклонно расти.
В настоящее время декомпенсация ХСН является частой причиной госпитализации [1]. Известно, что ХСН сочетается со многими заболеваниями и синдромами, которые оказывают как самостоятельное, так и сочетанное в комбинации с основным заболеванием влияние на частоту повторных госпитализаций и смертность. Выявление предикторов с наиболее значимым влиянием на частоту развития летальных исходов позволило бы на ранних этапах декомпенсации кровообращения определиться с прогнозом и корригировать терапию [2].
 Целью настоящего исследования явилось изучение влияния различных сопутствующих заболеваний и симптомов, формирующих фенотип пациентов, на прогноз при декомпенсации систолической ХСН.
Целью настоящего исследования явилось изучение влияния различных сопутствующих заболеваний и симптомов, формирующих фенотип пациентов, на прогноз при декомпенсации систолической ХСН.
Материал и методы
Проанализирована база данных «Павловского регистра» [3]. Регистр сформирован в 2009 г. и включает 1001 пациента с декомпенсацией ХСН. Проанализирован период наблюдения сроком 1 год с контрольными точками на 30-й, 90, 180 и 360-й дни со дня выписки. Клиническая характеристика пациентов представлена в табл. 1.
Критерии включения в исследование: возраст >18 лет,наличие систолической ХСН, причина госпитализации — декомпенсация ХСН, скорость клубочковой фильтрации (СКФ) по формуле MDRD>15 мл/мин/1,73 м2. Критерии исключения: алкогольная кардиомиопатия, фракция выброса (ФВ) левого желудочка (ЛЖ) >40%.
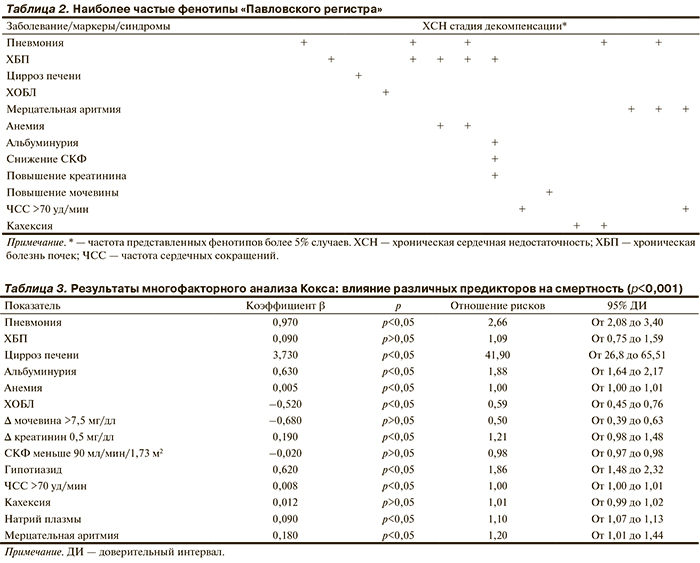
Характеристика групп больных. Анализ «Павловского регистра» показал, что наиболее частые сочетания декомпенсации кровообращения и какого-либо заболевания или синдрома, или лабораторного показателя являются параметры, приведенные в табл. 2. Таким образом, самыми частыми фенотипами являются сочетания ХСН+пневмония+хроническая болезнь почек (ХБП).
С целью выделения наиболее значимых предикторов смертности у больных ХСН построена модель пропорциональных рисков Кокса с зависящими от времени ковариатами (табл. 3). Согласно представленным данным, модель является достоверной (p<0,001), наиболее значимыми оказались следующие предикторы (значимость указана в порядке убывания): цирроз печени, пневмония, альбуминурия, прием тиазидного диуретика на догоспитальном этапе, мерцательная аритмия постоянной формы, повышение уровня креатинина и натрия в плазме крови на этапе госпитализация-выписка, наличие ХБП, дефицит тощей массы тела (кахексия), исходный уровень гемоглобина <110 г/л, частота сердечных сокращений (ЧСС) >70 уд/мин на момент выписки.
Проанализировано влияние комбинации предикторов на смертность в течение года. Анализ позволил выявить комбинации предикторов, оказывающих преимущественное влияние на ранний прогноз (в течение первых 6 мес), поздний прогноз (после 6 мес) и оказывающие одинаковое влияние на всем этапе наблюдения.
Статистическую обработку полученных данных проводили с помощью программного обеспечения Statistica 10.0. Нормальность распределения определялась с помощью критерия Шапиро—Уилка. Использовали методы непараметрической и параметрической статистики. Количественные показатели представлены в виде среднего значения (M)±стандартное отклонение (S). Проводили многофакторный анализ с помощью модели пропорциональных рисков Кокса. Анализ выживаемости выполняли с помощью метода Каплана—Мейера. Статистически значимыми признавали различия при р<0,05.
Результаты
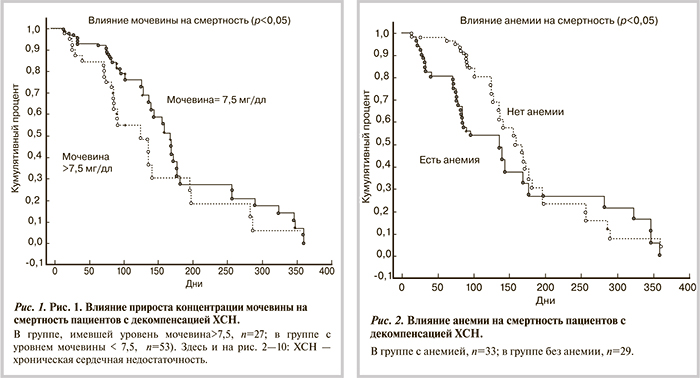
Ранние предикторы смертности. Анализ влияния прироста концентрации мочевины на этапе госпитализация-выписка на смертность пациентов с декомпенсацией ХСН (рис. 1) показал, что смертность начинает повышаться с 30-го дня после выписки из стационара, значимость влияния сохраняется до 150-го дня наблюдения. Бόльшая часть летальных исходов (48%) приходилась на период от 3 до 6 мес; 24% смертей приходилось на период до 60-го дня наблюдения. Менее значимым оказался период после 6 мес наблюдения, так как смертность в этот период составила 28%.
При изучении влияния анемии (исходный уровень гемоглобина <110 г/л) на смертность пациентов с декомпенсацией ХСН (рис. 2) показано, что снижение уровня гемоглобина также является ранним предиктором смерти таких пациентов. Как можно видеть из рисунка, расхождение кривых смертности начинается с первых дней от момента выписки и продолжается вплоть до 150-го дня наблюдения. Наиболее значительным уровень смертности оказался в первые 30 дней после выписки, составив 20%. Примерно тот же уровень смертности (25%) сохранялся в период с 60-го по 90-й день наблюдения. На последующих этапах наблюдения число летальных исходов было существенно меньше. С 200-го дня наблюдения отмечался рост смертности у пациентов без исходной анемии.
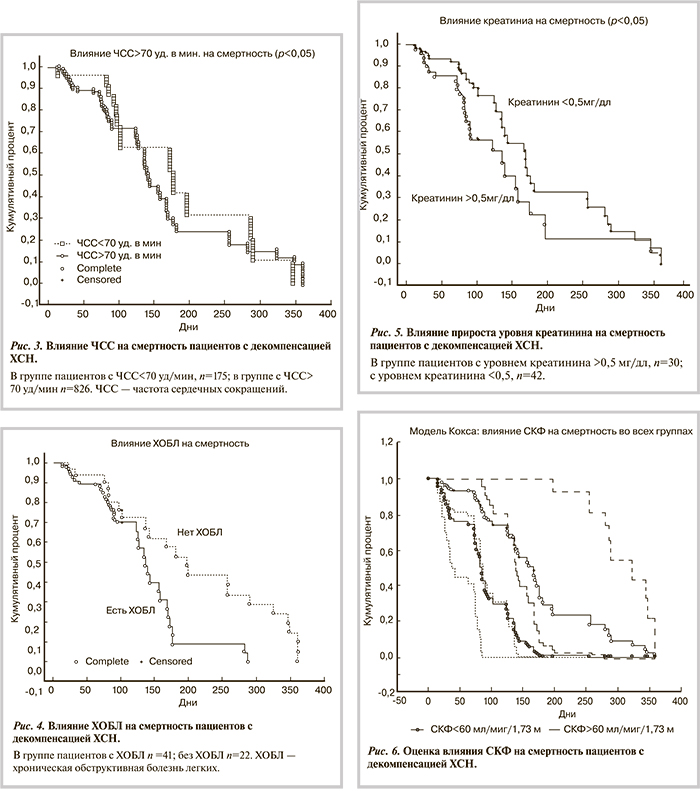
Анализ ЧСС показал, что у пациентов с ЧСС>70 уд/мин на момент выписки смертность существенно выше, чем у пациентов, имевших ЧСС<70 уд/мин (рис. 3). Как можно видеть из рисунка, кривая смертности начинает расходиться сразу же с момента выписки из стационара и продолжает нарастать до 90-го дня наблюдения (20%).
В последующий период анализируемые кривые пересекаются, что позволяет предполагать существенный вклад иных факторов.
Поздние предикторы. Анализ двух групп пациентов, страдающих хронической обструктивной болезнью легких — ХОБЛ (использующих комбинированную ингаляционную терапию: глюкокортикостероид+β2-агонисты), и без ХОБЛ приведен на рис. 4. Представленные данные свидетельствуют о том, что до 100-го дня наблюдения достоверных различий в группах нет. В последующем смертность возрастает в группе пациентов, использующих ингаляционную терапию, достоверность различий наступает со 170-го дня наблюдения.
Предикторы, влияющие на всем протяжении периода наблюдения. Анализ влияния уровня креатинина (прирост креатинина >0,5 мг/дл на этапе госпитализация-выписка) приведен на рис. 5. Данные показывают, что смертность в когорте пациентов с приростом уровня креатинина была достоверно выше на всем протяжении наблюдения. При этом 42% летальных исходов приходилось на первые 90 дней наблюдения.
Анализ влияния уровня СКФ на смертность приведен на рис. 6. Согласно полученным данным, в когорте пациентов с СКФ<60 мл/мин/1,73 м2 смертность достоверно выше на всем протяжении наблюдения. Следует отметить, что в первые 180 дней этот предиктор имел наибольшую значимость, в последующие 180 дней достоверность различий сохранялась, однако влияние предиктора ослабло. Анализ доверительных интервалов (ДИ) в обеих группах выявил их пересечения, что, несомненно, снижает ценность этого предиктора.
Анализ влияния дефицита тощей массы тела (>10% от должной) приведен на рис. 7. В когорте пациентов, имеющих дефицит тощей массы тела, летальный исход развивался достоверно чаще, чем у пациентов без дефицита на всем протяжении наблюдения. Наибольшее число летальных исходов (69%) отмечено в первые 180 дней наблюдения. В последующий период наблюдения роль предиктора сохранялась, однако его значение ослабло.
Роль комбинаций предикторов (фенотипы пациентов). Анализ комбинаций перечисленных предикторов показал, что самыми значимыми являются следующие фенотипы: ХСН+ХБП+пневмония, ХСН+пневмония, ХСН+цирроз печени, ХСН+ХБП+альбуминурия.
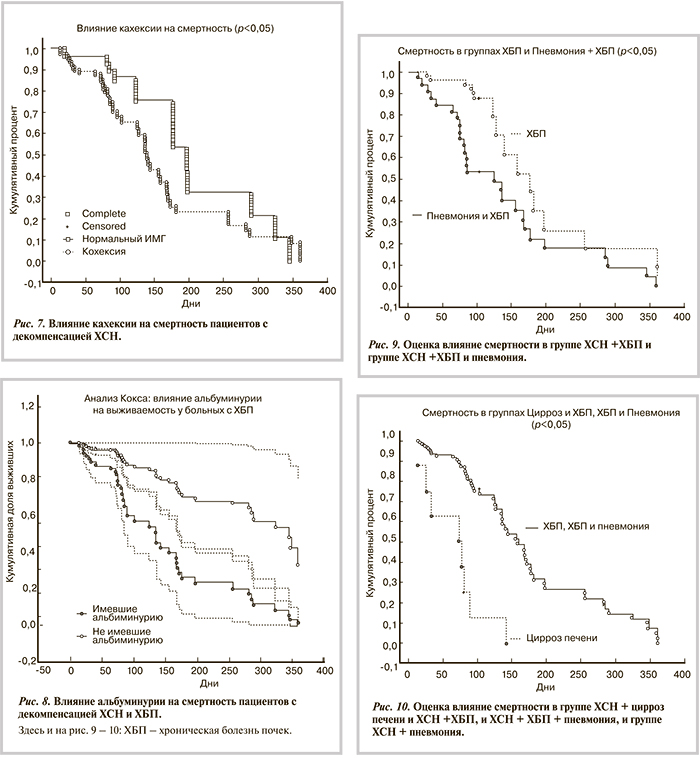
Анализ данных пациентов с фенотипом ХСН+ХБП+альбуминурия (>30 мг/сут и <30 мг/сут) показал, что наличие такого фенотипа достоверно увеличивает риск развития летального исхода на всем протяжении наблюдения (рис. 8).
Анализ смертности в когорте пациентов с фенотипом ХСН+ХБП+пневмония (рис. 9) показал, что риск смерти достоверно выше за весь период наблюдения. Следует отметить, что риск смерти у пациентов, получавших гидрохлоротиазид на догоспитальном этапе был достоверно выше, чем у пациентов, получавших петлевой диуретик торасемид. Анализ смертности у пациентов с фенотипом ХСН+пневмония показал, что фенотип ХСН+пневмония также влиял на риск развития летального исхода (сравнение с пациентами, страдавшими ХСН без пневмонии, так и имевшими фенотип ХСН+ХБП+пневмония), однако отношение риска (ОР) при этом фенотипе составляло 1,01, а при фенотипах сравнения — 0,8 и 2,3 соответственно.
Анализ смертности в когорте пациентов с фенотипом декомпенсация ХСН+цирроз печени (рис. 10) показал, что риск смерти у них был наибольшим из всех изучаемых фенотипов.
Обсуждение
Анализ предикторов смертности показал, что некоторые из них наиболее значимы в ранний период декомпенсации кровообращения, другие сохраняют свое значение на более поздних этапах, третьи — на протяжении всего периода наблюдения длительностью 1 год. К числу ранних относится уровень мочевины: по нашим данным, прогностическое значение имеет прирост концентрации мочевины более 7,5 мг/дл (1,2 ммоль/л). Так, в исследование D. Aronson и соавт. был включен 541 пациент с ХСН в состоянии декомпенсации, в течение периода наблюдения, равного 343±185 дней, 177 (33%) пациентов умерли. В результате проведенного анализа авторы пришли к выводу, что ОР смерти составило 2,3 (при 95% ДИ от 1,3 до 4,1; p<0,05), ОР повышения концентрации мочевины крови составило 2,3 при 95% ДИ от 1,4 до 3,8; p=0,0007 [3].
Однако в нашем исследовании изучался не исходный уровень мочевины, а динамика этого показателя. Прирост концентрации мочевины свидетельствует о функции не только почек, но и печени, что, по нашему мнению, более значимо [4]. В нашем исследовании показано, что именно прирост концентрации мочевины, а не исходный уровень обладает большей прогностической ролью.
СКФ оказывает сложное прогностическое влияние, так как ДИ пересекаются, что вызывает необходимость его совместного анализа с другими маркерами, например с альбуминурией. Наши данные во многом совпадают с данными исследования D.N. Reddan и соавт. [5], которые показали, что СКФ является независимым предиктором смерти у пациентов с ХСН: смертность начинала повышаться уже при СКФ <85 мл/мин. В этой группе пациентов дальнейшие снижение СКФ на 10 мл/мин увеличивало риск смерти на 14% (при 95% ДИ от 1,09 до 1,20; p<0,0001).
Исходный уровень креатинина обладает самостоятельной прогностической ролью. Так, в работе D.N. Reddan и соавт. показана прогностическая роль креатинина в отношении риска смерти: в группе с повышенным уровнем креатинина он был статистически значимо выше, чем в группе с нормальным уровнем креатинина (ОР 2,37 при 95%ДИ от 1,81 до 2,75; p<0,0001) [5]. Это также подтверждено в программе Euro Heart Failure Servey: по полученным данным, повышение уровня креатинина >150 ммоль/л встречается в 16% случаях, а ≥200 ммоль/л — в 7% [6]. По данным Канадского регистра, повышенный уровень креатинина ≥170 ммоль/л одинаково значимо влиял как на 30-дневную летальность — ОР 2,47 (при 95% ДИ от 1,84 до 3,29), так и на смертность через 1 год наблюдения — ОР 2,90 (при 95% ДИ от 2,33 до 3,63) [7]. Однако в нашей работе динамика уровня креатинина (более 0,5 мг/дл) показала бόльшую прогностическую значимость.
ХБП как интегральный показатель, объединяющий такие понятия, как альбуминурия, повышение уровня креатинина крови, многократно изучалось в мировой литературе. В исследовании A. Ahmed и соавт. из 7788 пациентов отобраны 3527 (45%) со СКФ <60 мл/мин. В исследовании показано, что у пациентов с ХБП риск смерти был достоверно выше (ОР 1,22 при 95% ДИ от 1,09 до 1,36; р<0,0001), причем это было справедливо как для диастолической дисфункции ЛЖ, так и для систолической ХСН [8].
Кроме того, одна из проблем состоит в том, что для расчета СКФ применяются разные методы. В настоящее время наибольшую роль, по данным М. Plischke и соавт., имеет CKD-EPI [9]. По данным K. Hebert и соавт., проводивших исследование в американской популяции амбулаторных пациентов с ХСН с ФВ ЛЖ<40% и СКФ <60 мл/мин/1,73 м2, риск смерти у пациентов с ХСН и ХБП составлял 2,4 (при 95% ДИ от 1,01 до 6,11; р=0,04) [10]. В российской популяции также показано, что наличие ХБП значимо влияло на смертность пациентов с систолической ХСН. По данным В.Н. Лариной и соавт., риск смерти у пожилых пациентов с ХСН, осложненной ХБП, составляет 0,29 [11].
Диагностика ХОБЛ у пациентов с ХСН на ранних этапах значительно затруднена в связи со сходством симптомов данных заболеваний. Кроме того, существует ряд факторов, которые влияют и на возникновение ХОБЛ, и на ХСН. Распространенность сочетания ХОБЛ и ХСН колеблется от 20 до 30%, по результатам различных исследований [12, 13]. По данным «Павловского регистра», у пациентов с ХОБЛ смертность составляет 30% к 150-му дню наблюдения, тогда как у пациентов без диагноза ХОБЛ — только к 250-му дню наблюдения. По данным канадского регистра, ХОБЛ, несомненно, вносит значительный вклад в увеличение смертности пациентов (отношение шансов 1,66 при 95% ДИ от 1,22 до 2,27; р=0,002) [7]. Однако неоднородность популяции пациентов с ХОБЛ затрудняет анализ этой группы. Анализ группы пациентов, использующих ингаляционные препараты, показал, что ХОБЛ оказывает влияние на отдаленный прогноз. Этот результат отличается от данных, приведенных в других исследованиях [14]. ХОБЛ оказывала прогностическое влияние независимо от выраженности нарушения функции внешнего дыхания, что, по-видимому, связано с более жестким отбором пациентов.
Как можно увидеть из приведенных результатов, одним из наиболее неблагоприятных, но при этом достаточно часто встречающихся фенотипов является сочетание ХСН, ХБП и пневмонии. По данным, полученным при анализе «Павловского регистра», сочетание ХБП и пневмонии встречается у 31% пациентов с декомпенсацией ХСН [3]. В Испании в крупном эпидемиологическом регистре, включающем 3800 человек, изучалось влияние пневмонии на смертность пациентов с ХБП [15].
Смертность у пациентов с ХБП в сочетании с пневмонией была почти в 2 раза выше, чем у пациентов с пневмонией без ХБП (15,8% против 8,3%), риск возникновения сердечно-сосудистых осложнений составлял 9,23 (при 95% ДИ от 1,39 до 61,1). Данные этого исследования подтверждают результаты, полученные в нашей работе: у пациентов с пневмонией и ХБП летальный исход наступал достоверно чаще и раньше, чем у больных с любыми другими фенотипами, кроме цирроза печени.
В нашем исследовании наличие цирроза печени оказалось самым значимым прогностическим фактором.
В Канадском регистре пациентов с декомпенсацией ХСН (n=4031) риск смерти пациентов с циррозом печени составлял 3,22 (при 95% ДИ от 1,08 до 9,65; p=0,04) [7].
Как следует из изложенного, одним из наиболее надежных предикторов смерти у пациентов с декомпенсацией ХСН являются маркеры поражения клубочкового аппарата почек, при этом недооценивается такая важная структура почек, как тубулоинтерстициальная ткань(ТИТ) — место приложения действия мочегонных препаратов [16]. Однако методом определения поражения ТИТ почек является натрийуретическая проба, но этот метод низко информативен при применении диуретиков, т.к. они значительно изменяют натрийурез. Несмотря на это снижение суточного натрийуреза менее 30 ммоль/л, бесспорно, свидетельствует о гиперволемическом расстройстве натриевого гомеостаза у пациентов с выраженной задержкой жидкости [17].
Так, в ряде исследований у пациентов с гипонатриемией изучалась и была доказана диагностическая ценность альтернативных маркеров низкого натрийуреза — мочевой кислоты [18]. Мочевая кислота является продуктом метаболизма пуринов, ее реабсорбция происходит в основном в проксимальным отделе петли Генле и никак не взаимодействует с диуретиками [18]. Предполагается, что реабсорбция уратов связана с реабсорцией натрия, хотя механизм этого до конца не изучен [19].
Заключение
Таким образом, классификация пациентов с декомпенсацией хронической сердечной недостаточностью по принципу фенотипов позволяет клиницисту на ранних этапах осуществлять прогностическую оценку.



