Патогенез сердечно-сосудистых заболеваний (ССЗ) является сложным и многофакторным процессом, при котором изменение сосудистой стенки выступает связующим звеном между действием факторов риска и поражением органов-мишеней. Результаты исследований, проведенных с применением биомолекулярных и генетических методов, позволило определить, что повреждение сосудистой стенки начинается с развития функциональных нарушений — дисфункции эндотелия (ДЭ). С развитием ДЭ патологический процесс в сосудистой стенке продолжает прогрессировать, способствуя формированию в ней структурных изменений — ремоделированию. Развитие ремоделирования определяет следующий структурный этап поражения сосуда [1]. Показано, что ремоделирование сосудов крупного калибра (повышение жесткости артерий) ассоциируется с повышенным риском развития CСЗ и сердечно-сосудистых осложнений [2]. Доказано, что структурные изменения сосудов микроциркуляторного русла вовлечены в патогенез развития гипертонической болезни, ишемической болезни сердца (ИБС), хронической сердечной недостаточности (ХСН) и сахарного диабета 2-го типа, ассоциируются с высоким риском развития ССЗ у здоровых лиц с факторами риска развития ССЗ и неблагоприятных исходов у пациентов с ССЗ атеросклеротического генеза [3]. ДЭ у пациентов с ХСН крупных периферических сосудов выступает независимым предиктором повторных госпитализаций по поводу декомпенсации ХСН, а также сердечной смерти. Отмечено повышение жесткости артериальной стенки у больных ХСН при сохраненной и сниженной фракции выброса (ФВ) левого желудочка (ЛЖ), которое коррелирует с тяжестью ХСН (уровень N-концевого предшественника мозгового натрийуретического пептида) и функциональным классом (ФК) стабильной стенокардии [4, 5].
 У больных ХСН отмечено снижение вазореактивности коронарных и периферических микрососудов [6—8]. Таким образом, в лечении пациентов с ССЗ особенно важно отдавать предпочтение тем препаратам, положительные воздействия которых на стенку сосудистого русла разных уровней с целью первичной профилактики поражения органов-мишеней ССЗ доказано.
У больных ХСН отмечено снижение вазореактивности коронарных и периферических микрососудов [6—8]. Таким образом, в лечении пациентов с ССЗ особенно важно отдавать предпочтение тем препаратам, положительные воздействия которых на стенку сосудистого русла разных уровней с целью первичной профилактики поражения органов-мишеней ССЗ доказано.
Согласно рекомендациям ВНОК, ингибиторы ангиотензинпревращающего фермента (АПФ) являются препаратами первого ряда в лечении больных артериальной гипертонией, ХСН. Среди ингибиторов АПФ самая большая доказательная база накоплена для периндоприла [9—13]. Таким образом, целью нашего исследования явилась оценка структурно-функциональных показателей артериального русла у пациентов с ХСН и их динамики через 6 мес лечения периндоприлом А (престариумом А).
Материал и методы
Обследованы 30 больных ХСН II— III ФК по классификации NYHA. Исследование проводилось на базе отделения кардиологии №1 УКБ №1 ГБОУ ВПО Первый МГМУ им. И.М. Сеченова Минздрава России, госпитализированных в отделение кардиологии №1 УКБ №1 ГБОУ ВПО Первый МГМУ им. И.М. Сеченова Минздрава России в период с 2012 по 2013 г. Протокол исследования был одобрен межвузовским комитетом по этике при Ассоциации медицинских и фармацевтических вузов.
Средний возраст больных составил 65 (61; 72) лет (от 45 до 70 лет), из них 20 (71%) мужчин и 8 (29%)женщин. Больные имели избыточную массу тела: средний индекс массы тела (ИМТ) — 27,7 кг/м2 (25,3; 30,8). Средний уровень общего холестерина составил 5 (4,0; 5,9) ммоль/л, триглицеридов — 1,6 (1,23; 2,9) ммоль/л, липопротеидов низкой плотности — 3,5 (2,5; 4) ммоль/л, глюкозы 5 (4,6; 5,5) ммоль/л. Гипертоническая болезнь (ГБ) в анамнезе выявлена у 30 (100%) больных, средняя длительность которой составила 6 (2,5; 17) лет.
ГБ преимущественно II степени повышения АД была у 17 (56%), I степень — у 8 (27%), III степень — у 5 (17%) больных. Средняя длительность стенокардии у больных группы ХСН составила 10 (5; 17) лет. При этом II ФК стенокардии отмечен у 24 (80%), III ФК — у 6 (20%) пациентов. У 21 (70%) пациента имелся инфаркт миокарда (ИМ) в анамнезе. Средняя длительность ХСН составила 6 (3; 9) лет. Средняя ФВ ЛЖ достигала 46 (44; 49)%.
 По ФК ХСН больные распределялись следующим образом: ФК II — у 18 (60%), ФК III — у 12 (40%). Сахарный диабет имелся у 7 (23%) пациентов, при этом средняя длительность СД 2-го типа составила 8 (7; 14) лет (табл. 1).
По ФК ХСН больные распределялись следующим образом: ФК II — у 18 (60%), ФК III — у 12 (40%). Сахарный диабет имелся у 7 (23%) пациентов, при этом средняя длительность СД 2-го типа составила 8 (7; 14) лет (табл. 1).
Все пациенты получали необходимую терапию основного заболевания, согласно российским рекомендациям ВНОК: ингибиторы АПФ или сартаны, β-адреноблокаторы, антиагреганты, статины, блокаторы медленных кальциевых каналов.
Дизайн исследования. Проведено открытое неконтролируемое исследование. До включения в исследование больные ХСН проходили обследование и лечение в условиях кардиологического отделения: физикальный осмотр, определение клинико-функционального состояния (тест с 6-минутной ходьбой, Миннесотский опросник качества жизни, шкала оценки клинического состояния по В.Ю. Марееву), стандартное лабораторно-инструментальное обследование больных ХСН. Пациенты с СД 2-го типа были обследованы в эндокринологическом стационаре для верификации диагноза и подбора гипогликемической терапии. Критерии включения: мужчины и женщины от 45 до 70 лет, ХСН ишемического генеза II—III ФК по классификации NYHA (нарушение систолической ФВ ЛЖ<50%) и диастолической (E/A<1) функции ЛЖ; СД 2-го типа, информированное согласие пациента на исследование. Критерии исключения: нестабильная стенокардия, декомпенсация ХСН, клапанные пороки сердца, некоронарогенные заболевания миокарда, постоянная форма фибрилляции предсердий, тяжелые заболевания печени и почек, онкологические заболевания, хронические вирусные и бактериальные инфекции. Всем участникам на этапе включения для оценки состояния сосудистого русла стенки крупных сосудов проводили фотоплетизмографию (ФПГ) и дуплексное сканирование плечевой артерии — ПА (1-я точка). Затем пациенты, которые находились на терапии другими ингибиторами АПФ, были переведены на периндоприл А в дозе 5 мг с последующей титрацией дозы до 10 мг при хорошей переносимости. Пациенты, которые ранее получали периндоприл А в дозе 5 мг, были переведены на периндоприл А в дозе 10 мг. Таким образом, 63% (n=19) пациентов получали престариум в дозе 10 мг и 37% (n=11) — в дозе 5 мг в течение 6 мес. Из исследования выбыли 2 пациента в связи с развитием кашля. Через 6 мес терапии периндоприлом А выполняли повторную оценку ДЭ и ремоделирования крупных сосудов (2-я точка).
 Для оценки структурно-функционального состояния стенки крупных сосудов (аорта, ПА, лучевая артерии) использован метод ФПГ — аппарат Ангиоскан-01 («Ангиоскан», Россия). Проводили контурный анализ пульсовой волны, оценку амплитуды пульсовой волны до и после пробы с реактивной гиперемией — РГ (нагнетание воздуха в манжету до 220 мм рт.ст. на 5 мин). Исследовали параметры ремоделирования стенки крупных сосудов (индекс жесткости, SI). Для определения функции эндотелия выполнялась проба с РГ. О функции эндотелия крупных сосудов судили по параметру сдвиг фаз (СФ).
Для оценки структурно-функционального состояния стенки крупных сосудов (аорта, ПА, лучевая артерии) использован метод ФПГ — аппарат Ангиоскан-01 («Ангиоскан», Россия). Проводили контурный анализ пульсовой волны, оценку амплитуды пульсовой волны до и после пробы с реактивной гиперемией — РГ (нагнетание воздуха в манжету до 220 мм рт.ст. на 5 мин). Исследовали параметры ремоделирования стенки крупных сосудов (индекс жесткости, SI). Для определения функции эндотелия выполнялась проба с РГ. О функции эндотелия крупных сосудов судили по параметру сдвиг фаз (СФ).
Дуплексное сканирование ПА выполняли на аппарате HDI 5000 в ходе проведения пробы с РГ, вызванной окклюзией ПА в течение 5 мин (по методу D. Celermajer) [14].
Определяли эндотелийзависимую вазодилатацию (ЭЗВД). Статистическую обработку данных проводили с использованием программного пакета Statistica for Windows, Release 7.0.
Количественные данные представлены в виде медианы и интерквартильного размаха. Качественные данные представляли в виде абсолютных (n) и относительных (%) значений. Достоверность различий количественных показателей определяли при помощи критерия Вилкоксона (сравнение двух связанных групп). Результаты считали статистически значимыми при р<0,05. Статистическую значимость межгрупповых различий по качественным признакам оценивали с применением точного критерия Фишера (таблицы 2×2).
Проверку гипотез осуществляли при уровне статистической значимости 0,05.
Результаты
По результатам выполненного исследования, у больных ХСН II—III ФК имеется ДЭ на уровне крупных сосудов, о чем свидетельствует снижение СФ, который составил 6,62 мс (2,4; 8,7) (табл. 2).
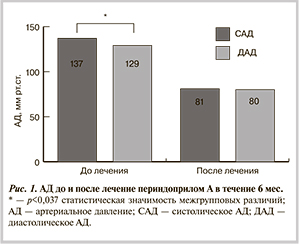
На фоне лечения периндоприлом А в течение 6 мес отмечено достоверное снижение среднесуточного систолического артериального давления (САД) со 137 (122; 154) до 129 (120; 133) мм рт.ст. (рис. 1). Кроме того, определялось снижение выраженности ДЭ на уровне крупных сосудов, по данным как ФПГ [СФ1 6,62 (2,4; 8,7) против СФ2 7,36 (3,8; 10,2); p=0,003; рис. 2], так и дуплексного сканирования ПА [ЭЗВД1 4,25 (3,9; 4,8) против ЭЗВД2 6,8 (5,1; 7,4); p=0,003; рис. 3].
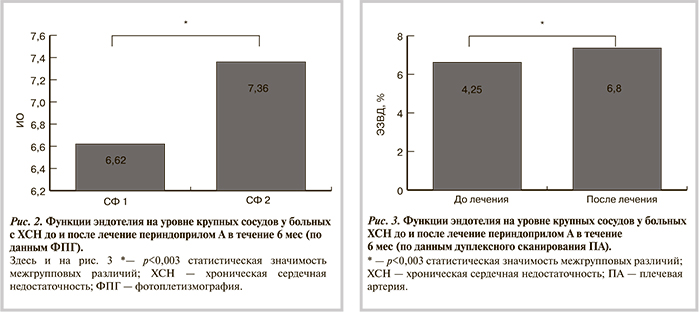
Таким образом, у больных ХСН и ГБ прием периндоприла А в дозе 5—10 мг/сут в течение 6 мес на фоне достоверного гипотензивного эффекта сопровождался достоверным улучшением функции эндотелия на уровне крупных сосудов, по данным как ФПГ, так и дуплексного сканирования ПА в ходе пробы с РГ.
Периндоприл А в продемонстрировал хорошую переносимость — 63% пациентов принимали препарат в дозе 10 мг/сут без развития побочных эффектов.



