Введение. Инфекции мочевыводящих путей занимают особую нишу в работе не только урологов, но и врачей других специальностей, работающих как в амбулаторном, так и в поликлиническом звене системы здравоохранения. Особое место отведено в данной группе пиелонефриту, который в ряде случаев требует безотлагательной госпитализации в урологический стационар, оперативного лечения и значительного нелегкого периода реабилитации. По характеру воспалительного процесса пиелонефрит классифицируется на острый (серозный или гнойный) и хронический. В процентном соотношении стационарных больных острый пиелонефрит доходит до 14%, хронический – до 30%. Доказано несколько способов инфицирования здоровой ткани почек. Как известно, существует восходящий способ проникновения инфекции в паренхиму почки, при котором лидируют грамотрицательные микроорганизмы, и гематогенный путь, при котором спектр микрофлоры уже чаще может быть представлен грамположительной флорой.
За последние 10 лет четко наметился выраженный рост заболеваний мочевыделительной системы, особенно воспалительного генеза как обструктивного так и необструктивного характера, а это определяет актуальность более глубокого уточнения этиопатогенеза данных нарушений, современной диагностики и, соответственно, направленной патогенетической терапии. Беря во внимание то, что было выполнено немало работ, раскрывающих ряд звеньев патогенеза острого пиелонефрита, в настоящее время не изучены отдельные вопросы, касающиеся состояния циркулирующих эритроцитов при обструктивных и необструктивных формах острого пиелонефрита. Не получил широкого распространения мониторинг уровня структурно-функциональных свойств циркулирующих эритроцитов в целях оценки эффективности проводимого лечения [1].
Эритроциты по своей физиологии не имеют ядра. Лишь малая часть ядерных элементов иногда определяется в пуповинной крови, при талассемии и серповидноклеточной анемии, а также в экстремальных для организма состояниях [2]. С течением эволюции из эритроцитов млекопитающих ушли ядро и ряд других важных органелл.
К последним относятся эндоплазматический ретикулум и рибосомы. Предполагается, что задача данного упразднения направлена на прибавление отношения площади поверхности к объему клетки, что вызывает значительный рост газообмена, емкости для клеточного гемоглобина (Hb) и модификации его особенности просачиваться сквозь небольшие капилляры [3–5].
Много ресурсов направлено к открытию механизмов формирования разнонаправленных приспособительных реакций организма: эндотелиальная дисфункция, синдром системного воспалительного ответа и т.д. Что важно: пересматривается и роль красных клеток крови в реакциях поддержания постоянства внутренней среды [6–8]. Сами по себе эритроциты полифункциональны и являются не только переносчиком газов. Их роль велика в гемореологии, иммунном и метаболическом функционале. Эритроциты задействованы в той или иной степени при всех патологических состояниях организма: будь то в ответ на влияние консервативной терапии или хирургических вмешательств, изменение температуры тела или повреждения агрессивно высокими или низкими температурами, отравления ядами [9–12].
Отсутствие масштабных публикаций о структуре и функции эритроцитов при воспалительных заболеваниях почек диктует острую необходимость их исследования с целью разработки способов коррекции выявленных изменений.
Целью исследования стало определение влияния стандартного лечения на нарушения структурно-функциональных свойств эритроцитов при остром необструктивном и обструктивном пиелонефрите.
Материалы и методы. В исследовании приняли участие 78 женщин (возраст – 52,7±3,8 года), находившихся на лечении в урологическом центре ЧУЗ «Центральная клиническая больница “РЖД-медицина”» (Москва) с установленным диагнозом «острый необструктивный (ОНП) или острый обструктивный пиелонефрит (ООП)». Пациентки были разделены по возрасту, сопутствующим заболеваниям.
Диагностика форм острого пиелонефрита основывалась на обнаружении системной воспалительной реакции в виде повышения температуры тела, озноба, увеличения частоты дыхательных движений, тахикардии; лейкоцитоза с палочкоядерным сдвигом лейкоцитарной формулы; лейкоцитурии; бактериурии более 104 КОЕ/мл; расширения чашечно-лоханочной системы (ЧЛС) и обнаружении блокированной почки (по данным ультразвукового исследования [УЗИ], экскреторной урографии или мультиспиральной компьютерной томографии [МСКТ]).
Пациенткам с ОНП (1-я группа, 39 человек) проводилась системная антибактериальная терапия (внутривенное введение одного или комбинации антибиотиков [цефалоспорины, фторхинолоны, аминогликозиды]), а также инфузионная терапия с целью дезинтоксикации.
Пациенткам 2-й группы (ООП, 39 человек) производилась чрескожная пункционная нефростомия (ЧПНС) под ультразвуковым контролем. По завершении дренирования начинали идентичное лечение, которое назначалось пациенткам первой группы.
Образцы биологического материала (кровь) получали при госпитализации и при выписке из урологического отделения (в срок 7–10 сут.). Группа контроля состояла из здоровых женщин того же возраста (15 человек).
Эритроциты выделяли с использованием общепринятой методики из гепаринизированной крови (10 мл) [13].
У пациенток определялись сорбционная емкость гликокаликса (СЕГ) и сорбционная способность эритроцитов (ССЭ) [14]. Для оценки перекисного окисления липидов (ПОЛ) в эритроцитах использовали общепринятые методики определения в плазме крови уровня малонового диальдегида (МДА) и ацилгидроперекисей (АГП). Антиоксидантную систему эритроцитов (активность супероксиддисмутазы [СОД] и каталазы) исследовали с помощью иммуноферментного анализа с применением наборов «Bender Medsystems» (Австрия) и «Cayman Chemical» (США) соответственно. Антиокислительную активность (АОА) оценивали посредством методики, основанной на ингибировании аскорбат- и ферроиндуцированного окисления твина-80 до МДА. Уровень стабильных метаболитов оксида азота (СМNO) определяли с помощью спектрофотометрического метода с применением реактива Грисса [15].
Для получения мембран эритроцитов использовали метод G. T. Dodge [16]; метод U. K. Laemli применялся для электрофоретического разделения мембранных белков [17], окрашивание электрофореграмм проводилось по модифицированной методике G. Fairbanks с использованием красителя Кумасси R250 [18].
Для денситометрирования электрофореграмм использовали лазерный денситометр «Ultroscan XL». Идентификация и расчет фракций белка выполнялись с помощью программы OneDscan. Количественное содержание фракций белка рассчитывалось на основе площади изучаемого белка с учетом известной массы и площади альбумина сыворотки человека в качестве белка-маркера. На основании полученных данных (в мкг) выполняли вычисление концентрации белка во фракциях с выражением в микрограммах на 1 мкл общего белка мембраны (в мг%). Для определения липидов мембран эритроцитов применяли метод жидкостной тонкослойной хроматографии, с целью идентификации липидных фракций использовали стандарт компании «Sigma» (США). Оценку полученных хроматограмм проводили денситометрическим методом посредством программы OneDscan [19].
Для статистической обработки материала использовали критерии вариационно-статистического анализа (расчет средних величин [M], средней арифметической ошибки [m]) с вычислением количественных данных U-теста (Манна–Уитни). Результаты считались достоверными при p<0,05.
Для расчета степени расстройств лабораторных показателей использовалась формула [16]:
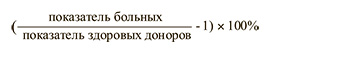
Примечание. Интервал 1–33% соответствует первой степени лабораторных расстройств, 34–65% – второй, 66% и более – третьей.
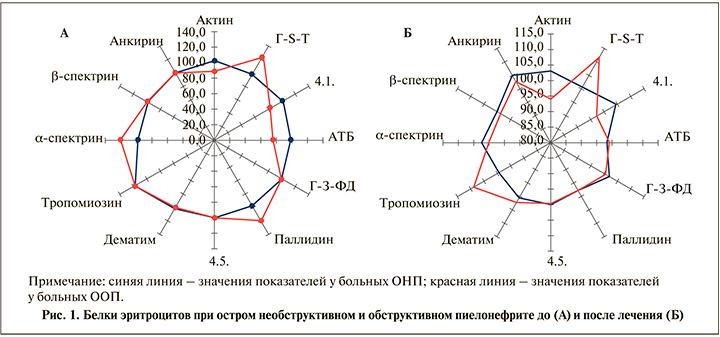
Результаты исследования. При необструктивной форме острого пиелонефрита до начала стандартного лечения выявлено увеличение в мембране эритроцитов только тропомиозина на 19,0% из всех исследованных белков. При выписке пациентов из стационара представительность его в мембране эритроцитов не отличалась от таковой здоровых доноров. При обструктивной форме пиелонефрита установлено повышение уровня α-спектрина в мембране эритроцита на 21,5%, паллидина на 20,2%, глутатион-S-трансферазы (Г-S-Т) на 23,2%, тропомиозина на 17,9% и снижение представительности белка полосы 4,1 на 15,9%, анионтранспортного белка (АТБ) на 23,7%, актина на 22,6%; уровни анкирина, β-спектрина, белка 4,9 (дематина), белка полосы 4,5 и глицеральальдегид-3-фосфатдегидрогеназы (Г-3-ФД) оставались на уровне здоровых. После проведенного стандартного лечения обструктивной формы пиелонефрита в мембране эритроцитов нормализовалось содержание α-спектрина, АТБ, белка полосы 4,1, паллидина и приближалось к значениям здоровых, но не до исходных полученных цифр, представительность актина, тропомиозина и Г-S-Т (рис. 1).
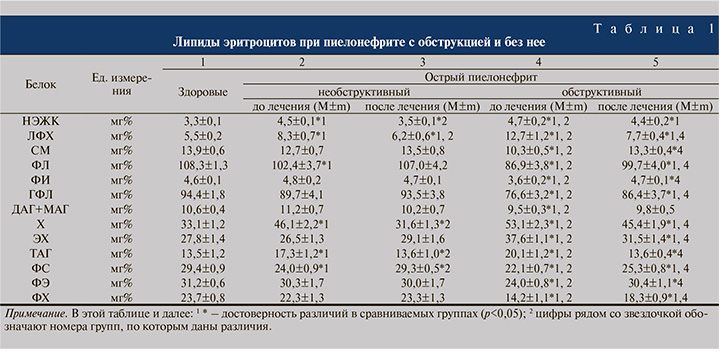
У пациентов с необструктивной формой острого пиелонефрита до лечения видим увеличение в мембране эритроцита представительности свободного холестерола (Х) на 39,3%, лизофосфатидилхолина (ЛФХ) на 50,9%, неэстерифицированных жирных кислот (НЭЖК) на 36,4%, триацилглицеролов (ТАГ) на 28,1%; снижение содержания глицерофосфолипидов (ГФЛ – сумма ФХ, ЛФХ, ФЭ, ФС и ФИ) на 5,4%, фосфатидилсерина (ФС) на 18,4%, при сохранении на уровне здоровых доноров уровня фосфатидилэтаноламина (ФЭ), фосфатидилхолина (ФХ), сфингомиелина (СМ), фосфатидилинозитола (ФИ), эфиров холестерола (ЭХ), фосфолипидов (ФЛ – сумма ГФЛ и СМ), суммы моно- и диацилглицеролов (ДАГ+МАГ). Анализ фракций липидов и их соотношений показал повышение соотношения Х/ФЛ, ЛФХ/ФХ, Х/ФС+ФИ при отсутствии изменений со стороны отношений ФХ/ФЭ, ФХ+СМ/ФЭ+ФС+ФИ, ФХ/СМ и Х/ЭХ. После проведенного лечения нормализовались все измененные представительности фракций липидов и их соотношения, за исключением коррекции содержания ЛФХ и увеличения отношения ФХ+СМ/ФЭ+ФС+ФИ (табл. 1, 2).
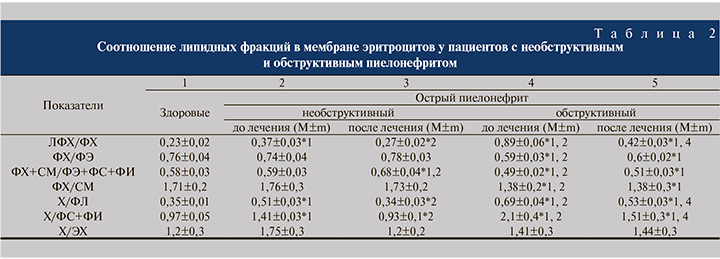
Анализ спектра липидов в мембране циркулирующих эритроцитов больных обструктивной формой пиелонефрита выявил изменения всех изученных фракций липидов мембраны эритроцитов, более выраженные как качественно, так и количественно по сравнению с необструктивной формой заболевания: повышение уровня ЛФХ на 130,9%, Х на 60,4%, ЭХ на 35,3%, ТАГ на 48,9%, НЭЖК на 42,4% снижение содержания ФХ на 40,1%, ФЭ на 23,1%, ФС на 24,8%, ФИ на 21,7%, ГФЛ на 18,9%, СМ на 25,9%, ФЛ на 19,8%, ДАГ+МАГ на 10,4%. Изучая распределение липидов, установлено падение соотношения ФХ/ФЭ, ФХ+СМ/ФЭ+ФС+ФИ, ФХ/СМ, более значительное увеличение соотношения ЛФХ/ФХ, Х/ФЛ, Х/ФС+ФИ. После терапии нормализовалась представительность ФЭ, ФИ, СМ, сумма ДАГ и МАГ, ГФЛ, ТАГ, без изменения на повышенном уровне осталась представительность НЭЖК и корригировалось содержание всех остальных исследованных фракций липидов и соотношение ЛФХ/ФХ, Х/ФЛ, Х/ФС+ФИ, остались без изменения по сравнению с состоянием до лечения ФХ/ФЭ, ФХ+СМ/ФЭ+ФС+ФИ, ФХ/СМ (рис. 3, 4).
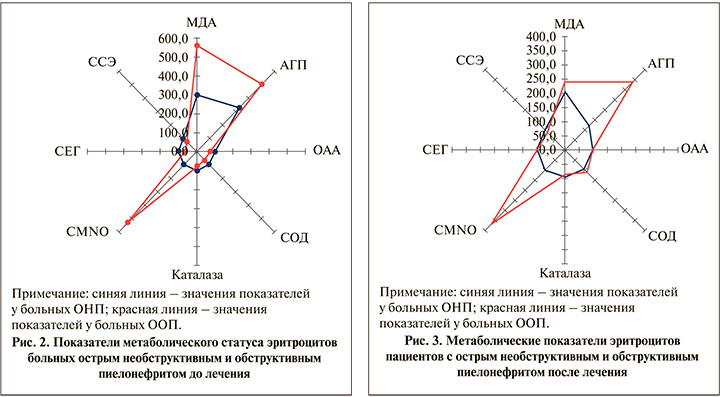
Работа по внутриэритроцитарному метаболизму показала интенсификацию реакций перекисного окисления липидов до общепринятой терапии пациентов с почечным воспалением при обструкции и без нее, что подтверждает рост в эритроцитах значений МДА в 3 и АГП в 3,3 раза. Также обнаружено отсутствие любой направленности факторов антиоксидантной защиты и сорбционной способности. По результатам лечения концентрация АГП нормализовалась, а сама концентрация МДА улучшилась, но не до уровня значений здоровых (рис. 2, 3).
У пациентов с обструктивной формой пиелонефрита выявлено выраженное усиление процессов ПОЛ (увеличение уровня АГП и МДА в 5 и 5,5 раз соответственно), возрастание содержания СМNO в 5 раз, уменьшение адсорбционных свойств эритроцитов (ССЭ и СЕГ в 1,4 и 1,5 раза соответственно) и также уменьшение факторов антиоксидантной защиты (активности каталазы и СОД в 1,3 и 1,5 раза соответственно, ОАА в 1,3 раза). Стандартное лечение улучшило показатели внутриэритроцитарного метаболизма: нормализовало ОАА, активность СОД и каталазы и СЕГ, корригировало, но не до уровня здоровых доноров ССЭ концентрацию МДА АГП и СМNO (рис. 3, 4).
Качественный и количественный анализы нарушенных исследованных лабораторных параметров показали, что до начала лечения острого необструктивного пиелонефрита 30% (12 из 40) исследованных структурно-функциональных свойств эритроцитов были изменены от значений нормы. Установлено, что 41,7% показателей были I степени, а 41,6 и 16,7% – II и III степеней соответственно. После стандартного лечения из числа измененных до лечения показателей таковых осталось 16,7% лабораторных параметров структуры и функции эритроцитов, были нормализованы и корригированы соответственно 83,3 и 16,7%, с I степенью нарушений осталось 16,7% параметров (табл. 3, 4).
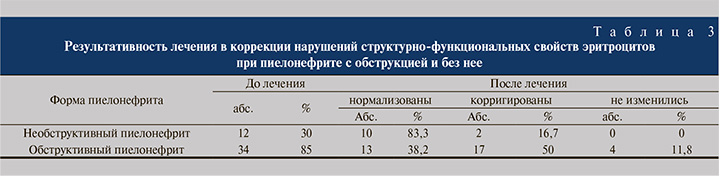

При обструктивной форме острого пиелонефрита до терапии были измененными от значений нормы 34 из 40 (85%) исследованных структурно-функциональных свойств эритроцитов, при этом I степень нарушений из них имели 44,1%, а II и III – 20,6 и 35,3% соответственно. Весьма становится важно и понятно, что нарушения со II–III степенями требуют проведения обязательной профильной коррекции [14–17]. После проведенного лечения из числа измененных до него показателей таковых остались 61,8% лабораторных параметров структурно-функциональных свойств эритроцитов, были нормализованы 38,2%, корригированы и остались на уровне до начала лечения соответственно 50 и 11,8%, с I степенью нарушений осталось 35,3% параметров, со II и III соответственно 14,7 и 11,8% (табл. 3, 4).
Проведенное стандартное лечение при обструктивной форме пиелонефрита не нормализует 61,8% измененных структурно-функциональных свойств эритроцитов, что обусловливает необходимость включения в лечебную программу препаратов с мембраностабилизирующими и антиоксидантными эффектами [18, 19].
Обсуждение. Описанные факты подтверждают то, что незначительно при необструктивной форме заболевания, но существенно при ООП в плазматической мембране эритроцитов происходит изменение содержания белков, определяющих структурообразование и стабилизацию основы мембраны клетки (анионтранспортный белок, α-спектрин, белок полосы 4,1, паллидин), внутриэритроцитарный обмен веществ (глутатион-S-трансфераза, анионтранспортный белок), форму и гибкость плазматической мембраны (тропомиозин, актин), в глубине red blood cell интенсифицируются реакции ПОЛ, отмечается развитие «окислительного стресса» с уменьшением ССЭ, снижаются в плазматической мембране уровни содержания ФЛ, ГФЛ, ДАГ+МАГ, при возрастании НЭЖК, ТАГ, Х, ЛФХ, ЭХ повышается соотношение Х/ФЛ, Х/ФС+ФИ, ЛФХ/ФХ, снижается отношение ФХ/СМ, ФХ/ФЭ, ФХ+СМ/ФЭ+ФС+ФИ. Следует отметить, что стандартное лечение при обструктивной форме острого пиелонефрита оказалось недостаточно эффективным в стабилизации изменений структурно-функциональных особенностей эритроцитов.
Плазматическая мембрана эритроцита является важнейшей структурой данной клетки, нарушения в строении которой и являются пусковым моментом возникновения различных заболеваний. Около 8% углеводов, 40% липидов, 52% белков – это состав мембраны эритроцита. Фосфолипиды (ФЛ) способствуют наличию жидкого непроницаемого барьера, поскольку гидрофильные группы ФЛ находятся на поверхности плазматической мембраны, ориентированы как в цитоплазму, так и наружу клетки. Гидрофобные акиловые неполярные хвосты формируют центральный слой, который динамически скрыт от цитоплазмы и плазмы крови. Белки асимметрично встроены в бимолекулярный липидный матрикс. ФЛ способствуют формированию особенной укладки в плазматической мембране эритроцита полипептидных цепей некоторых цитоскелетных (периферических) и всех трансмембранных белков (интегральных) [20–22].
Характерными признаками эритроцитарных мембран являются неравномерность распределения ФЛ, правильная асимметрия липидов в липидном бислое мебран, поддерживаемая белками. СМ, ФХ и Х доминируют в наружном слое плазматической мембраны, а ФЭ и ФС преимущественно формируют внутренний слой, это приводит к разнице заряда между слоями мембраны. ГФЛ также располагаются на наружной части мембраны и обладают еще большей асимметрией. Ганглиозиды, которые отличаются строением олигосахаридных цепей, формируют антигенные свойства красных кровяных клеток. Эстерифицированный холестерол, обладающий гидрофобными свойствами, располагается параллельно акиловым хвостам ФЛ, которые распределены достаточно равномерно между внутренним и внешним слоями. Относительное постоянство Х к ФЛ способствует уравновешиванию текучести мембраны и механической прочности. Снижение его уровня способствует потере прочности во время растяжения. При повышении содержания холестерола плазматическая мембрана приобретает прочность с потерей эластичности. ЛФХ также играет важную роль за счет способности снижать чувствительность эритроцита к действию наружных сигналов [23, 24].
Несмотря на то что Х и ФЛ являются основными структурами плазматической мембраны, большая часть специфических функций мембраны эритроцита осуществляется белковыми структурами. Важнейший фактор слаженного функционирования мембраны эритроцита – строгий порядок положения белковых макромолекул, выполняющих важнейшие функции в организме. Изменение конформационных свойств этих белков приводит к осмотическому напряжению цитоплазмы, приводящему к повышению вязкости мембраны и потере ее деформируемости [25, 26].
Окислительный стресс, вероятнее всего, и есть тот триггер, принимающий участие в патологии структурно-функциональных свойств красных клеток, вызывающий в дальнейшем модифицирование фосфолипидного слоя плазматических мембран, нарушающий белково-липидный баланс в мембране эритроцита и изменяющий представительность спектра белков. Все это приводит к изменению архитектоники оболочки и эпитопной структуры красных кровяных клеток [27–29].
Результат биологических и ультраструктурных сбоев эритроцитов – недостаток О2, сбой реологии и системы гемостаза крови на всех уровнях, нарушение работы эндотелия, сбой иммунорегуляции способны являться пусковым механизмом грозных осложнений острого почечного воспаления.
Заключение. Полученные данные расширяют представление урологов и врачей смежных специальностей о нарушениях структурно-функциональных свойств и показателей метаболического статуса эритроцитов при остром необструктивном и обструктивном пиелонефрите до лечения и после стандартного лечения. Продемонстрированные результаты исследования открывают перспективы изучения влияния препаратов, обладающих мембраностабилизирующими и антиоксидантными эффектами, на результаты лечения пациентов с воспалительными заболеваниями почек.



