Трансплантация почки в настоящее время является самым эффективным методом лечения пациентов с терминальной стадией хронической почечной недостаточности (ТХПН). Традиционно операция осуществляется из внебрюшинного доступа по Gibson: от симфиза латерально и вверх параллельно паховой связке. В последнее время стали появляться публикации о роботассистированной трансплантации почки [1]. Почечную вену донорской почки обычно анастомозируют с наружной подвздошной веной реципиента по типу «конец в бок», почечную артерию – с наружной подвздошной артерией по типу «конец в бок». При трупной трансплантации трансплантаты с почечной артерией или артериями берутся на протяжении с участком аорты – так называемой площадкой Карреля, наличие которой делает выполнение анастомоза по типу «конец в бок» более легким и безопасным и существенно облегчает наложение анастомоза в случае множественных артерий. При трансплантации от живого донора формирование аортальной площадки невозможно и к артерии реципиента пришивается собственно почечная артерия трансплантата.
Основными показаниями к трансплантатэктомии в раннем периоде после пересадки являются сосудистые осложнения (венозный тромбоз, псевдоаневризма артериального анастомоза, окклюзия почечной артерии); криз отторжения, резистентный к медикаментозному лечению; острый гнойно-деструктивный пиелонефрит трансплантата; первичное отсутствие функции; разрыв трансплантата. Как правило, трансплантатэктомия в раннем периоде выполняется по экстренным показаниям, почка удаляется вместе с капсулой, т.е. экстракапсулярно. Традиционным основанием для удаления нефункционирующего трансплантата в позднем периоде служат реакция хронического отторжения трансплантата, рецидивирующее течение пиелонефрита трансплантата, интермиттирующая макрогематурия, необходимость в освобождении места для последующей пересадки почки, опухоль трансплантата, выраженная протеинурия.
В основном трансплантатэктомия в позднем периоде выполняется субкапсулярно по Федорову и является процедурой с высокой (до 40%) частотой осложнений. Чаще это септические осложнения и кровотечение, реже наблюдаются повреждение кишки, мочевой свищ, травма запирательного нерва или бокового кожного нерва бедра [2]. После декапсуляции трансплантата из паренхимы открывается кровотечение, интенсивность которого зависит от кровоснабжения и характера патологического процесса. Ножка почки находится в массивном инфильтрате, поэтому на ее выделение уходит в среднем 30–40 мин, за это время кровопотеря из паренхимы достигает иногда 1000 мл. Остающаяся капсула почки может являться источником послеоперационного кровотечения и гнойно-септических осложнений. Усугубляет и способствует развитию септических осложнений низкая иммунологическая активность организма вследствие приема иммуносупрессоров (если они не отменены), рецидива ТХПН, проведения гемодиализа и сопутствующая сердечно-сосудистая патология.
При анализе собственных данных, основанных на 20 пациентах, которым проведена субкапсулярная трансплантатэктомия, установлено, что средняя продолжительность вмешательства составила 83 мин, средняя интраоперационная кровопотеря – 277 мл, интенсивное кровотечение в раннем послеоперационном периоде развилось у 2 (10%) пациентов, нагноение в ране – у 3 (15%).
Основные трудности выполнения лапароскопической трансплантатэктомии, препятствующие ее широкому внедрению, связаны с выраженным рубцовым процессом вокруг почки, инфильтрацией в области сосудов почки. Однако при определенном опыте в лапароскопической хирургии данное вмешательство вполне осуществимо и выглядит более привлекательным для определенной группы больных в первую очередь из-за снижения риска послеоперационных осложнений и более быстрой реабилитации пациента. Впервые об успешно выполненной лапароскопической трансплантатэктомии в 2010 г. сообщили M. Altinel и соавт. из Турции [3]. Вмешательство выполнено мужчине 45 лет спустя 3 года после прекращения функции пересаженной почки. Трансплантат располагался в правой подвздошной области, забрюшинно. Хирургическое пособие авторы начали с мобилизации правого отдела толстого кишечника, затем выделены общая подвздошная артерия, наружная подвздошная артерия, на которой был идентифицирован анастомоз с почечной артерией, ее клипировали Hem-O-Lok. Почечная вена была разделена с использованием 45/2,5 мм EndoGIA степлера. Кровопотеря была минимальной, время операции составило 100 мин, выписан больной на 3-и сутки. M. Mulloy и соавт. из г. Атланты (США, штат Джорджия) в 2014 г. опубликовали данные первой роботической трансплантатэктомии с лапароскопической ассистенцией у больного 34 лет с синдромом Альпорта. Почечный трансплантат располагался в правой подвздошной области. Авторы, так же как и в вышеописанном случае, оперативное пособие начали с мобилизации подвздошных сосудов. Перед тем как отсечь артерию транспланта, на нее был наложен зажим типа «бульдог» и оценен кровоток в системе бедренной артерии на ноге пальпаторно и с помощью эходопплерографии. После того как было установлено, что кровообращение в конечности не нарушено, проведено разделение почечной артерии при помощи лапароскопического степлера. Далее трансплантат был мобилизован, идентифицирован мочеточник, клипирован Hem-O-Lok и разделен, почечная вена была визуализирована в последнюю очередь, пересечена с помощью лапароскопического сосудистого степлера. Лапароскопическая ассистенция применена с целью использования сосудистого степлера, так как подобный роботический инструмент не прошел одобрения FDA на момент проведения вмешательства. Время операции составило 235 мин, кровопотеря – менее 25 мл, пациент выписан через сутки [4].
Приводим собственное клиническое наблюдение.
Б о л ь н а я Р. 42 лет поступила в приемное отделение ГБУЗ ГКБ № 52 ДЗ г. Москвы 04.02.16 с жалобами на повышение температуры тела до 38 °C, боль в левой подвздошной области, в области локализации трансплантированной почки в течение последних семи суток. Подобные жалобы пациентка отмечала в феврале 2015 г., проходила лечение в стационаре, где проводилась антибактериальная терапия по поводу активного пиелонефрита трансплантата с эффектом.
В анамнезе в 2000 г. диагностирована ТХПН в исходе хронического гломерулонефрита, начато лечение гемодиализом. В феврале 2010 г. выполнена трансплантация трупной почки в левую подвздошную область. В ноябре 2010 г. проходила стационарное лечение в связи с активным пиелонефритом трансплантата, подтвержденного данными биопсии. В декабре 2013 г. в связи с хронической трансплантационной гломерулопатией развился рецидив ТХПН, возобновлено лечение гемодиализом. Постепенно отменена иммуносупрессивная терапия, оставлен только метипред в дозе 4 мг в сутки. Из сопутствующих заболеваний у больной имелись бронхиальная астма, атопическая форма тяжелого, частично контролируемого течения и хронический гепатит С.
В 2013 г. по поводу третичного гиперпараритеоза перенесла тотальную паратиреоидэктомию с аутотранплантацией фрагмента околощитовидной железы в мышцу предплечья.
Объективно: состояние средней тяжести. Сознание ясное. Кожные покровы бледноватые, сухие. Периферических отеков нет. На левом предплечье пальпируется артериовенозная фистула, функция адекватная. Температура тела – 37,4 °С. Аускультативно над легкими дыхание везикулярное, хрипов нет. ЧДД – 18 в 1 мин. Тоны сердца приглушены, ритм правильный. АД – 120/70 мм рт.ст., ЧСС – 77 в 1 мин. Живот равномерно участвует в акте дыхания, мягкий, не вздут, безболезненный при пальпации. В левой подвздошной области определяется трансплантированная почка, не увеличена, несколько болезненна, плотной консистенции. Перитонеальных симптом нет. Печень не увеличена; селезенка, почки не пальпируются. Мочевой пузырь при пальпации не определяется. Наружные половые органы не изменены. Анурия. Ректально без особенностей, кал коричневого цвета.
Лабораторные данные: гемоглобин 118 г/л, эритроциты 3,84∙1012/л, тромбоциты 236∙109/л, лейкоциты 9,2∙109/л, глюкоза 3,22 ммоль/л, общий белок 81,1 г, мочевина 15,1 ммоль/л, креатинин 777,8 мкмоль/л, С-реактивный белок 197 мг/л, калий 5,6 ммоль/л, натрий 133 ммоль/л. Коагулограмма: МНО 1,26, АЧТВ 37,6 с, протромбиновый индекс 82,29%. На ЭКГ ритм синусовый, ЧСС 88 в 1 мин, нормальное положение ЭОС, нарушение реполяризации миокарда левого желудочка. При рентгенологическом исследовании органов грудной клетки патологических изменений в легких не выявлено. При УЗИ сморщенные собственные почки (размером 60х20 мм, дифференцировка слоев отсутствует, расширения чашечно-лоханочной системы нет с обеих сторон), трансплантат размером 95х60 мм, толщина паренхимы 15 мм, эхоструктура неоднородная, дифференцировка слоев сглажена, расширения чашечно-лоханочной системы нет.
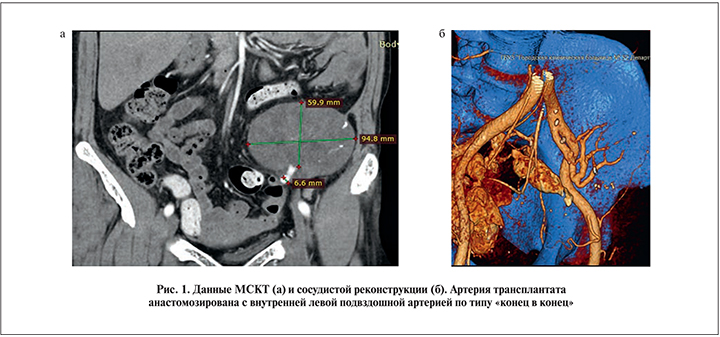
Мультиспиральная компьютерная томография (МСКТ) с контрастированием: трансплантат расположен в левой подвздошной области, размер его 60х95х66 мм, очагов патологической плотности в паренхиме не выявлено, замедление накопления контрастного препарата, экскреторная и венозная фазы не отмечены, артерия трансплантата отходит от внутренней подвздошной, анастомоз по типу «конец в конец» (рис. 1). После исследования больной проведен сеанс гемодиализа.
Спирометрия: умеренное снижение вентиляции легких по комбинированному типу. Проба с сальбутамолом положительная. Пациентка осмотрена хирургом, гинекологом, терапевтом – острого профильного заболевания не выявлено. Консультирована аллергологом, назначена терапия по поводу бронхиальной астмы в качестве предоперационной подготовки.
На основании полученных данных поставлен диагноз: основной – хронический гломерулонефрит; осложнения – ТХПН, лечение программным гемодиализом, аллотрансплантация почки от 26.02.10, хроническое отторжение трансплантата (активное течение хронического пиелонефрита трансплантата?), рецидив ТХПН с декабря 2013 г., анемия, третичный гиперпаратиреоз, тотальная паратиреоидэктомия с аутотранплантацией фрагмента околощитовидной железы в мышцу предплечья от 2013 г.; сопутствующий – вирусный гепатит С, бронхиальная астма, атопическая форма тяжелого, частично контролируемого течения.
Наличие боли в области трансплантата, его уплотнение и болезненность при пальпации, гипертермия – симптомы, характерные как для хронического отторжения, так и для активного течения пиелонефрита трансплантата. В данном случае выполнение анализов мочи, в том числе посева мочи, не представлялось возможным в связи с анурией, а данные МСКТ в отсутствие гнойно-деструктивного пиелонефрита неспецифичны, в связи с чем достоверно судить о характере патологического процесса было невозможно, подозрение на активное течение пиелонефрита основывалось на анамнезе. Тем не менее больной было показано оперативное лечение в объеме трансплантатэктомии. Принимая во внимание молодой возраст пациентки, отсутствие гнойной формы пиелонефрита, наличие трупного трансплантата (что исключало короткую сосудистую ножку почки), решено провести лапароскопическую экстракапсулярную трансплантатэктомию с целью минимизации риска послеоперационных осложнений. С больной проведена беседа о том, что это первый опыт подобного вмешательства, пациентка также информирована о возможной конверсии в открытое пособие, получено согласие на операцию.
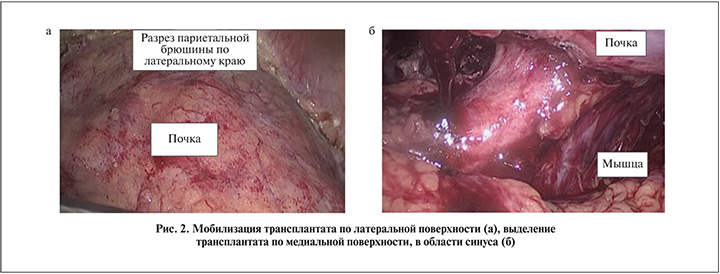
Операция выполнена под тотальной внутривенной анестезией с ИВЛ. Больная уложена в положение Тренделенбурга с наклоном стола вправо. Использовано четыре лапароскопических порта: 2 по 10 мм и 2 по 5 мм. Мы воздержались от первоначальной мобилизации подвздошных сосудов в связи с тем, что артерия трансплантата отходила от внутренней подвздошной артерии практически в зоне бифуркации общей подвздошной артерии. Первым этапом мобилизованы сигмовидная кишка и нисходящая часть толстого кишечника по латеральному краю, трансплантат по медиальному и латеральному краю с помощью ультразвуковых ножниц и аппарата Ligasure (рис. 2). Технические сложности на данном этапе обусловлены отсутствием послойности в тканях, основным ориентиром была поясничная мышца.
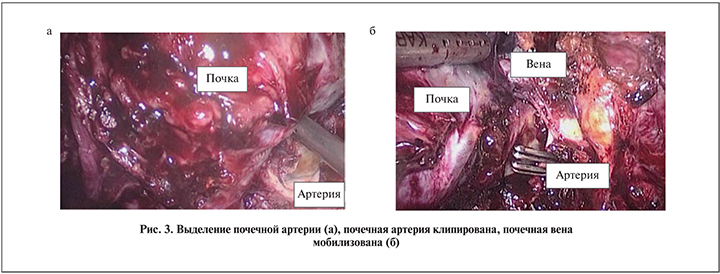
Далее начата мобилизация почки в области ворот, трудности были также связаны с выраженным рубцовым процессом и отсутствием послойности, основным ориентиром на данном этапе являлся край почки. Первым этапом выделена почечная артерия диаметром 6–7 мм, которая имела белесый цвет. Клипирована металлическими клипсами и пересечена ультразвуковыми ножницами, после этого визуализирована почечная вена, которая уходила латерально и вверх, вероятно, анастомозировала с наружной подвздошной веной. С веной проведены такие же манипуляции, что и с артерией (рис. 3). Такое расположение сосудистых анастомозов заставило нас предположить, что была пересажена правая почка.
После разделения почечной артерии и вены продолжена окончательная мобилизация почки, в основном с использованием Ligasure. Нам, к сожалению, не удалось четко идентифицировать мочеточник и лоханку. Почка эвакуирована путем морцелляции.
Гистологическое заключение: клубочки увеличены в размерах, имеют дольчатую структуру за счет эндокапиллярной пролиферации. Стенки капиллярных петель утолщены, имеются двойные контуры. Диффузный склероз интерстиция и атрофия канальцев. Диффузно-очаговая плотная инфильтрация интерстиция лимфоцитами с примесью значительного числа нейтрофилов. В зонах некроза определяются многочисленные лейкоциты с образованием микроабсцессов. Артерии – выраженный артериосклероз, артериолы – артериолосклероз. Кортикальный некроз с явлениями вторичного инфицирования. Хроническое отторжение трансплантата. Таким образом, у пациентки на фоне хронического отторжения имело место обострение хронического пиелонефрита трансплантированной почки.
Время операции составило 245 мин, интраоперационная кровопотеря – 350 мл. Брюшная полость дренирована двумя силиконовыми дренажами. Пациентка экстубирована на операционном столе. Активизирована через сутки. Течение послеоперационного периода гладкое. Проводилась антибактериальная, гастропротективная терапия, сеансы гемодиализа 3 раза в неделю, профилактика венозных тромбоэмболических осложнений, а также терапия по поводу бронхиальной астмы. Со вторых суток в анальгезии не нуждалась. Дренажи из брюшной полости удалены на 9-е сутки. Заживление послеоперационных ран первичным натяжением, швы сняты. Выписана из стационара на 10-е сутки. Пролонгированное дренирование брюшной полости и выписка пациентки на 10-е сутки были обусловлены желанием тщательного наблюдения за больной в раннем послеоперационном периоде с учетом первого опыта лапароскопической трансплантатэктомии.
Лапароскопическая трансплантатэктомия – технически сложное оперативное вмешательство, по времени более продолжительное, чем открытая операция. В связи с этим наилучшими кандидатами для лапароскопической трансплантатэктомии могут быть молодые пациенты без значимых сопутствующих заболеваний, без ранее выполненных операций на органах брюшной полости.
Существенным моментом является причина, по которой проводится трансплантатэктомия: мы убеждены в том, что гнойная форма пиелонефрита должна быть противопоказанием к лапароскопическому доступу.
Важным аспектом является то, какая почка пересажена больному: от живого или трупного донора. При наличии трупной почки создаются более благоприятные условия для операции, так как в этом случае сосуды длиннее по сравнению с таковыми трансплантата, взятого от живого донора.
При планировании операции необходимо иметь информацию о том, сколько основных артерий имеет трансплантат и каким путем они анастомозированы с сосудами реципиента. На наш взгляд, при анастомозе единственной почечной артерии с наружной подвздошной артерией операция представляется более простой, так как в этом случае можно начать сразу с мобилизации проксимального отдела наружной подвздошной артерии с последующим выделением почечной артерии и ранним прекращением артериального кровотока в почке. Анализ протокола операции пересадки почки, МСКТ с 3D-реконструкцией артериальных сосудов – неотъемлемая часть планирования операции. Томография помимо визуализации артериальных сосудов дает информацию о топографо-анатомических взаимоотношениях почки, кишечника, расположении элементов ножки почки по отношению друг к другу. Однако при анурии МСКТ позволит визуализировать только артериальные сосуды. В условиях отсутствия экскреторной, венозной фаз данные о расположении лоханки, почечной вены получить невозможно.
На основании собственного единичного опыта, малочисленных публикаций считаем, что последовательность выполнения лапароскопической трансплантатэктомии должна быть следующей: мобилизация толстого кишечника, общей подвздошной артерии, затем ее ветви, где локализуется анастомоз, разделение почечной артерии (перед этим целесообразно наложить сосудистый зажим и оценить пульсацию на артериях ноги), начало мобилизации трансплантата с латеральной поверхности с ориентиром на поясничную мышцу (необходимо следить за тем, чтобы не повредить бедренный нерв), по ходу мобилизации трансплантата идентификация почечной вены и мочеточника.
Несмотря на то что лапароскопическая трансплантатэктомия – по времени более продолжительная, чем открытая операция, процедура, такие аспекты, как снижение интраоперационной кровопотери, более быстрая реабилитация пациента, снижение рисков послеоперационных осложнений за счет удаления почки вместе с капсулой, уменьшение потребности в анальгезии, снижение продолжительности стационарного лечения, делают данное вмешательство привлекательным для хорошо отобранных больных. Однако более объективную оценку можно будет дать после получения опыта на большом количестве пациентов.



