Введение. Восстановление проходимости верхних мочевыводящих путей при протяженных сужениях и облитерациях мочеточников остается одной из основных проблем реконструктивной урологии. Подобные дефекты образуются преимущественно в результате ятрогенных повреждений при операциях на органах малого таза и брюшной полости, после лучевой терапии, эндоурологических вмешательств, а также вследствие таких заболеваний, как мочекаменная болезнь, туберкулез, ретроперитонеальный фиброз [1, 2].
Протяженные стриктуры мочеточника, распространяющиеся на его оба отдела или тотальное
поражение этого органа, зачастую не позволяют восстанавливать пассаж мочи с использованием неизмененных отделов мочевыводящих путей. Многочисленные попытки применения в качестве
трансплантатов различные ткани органической и неорганической природы оказались безуспешными. На практике оправдали себя только аутоорганы, которым свойственны перистальтические
сокращения, т.е. изолированные сегменты тонкой или толстой кишки, а в ряде случаев и червеобразный отросток [3, 4].
Впервые замещение мочеточника сегментом тонкой кишки в эксперименте выполнили в 1900
г. G. D’Urso и A. de Fabii [5], в клинике – в 1940 г. R. Nissen по поводу мочеточниковокожной фистулы, образовавшейся после уретеролитотомии. Данные контрольного обследования больного через 6 лет убедили автора в оправданности этой операции. Впоследствии K. Ultiszch произвел одновременную замену тазовых отделов обоих мочеточников кишкой по поводу двусторонних мочеточниковых свищей, развившихся после резекции сигмовидной кишки. В СССР кишечная пластика мочеточника впервые выполнена в эксперименте М. М. Заевлошиным и В. М. Гиньковским в 1938 г. [6]. По итогам операций на 9 собаках авторы пришли к выводу, что изолированная петля тонкой кишки является хорошим материалом для замещения мочеточника. В клиническую практику данное оперативное вмешательство в нашей стране внедрил А. П. Фрумкин в 1954 г. [7]. За последние 50 лет илеоуретеропластика получила более широкое признание. В эксперименте, а затем и в клинике было доказано, что при кишечном замещении мочеточника не наблюдается существенных нарушений водно-электролитного баланса. Накопление определенного опыта со временем позволило выполнять операцию больным с единственной почкой. Ф. А. Клепиков заместил мочеточник кишкой у 20 больных [8], а Д. В. Кан сообщил о результатах энтероуретеропластики для 28 пациентов, среди которых у 8 почка была единственной [9]. Несмотря на массу осложнений и высокую летальность, Д. В. Кан считал, что данная операция нередко остается последним шансом для больного сохранить функционирующую почку и избавиться от постоянного нефростомического дренажа. Вместе с тем за последние 20 лет в
отечественной литературе работ, посвященных данной проблеме, практически не было.
В настоящее время для кишечной пластики мочеточника наиболее часто используют изолированный участок подвздошной кишки. Анатомия данного отдела кишки, мобильность ее брыжейки позволяют использовать сегмент необходимой длины для частичного или полного замещения одного или обоих мочеточников. Как указывает В. С. Карпенко [10], привлекательным в тонкокишечной пластике мочеточника является то, что кишка-мочеточник сохраняет перистальтическую функцию и обеспечивает продвижение болюса мочи из почки в мочевой пузырь. При этом адаптивные изменения слизистой трансплантата носят незначительный характер. С этой целью неоднократно использовались и другие отделы желудочно-кишечного тракта. Так, анатомо-топографические особенности толстой кишки делают ее удобным пластическим материалом для реконструкции верхних мочевыводящих путей, однако, несмотря на кажущееся удобство расположения, ее использование не получило столь широкого клинического распространения.
В последнее время стали появляться работы, сообщающие о возможности выполнения данной операции с помощью эндовидеохирургии. Так I. Gill и соавт. в 2000 г. подробно описали технику лапароскопической илеоуретеропластики [11], а спустя 8 лет R. Joseph и соавт. [12] произвели роботассистированную операцию пациенту с протяженной стриктурой мочеточника единственной левой почки после уретеролитотрипсии. Применение эндовидеохирургической техники при данных операциях весьма перспективно, однако не всегда возможно. В особенности это касается пациентов с рецидивными постлучевыми стриктурами, выраженным ретроперитонеальным фиброзом и предшествующими операциями на брюшной полости. Несмотря на значительное развитие эндовидеохирургической техники, опыт подобных операций на сегодняшний день еще недостаточен
ввиду их редкости и технической сложности.
Целью работы явилось “изучение результатов кишечной пластики мочеточников”
Материалы и методы. С 2001 по 2012 г. кишечная пластика мочеточников выполнена 50 пациентам.
Среди них было 13 мужчин и 37 женщин. Возраст больных колебался от 18 до 69 лет и в среднем составил 47,2±11,5 лет. В 47 (94%) наблюдениях использовался изолированный сегмент подвздошной, в 3 (6%) – сигмовидной кишки. Следует отметить, что помимо этих 50 пациентов, которым операция
произведена с использованием изолированного сегмента подвздошной или сигмовидной кишки, включенных в эту работу, в 16 наблюдениях для замещения протяженных сужений мочеточников нами был использован червеобразный отросток, в том числе 3 аппендикоуретеропластики выполнены слева.
Причины, приведшие к обширным повреждениям мочеточников, представлены в табл. 1. Как видно из табл. 1, подавляющее большинство пациентов были ранее оперированы на органах малого таза по поводу онкологических заболеваний, прежде всего женских половых органов. К следующим по значимости причинам сужений мочеточников относятся лучевая терапия по поводу новообразований органов малого таза, эндоурологические операции (уретероскопия) больным с мочекаменной болезнью, рак мочевого пузыря и интерстициальный цистит.
Таблица 1. Причины дефектов мочеточников у больных, перенесших илеоуретеропластику.
Одностороннее замещение мочеточника произведено 33 (66%) пациентам, двусторонняя пластика – 17 (34%). Как видно из табл. 2, в подавляющем большинстве (94%) наблюдений для реконструкции мочевыводящих путей использовалась изолированная петля подвздошной кишки, которая, являясь универсальным пластическим материалом, позволяет замещать не только любой дефект мочеточников с обеих сторон, но и одновременно осуществлять реконструкцию мочевого пузыря. В одном случае левосторонняя илеоуретеропластика произведена в сочетании с замещением протяженного дефекта противоположного мочеточника червеобразным отростком.
Результаты и обсуждение. Послеоперационное ведение больных мало отличалось от используемого при лечении пациентов общехирургического профиля. Комплексная оценка основывалась на
данных клинических, лабораторных, рентгенологических, радиоизотопных, ультразвуковых, уродинамических, инструментальных и эндоскопических исследований.
Таблица 2. Виды кишечных пластик, выполненных по поводу обширных поражений мочеточников.
Послеоперационные осложнения развились у 7 (14%) пациентов (табл. 3). В раннем послеоперационном периоде осложнения имели место у 6 (12%) больных. Наиболее грозными из них стали спаечная кишечная непроходимость и тромбоз брыжейки трансплантата. Острая тонкокишечная
непроходимость имела место у 2 пациентов: после U-образного замещения протяженных дефектов
обоих мочеточников и после правосторонней илеоуретеропластики. В первом случае выполнена
релапаротомия, обходной илеотрансверзоанастомоз “бок в бок”, во втором — релапаротомия, рассечение спаек, санация и дренирование брюшной полости, интубация кишечника зондом Эббота.
Пациенту с тромбозом брыжейки трансплантата в результате перекрута его при попытке изоперистальтического расположения петли справа после двусторонней илеоуретеропластики произведено его удаление, почка дренирована нефростомой. В дальнейшем выполнена сигмоуретеропластика.
Таблица 3. Характер ранних и поздних послеоперационных осложнений после кишечной пластики
мочеточников и способы их коррекции.
В отдаленном послеоперационном периоде спустя 2,5 мес после операции у 1 (2%) больного образовалась стриктура уретероилеоцистоанастомоза. Проходимость мочевыводящих путей восстановлена путем антеградного бужирования стриктуры. Таким образом, осложнения, потребовавшие оперативного лечения, развились у 3 (6%) больных. Результаты повторных операций оказались успешными, без летальных исходов.
Функциональное состояние почек и верхних мочевыводящих путей в отдаленном послеоперационном периоде удалось оценить у 47 пациентов. Срок наблюдения составил от 3 мес до 11 лет (в среднем
6,3±0,8 года). Согласно данным литературы, наиболее частое функциональное нарушение после кишечной пластики мочеточников — пузырно-кишечный и пузырно-лоханочный рефлюкс [11]. Среди прооперированных нами больных активный пузырно-лоханочный рефлюкс имелся у 2 (4,2%) пациентов, страдавших нейрогенными расстройствами мочевого пузыря. Однако он не проявлялся клинически, не сопровождался гидроуретеронефрозом и рецидивирующей инфекцией мочевыводящих путей, так как больные прибегали к периодической самокатетеризации. Таким образом, ухудшения функционального состояния почек на стороне операции ни у одного из обследованных нами пациентов не выявлено.
Отдаленные результаты оперативного лечения – тот материал, в котором оперирующие урологи находят ответы на имеющиеся у них вопросы. Именно поэтому такие публикации пользуются
неизменным успехом. Сравнивая полученные нами результаты с данными литературы, хотим отметить,
что цифры, приводимые разными авторами, зачастую сильно разнятся. Так, F. Verduyct и соавт. [13]
собрали сведения о 18 из 22 оперированных за 20 лет больных, которым была выполнена одно- или
двусторонняя кишечная пластика мочеточников. Осложнения возникли у 9 (50%) больных. Три
пациента были оперированы в ранние сроки после операции: одному выполнена нефрэктомия по
поводу кровотечения, двоим – лапаротомия в связи с тонкокишечной непроходимостью. В отдаленном
периоде 6 пациентов потребовали оперативного вмешательства: двое перенесли нефрэктомию, трое
– лоханочно-подвздошный реанастомоз, один — нефролитотрипсию. Шесть пациентов страдали от
рецидивирующего пиелонефрита и двое получали консервативное лечение по поводу ацидоза.
В отдаленном периоде функция почки на стороне операции была сохранена у 15 (83,3%) пациентов.
В целом авторы положительно отзываются о кишечной пластике мочеточников, но, как и многие другие, считают ее показанной лишь больным, для которых не существует другого выбора.
S. Armatys и соавт. [14], оценив отдаленные результаты илеоуретеропластики для 91 пациента,
также сообщают о высокой частоте осложнений. Так, в раннем послеоперационном периоде они
возникли в 43% наблюдений, в отдаленном – в 23%. Однако авторы объясняют столь высокие
показатели тем, что 74 (81,3%) больных ранее были неоднократно оперированы или получали лучевую терапию. Особенно часто осложнения развивались у пациентов с забрюшинным постлучевым фиброзом. По данным клиники Медицинского центра Бургенстона (США), серьезные осложнения,
включая стенозы проксимального и дистального анастомозов, расхождения раны и усугубление
хронической почечной недостаточности возникли лишь у 6 (11,5%) из 52 больных [15]. В работе [16]
результаты кишечной пластики мочеточников, выполненной 89 пациентам, в 81% случаев оценены как положительные.
Таким образом, представленные различными клиниками данные о частоте послеоперационных осложнений и отдаленных функциональных результатах кишечной пластики мочеточников неоднозначны и являются предметом дискуссий. Основываясь на полученных нами результатах, считаем, что реконструкция мочеточников при помощи изолированного сегмента тонкой или толстой кишки, несмотря на продолжительность и сложность оперативного вмешательства, является относительно безопасной операцией, позволяющей восстанавливать свободный отток мочи из почек и избавлять пациента от мочевых свищей. Соблюдение показаний и противопоказаний при отборе больных для подобной операции является важнейшим условием достижения хорошего функционального результата. Вторым, не менее важным, условием является наличие в клинике урологов, имеющих опыт абдоминальной хирургии, и адекватное анестезиологическое обеспечение.
В качестве примера приводим клиническое наблюдение одной из подобных операций, выполненных в нашей клинике: левосторонней вертикальной илеоуретеропластики пациентке с протяженной стриктурой мочеточника нижней половины удвоенной почки.
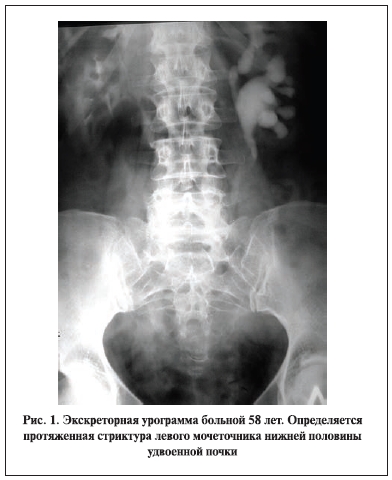
Б о л ь н а я 58 лет госпитализирована в нашу клинику 26.02.10 в плановом порядке с жалобами на тупые боли в левой поясничной области. Из анамнеза известно, что в сентябре 2009 г. выполнена уретеролитотрипсия по поводу камня левого мочеточника. Спустя несколько месяцев стала отмечать боли в пояснице слева, при УЗИ выявлен левосторонний гидроуретеронефроз. На экскреторных урограммах определено удвоение полостной системы обеих почек, функция правой почки удовлетворительная, слева выделение контраста резко замедлено, расширены чашечно-лоханочная система и верхние отделы левого мочеточника нижней половины удвоенной почки (рис. 1). С целью дренирования и выяснения функционального состояния левой почки выполнена чрескожная пункционная нефростомия. При антеградной и ретроградной уретеропиелографии визуализировалась протяженная стриктура левого мочеточника, захватывавшая его поясничный и тазовый отделы. С учетом сохранной функции почки и протяженности стриктуры решено произвести кишечную пластику левого мочеточника. Выполнена нижнесрединная лапаротомия. Левый мочеточник выделен в пределах
здоровых тканей, отсечен и интубирован. После резекции сегмента подвздошной кишки длиной около 20 см проходимость кишки восстановлена анастомозом “конец в конец” узловыми однорядными швами. Изолированный участок кишки расположили изоперистальтически, мочеточник на интубаторе имплантировали в кишку анастомозом “конец в конец” узловыми викриловыми швами 3/0 (рис. 2, а), сформировали кишечно-пузырное соустье (рис. 2, б). Интубатор вместе с катетером Фолея выведены наружу по уретре. Брюшная полость дренирована и послойно ушита наглухо. Осложнений после операции не наблюдалось, рана зажила первичным натяжением. Интубатор удален на 13-е сутки, выполнена антеградная пиелоуретерография: верхние мочевыводящие пути проходимы. Нефростома удалена, свищ закрылся, и пациентка выписана на амбулаторное лечение. При последнем контрольном обследовании
через 2,5 года после операции самочувствие больной хорошее, жалоб нет, функция левой почки удовлетворительная, полостная система незначительно расширена (рис. 3, а), электролитные нарушения отсутствуют. При цистоскопии хорошо визуализируются устье и просвет кишечного мочеточника (рис. 3, б).
Рисунок 3. Данные контрольного обследования спустя 2,5 года после илеоуретеропластики слева.
Заключение. Использование изолированного сегмента кишки позволяет замещать дефекты одного или обоих мочеточников любой локализации и протяженности. Существенную роль в малой популярности этого метода лечения играют опасения урологов в отношении угрозы послеоперационных осложнений: несостоятельности межкишечного анастомоза, некроза изолирован-ного кишечного сегмента, спаечной кишечной непроходимости, перитонита. Наиболее грозные из них развиваются, как правило, в раннем послеоперационном периоде. Данная операция должна выполняться в крупных урологических клиниках, имеющих большой опыт подобных вмешательств. Кишечная пластика мочеточника является достаточно эффективной операцией, позволяющей ликвидировать самые тяжелые поражения верхних мочевыводящих путей и получать хорошие результаты на отдаленных сроках.



