Несмотря на положительную динамику эпидемической ситуации по туберкулезу в РФ в течение последних 5 лет, она продолжает оставаться напряженной и неоднородной [1]. Успехи, достигнутые за последние десятилетия в борьбе с легочным туберкулезом, не отразились на динамике заболеваемости туберкулезом экстрапульмональной локализации, показатели которой составляют 2–4 случая на 100 тыс. населения [2–5]. Основной формой внелегочного туберкулеза в большинстве регионов России является мочеполовая, доля которой превышает 50% [4–6].
При туберкулезе почек вовлечение нижележащих отделов мочевого тракта с формированием его рубцовых сужений и деформаций имеет место в 25,4–84,7% случаев [6, 7], а в структуре причин образования стриктур мочеточника доля туберкулеза достигает 9–12,3% [8–10]. Механическая непроходимость различных отделов мочеточников — весьма частое и грозное патологическое состояние, неуклонно ведущее к гидронефротической трансформации, развитию пиелонефрита и гибели почки, что требует выполнения органоуносящей операции — нефрэктомии. Оставшаяся после удаления почки культя мочеточника нередко является очагом специфической инфекции, поддерживает дизурию, может малигнизироваться в отдаленном послеоперационном периоде [9]. В литературе нет указаний о преимуществах нефроуретерэктомии перед нефрэктомией в отношении купирования дизурии у больных туберкулезом почек.
 Широкое внедрение во фтизиоурологию раннего отведения мочи с помощью чрескожной пункционной нефростомии (ЧПНС) или внутреннего дренирования почки стентом привело к существенному снижению доли органоуносящих операций и росту числа вмешательств, направленных на восстановление проходимости мочеточника. Частота его множественных и протяженных сужений вследствие туберкулезного поражения достигает 16,7% [10, 11]. В этих случаях методом выбора является замещение мочеточника лоскутами мочевого пузыря или кишечника. В мировой литературе публикации, посвященные энтероуретеропластике больным туберкулезом, носят единичный характер. Эффективность и безопасность этих операций изучена недостаточно.
Широкое внедрение во фтизиоурологию раннего отведения мочи с помощью чрескожной пункционной нефростомии (ЧПНС) или внутреннего дренирования почки стентом привело к существенному снижению доли органоуносящих операций и росту числа вмешательств, направленных на восстановление проходимости мочеточника. Частота его множественных и протяженных сужений вследствие туберкулезного поражения достигает 16,7% [10, 11]. В этих случаях методом выбора является замещение мочеточника лоскутами мочевого пузыря или кишечника. В мировой литературе публикации, посвященные энтероуретеропластике больным туберкулезом, носят единичный характер. Эффективность и безопасность этих операций изучена недостаточно.
Поиск новых тактических и технических решений в лечении больных туберкулезом почки и мочеточника является важной социально значимой медицинской проблемой.
Цель исследования: повышение эффективности оперативного лечения туберкулеза почки с тотальным поражением мочеточника.
Материалы и методы. Изучены клиническое течение и результаты оперативного лечения 104 больных с протяженными или множественными стриктурами мочеточника специфической (n=92) и неспецифической (n=12) этиологии, оперированных в урологических клиниках Уральского и Санкт-Петербургского НИИ фтизиопульмонологии, а также Московского городского научно-практического центра борьбы с туберкулезом за 2005–2012 гг.
Критерием включения в исследование служило наличие специфического поражения мочевых органов или тотального, в т.ч. неспецифического, поражения мочеточника.
Среди больных было 59 (56,7%) мужчин и 45 (43,3%) женщин. Возраст колебался от 22 лет до 71 года (средний возраст – 51,2±0,6 года).
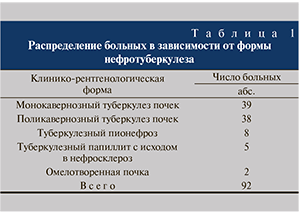
В зависимости от способа оперативного лечения пациенты разделены на 3 группы. В 1-ю вошли 48 (46,2%) больных нефротуберкулезом с отсутствием функции почки на стороне поражения в возрасте 52,5±2,7 года, которым осуществлено 48 нефрэктомий поясничным доступом. Вторую группу составил 31 (29,8%) пациент (средний возраст – 50,3±1,1 года), страдающий нефротуберкулезом с утратой функции почки, подвергнутый комбинированной нефроуретерэктомии. В 3-ю группу включены 25 (24%) больных со стриктурами мочеточников специфического (n=13) и неспецифического (n=2) происхождения в возрасте 51±0,6 года, которым выполнена уретеропластика с использованием кишечных аутотрансплантатов. Группы были сопоставимы по полу и возрасту (р>0,05). Клинико-рентгенологические формы нефротуберкулеза представлены в табл. 1. Для анализа состояния почек и мочеточников использовали понятие почечно-мочеточниковой единицы (ПМЕ), соответствующей одной функционирующей почке и одному мочеточнику.

Больным 2-й группы операцию начинали с трансуретрального иссечения устья мочеточника пораженной почки резектоскопом с «игольчатым» электродом (прямой петлей Turner–Warwick), отступя от него на 1 см. После появления жировой клетчатки по окружности разреза останавливали кровотечение путем коагуляции. Образовавшийся дефект мочевого пузыря размером 2 см не закрывали, так как мочу отводили уретральным катетером на 5–6 дней. По окончании эндоскопического этапа больного переводили в положение для люмботомии и открытым доступом удаляли почку с отсеченным мочеточником единым блоком.
Основными клиническими проявлениями заболевания у пациентов 1-й и 2-й групп были учащенное мочеиспускание, сопровождающееся императивными позывами с или без недержания мочи, т.е. имела место спастичность или гиперактивность мочевого пузыря. Всем больным проведены основной и сезонные курсы противотуберкулезной химиотерапии, при наличии сопутствующего пиелонефрита — антибактериальное лечение с использование препаратов широкого спектра действия.

Комплекс обследования состоял из клинических, лабораторных, радионуклидных, рентгенологических, ультразвуковых, инструментальных, эндоскопических, морфологических и уродинамических методов исследования. Клинический этап предусматривал тщательный сбор анамнеза, жалоб, совместное заполнение карты Международной системы суммарной оценки симптомов НМП (IPSS и QoL). Степень функциональных нарушений считали легкой при оценке, не превышавшей 7 баллов; умеренной — от 8 до 19 и тяжелой — от 20 до 35. Суточный ритм спонтанных мочеиспусканий регистрировали путем заполнения дневника, в котором отражалось количество мочеиспусканий и объем одномоментно выделенной мочи (функциональная емкость мочевого пузыря). Результаты лечения оценивали как хорошие при частоте мочеиспускания менее 8 раз, удовлетворительные — от 9 до 12 раз, неудовлетворительные — более 12 раз в сутки. Инструментом оценки качества жизни служил опросник SF-36 [12]. Анкетирование проводили до и через 2–4 мес после операции. Отдаленные результаты лечения изучены в период от 6 мес до 8 лет.
Статистическую обработку полученных результатов осуществляли с использованием методов параметрической и непараметрической статистики. Для описания средних групповых значений признаков рассчитывали средние арифметические и их стандартные ошибки, в ряде случаев и 95% доверительные интервалы. Для анализа межгрупповых различий применяли t-критерий Стьюдента. Критический уровень достоверности нулевой статистической гипотезы (об отсутствии различий) принимали равным 0,05. Расчеты выполнены в среде WindowsХР с использованием программ прикладного статистического анализа Statistica for Windows v 5.0 и Graph PadIn Stat tm (1994).
 Результаты и обсуждение. Для изучения функциональных резервов почки и целесообразности ее сохранения 35 больным нефротуберкулезом выполнена ЧПНС с последующей оценкой клубочковой фильтрации (КФ) путем осуществления раздельной пробы Реберга. С этой целью суточную мочу из дренированной почки и выпущенную самостоятельно собирали раздельно. Пробу ставили на следующие, 7–9-е и 14–16-е сутки после отведения мочи.
Результаты и обсуждение. Для изучения функциональных резервов почки и целесообразности ее сохранения 35 больным нефротуберкулезом выполнена ЧПНС с последующей оценкой клубочковой фильтрации (КФ) путем осуществления раздельной пробы Реберга. С этой целью суточную мочу из дренированной почки и выпущенную самостоятельно собирали раздельно. Пробу ставили на следующие, 7–9-е и 14–16-е сутки после отведения мочи.
Установлено, что шансы на восстановление функции почки зависели от ее инициального уровня. После ЧПНС в 15 (42,9%) ПМЕ парциальная составляющая КФ составила от 2,5 до 9 мл/мин, в среднем 7,6±1 мл/мин. При контрольном исследовании отмечена ее убыль в среднем на 0,5±0,2 на 7–9-е сутки и 1,1±0,4 мл/мин — на 14–16-е (p>0,05).
В остальных 20 (57,1%) случаях при колебаниях КФ от 11,2±2,3 до 19,1±2 (15,2±2,1) мл/мин зарегистрирован прирост этого показателя на 6,2±1,3 и 17,5± 3,1 мл/мин соответственно (p<0,05).
Показано, что при исходном уровне КФ менее 10 мл/мин резервные возможности почки при уретерогидронефрозе туберкулезной этиологии исчерпаны. Когда клиренс креатинина превышает эту величину, происходит восстановление функции деблокированной почки. В первом случае показана нефрэктомия или нефроуретерэктомия, во втором — реконструктивное вмешательство на мочеточнике.
В табл. 2 представлена сравнительная оценка результатов нефрэктомии и комбинированной нефроуретерэктомии. Длительность нефроуретерэктомии оказалась существенно большей, чем нефрэктомии не только за счет выполнения диссекции устья, которая продолжалась примерно 15 мин. Столько же времени занимала смена положения тела больного на операционном столе. Осложнения раннего послеоперационного периода в виде нагноения раны наблюдали только в 1-й группе. Достоверных различий в кровопотере, потребности в наркотических анальгетиках, сроках активизации пациента, начала перорального приема жидкости и пищи после операции не обнаружено. Таким образом, повышение радикальности операции за счет ее дополнения эндоскопическим компонентом незначительно повлияло на течение послеоперационного периода.
Существенных различий в исходном числе мочеиспусканий за сутки в обеих группах до оперативного лечения не было (p>0,05). Хороший результат в отношении купирования дизурии достигнут у 25 (52,1%) больных 1-й группы и у 21 (67,7%) — 2-й. Удовлетворительные результаты констатированы в 13 (27,1%) и 8 (25,8%) наблюдениях соответственно. Об отсутствии симптомов заявили 10 (20,8%) и 2 (6,5%) пациента соответственно. Таким образом, комбинированная нефроуретерэктомия способствовала уменьшению выраженности дизурии у 93,5% больных, а традиционная нефрэктомия — только у 79,2% (p<0,05).
Контрольные обследования пациентов в отдаленном послеоперационном периоде свидетельствовали о стойкости достигнутого в отношении дизурии эффекта. Колебания частоты суточных и ночных мочеиспусканий, функциональной емкости мочевого пузыря через 8–12 и 20–24 мес были незначительными. Несмотря на это, суммарный балл по шкале IPSS и индекс QoL продолжали постепенно снижаться, что, вероятно, указывает на адаптацию больного к остаточным проявлениям заболевания.
С помощью опросника SF-36 влияние оперативного лечения на связанное со здоровьем качество жизни изучено у 41 больного нефротуберкулезом (табл. 3). Показано, что нефрэктомия существенно изменила качество жизни по следующим характеристикам: физическое функционирование, ролевое функционирование, обусловленное физическим состоянием, интенсивность боли, общее состояния здоровья, жизненная активность и психическое здоровье. По параметрам социального и ролевого функционирования, обусловленного эмоциональным состоянием, изменение качества жизни оказалось недостоверным. Комбинированная нефроуретерэктомия значительно повлияла на все характеристики качества жизни, кроме параметра физического функционирования.
 Таким образом, комбинированная нефроуретерэктомия при специфическом поражении почек обладает существенными преимуществами, несмотря на большую длительность по сравнению с нефрэктомией. Обширность операционной травмы и кровопотеря вполне сопоставимы. Трансуретральный этап модифицированной операции достаточно прост в исполнении и не опасен экстравазацией мочи при адекватном дренировании мочевого пузыря. Удаление почки вместе с мочеточником больным нефротуберкулезом является профилактикой эмпием культи мочеточника, возможной ее малигнизации и персистенции дизурии, способствует значительному повышению качества жизни пациента.
Таким образом, комбинированная нефроуретерэктомия при специфическом поражении почек обладает существенными преимуществами, несмотря на большую длительность по сравнению с нефрэктомией. Обширность операционной травмы и кровопотеря вполне сопоставимы. Трансуретральный этап модифицированной операции достаточно прост в исполнении и не опасен экстравазацией мочи при адекватном дренировании мочевого пузыря. Удаление почки вместе с мочеточником больным нефротуберкулезом является профилактикой эмпием культи мочеточника, возможной ее малигнизации и персистенции дизурии, способствует значительному повышению качества жизни пациента.
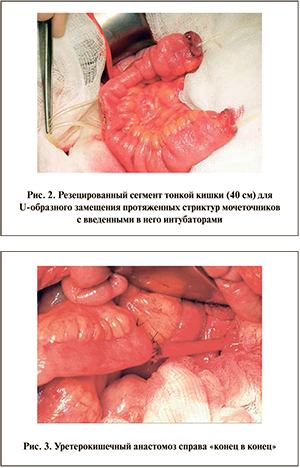
Кишечная пластика мочеточников выполнена 25 пациентам в возрасте от 35 до 69 лет. Для реконструкции в отношении 23 больных использовали подвздошную кишку (10 мужчин и 13 женщин), в отношении 2 (2 мужчин) — червеобразный отросток. Замещение сегментом кишки одного мочеточника произведено 21 пациенту, двух — 4 (рис. 1). Для 12 больных патологический процесс локализовался в тазовом отделе мочеточника. Из них 10 потребовалась замена дистальной части одного и 2 — двух мочеточников. При этом длина пораженного дистального участка составляла не менее 10 см и зона повреждения у всех пациентов распространялась выше подвздошных сосудов. В 2 наблюдениях выполнена аппендикопластика средней трети мочеточника, сочетавшаяся в 1 из них с замещением поясничного отдела лоскутом мочевого пузыря по Боари.
Тотальное замещение мочеточника сегментом подвздошной кишки произведено 13 пациентам: одностороннее — 11, двустороннее — 2. В целом 25 больным частично или полностью замещено кишечными сегментами 29 мочеточников. Из них более половины (16 [55,2%]) оперированы в связи с туберкулезным поражением, существенно реже – травматическим вследствие предшествующих оперативных вмешательств (4 [14%]). Каждая десятая операция выполнена по поводу нейромышечной дисплазии мочеточников (3 [10,3%]), постлучевых стриктур и облитераций (3 [10,3%]) и болезни Ормонда (3 [10,3%]). Ятрогенные повреждения мочеточника возникли вследствие иссечения натечного абсцесса — 1, уретеролитотомии в средней трети — 1, операции Боари — 1, экстирпации матки — 1.
Из ранних осложнений оперативного вмешательства зарегистрированы 1 (4%) некроз трансплантата и 1 (4%) несостоятельность межкишечного анастомоза. В первом наблюдении потребовалось удаление кишечного трансплантата и наружное дренирование почки, во втором — ревизия органов брюшной полости, межкишечный реанастомоз и интубация кишечника зондом Эббота. После некроза трансплантата удалось восстановить естественный пассаж мочи, выполнив повторную уретероилеопластику, во втором — справиться с перитонитом и парезом кишечника. Отдаленные результаты лечения в сроки от 0,5 до 3 лет изучены у 21 (84%), осложнения отмечены у 3 (14,3%) больных. Пузырно-кишечно-мочеточниковый рефлюкс при ретроградной цистографии выявлен только у 2 больных после замещения правого мочеточника кишечным сегментом длиной 10 см. Острый пиелонефрит диагностирован в 2 (9,5%) наблюдениях. Нарастание креатининемии имело место у 1 больной после тотального замещения обоих мочеточников и мочевого пузыря с одновременной цистоуретеропластикой.
При использовании подвздошной кишки для замещения мочевыводящих путей в результате резорбции электролитов может развиться гиперхлоремический метаболический ацидоз, который наиболее часто появляется при ХПН. Нами изучены средние показатели кислотно-основного и электролитного баланса крови в раннем послеоперационном периоде у 25 больных и через 6–12 мес – у 21.
В течение первого месяца после энтероуретеропластики среднее значение уровня калия в сыворотке крови составило 3,8±0,1 ммоль/л; хлора — 107,2±2,3 ммоль/л; дефицит оснований (ВЕ) — -1,43±1,8. В течение 6–12 мес после операции эти показатели оставались стабильными. Концентрация калия была 3,7±0,2 ммоль/л; хлора — 106,8±1,9 ммоль/л, недостаток оснований (ВЕ) — -2,15±1,9. Таким образом, использование для замещения мочеточника подвздошной кишки длиной не более 25 см не приводило к серьезным метаболическим и электролитным нарушениям. Благодаря широкому пузырно-кишечному анастомозу (рис. 2) не происходит застаивания мочи в кишечном трансплантате, уменьшается время ее контакта с кишечным эпителием. В таких условиях резорбция мочи и, следовательно, риск развития метаболического ацидоза сводятся к минимуму.
Для оценки качества жизни выполнено анкетирование с помощью общего опросника SF-36 23 больных, перенесших кишечные реконструкции мочеточников, до операции и через 4–6 мес после нее. Установлено, что пациенты с протяженными стриктурами мочеточников имеют низкие показатели качества жизни. В отдаленном периоде отмечено существенное улучшение качества жизни по всем показателям, особенно психического компонента здоровья, жизненной активности и ролевого функционирования, стойкое снижение интенсивности болевого симптома (p<0,05).
Таким образом, кишечная пластика мочеточников при их протяженных сужениях туберкулезного и другого генеза является эффективным способом восстановления уродинамики при невозможности использования тканей мочевого тракта.
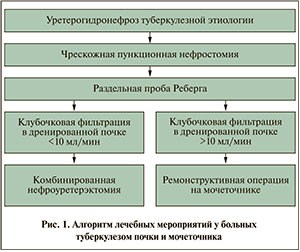
Все вышеизложенное позволило разработать алгоритм лечебных действий в отношении больных туберкулезом почки и мочеточника (рис. 3).
Выводы
- Изучение КФ, деблокированной путем ЧПНС почки, позволяет определять лечебную тактику: при ее величине менее 10 мл/мин методом выбора является органоуносящее оперативное вмешательство, при превышении этого показателя — органосохраняющее (реконструктивно-восстановительное).
- Нефроуретерэктомия по сравнению с нефрэктомией при нефротуберкулезе является более предпочтительной в связи с высокой частотой поражения мочеточника. Эта операция позволяет избегать нагноения его культи, персистенции дизурии, что значительно повышает качество жизни пациентов.
- Комбинированная нефроуретерэктомия по сравнению с традиционной нефрэктомией при туберкулезном поражении почек и мочевыводящих путей приводит к вдвое большему приросту функциональной емкости мочевого пузыря, сопровождается снижением выраженности расстройств мочеиспускания у 93,5 и 79,2% больных соответственно (p<0,05).
- Протяженные поражения мочеточников при невозможности восстановления тканями мочевого тракта являются показанием к выполнению реконструктивно-восстановительных операций с использованием участка тонкой кишки. Выполнение данных операций позволяет избавить 92% пациентов от пожизненного наружного дренирования почек, тем самым существенно улучшая качество их жизни.



