Введение. Гипогонадизм (андрогендефицит) у мужчин – это клинический и биохимический синдром, связанный с низким уровнем тестостерона, который может оказывать негативное влияние на множество органов и систем, ухудшая качество жизни и жизненный прогноз. Низкий уровень тестостерона может приводить к сексуальной дисфункции, снижению интенсивности формирования мышечной массы и костной минерализации, нарушению метаболизма жиров, снижению фертильности и когнитивной дисфункции [1, 2]. Кроме того, в последние годы появились сообщения, акцентирующие внимание на взаимосвязи заболеваний предстательной железы и андрогендефицита [3, 4]. Так, снижение уровня тестостерона установлено у 17–60% пациентов с длительным течением хронических воспалительных заболеваний простаты [4]. Это может быть обусловлено тем, что при андрогендефиците имеет место снижение экспрессии гена NOS (NO-синтазы) и снижение продукции NO в простате, что ведет к нарушению гемодинамики в ней [5]. Учитывая доказанное положительное влияние андрогенной терапии при андрогендефиците, вызывает интерес изучение ее эффективности и безопасности для мужчин с хроническим простатитом. Одним из эффективных препаратов, используемых для андрогенной терапии, является трансдермальный 1%-ный гель тестостерона (Андрогель®) [6].
В связи с этим нами было проведено исследование, основной целью которого стала оценка влияния лечения препаратом Андрогель® на качество жизни пациентов с андрогендефицитом (гипогонадизмом) и хроническим простатитом в условиях повседневной практики. Кроме того, вторичными целями исследования стали оценка влияния лечения препаратом Андрогель® на эректильную функцию пациентов с гипогонадизмом и хроническим простатитом в условиях повседневной практики, а также оценка профиля переносимости и безопасности.
Материалы и методы. В наблюдательное многоцентровое неинтервенционное исследование были включены мужчины с хроническим простатитом и впервые диагностированным андрогендефицитом, которым ранее не проводилась терапия тестостероном и которым был назначен 1%-ный гель тестостерона (Андрогель®). Решение врача о назначении пациенту данного препарата должно было быть принято независимо от включения пациента в исследование. Исследование было одобрено Независимым междисциплинарным комитетом по этической экспертизе клинических исследований в соответствии с требованиями надлежащей клинической практики, Хельсинкской декларации и локальными регуляторными требованиями. Все пациенты, включенные в исследование, подписали форму информированного согласия.
Медицинские данные собирались урологами и эндокринологами амбулаторного звена как частных, так и муниципальных учреждений здравоохранения городов России в период с мая по октябрь 2017 г. из 80 амбулаторных центров: О. В. Абаимов (Новосибирск); Н. Э. Авадиева (Ростов-на-Дону); Д. С. Алексанян (Санкт-Петербург); Ф. Р. Асфандияров (Астрахань); Р. Э. Байрамов (Симферополь); Д. С. Баранцев (Коломна); А. Л. Болдырев (Тюмень); Е. А. Быков (Н. Новгород); К. Г. Вартанян (Санкт-Петербург); Р. П. Василевский (Москва); В. В. Волженцев (Оренбург); С. В. Выборнов (Астрахань); А. Г. Глухов (Волгоград); К. Э. Емкужев (Пятигорск); Ф. Н. Зимин (Челябинск); А. А. Калашян (Омск); Ф. П. Капсаргин (Красноярск); Р. В. Карин (Пермь); Т. Ю. Катаева (Липецк); Л. А. Киселев (Казань); П. В. Кляузов (Новосибирск); Н. Н. Ковригина (Красноярск); А. С. Кондратьев (Москва); А. А. Копылов (Санкт-Петербург); Д. И. Коруняк (Воронеж); В. В. Косырев (Новосибирск); Г. В. Кочарян (Кисловодск); Д. В. Кочетков (Москва); В. В. Крук (Брянск); О. Б. Кулагина (Ярославль); А. О. Куликов (Москва); Н. Г. Кульченко (Троицк); К. В. Кумачев (Москва); Ж. П. Кушичева (Санкт-Петербург); В. В. Лебедев (Тамбов); О. Л. Ледовская (Екатеринбург); К. А. Лобкарев (Тольятти); Р. Ю. Луковсков (Волгоград); В. А. Луценко (Иркутск); А. С. Лычагин (Москва); А. А. Марков (Москва); Ф. Ш. Мангутов (Москва); А. В. Мерзляков (Оренбург); А. М. Метелкин (Пермь); Ш. А. Мирюнусов (Екатеринбург); Д. В. Михайлов (Самара); Д. В. Молоканов (Волгоград); Е. А. Москаленко (Санкт-Петербург); Д. Р. Мусякаев (Москва); Е. М. Мучник (Краснодар); Б. О. Мчедлидзе (Санкт-Петербург); Д. Ш. Немсадзе (Новосибирск); И. В. Никифоров (Москва); Омутных А. Н. (Пермь); А. А. Осташевский (Новосибирск); Р. Р. Панюхов (Санкт-Петербург); В. Н. Паршина (Москва); А. А. Патрикеев (Челябинск); А. В. Полищук. (Белгород); А. Н. Радаев (Самара); С. Н. Романова (Москва); И. М. Рохликов (Москва); А. В. Сагалов (Челябинск); А. А. Свирский (Симферополь); А. П. Сериков (Москва); А. П. Смерницкий (Москва); А. В. Смирнов (Пермь); О. В. Стасив (Иркутск); Д. Ю. Стерхов (Москва); И. В. Терехин (Ростов-на-Дону); К. А. Тирси (Москва); К. С. Трофимов (Раменское); М. Р. Хальзов (Курск); В. В. Хасанов (Казань); И. П. Ходченкова (Мытищи); В. А. Цирульников (Краснодар); А. А. Цыбулин (Москва); Ю. А. Чебаков (Омск); Е. Н. Черникова (Санкт-Петербург); А. В. Черновский (Казань); Д. В. Шафранов (Тюмень); С. М. Шиков (Серпухов); С. В. Шихотаров (Челябинск); О. Г. Шрамова (Красноярск).
Данная программа была открытой, без группы сравнения, и все изменения оценивались относительно базовых показателей. Критерии включения пациентов в исследования: мужской пол, возраст старше 18 лет, установленный диагноз дефицита тестостерона (гипогонадизма) в соответствии с действующими рекомендациями/стандартами; установленный диагноз хронического простатита в соответствии с действующими рекомендациями/стандартами, прием препарата Андрогель® менее 1 мес. до подписания информированного согласия. Критериями невключения были любые противопоказания, перечисленные в Инструкции по медицинскому применению лекарственного препарата Андрогель®.
В исследование были включены 403 пациента, из них 188 (46,7%) с бактериальной, 180 (44,7%) с абактериальной и 35 (8,7%) с неустановленной формами хронического простатита. Из них завершил исследование 401 человек. Двое (0,5%) выбыли из исследования в связи с неявкой на визиты. Клиническая характеристика пациентов, завершивших исследование, представлена в табл. 1.

Всем пациентам был назначен препарат Андрогель® (1%-ный гель тестостерона в пакетиках) в соответствии с Клиническими рекомендациями и Инструкцией по медицинскому применению препарата [1, 2, 6]. Гель наносили на сухую, чистую кожу плеч, надплечий и/или живота. Для подбора оптимальной дозировки препарата проводили регулярную оценку концентраций общего тестостерона крови – через 1 и 3 мес. после начала терапии. Если дозы 50 мг было недостаточно для поддержания уровня сывороточного тестостерона выше 12,1 нмоль/л, дозу увеличивали до 100 мг. Если уровень тестостерона на дозе 100 мг превышал нормальные значения, то дозу снижали до 50 мг. Наблюдений, когда при дозировке 50 мг уровень тестостерона был выше нормальных значений, в исследовании не было. Таким образом, ежедневные дозы препарата, которые применялись пациентами, составляли 50 и 100 мг (1 или 2 пакетика 1%-ного геля тестостерона).
Длительность наблюдения за пациентами составила 3 мес. После сбора первичных данных первый визит наблюдения был предусмотрен через 1 мес., второй – через 3 с момента назначения препарата тестостерона. «Окно» визитов составило ±4 дня от планируемых дат.
Эффективность терапии оценивали путем определения уровня общего тестостерона (на каждом визите) методом иммуноферментного анализа. Для разграничения нормального и сниженного уровней общего тестостерона было принято значение 12,1 нмоль/л в соответствии с современными рекомендациями [1, 2]. Кроме того, в динамике оценивали массу тела пациентов и окружность талии (на момент включения в исследование и через 3 мес. лечения).
На всех визитах осуществляли анкетирование.
С помощью опросника AMS выявляли и отслеживали динамику симптомов, характеризующих психологические, соматические и сексуальные проблемы, обусловленные недостатком тестостерона. С целью получения субъективной информации о выраженности симптомов нарушенного мочеиспускания и их влиянии на качество жизни использовали опросник МИЭФ-5, который содержал вопросы о том, как нарушения эрекции сказывались на сексуальной жизни в течение последних 4 недель, и опросник IPSS (Международная система суммарной оценки симптомов болезней предстательной железы).
Для мониторинга течения хронического простатита применяли индекс шкалы симптомов хронического простатита и синдрома тазовой боли у мужчин (NIH-CPSI). Данный опросник – необходимый и важнейший диагностический инструмент в работе с больными хроническим простатитом, симптомом хронической тазовой боли, позволяющий оценивать как степень тяжести заболевания, так и эффективность его лечения.
Оценку профиля переносимости и безопасности препарата Андрогель® осуществляли через 1 и 3 мес. после начала терапии в соответствии с клиническими рекомендациями [1, 2].
Статистический анализ проведен с помощью программного обеспечения SPSS 23 (IBM). Для анализа вида распределений применяли критерии Шапиро–Уилка и Колмогорова–Смирнова. Были рассчитаны изменения базовых показателей через 1 и 3 мес. терапии как в абсолютных, так и в процентных значениях с использованием парного t-теста, расчетом медиан и 95% доверительного интервала (95% ДИ) для медианы. Статистически значимыми считали различия при p<0,05.
Результаты. Как и следовало ожидать, проведенная андрогенная терапия способствовала устранению дефицита тестостерона у всех пациентов. Число пациентов, применявших препарат в суточной дозе 50 либо 100 мг, статистически значимо не изменилось.
Уровень тестостерона в течение всего периода наблюдения демонстрировал статистически значимую положительную динамику (табл. 2) и к концу исследования вырос на 6,9 (95% ДИ – 6,5–7,3) нмоль/л относительно исходных значений. Нормализация уровня тестостерона сопровождалась статистически значимым снижением массы тела и уменьшением окружности талии (табл. 2).

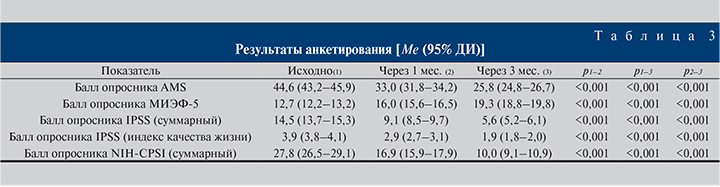
Нормализация уровня тестостерона сопровождалась статистически значимым уменьшением выраженности симптомов андрогенного дефицита, оцененных путем опросника AMS (табл. 3). Так, за весь период исследования оценка снизилась на 18,7 (95% ДИ – 17,5–19,9) балла. Эректильная функция мужчин также улучшилась, что выразилось в статистически значимом повышении балла в целом на 6,6 (95% ДИ – 6,1–7,1).
Со стороны симптомов болезней предстательной железы была отмечена статистически значимая положительная динамика: оценка по опроснику NIH-CPSI снизилась в среднем на 10,8 (95%ДИ – 9,8–11,7) балла к концу месяца терапии, по прошествии 3 мес. – на 17,7 (95% ДИ – 16,5–18,9) балла. Как суммарный балл опросника IPSS, так и индекс качества жизни IPSS за весь период наблюдения характеризовались снижением, которое в целом составило 8,7 (95% ДИ – 7,9–9,4) и 2,0 (95% ДИ – 1,9–2,2) балла соответственно (табл. 3).
Средняя продолжительность терапии тестостероном составила 92 дня. В ходе исследования не было зафиксировано ни одного серьезного нежелательного явления. Показатели гематокрита, уровня простатического специфического антигена и данные трансректального УЗИ оставались в пределах нормальных значений в течение 3 мес. терапии у всех пациентов. Патологических изменений грудных желез также не было выявлено. После окончания данного исследования терапию препаратом Андрогель® продолжили все пациенты, за исключением двух больных, данные которых оказались недоступными.
Обсуждение. Учитывая доказанную высокую эффективность использования препарата Андрогель® в условиях рутинной клинической практики [7], нормализация уровня тестостерона у мужчин, включенных в исследование, оказалась ожидаемым результатом. Проводимая терапия сопровождалась значительным регрессом симптомов гипогонадизма, что в очередной раз свидетельствует о ее высокой эффективности в отношении андрогендефицита и его осложнений. Полученные нами результаты согласуются с данными других исследователей [8]. Терапия препаратами тестостерона мужчин с гипогонадизмом влияет на телосложение, обусловливая уменьшение жировой массы и увеличение безжировой массы тела [9]. В ряде исследований применения тестостерона отмечено снижение содержания висцерального жира, что сопровождалось уменьшением окружности талии [10, 11], поэтому снижение массы тела и уменьшение окружности талии мужчин, отмеченные в нашем исследовании, также были ожидаемыми.
Кроме того, в нашем исследовании установлено положительное влияние коррекции андрогендефицита на эректильную функцию мужчин. В нескольких ретроспективных исследованиях был зафиксирован благоприятный эффект в отношении либидо, эрекции и эякуляции [12, 13]. Международное многоцентровое проспективное исследование с участием 1493 мужчин показало, что тестостеронзаместительная терапия достоверно улучшает либидо, эректильную функцию и ответ на терапию ингибиторами фосфодиэстеразы 5-го типа [14].
Наибольший интерес представляют результаты, свидетельствующие о снижении выраженности симптомов нарушенного мочеиспускания, хронического простатита и синдрома тазовой боли, что сопровождалось улучшением качества жизни. Получение этих результатов свидетельствует о новом перспективном направлении андрогенной терапии – возможности ее применения в качестве дополнительного метода, повышающего эффективность лечения хронического простатита при его сочетании с гипогонадизмом. Эффективность такого лечения продемонстрирована также в работах других авторов [15, 16]. При этом андрогенная терапия препаратом Андрогель® безопасна и не сопровождается серьезными нежелательными явлениями, что было показано как в нашем исследовании, так и в работах других исследователей [7, 17].
Заключение. Терапия трансдермальной формой тестостерона – 1%-ным гелем (Андрогель®) – высокоэффективное и безопасное средство устранения андрогендефицита (гипогонадизма). На фоне этого лечения пациентов нормализуется уровень тестостерона, регрессируют симптомы гипогонадизма, улучшаются половая функция и метаболические параметры. При наличии у мужчины хронического простатита использование андрогенной терапии, назначенной по показаниям (наличие синдрома гипогонадизма), является дополнительным эффективным методом улучшения общего состояния больных, поскольку она приводит к снижению выраженности симптомов нарушенного мочеиспускания, других симптомов хронического простатита и тазовой боли, что сопровождается улучшением качества жизни.



