Введение. В настоящее время гУРС активно применяется при лечении почечных камней [1–3]. Широкое развитие данной операции, несомненно, связано с активным внедрением гибких эндоскопов и лазерных литотрипторов. Этот метод стал более популярным среди урологов ввиду меньшей инвазивности по сравнению с перкутанной нефролитотрипсией. Согласно рекомендациям Европейской ассоциации урологов, гУРС является альтернативой дистанционной литотрипсии и методом лечения первой линии при небольших почечных камнях (<10 и 10–20 мм) и второй линии при почечных конкрементах >20 мм [4]. Рентгеновский контроль применяется на различных этапах данной операции: установка проводника и мочеточникового кожуха, пиелокаликоскопия, уточнение локализации камня или наличия резидуальных фрагментов, стентирование мочеточника. Использование флюороскопии при урологических вмешательствах сопряжено с такими рисками, как индуцирование злокачественных новообразований в результате радиационного облучения пациента и хирургической бригады [5–7]. Согласно данным Международной комиссии по радиологической защите, лучевая нагрузка, полученная во время диагностики камней, их лечения и последующего наблюдения, является кумулятивной, что особенно актуально в связи с частыми рецидивами мочекаменной болезни (МКБ) [5]. Данная настороженность послужила причиной поиска специалистами способов не только снижать, но и исключать лучевую нагрузку во время эндоурологических вмешательств [8]. Поэтому в литературе стали появляться публикации о результатах эндоскопических операций при камнях мочеточника без использования рентгеноскопии [9–15]. Первые работы касались результатов безрентгеновской контактной уретеролитотрипсии при камнях мочеточника [9–12, 14, 15].
В дальнейшем появились публикации о возможности выполнения РИРХ без флюороскопии, однако число подобных работ ограниченно [13, 16–20]. Целью нашей работы было оценить безопасность и эффективность безрентгеновской гУРС при лечении небольших камней почек.
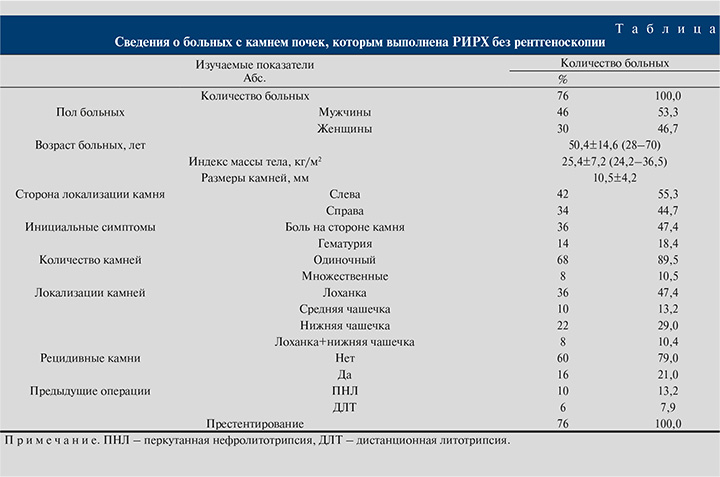
Материалы и методы. В данное исследование были включены результаты безрентгеновской гУРС у 76 больных, оперированных в Центре урологии с робот-ассистированной хирургией Мариинской больницы. Мужчин было 46 (53,3%), женщин – 30 (46,7%). Средний возраст больных составил 50,4±14,6 (от 28 до 70) года. Пациенты с аномалией развития почек, с двусторонними мочеточниковыми и почечными камнями, с операциями на ВМП в анамнезе были исключены из исследования. Всем пациентам выполнялись лабораторные анализы и нативная компьютерная томография в стандартном режиме для определения размеров и плотности камня, проводилось предоперационное стентирование мочеточника. Средний размер камня составил 10,5±4,2 мм. Характеристика больных, подвергнутых безрентгеновской гУРС, приведена в таблице.
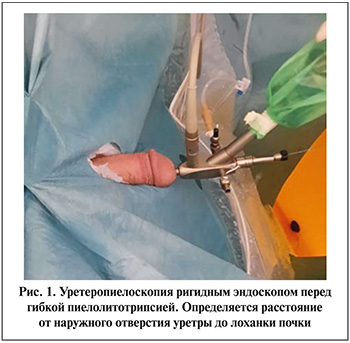

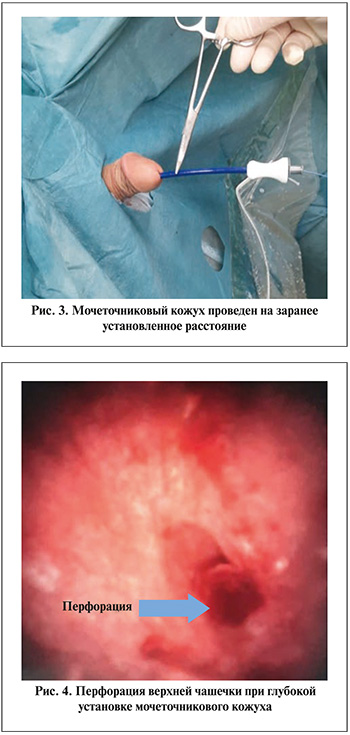
Все вмешательства были запланированы как гУРС. Операции выполнялись под общей анестезией в литотомическом положении. Все процедуры выполнены компетентным урологом с опытом более 250 гУРС. Непосредственно перед операцией обычно проводилась предоперационная антибактериальная терапия цефалоспорином третьего поколения. Флюороскопическая C-дуга всегда была в операционной для использования в случае необходимости. Вначале выполняли диагностическую уретерореноскопию с использованием ригидного уретероскопа 9,5 Шр для исключения каких-либо патологических изменений мочеточника (камень, стриктура или девиация), которые могут вызывать трудности при установке МК. Уретероскопия ригидным эндоскопом также позволяет расширять мочеточник, что может помогать при введении МК. УРС выполняли с помощью гидрофильного проводника 0,038-дюйма с гибким наконечником. Эндоскоп проводили до полостной системы почки, под контролем зрения устанавливали гибкую часть струны в лоханку. После локализации проксимального конца эндоскопа в лоханке для правильного и безопасного введения МК путем пометки на наружной части уретероскопа определяли расстояние для дальнейшего проведения МК (рис. 1). После установки струны уретероскоп извлекали, вновь с помощью сопоставления его и кожухом устанавливали глубину проведения последнего (рис. 2). Далее жесткий уретерореноскоп мимо струны проводили в мочевой пузырь для визуального контролирования адекватного проведения МК. На установленное расстояние кожух проводили по струне до тех пор, пока не возникало сопротивление или не наблюдалось какое-либо его отклонение. Обычно МК устанавливали на предварительно установленное расстояние, чтобы исключить перфорацию чашечно-лоханочной системы (ЧЛС) (рис. 3). При глубоком проведении МК наблюдали единичные случаи перфорации верхней чашечки кожухом, однако они не требовали активных действий (рис. 4). Для гибкой УРС использовали одноразовый эндоскоп Lithovue (Boston Scientific), который по кожуху проводили до ЧЛС, выполняли пиелокаликоскопию, уточняли особенности анатомии полостной системы и локализацию конкремента. При нахождении камня в нижней чашечке с помощью корзинки Дормиа смещали его в верхнюю чашечку или лоханку для более удобной фрагментации. Гольмиевый лазерный генератор Auriga 200 и лазерное волокно 230 мкм использовались у всех пациентов для контактной литотрипсии. При дроблении камня использовали режим сочетания высокой частоты (10–15 Гц) и низкой мощности (0,8–1,0 Дж). В конце операции проводили эндоскопическую ревизию ЧЛС для выявления резидуальных камней. Далее МК удаляли, выполняли УРС жестким эндоскопом для исключения какого-либо повреждения мочеточника. У 64 (84,2%) из 76 больных операцию заканчивали установкой стента диаметром 4,7 Fr и длиной 24 или 26 см. Локализацию верхнего конца стента определяли визуально и с помощью ультразвукового исследования (УЗИ) почки, а дистального – с помощью УРС. Стент обычно удаляли через 2–3 нед. после операции. У 12 (15,8%) больных после гУРС устанавливали мочеточниковый катетер на 1–2 дня.
Изучались такие показатели, как время операции и ее эффективность, число интра- и послеоперационных осложнений. Время операции измерялось от момента цистоскопии с удалением стента до повторного дренирования верхних мочевыводящих путей (ВМП). Послеоперационные осложнения были классифицированы по Clavien–Dindo. Эффективность гУРС оценивалась с помощью обзорной рентгенографии мочевыводящих путей для рентгеноконтрастных и нативной компьютерной томографии (КТ) для негативных камней перед выпиской из стационара. Операция считалась эффективной при отсутствии резидуальных камней или их наличии размером ≤3 мм.
Результаты. Операции были успешными и выполнены без рентгеновского контроля. Во всех случаях удалось установить МК и выполнить контактную пиелолитотрипсию. Время операции колебалось от 35 до 80 мин, в среднем составило 42,5±8,0 мин. После первого сеанса РИРХ была эффективной у 70 (92,1%) из 76 больных. У остальных 6 (7,9%) пациентов были выявлены резидуальные камни, которые полностью удалены после второго сеанса гУРС. Интраоперационные осложнения в виде перфорации верхней чашечки дистальным концом МК наблюдались у 2 (2,6%) больных, которая не требовала проведения каких-либо активных действий. Послеоперационные осложнения имели место у 10 (13,2%) пациентов. У 6 (7,9%) из них наблюдалась лихорадка, у 4 (5,3%) – гематурия. Серьезных осложнений, таких как перфорация мочеточника или сепсис, не было, гемотрансфузия не проводилась.
Дискуссия. РИРХ является эффективным и надежным методом лечения почечных камней с высоким процентом эффективности. Недостатком данной операции, как и других эндоурологических вмешательств, выполняемых при МКБ, является использование рентгеноскопии. Медицинское излучение представляет потенциальный риск канцерогенеза у пациентов и медицинского персонала. После хронического воздействия радиации могут развиваться злокачественные новообразования щитовидной железы, кожи, гематологические заболевания [21, 22]. Основным показателем воздействия излучения является время рентгеноскопии (ВР). При стандартных УРС, по данным R. S. Hsi и соавт. [10] оно составило 144 с, а G. O. Hellawell и соавт. [23] сообщили о среднем значении ВР около 78 (6–414) с. М. Е. Lipkin и соавт. [24] установили, что у 30 мужчин, не страдвших ожирением, которые подвергались УРС, среднее ВР было 47 с, а доза облучения – 0,31–7,17 мЗв.
Согласно их данным, 1 импульс/с примерно соответствует дозе облучения 0,01–0,02 мЗв, которая равна таковой (0,02 мЗв), получаемой при одном рентгеноскопическом снимке грудной клетки [25]. Эти данные показывают, что доза ионизирующего излучения составляет столько же, сколько объем радиации от одного снимка грудной клетки, умноженный на количество импульсов рентгеноскопии во время УРС. Поэтому пациент и медицинский персонал подвергаются воздействию высокой дозы ионизированного излучения, снижение которой имеет важное значение для безопасности гУРС.
Первое исследование УРС без рентгеноскопии было выполнено пациентам с камнями дистального отдела мочеточника [9]. Авторы сообщили о необходимости проведения рентгеноскопии у 4% пациентов, при этом никаких осложнений не было. В другом исследовании, в котором у половины больных были обнаружены камни проксимального и среднего отделов мочеточника, авторы сообщили, что рентгеноскопия потребовалась у 7,52%, а незначительные осложнения наблюдались у 11% пациентов [26].
В ретроспективном сравнительном исследовании, включившем 100 больных с камнями мочеточника и почек, G. Olgin и соавт. [11] описали методику безрентгеновской УРС у 50 пациентов. В этом исследовании УРС проводилась с использованием пошаговой методики, полученные результаты были схожими в двух группах (с рентгеном и без него). Авторы сообщили, что УРС без рентгена выполнима и эффективна для лечения камней почек и мочеточника.
За последние годы появились работы о результатах безрентгеновской РИРХ [13, 16 – 20]. H. I. Cimen и соавт. [17] выполнили безрентгеновскую РИРХ 93 пациентам. У всех больных они вначале выполняли уретероскопию ригидным эндоскопом, по струне под контролем уретероскопа устанавливали МК. Далее выполнялась гибкая уретеропиелоскопия с лазерной литотрипсией камня. Пациенты с предварительным стентированием были исключены из исследования. Средний размер камня составлял 14,7±5 (7–32) мм и 42 (45,1%) пациента имели камни нижней чашечки. В другом исследовании С. Senel и соавт. [18] исследовали 350 пациентов, перенесших РИРХ по поводу камней почки и верхних отделов мочеточника. В этом ретроспективном исследовании сравнивались две группы для РИРХ с рентгеноскопией и без нее. В группе без рентгеноскопии было 255 пациентов. Авторы установили, что между двумя группами не было никакой разницы в стоун-фри-статусе и количестве осложнений, которые составили 86,3 и 87,0%, 17,9 и 15,7% соответственно. Авторы пришли к выводу, что РИРХ является осуществимым и безопасным методом. М. Kiras и соавт. [19] выполнили гУРС 576 больным без использования рентгеноскопии, которая была успешной у 96,7% (у 557 из 576 пациентов), а остальным 19 больным потребовалась рентгеноскопия по различным причинам. Средний размер камня был 11,6±5,2 мм, а время операции – 39,4±8,2 мин. После первого сеанса эффективность гУРС составила 83,3%. Второй и третий сеансы были проведены 32 (5,7%) и 7 (1,2%) пациентам соответственно. В целом частота осложнений составила 11,8% и все осложнения были незначительными (I или II степень по Clavien–Dindo). Мы выполнили РИРХ без флюороскопии 76 больным с почечными камнями, чтобы исключить дозу рентгеновского облучения. Эффективность данной операции после первого сеанса составила 91,6%, а количество послеоперационных осложнений было минимальным.
Результаты различных авторов и наши данные показывают, что полностью безрентгеновская РИРХ технически возможна и наиболее оправдана в несложных клинических наблюдениях. Тем не менее следует помнить о возможных серьезных осложнениях безрентгеновской гУРС, особенно для начинающих эндоурологов. Установка МК сопровождена рисками повреждения целостности мочевых путей на любом уровне, что несомненно ограничивает энтузиазм в полном исключении рентгеновского сопровождения во время РИРХ. Данное заключение является одним из основных рекомендаций международного альянса по мочекаменной болезни от 2023 г. и должно соблюдаться до появления доказательств эффективности альтернативных методик с высокой степенью надежности [27]. В нашей работе были проанализированы результаты безрентгеновской гУРС в лечении пациентов без аномалии развития почек и с небольшим солитарным камнем в почке, а также без предыдущих операций на ВМП в анамнезе, что указывает на ограниченную возможность использования полученных результатов у всей популяции больных МКБ.
Также следует упомянуть, что кумулятивное облучение основывается не только на интраоперационной рентгеноскопии, но и на лучевых методах диагностики, выполненных на предоперационном этапе. Выполнение низкодозной КТ обеспечивает «безопасное окно облучения» для интраоперационной рентгеноскопии, обеспечивая итоговую лучевую нагрузку в пределах допустимого значения. Во всех включенных в нашу работу наблюдениях нативная КТ почек выполнялась в стандартном режиме, сопровождающаяся дозой облучения в среднем 10 мЗв.
С целью дальнейшего ограничения лучевой нагрузки именно в подобных случаях была рекомендована полностью безрентгеновская гУРС.
Однако мы не призываем молодых неопытных урологов прибегать к выполнению РИРХ без рентгеноскопии, что может быть причиной развития серьезных осложнений.
С накоплением определенного опыта у отобранной группы больных с солитарными камнями почек можно прибегать к безрентгеновской гУРС. Для этих целей также рекомендуем активно использовать в своей клинической практике 3D-модели ЧЛС, позволяющие предоперационно планировать предстоящее вмешательство и отрабатывать его этапы. Кроме того, эти операции выполняются в эндоурологической операционной, где постоянно имеется рентгеновская С-дуга, которую при необходимости всегда можно подключить.
Помимо преимуществ, связанных с безрентгеновской гУРС, следует указать на недостатки проведенного исследования. Во-первых, работа основана на ретроспективном анализе результатов и данных пациентов, что не исключает влияния на итоговую результативность операций других параметров. Во-вторых, в исследовании отсутствует контрольная группа для сравнения, что не позволяет более аргументированно утверждать об альтернативности безрентгеновской гУРС по стандартной технике. Поэтому необходимы дальнейшие проспективные рандомизированные исследования для сравнения результатов РИРХ с и без рентгеноскопии.
Заключение. Литературные и наши данные показывают, что гУРС без рентгеноскопии является эффективным и безопасным методом лечения камней почек у пациентов без аномалии ВМП и операций в анамнезе. Кроме того, этот метод может быть полезным в определенных клинических ситуациях, таких как МКБ у беременных, также является более удобным для хирургов, поскольку не нужно использовать тяжелые свинцовые фартуки. Тем не менее следует помнить об ассоциированных рисках и выполнять безрентгеновскую гУРС при наличии достаточного опыта у оперирующего хирурга.



